Advantage 40 Mg Lösung Zum Auftropfen Auf Die Haut Für Kleine Katzen Und Kleine Zierkaninchen
Fachinformation in Form der Zusammenfassung der Merkmale des Tierarzneimittels (Summary of Product Characteristics)
1. Bezeichnung des Tierarzneimittels:
Advantage 40 mg Lösung zum Auftropfen auf die Haut für kleine Katzen und kleine Zierkaninchen
2. Qualitative und quantitative Zusammensetzung:
Eine Pipette mit 0,4 ml enthält:
Wirkstoff(e):
Imidacloprid 40 mg
Sonstige Bestandteile:
Butylhydroxytoluol (E 321) 0,4 mg
Benzylalkohol 332,8 mg
Eine vollständige Auflistung der sonstigen Bestandteile finden Sie unter Abschnitt 6.1
3. Darreichungsform:
Lösung zum Auftropfen auf die Haut Klare hellgelbe bis leicht bräunliche Lösung
4. Klinische Angaben:
4.1 Zieltierart(en):
Katze und Zierkaninchen
4.2 Anwendungsgebiete unter Angabe der Zieltierart(en):
Zur Vorbeugung und Behandlung des Flohbefalls bei Katzen unter 4 kg Körpergewicht.
Zur Behandlung des Flohbefalls bei Zierkaninchen unter 4 kg Körpergewicht.
Die am Tier befindlichen Flöhe werden innerhalb eines Tages nach Behandlung abgetötet. Die einmalige Behandlung wirkt 3 bis 4 Wochen lang gegen Flöhe bei Katzen und bis zu einer Woche bei Zierkaninchen. Das Tierarzneimittel kann als Teil eines Behandlungsplans zur Kontrolle der Flohallergiedermatitis (FAD) verwendet werden, sofern diese zuvor durch einen Tierarzt diagnostiziert wurde.
4.3 Gegenanzeigen:
Nicht anwenden bei unter 8 Wochen alten Saugwelpen.
Nicht anwenden bei Kaninchen, die für den menschlichen Verzehr vorgesehen sind.
Nicht anwenden bei Zierkaninchen, die jünger als 10 Wochen alt sind.
Nicht anwenden bei bekannter Überempfindlichkeit gegenüber dem Wirkstoff oder einem der sonstigen Bestandteile.
4.4 Besondere Warnhinweise für jede Zieltierart:
Reinfestationen bedingt durch die Entwicklung von neuen Flöhen in der Umgebung des Tieres können für mindestens 6 Wochen nach Behandlungsbeginn andauern. Um auch diese Flöhe zu erfassen, können je nach der Stärke des Flohbefalls in der Umgebung mehr als eine Behandlung notwendig sein. Zur Unterstützung der Therapie wird empfohlen, auch das Lager der Tiere und die direkte Umgebung mit einem geeigneten Mittel gegen adulte Flöhe und deren Entwicklungsstadien zu behandeln. Um einen Neubefall aus der Umgebung zu reduzieren, wird empfohlen, alle Hunde, Katzen und Kaninchen in einem Haushalt zu behandeln. Die Behandlung von säugenden Katzen und Häsinnen kontrolliert zugleich den Flohbefall des Muttertieres und der Nachkommen.
Nasswerden des Tieres, z.B. nach heftigem Regen, beeinträchtigt die Wirksamkeit des Tierarzneimittels nicht. Allerdings kann in Abhängigkeit des Flohbefalls in der Umgebung eine Wiederholung der Behandlung notwendig werden. In solchen Fällen nicht häufiger als in wöchentlichen Abständen behandeln.
4.5 Besondere Vorsichtsmaßnahmen für die Anwendung:
Besondere Vorsichtsmaßnahmen für die Anwendung bei Tieren:
Das Tierarzneimittel ist zur äußerlichen Anwendung vorgesehen und darf dem Tier nicht eingegeben werden. Nur auf gesunde Hautpartien auftragen. Der Inhalt der Pipette darf nicht mit den Augen oder Schleimhäuten des Tieres in Berührung kommen.
Der Tierhalter soll darauf achten, dass sich frisch behandelte Tiere nicht gegenseitig an der Auftragsstelle lecken.
Besondere Vorsichtsmaßnahmen für den Anwender:
Nach der Anwendung Hände sorgfältig waschen. Auftretende Arzneimittelreste auf der Haut des Anwenders mit Wasser und Seife entfernen.
Personen mit empfindlicher Haut können bei Hautkontakt besonders empfindlich auf das Tierarzneimittel reagieren.
Augen- und Schleimhautkontakt vermeiden. Bei unbeabsichtigtem Augenkontakt sorgfältig mit Wasser ausspülen. Bei fortdauernder Haut- oder Augenreizung oder bei unbeabsichtigtem Verschlucken der Lösung ist ein Arzt zu konsultieren.
Während der Anwendung nicht essen, trinken oder rauchen.
4.6 Nebenwirkungen (Häufigkeit und Schwere):
Das Tierarzneimittel schmeckt bitter. Daher kann das Ablecken der Applikationsstelle unmittelbar nach dem Auftragen der Lösung Speicheln verursachen. Dies ist kein Anzeichen einer Vergiftung und klingt nach einigen Minuten ohne weitere Behandlung wieder ab (siehe auch Abschnitt 4.9, Art und Dauer der Anwendung).
In sehr seltenen Fällen können bei Katzen und Kaninchen Hautreaktionen wie vorübergehender Haarausfall, Rötung, Juckreiz und/oder eine entzündliche Reaktion an der Applikationsstelle auftreten. Bei Katzen wurde in Ausnahmefällen auch über Anzeichen von Unruhe, übermäßiges Speicheln und nervöse Symptome wie Koordinationsstörungen, Zittern und Abgeschlagenheit berichtet.
Das Auftreten von Nebenwirkungen nach Anwendung von Advantage 40 mg sollte dem Bundesamt für Verbraucherschutz und Lebensmittelsicherheit, Mauerstr. 39 - 42, 10117 Berlin oder dem pharmazeutischen Unternehmer mitgeteilt werden.
Meldebögen können kostenlos unter o.g. Adresse oder per E-Mail (uaw@bvl.bund.de) angefordert werden. Für Tierärzte besteht die Möglichkeit der elektronischen Meldung (Online-Formular auf der I nternetseite http://vet-uaw. de).
4.7 Anwendung während der Trächtigkeit, Laktation oder der Legeperiode:
Studien mit dem Wirkstoff Imidacloprid an Ratten und Kaninchen ergaben keine Anzeichen primär embryotoxischer, teratogener oder reproduktionstoxischer Wirkungen. Studien an trächtigen und laktierenden Katzen und ihren Welpen sind begrenzt. Bisherige Beobachtungen lassen jedoch keine Unverträglichkeiten bei diesen Tieren erwarten.
4.8 Wechselwirkungen mit anderen Arzneimitteln und andere Wechselwirkungen:
Es wurden keine Anzeichen einer klinischer Unverträglichkeit nach gleichzeitiger Gabe von Advantage in der doppelten therapeutischen Dosierung mit folgenden in der Veterinärmedizin gebräuchlichen Arzneistoffen beobachtet: Lufenuron, Pyrantel und Praziquantel (Katzen). Die Verträglichkeit von Advantage mit einer Reihe von weiteren Routinetherapien einschließlich Impfungen konnte unter Feldbedingungen ebenfalls gezeigt werden.
4.9 Dosierung und Art der Anwendung:
Dosierung und Behandlungsschema
|
Katze/ Kaninchen (kg KGW) |
Arzneimittel |
Anzahl Pipetten |
Imidacloprid (mg/kg KGW) |
|
< 4 kg |
Advantage 40 mg für kleine Katzen und kleine Zierkaninchen |
1 x 0,4 ml |
mindestens 10 |
Art der Anwendung
Eine Pipette aus der Packung entnehmen. Die Pipette dabei senkrecht nach oben halten, die Verschlusskappe drehen und abziehen. Die umgedrehte Verschlusskappe zum Entfernen der Pipettendichtung benutzen.
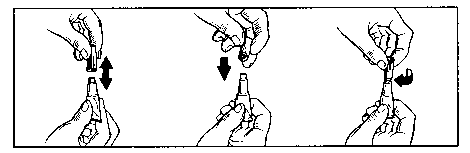
Anwendung bei der Katze
Das Fell des Tieres am Hinterkopf (im Nacken) scheiteln, so dass die Haut sichtbar wird. Setzen Sie die Pipettenspitze auf die Haut und drücken Sie die
Pipette mehrmals, um den Inhalt direkt auf der Haut zu entleeren. Die Pipette dabei senkrecht nach unten halten.

Anwendung beim Kaninchen
Das Fell des Tieres am Hinterkopf (im Nacken) scheiteln, so dass die Haut sichtbar wird. Setzen Sie die Pipettenspitze auf die Haut und drücken Sie die Pipette mehrmals, um den Inhalt direkt auf der Haut zu entleeren. Die Pipette dabei senkrecht nach unten halten.

Alle Tierarten:
Das Tierarzneimittel schmeckt bitter. Daher kann das Ablecken der Applikationsstelle unmittelbar nach dem Auftragen Speicheln verursachen. Dies ist kein Anzeichen einer Vergiftung und klingt nach einigen Minuten ohne Behandlung wieder ab. Korrektes Auftragen der Lösung direkt auf die Haut im Nacken kann das Ablecken der Auftragsstelle durch die Katze verhindern.
Advantage sollte nur auf gesunde Hautpartien aufgetragen werden. Der Tierhalter sollte darauf achten, dass sich frisch behandelte Tiere nicht gegenseitig an der Auftragsstelle lecken.
4.10 Überdosierung (Symptome, Notfallmaßnahmen und Gegenmittel), falls erforderlich:
Bei Katzen verursachte die wöchentliche Behandlung mit der 5-fachen therapeutischen Dosis über 8 Wochen keine Symptome klinischer Unverträglichkeit.
Bei Kaninchen verursachte die wöchentliche Behandlung mit bis zu 45 mg/kg Körpergewicht (das 4-fache der therapeutischen Dosis) über 4 Wochen keine Symptome klinischer Unverträglichkeit.
In seltenen Fällen kann es bei Katzen nach Überdosierung oder Ablecken der Applikationsstelle zu nervösen Beschwerden (Zuckungen, Zittern, Ataxie, Mydriasis, Miosis, Lethargie) kommen.
Eine Vergiftung nach unbeabsichtigter oraler Aufnahme des Arzneimittels beim Tier ist unwahrscheinlich. In diesem Fall sollte eine symptomatische
Therapie unter tierärztlicher Aufsicht erfolgen. Ein spezifisches Antidot ist nicht bekannt, jedoch kann die Verabreichung von Aktivkohle günstig sein.
4.11 Wartezeit(en):
Nicht bei Kaninchen anwenden, die für den menschlichen Verzehr vorgesehen sind.
5. Pharmakologische Eigenschaften
Pharmakotherapeutische Gruppe: Antiparasitikum ATCvet Code: QP53AX17
5.1 Pharmakodynamische Eigenschaften:
Imidacloprid [1-(6-Chloro-3-pyridylmethyl)-N-nitro-imidazolidin-2-ylidenamin] ist ein ektoparasitizider Wirkstoff und gehört zur Klasse der Chloronicotinyle. Chemisch gesehen handelt es sich bei Imidacloprid um ein Chloronicotinylnitroguanidin.
Die Substanz besitzt eine hohe Affinität für die nicotinergen Acetylcholinrezeptoren in der postsynaptischen Membran des Zentralnervensystems (ZNS) von Insekten. Aus der daraus resultierenden Inhibierung der cholinergen Signalübertragung mit nachfolgender Paralyse ergibt sich das insektizide Wirkprinzip. Da Imidacloprid einerseits nur schwache Wechselwirkungen mit nicotinergen Rezeptoren in Säugern zeigt, andererseits für die Substanz nur eine geringe Fähigkeit zur Penetration der Blut-Hirn-Schranke postuliert wird, beeinflusst Imidacloprid die Aktivität des ZNS in Säugern praktisch nicht. Die geringe Beeinflussung des Säugerorganismus durch Imidacloprid konnte auch in sicherheitspharmakologischen Studien gezeigt werden, in denen Kaninchen, Mäusen und Ratten sublethale Dosen systemisch verabreicht wurden.
Weitere Studien haben gezeigt, dass Imidacloprid neben seiner adultiziden Wirkung gegen Flöhe auch gegen Flohlarven in der Umgebung des behandelten Tieres wirkt. Flohlarven in der Umgebung des Tieres werden abgetötet, wenn sie mit einem behandelten Tier in Kontakt kommen.
5.2 Angaben zur Pharmakokinetik:
Advantage ist zur dermalen Anwendung vorgesehen. Bei Katzen verteilt sich die Lösung nach Anwendung auf der Haut rasch über die Körperoberfläche des Tieres. Studien zur akuten dermalen Toxizität in der Ratte sowie Verträglichkeitsstudien mit Überdosierung und Serumkinetikstudien an der Katze haben gezeigt, dass die systemische Resorption sehr gering, vorübergehend und für die klinische Wirksamkeit unbedeutend ist. Dies konnte weiterhin durch eine Studie bestätigt werden, in der Flöhe nach der Aufnahme von Blut von vorher behandelten Tieren nicht abgetötet wurden, sobald Haut und Fell der Tiere gründlich vom Wirkstoff gereinigt worden waren.
Pharmazeutische Angaben
6.
6.1 Verzeichnis der sonstigen Bestandteile:
Butylhydroxytoluol (E 321)
Benzylalkohol 4-Methyl-1,3-dioxolan-2-on
6.2 Inkompatibilitäten:
Keine bekannt.
6.3 Dauer der Haltbarkeit:
Haltbarkeit des Tierarzneimittels im unversehrten Behältnis: 5 Jahre
6.4 Besondere Lagerungshinweise:
Für dieses Tierarzneimittel sind keine besonderen Lagerungsbedingungen erforderlich.
Die Durchdrückpackung in der Faltschachtel aufbewahren.
6.5 Art und Beschaffenheit des Behältnisses:
Packungsgröße: 0,4 ml Lösung pro Pipette
Durchdrückpackung mit 2, 3, 4 oder 6 EinzeldosisPipetten
Behältnis: Pipetten aus weißem Polypropylen mit Kappen
Es werden möglicherweise nicht alle Packungsgrössen in den Verkehr gebracht.
6.6 Besondere Vorsichtsmaßnahmen für die Entsorgung nicht verwendeter
Tierarzneimittel oder bei der Anwendung entstehender Abfälle:
Nicht aufgebrauchte Tierarzneimittel sind vorzugsweise bei Schadstoffsammelstellen abzugeben. Bei gemeinsamer Entsorgung mit dem Hausmüll ist sicherzustellen, dass kein missbräuchlicher Zugriff auf diese Abfälle erfolgen kann. Tierarzneimittel dürfen nicht mit dem Abwasser bzw. über die Kanalisation entsorgt werden.
7. Zulassungsinhaber:
Bayer Vital GmbH Geschäftsbereich Tiergesundheit 51368 Leverkusen
8. Zulassungsnummer:
401516.00.00
9. Datum der Erteilung der Erstzulassung / Verlängerung der Zulassung:
10. Stand der Information
Verbot des Verkaufs, der Abgabe und/oder der Anwendung
Nicht zutreffend.
12.
Verschreibungsstatus / Apothekenpflicht
Apothekenpflichtig.