Afonilum Bio-R
((Wortlaut der für die Fachinformation vorgesehenen Angaben))
Fachinformation
1. Bezeichnung der Arzneimittel
Afonilum® retard forte, 375 mg Hartkapseln, retardiert Afonilum® Bio-R, 250 mg/375 mg Hartkapseln, retardiert
2. Qualitative und quantitative Zusammensetzung
Wirkstoff: Theophyllin
1 Hartkapsel, retardiert Afonilum® retard forte enthält 375 mg Theophyllin.
Afonilum® Bio-R besteht aus einer jeweils gleichen Anzahl grüner und blauer Hartkapseln, retardiert:
1 Hartkapsel, retardiert Afonilum® Bio-R (grün) enthält 250 mg Theophyllin (für den Tag).
1 Hartkapsel, retardiert Afonilum® Bio-R (blau) enthält 375 mg Theophyllin (für die Nacht).
Vollständige Auflistung der sonstigen Bestandteile, siehe Abschnitt 6.1.
3. Darreichungsform
Hartkapsel, retardiert (Retardkapsel)
4. Klinische Angaben
4.1 Anwendungsgebiete
Bronchospasmolytikum/Antiasthmatikum
Behandlung und Verhütung von Atemnotzuständen aufgrund von Einengung der Atemwege (Bronchokonstriktion) bei Patienten mit persistierendem Asthma bronchiale oder mittel- bis schwergradiger obstruktiver Atemwegserkrankung (z. B. chronische Bronchitis und Lungenemphysem).
Hinweis: Es wird empfohlen, die Dauertherapie dieser Erkrankungen mit Theophyllin in Kombination mit anderen, die Bronchien erweiternden und entzündungshemmenden Arzneimitteln, wie z. B. lang wirksamen Beta-Sympathomimetika und Glukocortikoiden durchzuführen.
Arzneimittel mit verzögerter Theophyllinfreisetzung, wie Afonilum retard mite, Afonilum retard, Afonilum retard forte und Afonilum Bio-R, sind nicht zur Akutbehandlung des Status asthmaticus oder der akuten Bronchospastik bestimmt.
Afonilum sollte nicht als Mittel der ersten Wahl zur Behandlung von Asthma bei Kindern angewendet werden.
4.2 Dosierung und Art der Anwendung Dosierung:
Afonilum ist individuell nach Wirkung und Verträglichkeit zu dosieren. Die Dosierung sollte möglichst anhand der Theophyllin-Serumkonzentration ermittelt werden (anzustrebender Bereich: 8 - 20 gg/ml). Kontrollen des Theophyllin-Serumspiegels sind insbesondere auch bei mangelhafter Wirksamkeit oder dem Auftreten unerwünschter Wirkungen angezeigt.
Zur Bestimmung der Initialdosis ist eine eventuelle Vormedikation mit Theophyllin oder seinen Verbindungen hinsichtlich einer Dosisverminderung zu berücksichtigen.
Für die Ermittlung der Dosis ist das Normalgewicht als Körpergewicht einzusetzen, da Theophyllin nicht vom Fettgewebe aufgenommen wird.
Für Erwachsene beträgt die tägliche Erhaltungsdosis von Theophyllin ca. 11 bis 13 mg je kg Körpergewicht.
Raucher benötigen im Vergleich zu nichtrauchenden Erwachsenen eine höhere körpergewichtsbezogene Theophyllin-Dosis, da die Eliminationsrate erhöht ist. Bei Rauchern, die das Rauchen einstellen, sollte wegen des Anstiegs des Theophyllin-Spiegels vorsichtig dosiert werden.
Bei Patienten mit Herzinsuffizienz, schwerem Sauerstoffmangel, chronisch obstruktiver Lungenerkrankung, Lungenentzündung, akutem Lungenödem, Virusinfektionen (insbesondere Influenza), bei anhaltendem Fieber, im höheren Lebensalter sowie bei der Behandlung mit bestimmten anderen Medikamenten (siehe unter 4.5 „Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen") und nach erhöhtem Alkoholgenuss ist die TheophyllinAusscheidung sehr häufig verlangsamt. Weiterhin ist über eine reduzierte TheophyllinAusscheidung nach Influenza- und BCG-Impfung berichtet worden, so dass bei gleichzeitiger Behandlung ebenfalls eine Dosisminderung erforderlich sein könnte.
• Patienten mit Leber- und/oder Nierenfunktionsstörungen
Bei Patienten mit eingeschränkter Leberfunktion ist die Theophyllin-Ausscheidung sehr häufig verlangsamt.
Bei höhergradigen Nierenfunktionsstörungen kann es zu einer Anhäufung (Kumulation) von Theophyllinmetaboliten kommen.
Solche Patienten benötigen daher geringere Dosen, und Steigerungen müssen mit besonderer Vorsicht erfolgen.
• Kinder
Afonilum retard forte/Bio-R sollte bei Kindern unter 12 Jahren nicht angewendet werden. Es stehen andere Dosisstärken und Darreichungsformen zur Verfügung, die bei Kindern unter 12 Jahren besser geeignet sind.
Kinder benötigen im Vergleich zu nichtrauchenden Erwachsenen eine höhere körpergewichtsbezogene Theophyllin-Dosis, da bei dieser Patientengruppe die Eliminationsrate höher ist.
Afonilum darf bei Kindern unter 6 Monaten nicht angewendet werden (siehe Abschnitt 4.3).
• Ältere Patienten
Bei älteren Patienten (ab 60. Lebensjahr) ist die Theophyllin-Ausscheidung verlangsamt.
Die Anwendung von Afonilum bei alten, polymorbiden, schwerkranken und/oder intensivmedizinisch therapierten Patienten ist mit einem erhöhten Intoxikationsrisiko verbunden und soll daher durch therapeutisches Drug-Monitoring (TDM) kontrolliert werden (siehe auch 4.4 „Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung“).
Empfohlenes Dosierungsschema:
Soweit nicht anders verordnet, sind je nach Lebensalter folgende Erhaltungs-Dosierungen zu empfehlen:
|
Alter in Jahren |
Körpergewicht in kg* |
tägliche Dosis in mg Theophyllin je kg Körpergewicht* |
tägliche Dosis in mg Theophyllin |
tägliche Anzahl der Retardkapseln |
|
Jugendliche, 12 - 16 Jahre |
40 - 60 |
18 |
720 - 1080 |
siehe Dosierungs beispiele unten |
|
Erwachsene und Jugendliche ab 16 Jahren (Nichtraucher) |
60 - 70 |
11 - 13 |
660/780 - 770/910 |
siehe Dosierungsbeispiele unten |
|
Raucher |
60 - 70 |
18 |
1080 - 1260 |
nach Anweisung des Arztes |
*Bei adipösen Patienten ist hier das Normalgewicht einzusetzen.
Die Tagesdosis soll auf eine morgendliche und eine abendliche Dosis verteilt werden. Dosierungsbeispiele
Jugendliche 12 - 16 Jahre (40 - 60 kg KG), Tagesbedarf ca. 18 mg/kg KG:
2 Hartkapseln, retardiert Afonilum Bio-R pro Tag (1 grüne Retardkapsel morgens, 1 blaue
Retardkapsel abends)
oder
2-mal täglich 1 Hartkapsel, retardiert Afonilum retard forte (entsprechend 2 Retardkapseln pro Tag).
Jugendliche ab 16 Jahren und Erwachsene (60 - 70 kg KG), Nichtraucher, Tagesbedarf ca. 11 -13 mg/kg KG:
2 Hartkapseln, retardiert Afonilum Bio-R pro Tag (1 grüne Retardkapsel morgens, 1 blaue
Retardkapsel abends)
oder
2-mal täglich 1 Hartkapsel, retardiert Afonilum retard forte (entsprechend 2 Retardkapseln pro Tag).
Afonilum Bio-R ist für die Erhaltungstherapie bei Patienten bestimmt, die einen nachgewiesenen Tagesbedarf von 625 mg Theophyllin haben.
Afonilum retard forte ist für die Erhaltungstherapie bei Patienten bestimmt, die einen nachgewiesenen Tagesbedarf um 750 mg Theophyllin haben.
Wird von einem nicht retardierten auf ein retardiertes Theophyllin-Präparat gewechselt, so ist zu beachten, dass die angegebene Tagesdosis eventuell reduziert werden kann. Bei der Umstellung von einem retardierten Theophyllinpräparat auf ein anderes, z. B. von einem anderen Hersteller, sollte der Theophyllinserumspiegel (Theophyllinmenge im Blut) kontrolliert werden, da sich die Präparate in ihrer Bioverfügbarkeit unterscheiden können. Dies ist ebenfalls bei der Verabreichung von hohen Dosen empfehlenswert.
Sollte es zu unerwünschten Reaktionen oder Überdosierungserscheinungen kommen, so sollte je nach Schweregrad die nächste Dosis ausgelassen oder um 50 % vermindert werden. Eine notwendige Dosiskorrektur sollte möglichst anhand des Theophyllin-Spiegels im Serum (TDM) ermittelt werden.
Art der Anwendung
Afonilum soll nach den Mahlzeiten unzerkaut mit reichlich Flüssigkeit eingenommen werden.
Die Behandlung sollte möglichst am Abend kurz vor dem Schlafengehen beginnen und langsam über 2 - 3 Tage gesteigert werden.
Die Einzeldosen sollen in gleichmäßigen Abständen über 24 Stunden verteilt eingenommen werden, bei 2-mal täglicher Gabe üblicherweise morgens und abends.
Afonilum Bio-R eignet sich für Patienten, die eine ausgeprägte tageszeitliche Schwankung ihrer Atemnotbeschwerden mit Schwerpunkt in den frühen Morgenstunden aufweisen.
Afonilum Bio-R enthält grüne Hartkapseln, retardiert mit einer Tagesdosierung von 250 mg Theophyllin und blaue Hartkapseln, retardiert mit einer Nachtdosierung von 375 mg Theophyllin. Soweit vom Arzt nicht anders verordnet, sollen die Patienten 1 grüne Hartkapsel, retardiert für den Tag nach dem Frühstück und 1 blaue Hartkapsel, retardiert für die Nacht vor dem Schlafengehen unzerkaut mit reichlich Flüssigkeit einnehmen.
Im Bedarfsfall können die Steckkapseln durch gleichzeitiges Drehen und Ziehen geöffnet und der Inhalt unzerkaut mit reichlich Flüssigkeit eingenommen werden, ohne dass das Retardprinzip beeinträchtigt wird.
Die Dauer der Anwendung richtet sich nach Art, Schwere und Verlauf der Erkrankung und wird vom behandelnden Arzt bestimmt.
4.3 Gegenanzeigen
Afonilum darf nicht angewendet werden bei:
- bekannter Überempfindlichkeit gegen Theophyllin oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile von Afonilum,
- frischem Herzinfarkt,
- akuten tachykarden Arrhythmien
- Kindern unter 6 Monaten (siehe auch Abschnitt 4.2).
4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung
Afonilum sollte nur bei strengster Indikation und mit Vorsicht angewendet werden bei:
- instabiler Angina pectoris,
- Patienten mit Neigung zu tachykarden Arrhythmien,
- schwerem Bluthochdruck,
- hypertropher obstruktiver Kardiomyopathie,
- Hyperthyreose,
- epileptischem Anfallsleiden in der Vorgeschichte,
- Magen- und/oder Zwölffingerdarmgeschwür,
- Porphyrie,
- schweren Leber- oder Nierenfunktionsstörungen.
Die Anwendung von Afonilum bei alten, polymorbiden, schwerkranken und/oder intensivmedizinisch therapierten Patienten ist mit einem erhöhten Intoxikationsrisiko verbunden und soll daher durch therapeutisches Drug-Monitoring (TDM) kontrolliert werden (siehe auch 4.2 "Dosierung und Art der Anwendung").
Bei Patienten, die eine Elektrokrampftherapie erhalten, ist besondere Vorsicht geboten, da Theophyllin die Anfälle verlängern kann. Das Auftreten eines Status epilepticus ist möglich.
Sollte die empfohlene Dosierung keine ausreichende Wirkung zeigen und falls Nebenwirkungen auftreten, sollte die Serumkonzentration von Theophyllin überwacht werden.
Akute fiebrige Erkrankungen:
Fieber vermindert die Clearance von Theophyllin. Um Intoxikationen zu vermeiden, kann eine Reduzierung der Dosis notwendig sein.
Aufgrund des hohen Wirkstoffgehaltes sind Afonilum Bio-R und Afonilum retard forte für Kinder unter 12 Jahren nicht geeignet.
4.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen
Theophyllin wird in der Leber u. a. über das Enzym CYP1A2 metabolisiert. Die gleichzeitige Anwendung von Arzneimitteln, die dieses Enzym beeinflussen, kann zu Änderungen des Theophyllin-Abbaus führen.
Theophyllin wirkt synergistisch (gleichgerichtet verstärkend) mit anderen xanthinhaltigen Medikamenten, Betasympathomimetika, Coffein und ähnlichen Stoffen.
Ein beschleunigter Theophyllin-Abbau und/oder eine verminderte Bioverfügbarkeit sowie eine verminderte Wirksamkeit finden sich
- bei Rauchern
- bei gleichzeitiger Behandlung mit Barbituraten (besonders Phenobarbital oder Pentobarbital), Carbamazepin, Phenytoin, Rifampicin, Primidon, Sulfinpyrazon, Ritonavir, Johanniskraut (Hypericum perforatum) und Aminoglutethimid.
Bei gleichzeitiger Behandlung mit einem dieser Arzneimittel sollte der Theophyllin-Spiegel kontrolliert und gegebenenfalls eine Dosisanpassung durchgeführt werden. Dies gilt auch nach dem Absetzen eines dieser Medikamente.
Verzögerter Abbau und/oder Erhöhung des Theophyllin-Blutspiegels mit einer erhöhten Überdosierungsgefahr und vermehrtem Nebenwirkungsrisiko können bei gleichzeitiger Behandlung mit folgenden Arzneimitteln auftreten:
oralen Kontrazeptiva („Pille“) aufgrund des Östrogenanteils, Makrolid-Antibiotika (z. B. Erythromycin, Clarithromycin, Josamycin, Spiramycin, Troleandomycin), Imipenem, Chinolone (Gyrase-Hemmstoffe, s. u.), Isonikotinsäurehydrazid, Tiabendazol, Calcium-Antagonisten (z. B. Verapamil, Diltiazem), Propranolol, Propafenon, Mexiletin, Ticlopidin, Cimetidin, Allopurinol, alphaInterferon, Rofecoxib, Pentoxifyllin, Fluvoxamin, Viloxazin, Disulfiram, Zileuton, Phenylpropanolamin, Influenza- und BCG-Vakzinen. Außerdem ist eine Wirkungsverstärkung von Theophyllin durch Alkohol, Methotrexat oder Tacrin möglich. Hierbei kann eine Dosisverminderung von Theophyllin angezeigt sein.
Einzelnen Berichten zufolge sind auch bei gleichzeitiger Behandlung mit Ranitidin, Aciclovir oder Zafirlukast Überdosierungserscheinungen von Theophyllin beobachtet worden. Da eine Wechselwirkung nicht hinreichend sicher ausgeschlossen werden kann, sollte bei gleichzeitiger Behandlung die individuell erforderliche Theophyllin-Dosis daher besonders sorgfältig ermittelt werden.
Bei paralleler Behandlung mit Ciprofloxacin ist die Theophyllin-Dosis auf maximal 60 %, bei Anwendung von Enoxacin auf maximal 30 % und bei Anwendung von Grepafloxacin oder Clinafloxacin auf 50 % der empfohlenen Dosis zu reduzieren. Auch andere Chinolone (z. B. Pefloxacin, Pipemidsäure) können die Wirkung von Theophyllin-Arzneimitteln verstärken. Es wird daher dringend empfohlen, bei gleichzeitiger Behandlung mit Chinolonen therapiebegleitende engmaschige Theophyllin-Konzentrationsbestimmungen durchzuführen.
Bei gleichzeitiger Behandlung mit Isoniazid kann der Theophyllin-Spiegel steigen oder auch abfallen. Theophyllinspiegelkontrollen sind angezeigt.
Die Wirkung von Lithiumcarbonat, Beta-Rezeptorenblockern, Adenosin und Benzodiazepinen kann durch gleichzeitige Gabe von Afonilum abgeschwächt werden.
Bei gleichzeitiger Gabe von Theophyllin und Diazepam können höhere Diazepamdosen erforderlich sein, um den gewünschten Beruhigungseffekt zu erzielen. Der Abbruch der Behandlung mit Theophyllin kann zu Atemdepression führen, wenn nicht parallel die Diazepamdosis gesenkt wird.
Theophyllin verstärkt die harntreibende Wirkung von Diuretika.
Eine Verminderung der Theophyllin-Wirkung ist bei gleichzeitiger Gabe von Digoxin, Isoproterenol (i.v.) oder Moricizin möglich.
Bei gleichzeitiger Gabe von Theophyllin und Formoterol sind Eosinopenie und Hypokaliämie möglich.
Es liegen Hinweise vor, dass eine Senkung der Krampfschwelle des Gehirns bei gleichzeitiger Gabe von bestimmten Fluorochinolonen oder Imipenem auftreten kann.
Die Anwendung von Halothan kann bei Patienten, die Afonilum erhalten, zu schweren Herzrhythmusstörungen führen.
Beachten Sie bitte, dass diese Angaben auch für vor Kurzem angewandte Arzneimittel gelten können.
Aufgrund der vielfältigen Wechselwirkungen von Theophyllin sind Serumspiegelkontrollen bei längerfristiger Einnahme von Afonilum mit anderen Medikamenten allgemein ratsam.
4.6 Fertilität, Schwangerschaft und Stillzeit
Schwangerschaft
Zu einer Anwendung von Theophyllin während des ersten Schwangerschaftstrimenons liegen bislang keine ausreichenden Erfahrungen vor, daher sollte eine Anwendung von Afonilum in dieser Zeit vermieden werden.
Während des zweiten und dritten Trimenons sollte Theophyllin nur nach strenger Nutzen-Risiko-Abwägung angewendet werden, da es die Plazenta passiert und im Feten sympathomimetisch wirken kann.
Mit zunehmender Dauer der Schwangerschaft können die Plasmaproteinbindung sowie die Clearance von Theophyllin abnehmen, so dass eine Dosisreduzierung zur Vermeidung unerwünschter Wirkungen notwendig werden kann.
Wird eine Patientin am Ende der Schwangerschaft mit Theophyllin behandelt, kann es zur Wehenhemmung kommen. Pränatal exponierte Neugeborene müssen sorgfältig auf Theophyllin-Wirkungen überwacht werden.
Stillzeit
Theophyllin geht in die Muttermilch über, es können therapeutische Serumkonzentrationen beim Kind erreicht werden. Aus diesem Grund ist die therapeutische Theophyllin-Dosis bei einer stillenden Patientin so niedrig wie möglich zu halten. Das Stillen sollte möglichst unmittelbar vor der Gabe des Arzneimittels erfolgen. Das gestillte Kind muss sorgfältig auf ein mögliches Auftreten von Theophyllin-Wirkungen hin überwacht werden. Sollten höhere therapeutische Dosen notwendig sein, muss abgestillt werden.
Fertilität
Es liegen keine klinischen Daten zum Einfluss von Theophyllin auf die Fertilität in Menschen vor. In tierexperimentellen Studien zeigte Theophyllin negative Auswirkungen auf die weibliche und männliche Fertilität (s. Abschnitt 5.3).
4.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen
Diese Arzneimittel können auch bei bestimmungsgemäßem Gebrauch das Reaktionsvermögen so weit verändern, dass die Fähigkeit zur aktiven Teilnahme am Straßenverkehr, zum Bedienen von Maschinen oder zum Arbeiten in größerer Höhe oder ohne sicheren Halt beeinträchtigt wird. Dies gilt in verstärktem Maße im Zusammenwirken mit Alkohol oder Medikamenten, die ihrerseits das Reaktionsvermögen beeinträchtigen können.
4.8 Nebenwirkungen
Stoffwechsel, Elektrolyte
Störung des Elektrolytgleichgewichts, Hypokaliämie, Anstieg von Serum-Calcium und -Kreatinin sowie Hyperglykämie und Hyperurikämie, Störungen des Säure-BasenHaushalts.
Immunsystem
Überempfindlichkeit gegenüber Theophyllin (u. a. Hautausschlag, Juckreiz, Urticaria, Bronchospasmen) einschließlich anaphylaktischer Reaktionen.
Nervensystem
Kopfschmerzen, Erregungszustände, Tremor, Unruhe, Schlaflosigkeit, Krampfanfälle, Schwindel.
Psychiatrische Erkrankungen
Beunruhigung, Ruhelosigkeit, Reizbarkeit, Nervosität.
Herz-Kreislauf-System
Beschleunigter oder unregelmäßiger Herzschlag, Rhythmusstörungen, ventrikuläre Arrhythmien, Tachykardie, Sinustachykardie, supraventrikuläre Tachykardie, Vorhoftachykardie und Vorhofflattern, ventrikuläre Extrasystolen, Vorhofflimmern- und flattern, Palpitationen, Blutdruckabfall.
Gefäßerkrankungen
Hypotonie, Schock.
Magen-Darm-Trakt
Magen-Darm-Beschwerden, einschließlich Blutung, Übelkeit, Erbrechen, Durchfall.
Stimulation der Magensäuresekretion, Bauchschmerzen, Bluterbrechen.
Infolge der Tonusverminderung im unteren Ösophagussphinkter kann ein bestehender gastroösophagealer Reflux in der Nacht verstärkt werden, mögliche AsthmaProvokationen durch Aspiration können auftreten.
Erkrankungen der Atemwege, des Brustraums und des Mediastinums Tachypnoe.
Skelettmuskulatur-, Bindegewebs- und Knochenerkrankungen Rhabdomyolyse.
Urogenitaltrakt
Akutes Nierenversagen, verstärkte Diurese.
Ausgeprägtere Nebenwirkungen können bei individueller Überempfindlichkeit oder einer Überdosierung (Theophyllin-Serumspiegel über 20 gg/ml) auftreten (siehe 4.9).
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung dem
Bundesinstitut für Arzneimittel und Medizinprodukte
Abt. Pharmakovigilanz
Kurt-Georg-Kiesinger Allee 3
D-53175 Bonn
Website: www.bfarm.de
anzuzeigen.
4.9 Überdosierung
a) Symptome der Intoxikation
Bei therapeutischen Theophyllin-Serumspiegeln bis 20 gg/ml sind die bekannten Nebenwirkungen wie Magen-Darm-Beschwerden (Übelkeit, Magenschmerzen, Erbrechen, Diarrhö), zentralnervöse Erregbarkeit (Unruhegefühl, Kopfschmerzen, Schlaflosigkeit, Schwindel) und kardiale Störungen (Rhythmusstörungen) - je nach individueller Empfindlichkeit - ausgeprägt.
Bei Theophyllin-Serumspiegeln zwischen 20 und 25 gg/ml finden sich in der Regel die bekannten Theophyllinnebenwirkungen (siehe Abschnitt 4.8) mit gesteigerter Intensität.
Vor allem bei erhöhten Theophyllin-Serumspiegeln von mehr als 25 gg/ml können toxische Wirkungen wie Krampfanfälle, plötzlicher Blutdruckabfall, ventrikuläre Arrhythmien, Herz-
Kreislaufversagen, Rhabdomyolyse und schwere Magen-Darm-Erscheinungen (u. a. gastrointestinale Blutungen) auftreten.
Solche Reaktionen können auch ohne die Vorboten leichterer Nebenwirkungen auftreten. Insbesondere Kinder reagieren empfindlich auf Theophyllinüberdosierungen. Bei einer Vergiftung mit retardierten Theophyllinpräparaten können die Symptome verzögert auftreten.
Bei erhöhter individueller Theophyllin-Empfindlichkeit sind schwerere Überdosierungserscheinungen auch schon unterhalb der genannten Serumkonzentrationen möglich.
b) Therapie bei Intoxikationen
Bei leichten Überdosierungserscheinungen
Das entsprechende Präparat sollte abgesetzt und der Theophyllin-Serumspiegel bestimmt werden. Bei Wiederaufnahme der Behandlung sollte die Dosis entsprechend vermindert werden.
Therapie aller Theophyllinintoxikationen
Bis zu zwei Stunden nach Einnahme kann eine Magenspülung sinnvoll sein. Zur weiteren Giftentfernung sollte wiederholt Aktivkohle, ggf. in Kombination mit einem schnell wirksamen Laxans (z. B. Glaubersalz) verabreicht werden.
Aufgrund der hohen Morbidität und Mortalität Theophyllin-induzierter Anfälle, sollte die Behandlung schnell und aggressiv erfolgen. Außerordentlich effektiv ist die orale Behandlung mit Aktivkohle (0,5 g/kg bis zu 20 g). Die Dosis sollte mindestens einmal 1 bis 2 Stunden nach der
1. Verabreichung wiederholt werden. Sie blockiert auch noch mehrere Stunden nach der Einnahme die Absorption von Theophyllin im Gastrointestinaltrakt. Die einmalige Verabreichung von Sorbitol kann den Stuhlgang fördern, so dass die Ausscheidung des an die Aktivkohle gebundenen Theophyllins erleichtert wird. Emetika fördern zwar das Erbrechen, aber sie vermindern nicht die Theophyllinabsorption, außer diese werden innerhalb von 5 Minuten nach der Einnahme des Theophyllins gegeben. Selbst dann sind Emetika weniger wirksam als Aktivkohle. Elektrokardiographisches Monitoring sollte von Beginn an erfolgen und so lange fortgesetzt werden, bis die Serumtheophyllin-Spiegel wieder im Normbereich liegen. Gleiches gilt für die Kontrolle der Serumelektrolyte und der Glucose. Monitoring und Therapie sollten fortgeführt werden, bis die Serumkonzentration unter 20 gg/ml liegt.
Spezielle Empfehlungen Serumkonzentration > 20 < 30 gg/ml
1. Verabreichung einer Einzeldosis Aktivkohle
2. Überwachung des Patienten auch im Hinblick auf die Serum-Theophyllinkonzentration im Abstand von 2 bis 4 Stunden, um einen Konzentrationsanstieg ausschließen zu können.
Serumkonzentration > 30 < 100 gg/ml
1. Mehrfache Verabreichung von Aktivkohle und Maßnahmen zur Beherrschung des Erbrechens
2. Überwachung des Patienten und alle 2 bis 4 Stunden regelmäßige Kontrolle der
Theophyllinkonzentrationen zur Kontrolle der Therapie und ggf. als Entscheidungsgrundlage für weitere Maßnahmen.
3. Durchführung von z. B. Hämoperfusion, falls Erbrechen, Anfälle oder Arrhythmien nicht adäquat behandelt werden können.
Serumkonzentration > 100 gg/ml
1. Prophylaktische antikonvulsive Therapie sollte in Betracht gezogen werden.
2. Mehrfache Verabreichung von Aktivkohle und Maßnahmen zur Beherrschung des Erbrechens
3. z. B. Hämoperfusion sollte auch dann erwogen werden, wenn der Patient keine Anfälle hat.
4. Überwachung des Patienten und alle 2 bis 4 Stunden regelmäßige Kontrolle der
Theophyllinkonzentrationen zur Kontrolle der Therapie und ggf. als Entscheidungsgrundlage für weitere Maßnahmen.
Weitere Maßnahmen
Bei zentralnervösen Reaktionen (z. B. Unruhe und Krämpfen):
Diazepam i.v., 0,1 - 0,3 mg/kg Körpergewicht (KG), bis zu 15 mg
Bei vitaler Bedrohung:
- Überwachung lebenswichtiger Funktionen
- Freihalten der Atemwege (Intubation)
- Zufuhr von Sauerstoff
- bei Bedarf i.v. Volumensubstitution mit Plasmaexpandern
- Kontrolle und evtl. Korrektur des Wasser- und Elektrolythaushalts
- Hämoperfusion (s. u.)
Bei bedrohlichen Herzrhythmustörungen:
I.v. Gabe von Propranolol bei Nicht-Asthmatikern
(1 mg bei Erwachsenen, 0,02 mg/kg KG bei Kindern), diese Dosis kann alle 5 - 10 Minuten bis zur Rhythmus-Normalisierung oder bis zur Höchstdosis von 0,1 mg/kg wiederholt werden.
Vorsicht:
Propranolol kann bei Asthmatikern schwere Bronchospasmen auslösen. Bei Asthma-Patienten sollte deshalb Verapamil verabreicht werden.
Bei besonders schweren Intoxikationen, die auf die genannten Maßnahmen nicht ausreichend ansprechen, sowie bei sehr hohem Theophyllin-Serumspiegel kann durch Hämoperfusion oder Hämodialyse eine schnelle und vollständige Entgiftung erreicht werden. Im Allgemeinen kann hiervon jedoch abgesehen werden, da Theophyllin ausreichend rasch metabolisiert wird.
Extrakorporale Methoden zur Senkung der Serum-Theophyllinkonzentration Indem die Theophyllinclearance durch extrakorporale Methoden steigt, kann die Serumkonzentration rasch sinken. Hämoperfusion mit Aktivkohle ist dabei die wirksamste Methode, wobei die Theophyllinclearance bis zum 6-fachen ansteigt, allerdings können dabei schwere Komplikationen wie Blutdruckabfall, Hypokalzämie, verminderte Thrombozytenzahl und Blutungsneigung auftreten. Hämodialyse ist dabei vergleichbar wirksam wie die mehrfache Aktivkohlegabe und hat ein geringeres Risiko für schwerwiegende Komplikationen als die Hämoperfusion mit Aktivkohle. Die Serum-Theophyllinkonzentrationen können aufgrund der Rückverteilung von Theophyllin aus dem Gewebe nach Beendigung der Aktivkohlehämoperfusion oder Hämodialyse wieder auf 5 bis 10 gg/ml ansteigen.
Die weitere Behandlung einer Vergiftung mit Afonilum richtet sich nach dem Ausmaß, dem Verlauf sowie den vorliegenden Symptomen.
5. Pharmakologische Eigenschaften
5.1 Pharmakodynamische Eigenschaften
Pharmakotherapeutische Gruppe: Methylxanthine (Purin-Derivate).
ATC-Code: R03DA04.
Das breite pharmakologische Wirkungsspektrum umfasst:
Wirkungen auf das respiratorische System:
- Relaxation der glatten Bronchialmuskulatur und der Pulmonalgefäße,
- Besserung der mukoziliären Clearance,
- Hemmung der Freisetzung von Mediatoren aus Mastzellen und anderen Entzündungszellen,
- Abschwächung der provozierten Bronchokonstriktion,
- Abschwächung der asthmatischen Sofort- und Spätreaktion,
- Verstärkung der Zwerchfellkontraktion.
Extrapulmonale Wirkungen:
- Minderung des Dyspnoeempfindens,
- Gefäßdilatation,
- Relaxation der glatten Muskulatur (z. B. Gallenblase, Gastrointestinaltrakt),
- Inhibierung der Kontraktilität des Uterus,
- positive Ino- und Chronotropie am Herzen,
- Stimulation der Skelettmuskulatur,
- Steigerung der Diurese,
- Stimulation von Sekretions- und Inkretionsorganen (z. B. vermehrte Salzsäure-Sekretion im Magen, verstärkte Freisetzung von Katecholaminen aus der Nebenniere).
Die Wirkungsmechanismen von Theophyllin sind bisher noch nicht vollständig geklärt.
Eine Hemmung der Phosphodiesterase mit einem intrazellulären cAMP-Anstieg spielt möglicherweise nur bei Konzentrationen eine Rolle, die im oberen therapeutisch genutzten Bereich liegen. Andere diskutierte Mechanismen umfassen einen Antagonismus zu Adenosin-Rezeptoren, (Prostaglandin-Antagonismus), Hemmung der Synthese von Entzündungsmediatoren, Induktion von Apoptose sowie eine Translokation von intrazellulärem Kalzium.
5.2 Pharmakokinetische Eigenschaften
Theophyllin wird nach oraler Gabe vollständig resorbiert.
Dabei kann bei Retardformen durch Nahrungsaufnahme sowohl die Resorptionsgeschwindigkeit (Verzögerung oder Beschleunigung, "dose-dumping") als auch die relative Bioverfügbarkeit beeinflusst werden.
Untersuchungen nach Mehrfachgaben (2-mal tägliche Gabe, Dosierungsintervall 12 Stunden) zu Afonilum retard forte (375 mg Theophyllin) nach Nüchterngabe und Einnahme nach einer fettreichen Mahlzeit ergaben keine Hinweise auf Interaktionen zwischen dem Arzneimittel und Nahrung. Die relative postprandiale Bioverfügbarkeit beträgt 102 % im Vergleich zur Nüchterngabe. Die Bioäquivalenz zwischen Nüchterngabe und Einnahme nach dem Essen konnte bestätigt werden.
Da das galenische Retardierungsprinzip für alle Dosisstärken von Afonilum-Retardformulierungen (125 mg, 250 mg, 375 mg) identisch ist, ist die In-vitro-Wirkstofffreisetzung unabhängig von der Dosis.
Die maximale Konzentration im Steady State (Cmax/ss) von Afonilum retard forte wurde im Nüchternzustand mit 9,16 gg/ml (geometrischer Mittelwert) und nach Nahrungsaufnahme mit 9,42 gg/ml (geometrischer Mittelwert) bestimmt.
Die bronchodilatatorische Wirkung von Theophyllin korreliert mit der Serumkonzentration. Ein optimaler therapeutischer Effekt bei kalkulierbarem Nebenwirkungsrisiko wird mit Serumspiegeln von 8 - 20 gg/ml erzielt.
Die Plasmaproteinbindung von Theophyllin beträgt im therapeutischen Konzentrationsbereich etwa 60 % (bei Neugeborenen und Erwachsenen mit Leberzirrhose ca. 40 %). Aus der Blutbahn verteilt sich die Substanz in alle Kompartimente des Körpers mit Ausnahme des Fettgewebes.
Die Elimination von Theophyllin erfolgt durch Biotransformation in der Leber durch das Cytochrom P450-Enzymsystem (u. a. CYP1A2, CYP2E1, CYP3A4) und durch renale Exkretion. Beim Erwachsenen werden etwa 7 - 13 % der Substanz unverändert im Harn ausgeschieden. In der pädiatrischen Population wird Theophyllin überwiegend über die Nieren ausgeschieden.
Beim Neugeborenen werden hingegen ca. 50 % unverändert und erhebliche Teile in Form von Coffein eliminiert.
Wirksame Serumkonzentrationen: 5 - 12 gg/ml (20 gg/ml) sollen nicht überschritten werden).
Die Hauptmetaboliten sind 1,3-Dimethyl-Harnsäure (ca. 40 %), 3-Methyl-Xanthin (ca. 36 %) und 1-Methyl-Harnsäure (ca. 17 %). Davon ist noch das 3-Methyl-Xanthin pharmakologisch aktiv, jedoch schwächer als Theophyllin.
Die hepatische Theophyllin-Metabolisierung schwankt beträchtlich interindividuell, so dass Clearance, Serumkonzentrationen und Eliminationshalbwertszeiten erheblich variieren.
Die wichtigsten Einflussfaktoren auf die Theophyllin-Clearance sind (siehe auch Ziffer 4.2 „Dosierung und Art der Anwendung“):
- Lebensalter,
- Körpergewicht,
- Ernährung,
- Rauchgewohnheiten (bei Rauchern wird Theophyllin bedeutend schneller metabolisiert),
- Einnahme von bestimmten Medikamenten (siehe Ziffer 4.5 "Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen"),
- Erkrankungen und/oder Funktionsstörungen von Herz, Lunge, Leber,
- Virusinfektionen.
Bei Nierenfunktionsstörungen kann es zu einer Kumulation von z. T. pharmakologisch aktiven Theophyllin-Metaboliten kommen. Die Clearance ist außerdem bei körperlicher Belastung und ausgeprägter Hypothyreose vermindert und bei schwerer Psoriasis erhöht.
Die Eliminationsgeschwindigkeit ist zunächst konzentrationsabhängig. Bei Serumkonzentrationen im oberen therapeutischen Bereich tritt ein Sättigungseffekt der Clearance auf, so dass schon geringe Dosiserhöhungen einen überproportionalen Anstieg des Theophyllin-Serumspiegels verursachen.
Auch die Plasmahalbwertszeit von Theophyllin zeigt große Unterschiede. Sie beträgt bei nichtrauchenden, erwachsenen Asthmatikern ohne sonstige Begleiterkrankungen 7 - 9 Stunden, bei Rauchern 4 - 5 Stunden, bei Kindern 3 - 5 Stunden, und sie kann bei Frühgeborenen und Patienten mit Lungenerkrankungen, Herzinsuffizienz oder Lebererkrankungen mehr als 24 Stunden betragen.
Mit zunehmender Dauer der Schwangerschaft kann das Verteilungsvolumen von Theophyllin ansteigen, die Plasmaproteinbindung und die Clearance abnehmen, was eine Dosisreduzierung zur Vermeidung unerwünschter Wirkungen notwendig machen kann.
Theophyllin wird diaplazentar übertragen und geht in die Muttermilch über.
Untersuchungen zeigten einen Milch/Plasma-Quotienten von 0,6 - 0,89, was je nach kindlicher Clearance-Rate und mütterlichem Serumspiegel für eine Akkumulation beim gestillten Säugling ausreichen kann.
Bioverfügbarkeit
Absolute Bioverfügbarkeit
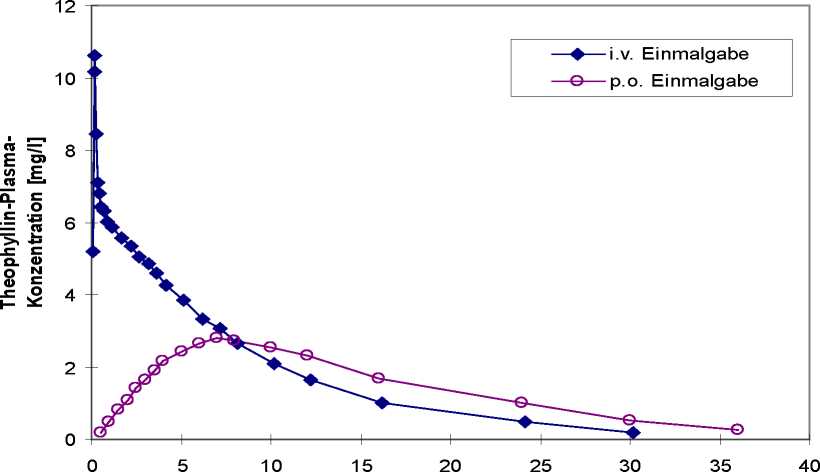
Eine im Jahr 1992 durchgeführte Untersuchung an 20 Probanden ergab nach Einmalgabe von 1 Hartkapsel, retardiert Afonilum retard (250 mg Theophyllin) p.o. im Vergleich zu einer intravenösen Kurzzeitinfusion (10 Minuten) mit Afonilum® novo, Injektionslösung, (250 mg Theophyllin) eine absolute Bioverfügbarkeit von 92,04 % (geometrisches Mittel).
Zeit [h]
Theophyllin-Plasmakonzentrationen [mg/l] nach p.o. Einmalgabe von 1 Hartkapsel, retardiert Afonilum retard (250 mg Theophyllin) im Vergleich zur i.v. Einmalgabe von Afonilum novo, Injektionslösung (250 mg Theophyllin, entspricht 12,5 ml), (geometrische Mittelwerte).
Relative Bioverfügbarkeit (Prüfung auf Nahrungsmitteleinfluss)
Eine im Jahre 1991 durchgeführte Untersuchung an 20 Probanden ergab beim Vergleich der Theophyllinkonzentrations-Zeitverläufe nach Nüchterngabe (Referenz) und Einnahme nach einer fettreichen Mahlzeit (Test) keine Änderung der Bioverfügbarkeit. Hinweise auf eine Arzneimittel-/Nahrungsmittel-Interaktion wurden nicht festgestellt. Die Untersuchungen wurden nach p. o. Mehrfachgabe von Afonilum retard forte (2-mal 375 mg Theophyllin pro Tag, Dosierungsintervall (t = 12 Stunden) im Steady State durchgeführt.
|
Afonilum retard forte (Nahrungsbedingungen) |
Afonilum retard forte (Nüchterngabe) | |
|
Fläche unter der Konzentrati-ons-Zeit-Kurve (AUC^h) [mg x h/l] |
89,44 (58,08 - 153,86) |
87,38 (58,97 - 160,37) |
|
Maximale Plasmakonzentration (Cmax/ss) [mg/l] |
9,42 (6,32 - 15,42) |
9,16 (6,07 - 16,05) |
|
Minimale Plasmakonzentration (Cmin/ss) [mg/l] |
5,16 (2,81 - 10,46) |
5,18 (2,96 - 10,28) |
|
Prozentuale Peak-trough-Fluktuation (PTF) [%] |
55,93 (38,93 - 84,30) |
53,28 (32,66 - 73,54) |
|
Prozentuale AUC-Fluktuation t = 12 h [%] |
13,49 (7,91 - 24,37) |
12,42 (5,67 - 20,09) |
|
Mittlere Verweilzeit (MRTss) [h] |
13,80 (10,25 - 17,76) |
14,92 (11,80 - 17,17) |
(Geometrische Mittelwerte, Streubreiten in Klammern)
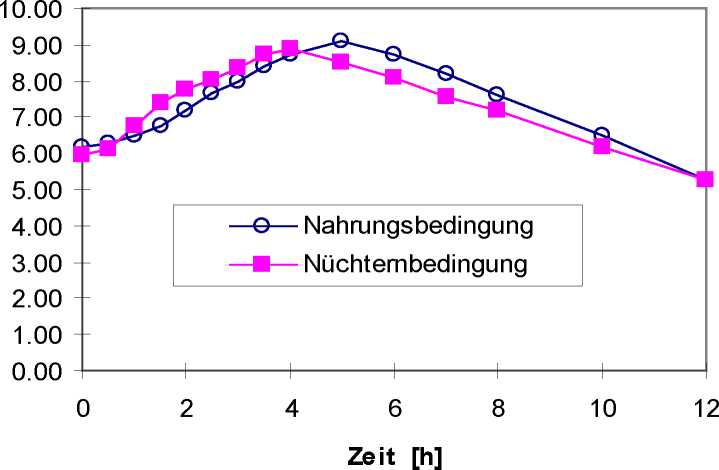
Theophyllin-Plasmakonzentrationen [mg/l] im Steady State nach p.o. Mehrfachgabe von Afonilum retard forte (2-mal 375 mg Theophyllin/Tag, Dosierungsintervall 12 Stunden) unter Nüchternbedingungen im Vergleich zur Gabe nach einer fettreichen Mahlzeit (geometrische Mittelwerte).
Bioverfügbarkeit nach Mehrfachgaben
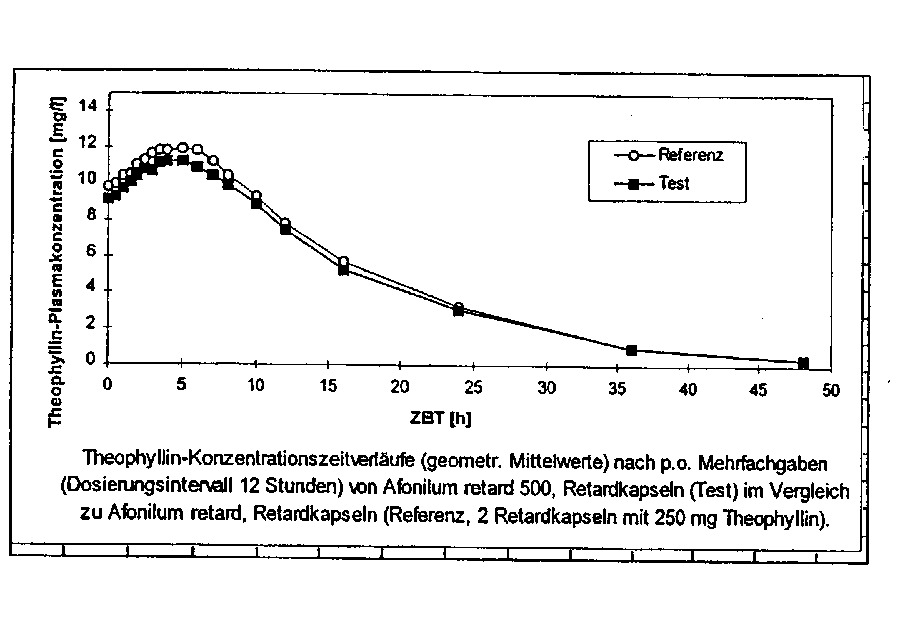
Eine im Jahr 1993 durchgeführte Bioverfügbarkeitsuntersuchung an 18 Probanden mit Afonilum retard 500 (Test) und kombinierter Gabe von 2 Hartkapseln, retardiert Afonilum retard (Referenz) unter p. o. Mehrfachgaben von 2x täglich 500 mg Theophyllin, Dosierungsintervall 12 Stunden, ergab unter Steady-State-Bedingungen im Vergleich zur Referenz:
|
Testpräparat |
Referenzpräparat | |
|
Fläche unter der Konzentrati-ons-Zeit-Kurve (AUCT=12h) [mg x h/l] |
119,48 (79,36 - 172,73) |
126,80 (69,16 - 228,51) |
|
Maximale Plasmakonzentration (Cmax/ss) nüchtern [mg/l] |
11,71 (7,97 - 17,34) |
12,45 (7,12 - 22,03) |
|
Minimale Plasmakonzentration (Cmin/ss) [mg/l] |
7,45 (4,31 - 11,22) |
7,73 (3,29 - 15,60) |
|
Prozentuale Peak-trough-Fluktuation (PTF) [%] |
40,72 (23,11 - 70,19) |
43,15 (30,28 - 66,45) |
|
Plateauzeit (HVD) [h] |
11,98 (11,56 - 12,00) |
11,98 (11,57 - 12,00) |
|
Mittlere Verweilzeit (MRTss) [h] |
15,19 (11,24 - 18,93) |
15,06 (10,83 - 20,84) |
Angaben der Werte als geometrische Mittelwerte und Streubreite
5.3 Präklinische Daten zur Sicherheit
a) Akute Toxizität
Siehe unter Ziffer 4.9 "Überdosierung".
b) Chronische Toxizität
Untersuchungen zur chronischen Toxizität an Hunden und Ratten erbrachten keine Hinweise auf substanzbedingte toxische Effekte.
c) Mutagenes und tumorerzeugendes Potenzial
Theophyllin wirkt am Säuger In-vivo und bei In-vitro-Versuchen mit Einbeziehung des Säugermetabolismus nicht mutagen. Positive In-vitro-Befunde wurden in Versuchen ohne Einbeziehung des Säugermetabolismus beschrieben. Da bekannt ist, dass Theophyllin unter In-vivo-Bedingungen schnell demethyliert wird, sind diese In-vitro-Ergebnisse für den Menschen von geringer Relevanz.
Langzeituntersuchungen am Tier auf ein tumorerzeugendes Potenzial von Theophyllin wurden bisher nicht durchgeführt.
d) Reproduktionstoxizität
Theophyllin ist embryotoxisch und teratogen und zeigt im Tierversuch eine dosisabhängige Wirkung auf die weibliche und männliche Fertilität.
Im Kaninchen trat der teratogene Effekt bei einer Plasmakonzentration auf, die ca. fünffach höher als die angestrebte Plasmakonzentration beim Menschen ist.
6. Pharmazeutische Angaben
6.1 Liste der sonstigen Bestandteile
Afonilum retard forte:
Ethylcellulose, gefälltes Siliciumdioxid, Gelatine, Indigocarmin, Natriumdodecylsulfat, Talkum, Titandioxid.
Afonilum Bio-R:
Grüne Hartkapseln, retardiert wie Afonilum retard, blaue Hartkapseln, retardiert wie Afonilum retard forte.
6.2 Inkompatibilitäten
Nicht zutreffend.
6.3 Dauer der Haltbarkeit
Die Haltbarkeit beträgt 5 Jahre.
Diese Arzneimittel sollen nach Ablauf des Verfallsdatums nicht mehr angewendet werden.
6.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung
Keine.
6.5 Art und Inhalt des Behältnisses
Art des Behältnisses: Blisterpackung Afonilum retard forte
Originalpackung mit 20 Hartkapseln, retardiert Originalpackung mit 50 Hartkapseln, retardiert Originalpackung mit 100 Hartkapseln, retardier
Afonilum Bio-R
Originalpackung mit 20 Hartkapseln, retardiert Originalpackung mit 50 Hartkapseln, retardiert Originalpackung mit 100 Hartkapseln, retardiert Klinikpackung mit 40 Hartkapseln, retardiert Klinikpackung mit 200 (5 x 40) Hartkapseln, retardiert
6.6 Besondere Vorsichtsmaßnahmen für die Beseitigung
Keine besonderen Anforderungen.
7. Inhaber der Zulassung
Mylan Healthcare GmbH
Freundallee 9A
30173 Hannover
Telefon: 0511 / 6750-2400
Telefax: 0511 / 6750-3120
E-Mail: mylan.healthcare@mylan.com
8. Zulassungsnummern
Afonilum retard forte 1444.02.00
Afonilum Bio-R 7360.00.00
9. Datum der Erteilung der Zulassung/Verlängerung der Zulassung
Afonilum retard forte 12.12.1983//16.03.1992/28.10.1998/31.07.2007
Afonilum Bio-R 02.12.1985/01.10.1998/31.07.2007
10. Stand der Information
April 2015
11. Verkaufsabgrenzung
Verschreibungspflichtig.
Seite 17 von 17