Allergodil Nasenspray
Gebrauchsinformation: Information für Anwender
Allergodil® Nasenspray 1 mg / 1 ml Nasenspray, Lösung Azelastinhydrochlorid
Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen, denn sie enthält wichtige Informationen.
- Heben Sie die Packungsbeilage auf. Vielleicht möchten Sie diese später nochmals lesen.
- Wenn Sie weitere Fragen haben, wenden Sie sich an Ihren Arzt oder Apotheker.
- Dieses Arzneimittel wurde Ihnen persönlich verschrieben. Geben Sie es nicht an Dritte weiter. Es kann anderen Menschen schaden, auch wenn diese die gleichen Beschwerden haben wie Sie.
- Wenn Sie Nebenwirkungen bemerken, wenden Sie sich an Ihren Arzt oder Apotheker. Dies gilt
auch für Nebenwirkungen, die nicht in dieser Packungsbeilage angegeben sind. Siehe Abschnitt 4.._
Was in dieser Packungsbeilage steht:
1. Was ist Allergodil Nasenspray und wofür wird es angewendet?
2. Was sollten Sie vor der Anwendung von Allergodil Nasenspray beachten?
3. Wie ist Allergodil Nasenspray anzuwenden?
4. Welche Nebenwirkungen sind möglich?
5. Wie ist Allergodil Nasenspray aufzubewahren?
6. Inhalt der Packung und weitere Informationen
1. Was ist Allergodil Nasenspray und wofür wird es angewendet?
Allergodil Nasenspray ist ein Antiallergikum/Antihistaminikum und enthält den Wirkstoff Azelastinhydrochlorid.
Allergodil Nasenspray wird angewendet zur symptomatischen Behandlung von Heuschnupfen (saisonale allergische Rhinitis) und ganzjährigem allergischen Schnupfen (perenniale allergische Rhinitis) bei Erwachsenen, Jugendlichen und Kindern ab 6 Jahren.
2. Was sollten Sie vor der Anwendung von Allergodil Nasenspray beachten?
Allergodil Nasenspray darf nicht angewendet werden,
wenn Sie allergisch gegen Azelastinhydrochlorid oder einen der in Abschnitt 6. genannten sonstigen Bestandteile dieses Arzneimittels sind. .
Warnhinweise und Vorsichtsmaßnahmen
Bitte sprechen Sie mit Ihrem Arzt oder Apotheker, bevor Sie Allergodil Nasenspray.anwenden.
Kinder
Dieses Arzneimittel ist nicht für die Anwendung bei Kindern unter 6 Jahren bestimmt.
Ältere Menschen
Für ältere Patienten sind keine besonderen Hinweise zu beachten.
Anwendung von Allergodil Nasenspray zusammen mit anderen Arzneimitteln
Informieren Sie Ihren Arzt oder Apotheker wenn Sie andere Arzneimittel anwenden, kürzlich andere Arzneimittel angewendet haben oder beabsichtigen andere Arzneimittel anzuwenden. Wechselwirkungen mit anderen Arzneimitteln sind bislang nicht beobachtet worden.
Anwendung von Allergodil Nasenspray zusammen mit Nahrungsmitteln, Getränken und Alkohol
Wechselwirkungen mit Nahrungsmitteln und Getränken sind bisher nicht beobachtet worden
Generell sollte aber bei einer medikamentösen Behandlung auf die Einnahme alkoholischer Getränke verzichtet werden.
Schwangerschaft und Stillzeit
Wenn Sie schwanger sind oder stillen, oder wenn Sie vermuten, schwanger zu sein oder beabsichtigen, schwanger zu werden, fragen Sie vor der Anwendung dieses Arzneimittels Ihren Arzt oder Apotheker um Rat.
Schwangerschaft
Obwohl es bis weit über den therapeutischen Dosierungsbereich hinaus aus tierexperimentellen Studien keine Anhaltspunkte für eine fruchtschädigende Wirkung gibt, entspricht es der gegenwärtigen allgemeinen Auffassung über den Arzneimittelgebrauch, Allergodil Nasenspray im ersten Drittel der Schwangerschaft nicht anzuwenden.
Stillzeit
Da ausreichende Erfahrungen noch nicht vorliegen, sollte Allergodil Nasenspray während der Stillzeit nicht appliziert werden.
Verkehrstüchtigkeit und Fähigkeit zum Bedienen von Maschinen
Bei Anwendung von Allergodil Nasenspray sind in Einzelfällen Beschwerden wie Abgeschlagenheit, Mattigkeit, Erschöpfung, Schwindel- oder Schwächegefühl, die auch durch das Krankheitsgeschehen bedingt sein können, möglich. In diesen Fällen kann die Fähigkeit zum Führen eines Kraftfahrzeuges und zur Bedienung von Maschinen beeinträchtigt sein. Dies gilt in verstärktem Maße im Zusammenwirken mit Alkohol und Medikamenten, die ihrerseits das Reaktionsvermögen beeinträchtigen können.
3. Wie ist Allergodil Nasenspray anzuwenden?
Wenden Sie dieses Arzneimittel immer genau nach Absprache mit Ihrem Arzt oder Apotheker an. Fragen Sie bei Ihrem Arzt oder Apotheker nach, wenn Sie sich nicht sicher sind.
Falls vom Arzt nicht anders verordnet, beträgt die empfohlene Dosis: 2-mal täglich (morgens und abends) 1 Sprühstoß Allergodil Nasenspray pro Nasenloch (entspricht 0,56 mg Azelastinhydrochlorid/T ag).
Art der Anwendung
Die Anwendung von Allergodil Nasenspray soll bei aufrechter Kopfhaltung erfolgen (siehe Anleitung/Bildfolge).
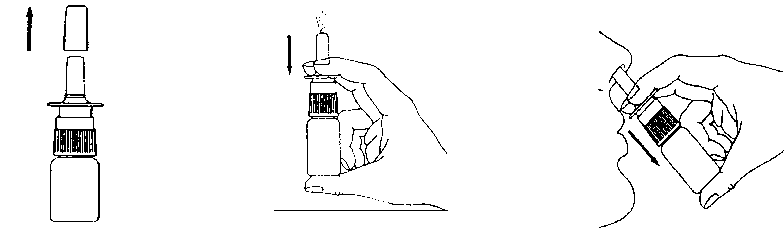
1. Nach Abziehen der Schutzkappe....
3. Einen Sprühstoß pro Nasenloch bei aufrechter Kopfhaltung einsprühen.
2.....ist nur bei der ersten
Anwendung mehrmals zu pumpen, bis gleichmäßiger Sprühnebel austritt.
4. Schutzkappe wieder aufstecken.
Dauer der Anwendung
Die Dauer der Anwendung von Allergodil Nasenspray richtet sich nach Art, Schwere und Verlauf der Beschwerden.
Allergodil Nasenspray ist zur Langzeitbehandlung geeignet.
Bitte sprechen Sie mit Ihrem Arzt oder Apotheker, wenn Sie den Eindruck haben, dass die Wirkung von Allergodil Nasenspray zu stark oder zu schwach ist.
Wenn Sie eine größere Menge von Allergodil Nasenspray angewendet haben, als Sie sollten
Allergodil Nasenspray wird lokal in der Nase angewendet. Aufgrund der geringen Wirkstoffmenge ist selbst auch bei extremer lokaler Überdosierung nicht mit Vergiftungserscheinungen zu rechnen. Sollten jedoch versehentlich größere Mengen verschluckt werden (z. B. der Inhalt der Flasche durch ein Kind), sollte auf jeden Fall der Arzt zu Rate gezogen werden.
Erfahrungen beim Menschen nach Anwendung toxischer (sehr hoher, giftiger) Dosen von Azelastinhydrochlorid liegen nicht vor. Aufgrund tierexperimenteller Befunde ist bei extremer Überdosierung und Intoxikation (Vergiftung) jedoch mit zentralnervösen Erscheinungen (z. B. Unruhe, Erregung oder stark ausgeprägte, andauernde Müdigkeit oder Schläfrigkeit) zu rechnen. Die Behandlung sollte daher symptomatisch erfolgen.
Wenn Sie die Anwendung von Allergodil Nasenspray vergessen haben
Sollten Sie einmal die Anwendung von Allergodil Nasenspray vergessen haben, sind keine speziellen Maßnahmen erforderlich. Setzen Sie die Therapie mit der gleichen Dosierung zum nächsten vorgesehenen Zeitpunkt fort. Bei Bedarf können Sie Allergodil Nasenspray auch zwischen zwei vorgesehenen Zeitpunkten anwenden.
Wenn Sie die Anwendung von Allergodil Nasenspray abbrechen
Die Behandlung mit Allergodil Nasenspray sollte nach Möglichkeit regelmäßig bis zum Erreichen der Beschwerdefreiheit erfolgen. Sollten Sie die Anwendung von Allergodil Nasenspray unterbrechen, so müssen Sie damit rechnen, dass sich bald wieder die typischen Symptome Ihrer Erkrankung zeigen.
Wenn Sie weitere Fragen zur Anwendung dieses Arzneimittels haben, wenden Sie sich an Ihren Arzt oder Apotheker.
Welche Nebenwirkungen sind möglich?
4.
Wie alle Arzneimittel kann auch dieses Arzneimittel Nebenwirkungen haben, die aber nicht bei jedem aufitreten müssen.
Bei den Häufigkeitsangaben zu Nebenwirkungen werden folgende Kategorien zugrunde gelegt:
|
Sehr häufig: |
Häufig: |
|
mehr als 1 Behandelter von 10 |
1 bis 10 Behandelte von 100 |
|
Gelegentlich: |
Selten: |
|
1 bis 10 Behandelte von 1.000 |
1 bis 10 Behandelte von 10.000 |
|
Sehr selten: | |
|
weniger als 1 Behandelter von 10.000 | |
|
Nicht bekannt: Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar | |
Häufig: Bitterer Geschmack meist aufgrund unsachgemäßer Anwendung (zurückgeneigtem Kopf, s. Dosierungsanleitung), der zuweilen Übelkeit verursachen kann.
Gelegentlich: Reizung der bereits entzündlich veränderten Nasenschleimhaut (Brennen, Kribbeln), Niesen, Nasenbluten
Selten: Übelkeit
Sehr selten: Überempflindlichkeitsreaktionen, Hautausschlag, Juckreiz, Nesselsucht, Abgeschlagenheit (Mattigkeit, Erschöpfung), Schwindel- oder Schwächegefühl, die auch durch das Krankheitsgeschehen selbst bedingt sein können
Gegenmaßnahmen
Die o. g. Nebenwirkungen treten in der Regel vorübergehend auf. Besondere Gegenmaßnahmen sind deshalb nicht zu ergreifen.
Sollten Sie in Ihrem Mund nach der Anwendung von Allergodil Nasenspray einen bitteren Geschmack verspüren, so können Sie diesem mit einem alkoholfreien Getränk (z. B. Saft, Milch) entgegenwirken.
Meldung von Nebenwirkungen
Wenn Sie Nebenwirkungen bemerken, wenden Sie sich an Ihren Arzt oder Apotheker. Dies gilt auch für Nebenwirkungen, die nicht in dieser Packungsbeilage angegeben sind. Sie können Nebenwirkungen auch direkt beim Bundesinstitut für Arzneimittel und Medizinprodukte, Abt. Pharmakovigilanz, Kurt-Georg-Kiesinger Allee 3, D-53175 Bonn (Website: http://www.bfarm.de) anzeigen.
Indem Sie Nebenwirkungen melden, können Sie dazu beitragen, dass mehr Informationen über die Sicherheit dieses Arzneimittels zur Verfügung gestellt werden.
5. Wie ist Allergodil Nasenspray aufzubewahren?
Bewahren Sie dieses Arzneimittel für Kinder unzugänglich auf.
Sie dürfen dieses Arzneimittel nach dem auf dem Etikett und dem Umkarton angegebenen Verfalldatum nicht mehr verwenden. Das Verfalldatum bezieht sich auf den letzten Tag des angegebenen Monats.
Aufbewahrungsbedingungen
Nicht unter 8 °C lagern.
Hinweis auf Haltbarkeit nach Anbruch
Allergodil Nasenspray soll nach Anbruch der Flasche nicht länger als 6 Monate verwendet werden.
Sie dürfen dieses Arzneimittel nicht verwenden, wenn Sie Folgendes bemerken:
Sollte Allergodil Nasenspray versehentlich längere Zeit unter +8 °C (z. B. im Kühlschrank) gelagert werden, beginnt der Wirkstoff von Allergodil Nasenspray teilweise auszukristallisieren. Diese Kristallbildung („Ausflockung”) ist sichtbar, wenn die Flasche gegen das Licht gehalten wird. Diese Lösung sollte nicht verwendet werden.
Durch längere Lagerung (einige Stunden) der Lösung bei Raumtemperatur lösen sich die Kristalle jedoch wieder vollständig. Diese klare Lösung (keine Ausflockung mehr sichtbar) kann dann weiter verwendet werden.
Entsorgen Sie Arzneimittel nicht im Abwasser oder Haushaltsabfall. Fragen Sie Ihren Apotheker, wie das Arzneimittel zu entsorgen ist, wenn Sie es nicht mehr benötigen. Sie tragen damit zum Schutz der Umwelt bei.
6. Inhalt der Packung und weitere Informationen Was Allergodil Nasenspray enthält
Der Wirkstoff ist Azelastinhydrochlorid.
1 Sprühstoß zu 0,14 ml enthält 0,14 mg Azelastinhydrochlorid.
Die sonstigen Bestandteile sind:
Natriumedetat, Hypromellose, Natriummonohydrogenphosphat-Dodecahydrat, Citronensäure, Natriumchlorid, gereinigtes Wasser.
Wie Allergodil Nasenspray aussieht und Inhalt der Packung
Allergodil Nasenspray ist eine klare, farblose Lösung zum Einsprühen in die Nase (nasale Anwendung).
Allergodil Nasenspray ist einer braunen Glasflasche mit Sprühpumpe in folgenden Packungsgrößen erhältlich:
Originalpackung zu 10 ml (N1) Nasenspray, Lösung Originalpackung zu 17 ml (N2) Nasenspray, Lösung Anstaltspackung mit 10 x 10 ml Nasenspray Lösung
Pharmazeutischer Unternehmer
MEDA Pharma GmbH & Co. KG Benzstraße 1 61352 Bad Homburg Telefon (06172) 888-01
Telefax (06172) 888-27 40 medinfo@medapharma.de
Hersteller
MEDA Pharma GmbH & Co. KG Benzstraße 1 61352 Bad Homburg Telefon: (06172) 888-01 Telefax: (06172) 888-2740
alternativ: MEDA Manufacturing GmbH Neurather Ring 1 51603 Köln Telefon: (0221) 6472-0 Telefax: (0221) 6472 -606
Diese Gebrauchsinformation wurde zuletzt überarbeitet im September 2014.
Allergodil Nasenspray ist verschreibungspflichtig.
Eine Allergie ist eine Überreaktion des körpereigenen Abwehrsystems auf harmlose Stoffe. Eine Allergie kann z. B. durch den Kontakt mit Blütenpollen, Hausstaubmilben, Katzen- oder Hundehaar ausgelöst werden.
Ihr Arzt hat Ihnen zur Linderung Ihrer allergischen Beschwerden Allergodil Nasenspray mit dem Wirkstoff Azelastinhydrochlorid verschrieben. Dieser Wirkstoff blockiert die Effekte von Histamin und anderen entzündlich wirkenden Stoffen, die bei einer Allergie vermehrt freigesetzt werden. Allergodil Nasenspray hemmt u. a. überhöhte Nasensekretion, quälenden Niesreiz und Schwellung der Nasenschleimhaut. Da Allergodil Nasenspray direkt auf die Nasenschleimhaut einwirkt, werden trotz der geringen Wirkstoffdosierung die allergischen Beschwerden an der Nase schnell und wirksam vermindert.
Wir wünschen Ihnen gute Besserung mit Allergodil Nasenspray.
Ihre MEDA Pharma GmbH & Co. KG
6