Amiped 10% Infusionslösung
1. BEZEICHNUNG DES ARZNEIMITTELS
Amiped 10% Infusionslösung
2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Die Infusionslösung enthält:
|
Aminosäuren: |
pro 1 ml |
pro 100 ml |
pro 250 ml |
|
Isoleucin |
5,10 mg |
0,51 g |
1,28 g |
|
Leucin |
7,60 mg |
0,76 g |
1,90 g |
|
Lysin Monohydrat (entsprechend Lysin) |
9,88 mg (8,80 mg) |
0,99 g (0,88 g) |
2,47 g (2,20 g) |
|
Methionin |
2,00 mg |
0,20 g |
0,50 g |
|
Phenylalanin |
3,10 mg |
0,31 g |
0,78 g |
|
Threonin |
5,10 mg |
0,51 g |
1,28 g |
|
Tryptophan |
4,00 mg |
0,40 g |
1,00 g |
|
Valin |
6,10 mg |
0,61 g |
1,53 g |
|
Arginin |
9,10 mg |
0,91 g |
2,28 g |
|
Histidin |
4,60 mg |
0,46 g |
1,15 g |
|
Alanin |
15,90 mg |
1,59 g |
3,98 g |
|
Glycin |
2,00 mg |
0,20 g |
0,50 g |
|
Asparaginsäure |
6,60 mg |
0,66 g |
1,65 g |
|
Glutaminsäure |
9,30 mg |
0,93 g |
2,33 g |
|
Prolin |
6,10 mg |
0,61 g |
1,53 g |
|
Serin |
2,00 mg |
0,20 g |
0,50 g |
|
N-Acetyltyrosin (Ph.Eur.) (entsprechend Tyrosin) |
1,30 mg (1,06 mg) |
0,13 g (0,11 g) |
0,33 g (0,27 g) |
|
Acetylcystein (entsprechend Cystein) |
0,700 mg (0,520 mg) |
0,070 g (0,052 g) |
0,175 g (0,13 g) |
|
Taurin |
0,300 mg |
0,030 g |
0,075 g |
|
pro 1 ml |
pro 100 ml |
pro 250 ml | |
|
Aminosäurengehalt |
0,1 g |
10 g |
25 g |
|
Stickstoffgehalt |
0,0152 g |
1,52 g |
3,8 g |
Vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt 6.1.
3. DARREICHUNGSFORM
Infusionslösung
Klare, farblose bis hellgelbe Lösung
|
Energie [kJ/l (kcal/l)] |
1.700 (400) |
|
Theoretische Osmolarität [mOsm/l] |
790 |
|
Acidität (Titration auf pH 7,4) |
23 mmol |
|
PH_ |
ca. 6,1 |
4. KLINISCHE ANGABEN
4.1 Anwendungsgebiete
Versorgung von Neugeborenen und Frühgeborenen, Säuglingen, Kleinkindern und Kindern mit Aminosäuren im Rahmen einer parenteralen Ernährung in Kombination mit energie- (Glucose und Lipide) und elektrolythaltigen Lösungen, wenn eine orale oder enterale Ernährung unmöglich, unzureichend oder kontraindiziert ist.
4.2 Dosierung und Art der Anwendung
Dosierung
Kinder und Jugendliche
Die unten angegebenen Dosierungen für diese Altersgruppen sind Mittelwerte zur Orientierung. Die genaue Dosierung sollte individuell nach Alter, Entwicklungsstand, vorherrschender Erkrankung und Art der Therapie angepasst werden.
Die Dosierung sollte unter dem Zielwert der Infusionsrate begonnen und innerhalb der ersten Stunde auf den Zielwert erhöht werden.
Die parenterale Zufuhr folgender Aminosäurenmengen wird für die meisten pädiatrischen Patienten als angemessen betrachtet:
Frühgeborene: 1,5-4,0 g Aminosäuren/kg Körpergewicht pro Tag = 15-40 ml/kg Körpergewicht pro Tag
Neugeborene (0-27 Tage): 1,5-3,0 g Aminosäuren/kg Körpergewicht pro Tag = 15-30 ml/kg Körpergewicht pro Tag
Säuglinge und Kleinkinder (28 Tage bis 23 Monate): 1,0 - 2,5 g Aminosäuren/kg Körpergewicht pro Tag = 10 - 25 ml/kg Körpergewicht pro Tag
Kinder (2 bis 11 Jahre): 1,0-2,0 g Aminosäuren/kg Körpergewicht pro Tag = 10-20 ml/kg Körpergewicht pro Tag
Bei schwerkranken Kindern kann die angebrachte Aminosäurenzufuhr höher liegen (bis zu 3,0 g Aminosäuren/kg Körpergewicht pro Tag).
Maximale Infusionsgeschwindigkeit bis zu 0,1 g Aminosäuren/kg Körpergewicht und Stunde, entsprechend etwa 1 ml/kg Körpergewicht und Stunde.
Art der Anwendung
Intravenöse Anwendung.
Aufgrund der hohen Osmolarität darf unverdünntes Amiped 10% nur über eine zentrale Vene verabreicht werden. Eine ausreichende Verdünnung von Amiped 10%, zum Beispiel mit Wasser für Injektionszwecke oder einer geeigneten Lösung, senkt jedoch die Osmolarität und ermöglicht eine periphere Infusion.
Bei gleichzeitiger ausreichender Versorgung mit Energie und Elektrolyten bestehen keine Einschränkungen für die Verabreichung im Rahmen eines parenteralen Ernährungsregimes.
Amiped 10% stellt lediglich die Grundlage für eine parenterale Ernährung dar. Bei Patienten, die ausschließlich parenteral ernährt werden, ist die gleichzeitige Substitution von Energieträgern (unter Berücksichtigung des Bedarfs an essentiellen Fettsäuren), Elektrolyten, Vitaminen und Spurenelementen erforderlich.
4.3 Gegenanzeigen
- Überempfindlichkeit gegen die Wirkstoffe oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile.
- Zustände einer Überwässerung, Hypokaliämie
- Angeborene Störungen des Aminosäurenstoffwechsels
- Akute metabolische Störungen durch Hypoxie und Acidose
- Lebensbedrohliche Kreislaufinstabilität
- Akutes Lungenödem
- Dekompensierte Herzinsuffizienz
Wie bei allen aminosäurenhaltigen Lösungen sind schwere Leberinsuffizienz, Leberkoma und schwere Niereninsuffizienz ohne Nierenersatztherapie Kontraindikationen für Amiped 10%.
4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung
Vorsicht ist geboten, wenn die Serumosmolarität erhöht ist.
Vorsicht ist geboten, wenn die Flüssigkeitszufuhr eingeschränkt werden muss, wie z. B. bei einer Hyponatriämie.
Eine häufigere Überwachung des klinischen Zustands und der entsprechenden Laborwerte ist insbesondere bei Patienten mit folgenden Störungen erforderlich:
- Störungen des Aminosäurenstoffwechsels
- Leberfunktionsstörungen, aufgrund des Risikos eines erneuten Auftretens oder einer Verschlechterung bestehender neurologischer Störungen im Zusammenhang mit einer Hyperammonämie.
- Niereninsuffizienz, insbesondere bei bestehender Hyperkaliämie, oder bei Vorliegen von
Risikofaktoren für die Entwicklung oder Verschlechterung einer metabolischen Acidose oder Hyperazotämie aufgrund einer eingeschränkten Nierenclearance.
Die Dosierung sollte dem Alter, dem Ernährungszustand und der zugrunde liegenden Erkrankung angepasst werden. Siehe Abschnitt 4.2.
Darüber hinaus ist es unerlässlich, dass die Therapie durch adjuvante Energiequellen (Glucose und Lipide), Vitamine und Spurenelemente ergänzt wird.
Spurenelemente sollten in Form von Zubereitungen für Kinder und Jugendliche verabreicht werden.
Bevor Amiped 10% über eine periphere Vene verabreicht wird, muss es ausreichend mit einer geeigneten Lösung verdünnt werden. Siehe Abschnitt 4.2.
Flüssigkeits- und Elektrolythaushalt, Serumosmolarität, Säure-Basen-Gleichgewicht, Blutzuckerspiegel, Nierenfunktion und Leberwerte sollten während der gesamten Dauer der parenteralen Therapie überwacht werden, wobei die Häufigkeit der Überwachung durch die Schwere der Grunderkrankung und den klinischen Zustand des Patienten bestimmt wird.
Die Konzentrationen von Harnstoff-Stickstoff und Ammoniak im Serum sollten bestimmt werden.
Während einer Langzeitanwendung (mehrere Wochen) sollten Blutbild und Gerinnungsfaktoren besonders sorgfältig überwacht werden.
4.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen
Es sind keine Wechselwirkungen bekannt.
4.6 Fertilität, Schwangerschaft und Stillzeit
Amiped 10% ist ausschließlich für die Anwendung bei Kindern (unter zwölf Jahren) bestimmt.
4.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen
Nicht zutreffend.
4.8 Nebenwirkungen
Insbesondere zu Beginn der parenteralen Ernährung können Nebenwirkungen auftreten, die jedoch nicht spezifisch durch das Arzneimittel bedingt sind, sondern generell im Zusammenhang mit einer parenteralen Ernährung zu beobachten sind.
Gelegentlich (> 1/1.000, < 1/100):
Erkrankungen des Gastrointestinaltrakts: Übelkeit, Erbrechen Allgemeine Erkrankungen: Kopfschmerzen, Schüttelfrost, Fieber
Eine Thrombophlebitis kann infolge der hohen Osmolarität der Lösung auftreten, wenn das Arzneimittel ohne ausreichende Verdünnung über eine periphere Vene verabreicht wird.
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung dem Bundesinstitut für Arzneimittel und Medizinprodukte, Abt. Pharmakovigilanz, Kurt-Georg-Kiesinger-Allee 3, D-53175 Bonn, Website: www.bfarm.de anzuzeigen.
4.9 Überdosierung
Symptome
Zu hohe Infusionsraten können zu Unverträglichkeitsreaktionen führen, die sich in Form von Übelkeit, Erbrechen, Flushing mit Rötung des Kopfes, Wärmegefühl und renalen Aminosäurenverlusten mit nachfolgenden Aminosäurenimbalancen manifestieren.
Behandlung
Im Falle von Unverträglichkeitsreaktionen sollte die Aminosäureninfusion vorübergehend unterbrochen und später mit einer niedrigeren Infusionsrate wiederaufgenommen werden.
5. PHARMAKOLOGISCHE EIGENSCHAFTEN
5.1 Pharmakodynamische Eigenschaften
Pharmakotherapeutische Gruppe:
Lösungen zur parenteralen Ernährung, Aminosäuren ATC-Code: B05BA01
Wirkmechanismus
Die Infusionslösung enthält 19 Aminosäuren zur Deckung des qualitativen Proteinbedarfs des Kindes:
- alle für Kinder essentiellen und semiessentiellen Aminosäuren
Im Vergleich zu herkömmlichen Aminosäurenlösungen enthält Amiped 10%:
- einen relativ hohen Anteil an Lysin
- Taurin
- einen relativ niedrigen Anteil an Methionin
- einen niedrigen Anteil an Phenylalanin und Prolin.
Die Lösungen enthalten keine zusätzlichen Elektrolyte, um einen Einfluss auf die Elektrolytbehandlung des Kindes im Falle einer Reanimation auszuschließen.
Pharmakodynamische Wirkungen
Aminosäuren stellen die Bausteine für die Proteinsynthese dar. Reine Aminosäurenlösungen werden im Rahmen einer parenteralen Ernährungstherapie zusammen mit Energieträgern und anderen Nährstoffen wie Elektrolyten, Spurenelementen, Vitaminen und Flüssigkeit verabreicht, um den Ernährungszustand des Organismus zu erhalten und zu verbessern bzw. einen etwaigen Verlust an Substanzen zu minimieren.
5.2 Pharmakokinetische Eigenschaften
Resorption
Amiped 10% wird intravenös infundiert. Daher sind alle Substrate für den Stoffwechsel unmittelbar verfügbar.
Verteilung
Die Konzentrationen der freien Aminosäuren im Plasma sind erheblichen Schwankungen unterworfen. Dies gilt sowohl für die einzelnen Aminosäuren als auch für die Summe der Aminosäurenkonzentrationen. Im Gegensatz dazu bleibt das Verhältnis zwischen den Aminosäuren relativ konstant, unabhängig von der Aminosäurengesamtkonzentration oder den absoluten Konzentrationen der einzelnen Aminosäuren. Es scheint, dass der Organismus versucht, das Substrat „Aminosäuren“ innerhalb eines physiologischen Referenzbereichs auf einem konstanten Niveau zu halten und Verschiebungen der Gleichgewichte innerhalb der Aminosäurenmuster so weit wie möglich zu vermeiden. Bei erhaltenen Kompensationsmöglichkeiten des Organismus führen in den meisten Fällen erst drastische Veränderungen der Substratzufuhr zu einer Störung der Aminosäurenhomöostase im Blut. Typische pathologische Veränderungen im Aminosäurenprofil des Plasmas sind nur zu erwarten, wenn die Regulierungsfähigkeit von wichtigen Stoffwechselorganen, z. B. der Leber oder der Nieren, erheblich beeinträchtigt ist. Falls erforderlich, können zur Behandlung derartiger Veränderungen mit dem Ziel der Wiederherstellung der Homöostase spezielle Aminosäurenlösungen mit besonderer Zusammensetzung verwendet werden.
Unter pathologischen Bedingungen treten ohne exogene Zufuhr von Aminosäuren beträchtliche typische Veränderungen im Plasma-Aminosäurenmuster auf, die in der Regel sowohl die absolute Konzentration einzelner Aminosäuren als auch deren prozentuale Zusammensetzung im Plasma beeinflussen.
Biotransformation
Aminosäuren in ihrer Gesamtheit sind ein komplexes System von Substanzen, die sich gegenseitig beeinflussen. Auf der einen Seite besteht eine direkte Stoffwechselabhängigkeit zwischen einzelnen Aminosäuren (Beispiel: Tyrosin wird durch Hydroxylierung aus Phenylalanin gebildet). Andererseits können andere Stoffwechselmechanismen im Organismus empfindlich auf eine Verschiebung innerhalb des Aminosäurenmusters durch Veränderung der Konzentration einzelner Aminosäuren oder Aminosäurengruppen (z. B. Veränderungen im Verhältnis zwischen aromatischen Aminosäuren und Aminosäuren mit verzweigten Ketten) reagieren. Darüber hinaus können Verschiebungen innerhalb einer Aminosäurengruppe mit ähnlicher chemischer Konfiguration und ähnlichem Stoffwechselverhalten Auswirkungen auf den Gesamtstoffwechsel des Organismus haben.
5.3 Präklinische Daten zur Sicherheit
Es wurden keine präklinischen Studien mit Amiped 10% durchgeführt.
PHARMAZEUTISCHE ANGABEN
6.
6.1 Liste der sonstigen Bestandteile
Citronensäure-Monohydrat (zur pH-Einstellung)
Wasser für Injektionszwecke.
6.2 Inkompatibilitäten
Dieses Arzneimittel darf, außer mit den unter Abschnitt 6.6 aufgeführten, nicht mit anderen Arzneimitteln gemischt werden.
6.3 Dauer der Haltbarkeit
- Ungeöffnet (Beutel in Umhüllung):
2 Jahre
- Nach Anbruch:
Das Arzneimittel sollte sofort verwendet werden.
- Nach dem Mischen mit anderen Komponenten einer parenteralen Ernährung:
Die chemische und physikalische Stabilität nach Mischung mit anderen Komponenten der parenteralen Ernährung wurde für 24 Stunden bei 2-8°C plus 24 Stunden bei 37°C nachgewiesen. Nach Beimischung von Zusatzstoffen muss die Lösung vor Licht geschützt aufbewahrt werden.
Aus mikrobiologischer Sicht sollte das Arzneimittel unmittelbar verwendet werden. Wenn es nicht sofort verwendet wird, liegen die Aufbewahrungszeiten und -bedingungen vor der Anwendung in der Verantwortung des Anwenders.
6.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung
Nicht einfrieren. Bei versehentlichem Einfrieren Beutel verwerfen.
Aufbewahrungsbedingungen nach Beimischung von Zusatzstoffen siehe Abschnitt 6.3.
6.5 Art und Inhalt des Behältnisses und spezielles Zubehör für den Gebrauch, die Anwendung oder die Implantation
Amiped 10% wird in flexiblen Beuteln aus mehrschichtiger Folie (Polypropylen, Styrol-Ethylen-Butylen-Styrol (SEBS) und Copolyesterether) geliefert. Die innere, in Kontakt mit der Lösung stehende Schicht besteht aus Polypropylen. Die Beutel enthalten 100 ml oder 250 ml.
Der Beutel ist in einer schützenden Umhüllung verpackt. Ein Sauerstoffabsorber (Beutel aus einem inerten Material, der pulverförmiges Eisenhydroxid enthält) ist zwischen dem Beutel und der Umhüllung platziert.
Die verschiedenen Behältnisgrößen werden in Kartons mit 12 Beuteln geliefert.
Packungsgrößen: 12 x 100 ml und 12 x 250 ml.
Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht.
6.6 Besondere Vorsichtsmaßnahmen für die Beseitigung und sonstige Hinweise zur Handhabung
Keine besonderen Anforderungen für die Beseitigung von Behältnis, Umhüllung und Sauerstoffabsorber.
Nicht verwenden, wenn die Umhüllung geöffnet wurde oder beschädigt ist. Ausschließlich Beutel verwenden, die unbeschädigt sind und in denen die Aminosäurenlösung klar und frei von Partikeln ist.
Amiped 10% sollte nur mit anderen I.V.-Lösungen gemischt werden, wenn die Kompatibilität im Vorfeld nachgewiesen wurde.
Daten zur Kompatibilität verschiedener Zusatzstoffe (z. B. Glucose, Lipide, Elektrolyte, Spurenelemente, Vitamine) und zur entsprechenden Dauer der Haltbarkeit solcher Mischungen können beim Hersteller angefordert werden.
Amiped 10% wird in Behältnissen für den einmaligen Gebrauch geliefert. Nicht verwendete Lösung ist zu verwerfen.
Vor der Infusion muss die Lösung immer auf Raumtemperatur gebracht werden.
Es ist wesentlich, dass jegliche Beimischung unter Anwendung strenger aseptischer Techniken erfolgt, da diese Nährstoffmischung ein mikrobielles Wachstum unterstützt.
Amiped 10% Handhabung
Abbildung A: Beutel und Umhüllung
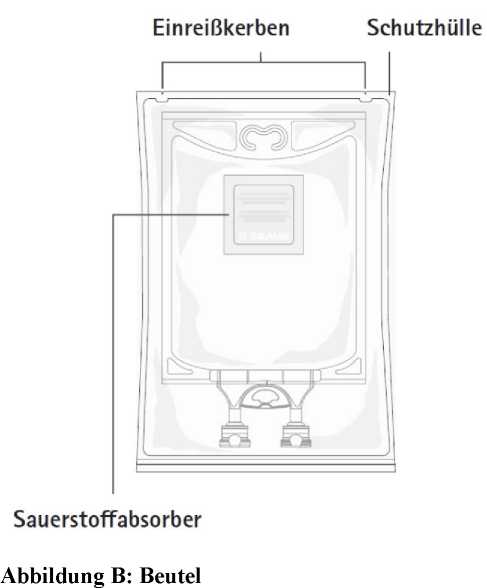
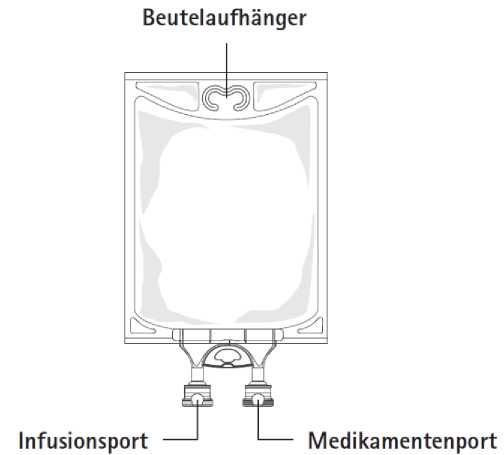
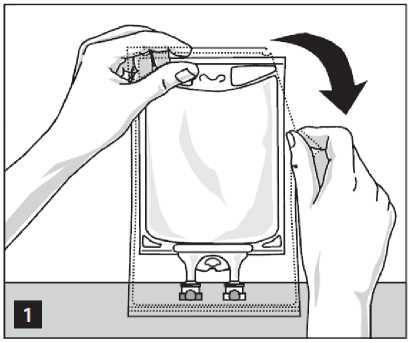
Öffnen:
Den Beutel aus der Schutzumhüllung nehmen, indem Sie diese von den Einreißkerben oben her aufreißen und das Lösungsbehältnis entnehmen (Abbildung 1).
Umhüllung und Sauerstoffabsorber entsorgen.
Auf Undichtigkeiten prüfen. Ist der Beutel undicht, das Arzneimittel verwerfen, da die Sterilität nicht gewährleistet ist.
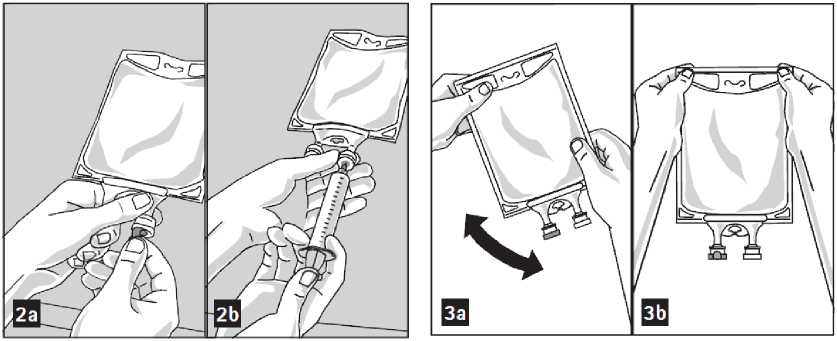
Beimischung von Arzneimitteln:
Mischungen müssen unter Einhaltung streng aseptischer Techniken hergestellt werden. Kompatible Arzneimittelzusätze können über den Medikamentenport (transparent) hinzugefügt werden.
1. Bereiten Sie den Medikamentenport (transparent) durch Entfernen der Aluminiumfolie vor (Abbildung 2a). Bitte beachten Sie: Der Bereich unter der Folie des Medikamentenports ist steril.
2. Durchstechen Sie den wiederverschließbaren Medikamentenport und injizieren Sie den Zusatz/die Zusätze (Abbildung 2b).
3. Mischen Sie die Lösung und das Arzneimittel gründlich (Abbildung 3a).
4. Der Medikamentenport kann vor einer erneuten Punktion mit Desinfektionsmittel (z. B. Isopropanol) abgewischt werden.
5. Prüfen Sie die Mischung visuell auf Partikel (Abbildung 3b).
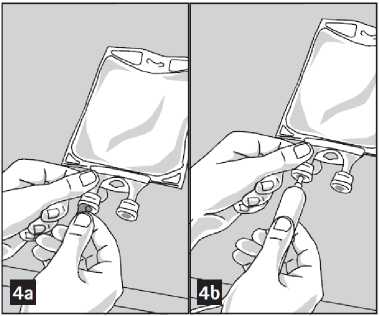
Vorbereitung für die Verabreichung:
1. Entfernen Sie die Aluminiumfolie des Infusionsports (grün) am unteren Rand des Behältnisses (Abbildung 4a) und befestigen Sie das Verabreichungssystem (Abbildung 4b): Verwenden Sie ein nicht belüftetes Infusionsset oder schließen Sie bei einem belüfteten Set das Belüftungsventil. Befolgen Sie die Anweisungen für die Anwendung des Infusionssets. Bitte beachten Sie: Der Bereich unter der Folie des Infusionsports ist steril.
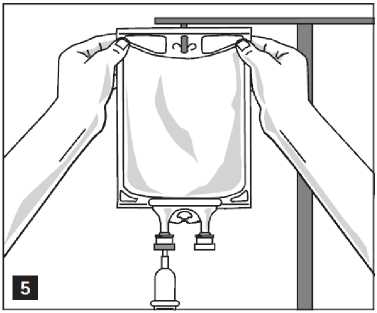
2. Hängen Sie den Beutel an einen Infusionsständer (Abbildung 5).
Zusätzliche Informationen:
Das Behältnis ist frei von PVC, DEHP und Latex.
7. INHABER DER ZULASSUNG
B. Braun Melsungen AG Carl-Braun-Straße 1 34212 Melsungen Deutschland
Postanschrift:
34209 Melsungen Deutschland
Telefon: +49-(0)-5661-71-0
Fax: +49-(0)-5661-4567
8. ZULASSUNGSNUMMER 89202.00.00
9. DATUM DER ERTEILUNG DER ZULASSUNG
07.11.2014
10. STAND DER INFORMATION
Januar 2014
11. VERKAUFSABGRENZUNG
Verschreibungspflichtig
11