Antelepsin 2Mg
FACHINFORMATION
1. BEZEICHNUNG DES ARZNEIMITTELS
Antelepsin 0,5 mg, Tabletten Antelepsin 2 mg, Tabletten
2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Antelepsin 0,5 mg
1 Tablette enthält 0,5 mg Clonazepam Antelepsin 2 mg
1 Tablette enthält 2 mg Clonazepam
Sonstige Bestandteile mit bekannter Wirkung:
Antelepsin 0,5 mg: 121,3 mg Lactose-Monohydrat pro Tablette.
Antelepsin 2mg: 121,4 mg Lactose-Monohydrat pro Tablette.
Vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt 6.1.
3. DARREICHUNGSFORM
Tablette
Antelepsin 0,5 mg
Rötlich-weiße, runde Tablette mit flacher Oberfläche und abgeschrägten Kanten. Auf der Vorderseitebefindet sich eine einfache Bruchkerbe, auf der Rückseite die Prägung „0.5“.
Die Tablette kann in gleiche Dosen geteilt werden.
Antelepsin 2 mg
Weiße, runde Tablette mit flacher Oberfläche und abgeschrägten Kanten. Auf der Vorderseite befindet sich eine einfache Bruchkerbe, auf der Rückseite die Prägung „2.0“.
Die Tablette kann in gleiche Dosen geteilt werden.
4. KLINISCHE ANGABEN
4.1 Anwendungsgebiete
Generalisierte Epilepsien vom Typ des Petit Mal, insbesondere bei Säuglingen, Kindern und Jugendlichen (z.B. West Syndrom, Lennox-Gastaut Syndrom) sowie bei Absence-Epilepsien und anderen myoklonischen Syndromen, wenn andere Antiepileptika nicht anwendbar sind oder alleine nicht ausreichen.
REM-Schlaf-Verhaltensstörung bei Erwachsenen
- wenn ein erhöhtes Verletzungsrisiko für den Patienten oder dessen Schlafpartner besteht oder
- bei Auftreten von furchterregenden Trauminhalten, die vom Patienten nicht toleriert werden können, oder
- wenn der Patient bedingt durch eine schlechte Schlafqualität in der Nacht während des Tages
beeinträchtigt ist.
4.2 Dosierung und Art der Anwendung
Dosierung
Die Dosierung von Antelepsin muss individuell angepasst werden und ist abhängig vom Alter des Patienten, der klinischen Reaktion und der Verträglichkeit.
Zur Vermeidung von Nebenwirkungen am Anfang der Behandlung ist es wichtig, mit niedrigen täglichen Dosen zu beginnen. Die Dosierung ist schrittweise bis zur Erreichung der für den Patienten notwendigen täglichen Erhaltungsdosis zu erhöhen. Die tägliche Erhaltungsdosis sollte im Verlauf von 2 bis 4 Behandlungswochen erreicht werden.
Generalisierte Epilepsien vom Typ des Petit Mal, Absence-Epilepsien, myoklonisches Syndrom Erwachsene
Initial werden 1 mg Clonazepam pro Tag verabreicht, ältere oder besonders empfindliche Patienten erhalten 0,5 mg Clonazepam pro Tag. Die initiale Tagesdosis wird auf 2 Einnahmen verteilt. Die Dosis kann etwa alle 3-5 Tage um 0,5-1 mg Clonazepam bis zur individuellen Erhaltungsdosis gesteigert werden. Die mittlere Erhaltungsdosis beträgt 4-8 mg Clonazepam/Tag. Eine Tagesdosis von 20 mg Clonazepam darf nicht überschritten werden. Bei älteren Patienten ist in der Regel eine niedrigere Dosierung ausreichend. Die Erhaltungsdosis ist auf 3-4 Einzelgaben über den Tag zu verteilen.
Kinder
Kinder erhalten eine Initialdosis von 0,01 mg/kg Körpergewicht pro Tag, die auf 2 Einnahmen verteilt und alle 3-5 Tage um 0,01 mg/kg/Tag erhöht wird. Mittlere Erhaltungsdosen betragen 0,1-0,2 mg/kg/Tag. Die Erhaltungsdosis ist auf 3-4 Einzelgaben über den Tag zu verteilen.
Für die Erhaltungsdosis können - in Abhängigkeit vom Alter - die in der Tabelle aufgeführten Richtlinien befolgt werden.
|
mittlere Tagesdosis in mg | |
|
Säuglinge |
0,5 - 1 |
|
Kleinkinder |
1,5 - 3 |
|
Kinder im Schulalter |
3 - 6 |
|
Erwachsene |
4 - 8 |
REM-Schlaf-Verhaltensstörung
Die Initialdosis beträgt 0,25-0,5 mg Clonazepam, die 120 bis 30 Minuten vor dem Schlafengehen verabreicht werden soll. Die Dosis kann etwa alle 3-5 Tage um 0,25-0,5 mg gesteigert werden. Die Tagesdosis von 2 mg darf dabei nicht überschritten werden.
Art der Anwendung
Die Tabletten sind unzerkaut mit etwas Flüssigkeit (z.B. einem Glas Wasser) einzunehmen. Die Tabletten sind halbierbar.
Die Epilepsiebehandlung ist eine Langzeitbehandlung.
Wie für alle antiepileptischen Mittel gilt auch für Antelepsin, dass seine Verabreichung nicht plötzlich beendet werden darf, sondern dass die Dosis schrittweise verringert werden muss (s. Pkt. 4.8).
4.3 Gegenanzeigen
Antelepsin darf nicht angewendet werden bei
- Überempfindlichkeit gegen den Wirkstoff, andere Benzodiazepine oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile
- bestehender oder früherer Abhängigkeitserkrankung (Medikamente, Drogen oder Alkohol)
- Myasthenia gravis.
4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung
Antelepsin darf nur unter besonderer Vorsicht angewendet werden bei
- spinalen oder cerebralen Ataxien
- akuter Vergiftung mit Alkohol, anderen Antiepileptika, Schlaf- oder Schmerzmitteln, sowie
- Psychopharmaka (Neuroleptika, Antidepressiva sowie Lithium)
- schwerer Leber- oder Nierenerkrankung
- akutem Engwinkelglaukom
- Schlafapnoe-Syndrom
- vorbestehender Erkrankung der Atmungsorgane (z.B. chronisch-obstruktive Lungenerkrankung)
- bekannter Fallneigung, die nicht durch REM-Schlaf-Verhaltensstörung bedingt ist
Spezifische Patientengruppen
Ältere Patienten
In der Literatur gibt es Hinweise, dass die Einnahme von Benzodiazepinen das Auftreten einer Demenz bei älteren Menschen begünstigen kann.
Sonstige Hinweise:
In höherem Lebensalter, bei vorbestehender Hirnschädigung sowie bei gleichzeitiger Behandlung mit anderen zentral wirksamen Medikamenten oder Antikonvulsiva (s. Pkt. 4.5) ist eine besonders sorgfältige individuelle Dosierung erforderlich.
Patienten mit Depressionen und/oder Suizidversuchen in der Vorgeschichte sollten unter engmaschiger Überwachung behandelt werden.
Suizidgedanken und suizidales Verhalten
Über suizidale Gedanken und suizidales Verhalten wurde bei Patienten, die mit Antiepileptika in verschiedenen Indikationen behandelt wurden, berichtet. Eine Metaanalyse randomisierter, placebokontrollierter Studien mit Antiepileptika zeigte auch ein leicht erhöhtes Risiko für das Auftreten von Suizidgedanken und suizidalem Verhalten. Der Mechanismus für die Auslösung dieser Nebenwirkung ist nicht bekannt und die verfügbaren Daten schließen die Möglichkeit eines erhöhten Risikos bei der Einnahme von Clonazepam nicht aus.
Deshalb sollten Patienten hinsichtlich Anzeichen von Suizidgedanken und suizidalen Verhaltensweisen überwacht und eine geeignete Behandlung in Erwägung gezogen werden. Patienten (und deren Betreuern) sollte geraten werden medizinische Hilfe einzuholen, wenn Anzeichen für Suizidgedanken oder suizidales Verhalten auftreten.
Sonstiger Bestandteil von Antelepsin
Patienten mit der seltenen hereditären Galactose-Intoleranz, Lactase-Mangel oder Glucose-Galactose-Malabsorption sollten Antelepsin nicht einnehmen.
Empfehlungen des Sachverständigenausschusses der Bundesregierung für den Arzt zur sachgerechten Anwendung von Benzodiazepin-haltigen Arzneimitteln
Benzodiazepine sind Arzneistoffe, die überwiegend zur vorübergehenden Behandlung schwerer Angstzustände, Schlafstörungen sowie zur Behandlung von Muskelverspannungen und Epilepsien eingesetzt werden. Nach bisherigen Erkenntnissen werden Benzodiazepine zu häufig und über eine zu lange Zeit verordnet, was zu einer Abhängigkeitsentwicklung führen kann. Dieses Risiko steigt mit der Höhe der Dosis und der Dauer der Anwendung an. Neben ihrem Abhängigkeitspotential haben Benzodiazepine weitere unerwünschte Arzneimittelwirkungen, z.B. Beeinträchtigung des Reaktionsvermögens, verstärktes Wiederauftreten der ursprünglichen Symptomatik nach Absetzen der Medikation (Rebound-Schlaflosigkeit, Rebound-Angst, delirante Syndrome, Krämpfe), Gedächtnisstörungen sowie neuropsychiatrische Nebenwirkungen. Sie können auch die pharmakokinetischen Eigenschaften anderer Arzneistoffe beeinflussen. Neben der Abhängigkeitsentwicklung gibt auch der Missbrauch von Benzodiazepinen seit längerem Anlass zur Besorgnis.
Deshalb sind von den verordnenden Ärzten die folgenden Richtlinien zu beachten, die unter Berücksichtigung von Veröffentlichungen der Arzneimittelkommission der Deutschen Ärzteschaft und der Arbeitsgemeinschaft Neuropsychopharmakologie und Pharmakopsychiatrie formuliert wurden:
1. Sorgfältige Indikationsstellung!
2. Bei Patienten mit einer Abhängigkeitsanamnese ist besondere Vorsicht geboten. In der Regel keine
Verschreibung.
3. In der Regel kleinste Packungseinheit verordnen.
4. In möglichst niedriger, aber ausreichender Dosierung verordnen. Dosis möglichst frühzeitig
reduzieren bzw. Dosierungsintervall in Abhängigkeit von der Wirkungsdauer vergrößern.
5. Therapiedauer vor Behandlungsbeginn mit dem Patienten vereinbaren und Behandlungsnotwendigkeit
in kurzen Zeitabständen überprüfen. Eine Therapiedauer von länger als zwei Monaten ist wegen des mit der Dauer der Benzodiazepineinnahme steigenden Risikos einer Abhängigkeitsentwicklung nur in begründeten Ausnahmefällen möglich. Es gibt Abhängigkeit auch ohne Dosissteigerung sowie die sogenannte „Niedrigdosis-Abhängigkeit“!
6. Innerhalb der Therapiedauer möglichst frühzeitig schrittweise Dosisreduktion (Ausschleichen) bzw.
Vergrößerung des Dosierungsintervalls, um Entzugssymptome, wie z.B. Unruhe, Angst, Schlafstörungen, delirante Syndrome oder Krampfanfälle zu vermeiden.
7. Aufklärung des Patienten, dass Benzodiazepine keinesfalls an Dritte weiterzugeben sind.
8. Verordnungen von Benzodiazepinen sollten vom Arzt stets eigenhändig ausgestellt und dem Patienten
persönlich ausgehändigt werden.
9. Beachtung der Fach- und Gebrauchsinformation sowie der einschlägigen wissenschaftlichen
Veröffentlichungen.
10. Alle Abhängigkeitsfälle über die jeweiligen Arzneimittelkommissionen der Kammern der Heilberufe
dem Bundesinstitut für Arzneimittel und Medizinprodukte zur Kenntnis bringen.
4.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen
Clonazepam kann gleichzeitig mit einem oder mehreren antiepileptischen Mitteln verabreicht werden. In diesem Fall muss die Dosierung jedes einzelnen Mittels angepasst werden, um einen optimalen Effekt zu erzielen.
Gleichzeitig verabreichte enzyminduzierende Medikamente wie z.B. Barbiturate, Phenytoin und Carbamazepin können die Metabolisierung von Clonazepam beschleunigen, ohne seine Proteinbindung zu beeinflussen. Dagegen scheint Clonazepam selbst keine Induktion seiner metabolisierenden Enzyme zu bewirken. Bei gleichzeitiger Behandlung mit Phenytoin oder mit Primidon wurde vereinzelt ein Anstieg des Phenytoin- bzw. des Primidonspiegels im Serum beobachtet.
Die Kombination von Clonazepam mit Valproinsäure kann gelegentlich zur Ausbildung eines Petit-malStatus führen. Bei gleichzeitiger Anwendung mit anderen zentral wirksamen Medikamenten, wie z.B. weitere Antikonvulsiva, Narkosemittel, Schlafmittel, Psychopharmaka, teils auch Schmerzmittel, kann es zu einer gegenseitigen Verstärkung der Wirkungen kommen. Dies gilt insbesondere im Zusammenwirken mit Alkohol. Für Patienten, die wegen einer Epilepsie mit Clonazepam behandelt werden, besteht absolutes Alkoholverbot, da Alkohol die Wirkung von Clonazepam verändern, den Behandlungserfolg beeinträchtigen bzw. unvorhersehbare Nebenwirkungen hervorrufen kann.
4.6 Fertilität, Schwangerschaft und Stillzeit
Bevor eine Behandlung mit Antiepileptika bei Frauen im gebärfähigen Alter begonnen wird, sollte der Rat eines Spezialisten eingeholt werden.
Wenn eine Frau plant schwanger zu werden, sollte die Notwendigkeit einer antiepileptischen Therapie überdacht werden. Wenn die Behandlung mit Antiepileptika als unverzichtbar erachtet wird, sollten die im Folgenden beschriebenen Vorsichtsmaßnahmen berücksichtigt werden, um das potenzielle teratogene Risiko zu minimieren.
Schwangerschaft
Risiken, die mit der Epilepsie und mit Antiepileptika im Allgemeinen in Verbindung gebracht werden, basieren auf Erfahrungen behandelter Schwangerer.
Es konnte gezeigt werden, dass die Rate von Missbildungen bei Nachkommen von Müttern, die unter Epilepsie leiden und antiepileptisch behandelt werden, 2- bis 3-mal höher ist als die Rate (etwa 3 %), die von der Gesamtpopulation berichtet wird.
Die Missbildungen betreffen am häufigsten Lippen-Gaumen-Spalten, kardiovaskuläre Fehlbildungen und Neuralrohrdefekte.
Eine Kombinationstherapie mit verschiedenen Antiepileptika ist im Vergleich zur Monotherapie mit einem höheren Risiko für kongenitale Fehlbildungen verbunden. Deshalb sollte, wenn möglich, eine Monotherapie durchgeführt werden.
Selten wurden Entwicklungsverzögerungen bei Kindern, die von Müttern geboren wurden, die an Epilepsie litten, beobachtet. Eine Differenzierung, ob genetische Faktoren, soziale Umweltfaktoren, die mütterliche Epilepsie oder die antiepileptische Behandlung diesen Entwicklungsverzögerungen zu Grunde liegen, ist nicht möglich.
Trotz der möglichen Risiken sollte die Behandlung mit Antiepileptika während der Schwangerschaft nicht ohne ärztliche Zustimmung unterbrochen werden, da ein plötzlicher Therapieabbruch bzw. eine unkontrollierte Verminderung der Dosis zu epileptischen Anfällen führen können, welche ernste Konsequenzen für beide, die Mutter und den Fötus, haben könnten.
Risiken, die mit Clonazepam in Verbindung gebracht werden
Falls einer Patientin im reproduktionsfähigen Alter Clonazepam verschrieben wird, sollte diese darauf hingewiesen werden, sich unverzüglich mit ihrem Arzt in Verbindung zu setzen, wenn sie schwanger zu werden wünscht oder eine Schwangerschaft vermutet. Clonazepam sollte während der Schwangerschaft nur bei zwingender Indikation und, besonders im ersten Trimenon, in der niedrigsten anfallskontrollierenden Dosis verordnet werden.
Das Missbildungsrisiko scheint beim Menschen nach Einnahme therapeutischer Dosen von Benzodiazepinen in der Frühschwangerschaft gering zu sein, obwohl einige epidemiologische Studien Anhaltspunkte für ein erhöhtes Risiko für Gaumenspalten ergaben.
Es liegen Fallberichte über Fehlbildungen und geistige Retardierung von pränatal exponierten Kindern nach Überdosierung oder Vergiftung mit Benzodiazepinen vor.
Risiken für Neugeborene
Die Neugeborenen von Frauen, die während der Schwangerschaft längere Zeit Benzodiazepine eingenommen haben, können eine körperliche Abhängigkeit entwickeln. Diese Kinder zeigen Entzugssymptome in der Postpartalphase.
Wenn Clonazepam aus zwingenden Gründen in hohen Dosen während der Spätschwangerschaft oder während der Geburt verabreicht wird, sind Auswirkungen auf das Neugeborene wie Ateminsuffizienz, Hypothermie, Hypotonie und Trinkschwäche (floppy infant syndrome) zu erwarten.
Stillzeit
Clonazepam geht in die Muttermilch über; nach wiederholter Gabe muss mit einer Akkumulation gerechnet werden. Daher sollte Clonazepam in der Stillzeit nicht angewendet werden. Wenn eine wiederholte oder hohe Dosierung von Clonazepam in der Stillzeit zwingend indiziert ist, ist abzustillen.
4.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen
Antelepsin hat großen Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen. Clonazepam kann auch bei bestimmungsgemäßem Gebrauch das Reaktionsvermögen so weit verändern, dass die Fähigkeit zur aktiven Teilnahme am Straßenverkehr oder zum Bedienen von Maschinen erheblich beeinträchtigt wird. Dies gilt in verstärktem Maße im Zusammenwirken mit Alkohol. Deshalb sollten das Führen von Fahrzeugen, die Bedienung von Maschinen oder sonstige gefährliche Tätigkeiten ganz, zumindest jedoch während der ersten Tage der Behandlung unterbleiben.
Die Entscheidung trifft in jedem Einzelfall der behandelnde Arzt unter Berücksichtigung der individuellen Reaktion und der jeweiligen Dosierung.
4.8 Nebenwirkungen
Bei den Häufigkeitsangaben zu Nebenwirkungen werden folgende Kategorien zugrunde gelegt:
sehr häufig (> 1/10) häufig (> 1/100 bis < 1/10) gelegentlich (> 1/1.000 bis < 1/100) selten (> 1/10.000 bis < 1/1.000) sehr selten (< 1/10.000)
nicht bekannt (Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar)
Mit folgenden Nebenwirkungen ist häufig zu rechnen:
Müdigkeit, Schläfrigkeit, Mattigkeit, verminderter Muskeltonus, Schwindelgefühl, Benommenheit,
Ataxie. Diese Erscheinungen sind im Allgemeinen vorübergehend und verschwinden meist spontan oder nach Dosisreduktion. Sie können auch durch eine langsame Steigerung der Dosis zu Behandlungsbeginn zum Teil verhindert werden.
Erkrankungen des Blutes und des Lymphsystems Gelegentlich: Thrombozytopenie
Erkrankungen des Immunsvstems Sehr selten: anaphylaktischer Schock
Endokrine Erkrankungen
Sehr selten: rückbildungsfähige vorzeitige Entwicklung der Geschlechtsmerkmale bei Kindern (inkomplette Pubertas praecox)
Psychiatrische Erkrankungen Gelegentlich: Libidoverlust
Nicht bekannt: Desorientierung, Angstzustände, Unruhe und Nervosität, Erregbarkeit, Reizbarkeit, aggressives Verhalten sowie Schlafstörungen, Alpträume und lebhafte Träume
Durch Clonazepam können Depressionen ausgelöst werden, die jedoch auch mit der Grunderkrankung im Zusammenhang stehen können.
Erkrankungen des Nervensystems
Häufig: Ataxie, verminderter Muskeltonus, Schwindelgefühl, Schläfrigkeit und Benommenheit Gelegentlich: Kopfschmerzen
Nicht bekannt: Anterograde Amnesie, verlängerte Reaktionszeit und Konzentrationsstörungen Insbesondere bei Langzeitbehandlung und bei hoher Dosierung können reversible Störungen wie Dysarthrie und Nystagmus auftreten.
In der Literatur gibt es Hinweise, dass die Einnahme von Benzodiazepinen das Auftreten einer Demenz bei älteren Menschen begünstigen kann.
Augenerkrankungen
Eine reversible Diplopie (Doppeltsehen) ist insbesondere bei Langzeitbehandlung und bei hoher Dosierung möglich.
Erkrankungen der Atemwege, des Brustraums und des Mediastinums Gelegentlich: Kehlkopfödem und Brustschmerzen Sehr selten: Atemdepression
Die atemdepressive Wirkung kann bei Atemwegsobstruktion und bei vorbestehender Hirnschädigung verstärkt in Erscheinung treten, oder wenn andere atemdepressiv wirkende Medikamente verabreicht wurden. Sie lässt sich in der Regel durch sorgfältige und individuelle Einstellung der Dosis vermeiden. Clonazepam kann bei Säuglingen und Kleinkindern zu vermehrtem Speichelfluss und zu Bronchialhypersekretion führen, weshalb auf die Freihaltung der Atemwege geachtet werden muss.
Erkrankungen des Gastrointestinaltrakts Gelegentlich: Übelkeit und epigastrischen Beschwerden
Erkrankungen der Haut und des Unterhautzellgewebes
Gelegentlich: Angioödem, Urtikaria, Pruritus, Hautausschlag, vorübergehender Haarausfall und Pigmentverschiebung
Erkrankungen der Nieren und Harnwege Gelegentlich: Harninkontinenz
Erkrankungen der Geschlechtsorgane und der Brustdrüse Gelegentlich: Impotenz
Allgemeine Erkrankungen und Beschwerden am Verabreichungsort Häufig: Müdigkeit und Mattigkeit
Toleranzentwicklung und Abhängigkeitspotential
Eine Toleranzentwicklung ist nach längerdauernder Anwendung möglich, dabei können erneut Anfälle auftreten.
Die Behandlung mit Benzodiazepinen wie Clonazepam kann zur psychischen und/oder physischen Abhängigkeit führen. Das Risiko ist größer nach hohen Dosen und Langzeitverabreichung und insbesondere bei Patienten mit Alkoholismus, Drogenabhängigkeit, auffälligen Persönlichkeitsmerkmalen oder anderen schweren seelischen Erkrankungen in der Vorgeschichte.
Durch plötzliches Absetzen können Entzugserscheinungen auftreten. Die Dauer ist unterschiedlich und reicht von wenigen Stunden bis zu einer Woche oder länger. In weniger schweren Fällen bleiben die Erscheinungen auf Zittern, Unruhe, Schlafstörungen, Angst, Kopfschmerzen und Konzentrationsschwäche beschränkt. Es können jedoch auch Erscheinungen wie Schwitzen, Muskel- und Magen-Darm-Krämpfe, epileptische Anfälle, die mit der zugrunde liegenden Erkrankung zusammenhängen, Wahrnehmungsstörungen und in seltenen Fällen Delirium und schwere Krampfzustände auftreten. Beim Auftreten von Entzugserscheinungen ist ärztliche Betreuung des Patienten erforderlich. Plötzliches Absetzen sollte vermieden und die Behandlung mit ausschleichenden Dosen beendet werden.
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung dem
Bundesinstitut für Arzneimittel und Medizinprodukte, Abt. Pharmakovigilanz, Kurt-Georg-Kiesinger Allee 3, D-53175 Bonn, Website: http://www.bfarm.de anzuzeigen.
4.9 Überdosierung
Symptome, Notfallmaßnahmen. Gegenmittel
a) Symptome der Intoxikation
Die Symptome einer Überdosierung oder Intoxikation sind in Abhängigkeit von Alter, Körpergewicht und individueller Reaktion sehr unterschiedlich ausgeprägt. Sie reichen von Müdigkeit, Benommenheit über Ataxie, Somnolenz, Sopor bis zum Koma mit Atemdepression und Kreislaufkollaps.
b) Therapie von Intoxikationen
Neben der Kontrolle von Atmung, Pulsfrequenz und Blutdruck sind Magenspülungen, i.v. Flüssigkeitsersatz sowie allgemeine unterstützende Maßnahmen und die Vorbereitung von Notfallmaßnahmen für eventuell eintretende Atemwegsobstruktionen indiziert. Hypotension kann mit Sympathomimetika behandelt werden.
Warnhinweise:
Die Anwendung des Benzodiazepinantagonisten Flumazenil ist nicht angezeigt bei Patienten mit Epilepsie, die Benzodiazepine zur Behandlung erhalten. Die Antagonisierung der Benzodiazepine kann bei solchen Patienten zu Konvulsionen führen.
5. PHARMAKOLOGISCHE EIGENSCHAFTEN
5.1 Pharmakodynamische Eigenschaften
Pharmakotherapeutische Gruppe: Benzodiazepin-Derivate ATC-Code: N03AE01
Clonazepam besitzt wie andere Benzodiazepine beruhigende, schlafanstoßende, anxiolytische, muskelrelaxierende und antikonvulsive Eigenschaften. Die antikonvulsive Wirkung ist stärker ausgeprägt als die anderen Wirkungsqualitäten. Der Wirkungsmechanismus besteht in der Verstärkung der im ZNS natürlicherweise vorhandenen Hemm-Mechanismen, an denen der Neurotransmitter GABA (y-Aminobuttersäure) beteiligt ist.
5.2 Pharmakokinetische Eigenschaften
Nach oraler Gabe von Clonazepam wird die maximale Plasmakonzentration durchschnittlich nach 2 bis 3 Stunden erreicht. Die Verteilungshalbwertszeit von Clonazepam beträgt im Mittel 1,7 Stunden. Der Steady state wird nach 4 bis 6 Tagen erreicht. Von der oral applizierten Dosis werden ca. 50% renal, 9 bis 26% mit den Fäzes ausgeschieden.
Die Eliminationshalbwertszeit für Clonazepam beträgt 30 bis 40 Stunden. Als Hauptmetaboliten entstehen das 7-Amino-Derivat, das 7-Acetamino-Derivat und geringe Mengen des 3-Hydroxy-Derivates, wobei diese Metaboliten keine klinisch relevante pharmakologische Aktivität zeigen. Die Plasmaproteinbindung beträgt 83 bis 87%.
Eine im Jahr 1998 durchgeführte Bioverfügbarkeitsstudie an 18 männlichen Probanden im Alter von 24 bis 42 Jahren ergab nach Verabreichung einer Einzelgabe von 4 Tabletten Antelepsin 0,5 mg im Vergleich zum Referenzpräparat folgende Werte:
Antelepsin 0,5 mg
|
Antelepsin 0,5 mg |
Referenzpräparat | |
|
maximale Plasmakonzentration Cmax [ng/ml] |
8,85 ± 2,03 |
11,1 ± 2,48 |
|
Zeitpunkt der maximalen Plasmakonzentration tmax [h] |
2,06 ± 1,30 |
1,47 ± 0,71 |
|
Fläche unter der KonzentrationsZeit-Kurve AUC0-^ [ngxh/ml] |
390 ± 71,6 |
433 ± 62,0 |
Angabe der Werte als Mittelwerte und Standardabweichung
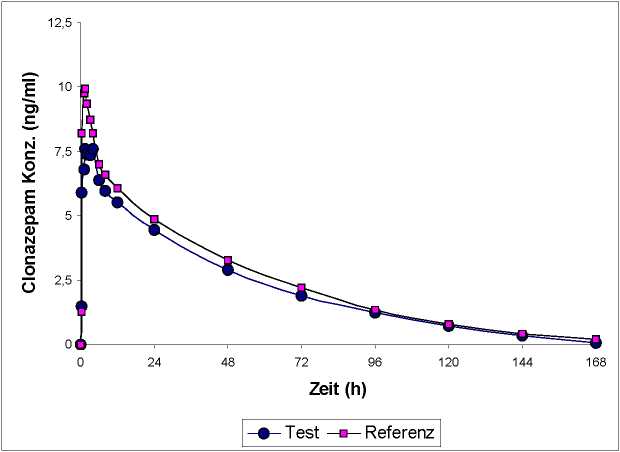
Die Kurven zeigen die mittleren Clonazepam-Plasmakonzentrationen von 18 gesunden Probanden nach Einnahme von 4 Tabletten Antelepsin 0,5 mg bzw. 4 Tabletten eines Referenzpräparates mit 0,5 mg Clonazepam unter standardisierten Ernährungsbedingungen.
Antelepsin 2 mg
Eine im Jahr 1998 durchgeführte Bioverfügbarkeitsstudie an 18 männlichen Probanden im Alter von 21 bis 38 Jahren ergab nach Verabreichung einer Einzelgabe von 1 Tablette Antelepsin 2 mg im Vergleich zum Referenzpräparat folgende Werte:
|
Antelepsin2 mg |
Referenzpräparat | |
|
maximale Plasmakonzentration Cmax [ng/ml] |
8,94 ± 1,62 |
9,36 ± 2,15 |
|
Zeitpunkt der maximalen Plasmakonzentration tmax [h] |
2,24 ± 1,51 |
2,23 ± 1,37 |
|
Fläche unter der KonzentrationsZeit-Kurve AUC0-^ [ngxh/ml] |
388 ± 79,8 |
413 ± 87,2 |
Angabe der Werte als Mittelwerte und Standardabweichung
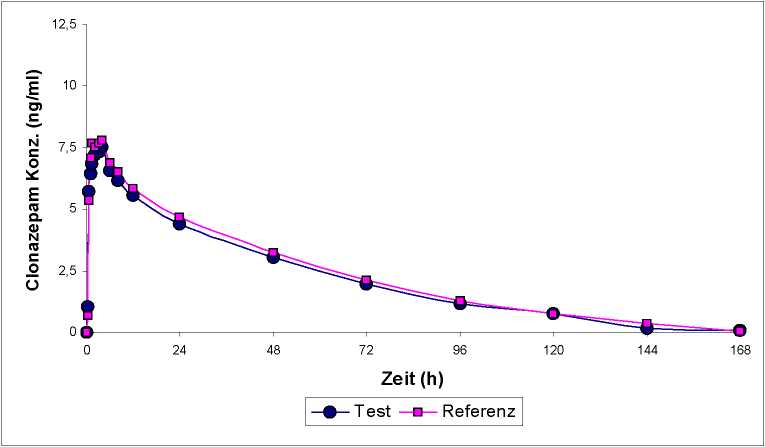
Die Kurven zeigen die mittleren Clonazepam-Plasmakonzentrationen von 18 gesunden Probanden nach Einnahme von 1 Tablette Antelepsin 2 mg bzw. 1 Tablette eines Referenzpräparates mit 2 mg Clonazepam unter standardisierten Ernährungsbedingungen.
Unter den gewählten Bedingungen konnte Bioäquivalenz von Antelepsin 0,5 mg und Antelepsin 2 mg zum Referenzpräparat in Bezug auf Ausmaß und Geschwindigkeit der Resorption nachgewiesen werden.
5.3 Präklinische Daten zur Sicherheit
In Untersuchungen zur chronischen Toxizität wurden nach hohen Dosen Leberenzymerhöhung, Lebergewichtserhöhung und Fetteinlagerung in der Leber beobachtet.
In-vitro- und In-vivo-Untersuchungen ergaben keine Hinweise auf eine Genotoxizität von Clonazepam.
Langzeituntersuchungen zum kanzerogenen Potential von Clonazepam liegen nicht vor.
In Studien zur Reproduktionstoxizität ergaben sich Anhaltspunkte für teratogene Effekte bei Mäusen, jedoch nicht bei Ratten und Kaninchen. Die Gabe von Clonazepam in der Spätträchtigkeit führte bei Ratten zu einer langdauernden Suppression der zellulären Immunantwort der Nachkommen. Es gibt Hinweise auf Verhaltensstörungen der Nachkommen von benzodiazepinexponierten Muttertieren.
6. PHARMAZEUTISCHE ANGABEN
6.1 Liste der sonstigen Bestandteile
Mikrokristalline Cellulose Lactose-Monohydrat Magnesiumstearat (Ph.Eur.)
Maisstärke
Antelepsin 0,5 mg zusätzlich Eisenoxid rot (E 172)
6.2 Inkompatibilitäten
Nicht zutreffend
6.3 Dauer der Haltbarkeit
3 Jahre
6.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung
Keine
6.5 Art und Inhalt des Behältnisses
50, 100 oder 200 Tabletten abgepackt in Polypropylen/Alu-Blisterpackungen Klinikpackung 500 (10x50) Tabletten
Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht.
6.6 Besondere Vorsichtsmaßnahmen für die Beseitigung
Keine besonderen Anforderungen für die Beseitigung.
7. INHABER DER ZULASSUNG
DESITIN ARZNEIMITTEL GMBH Weg beim Jäger 214 22335 Hamburg Telefon: (040) 5 91 01-525 Telefax: (040) 5 91 01-377
8. ZULASSUNGSNUMMER(N)
Antelepsin 0,5 mg: 45191.00.00 Antelepsin 2 mg: 45191.01.00
9. DATUM DER ERTEILUNG DER ZULASSUNG/VERLÄNGERUNG DER ZULASSUNG
Antelepsin 0,5 mg:
Datum der Erteilung der Zulassung 26.Juli 2001
Datum der letzten Verlängerung der Zulassung 19. November 2008
Antelepsin 2 mg:
Datum der Erteilung der Zulassung 26.Juli 2001
Datum der letzten Verlängerung der Zulassung 19.November 2008
10. STAND DER INFORMATION
{MM.JJJJ}
11. VERKAUFSABGRENZUNG
Verschreibung spflichtig
- 12 -