Capros 60Mg
F achinformation
(Zusammenfassung der Merkmale des Arzneimittels / SPC)
1. BEZEICHNUNG DES ARZNEIMITTELS
Capros 10 mg Hartkapsel, retardiert Capros 30 mg Hartkapsel, retardiert Capros 60 mg Hartkapsel, retardiert Capros 100 mg Hartkapsel, retardiert
2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
1 Hartkapsel, retardiert enthält 10 / 30 / 60 / 100 mg Morphinsulfat entsprechend 7,5 / 22,6 / 45,1 / 75,2 mg Morphin.
Sonstiger Bestandteil mit bekannter Wirkung:
1 Hartkapsel Capros 10 mg / 30 mg / 60 mg / 100 mg enthält 8,9 mg / 26,7 mg / 53,3 mg / 88,8 mg Sucrose.
Vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt 6.1.
3. DARREICHUNGSFORM
Hartkapsel, retardiert
Capros 10 mg Hartkapseln, retardiert, sind undurchsichtig dunkelgelb mit dem Aufdruck „Capros 10 mg“ auf der Kapselhülle.
Capros 30 mg Hartkapseln, retardiert, sind hellblau mit dem Aufdruck „Capros 30 mg“ auf der Kapselhülle.
Capros 60 mg Hartkapseln, retardiert, sind durchsichtig farblos mit dem Aufdruck „Capros 60 mg“ auf der Kapselhülle.
Capros 100 mg Hartkapseln, retardiert, sind undurchsichtig weiß mit dem Aufdruck „Capros 100 mg“ auf der Kapselhülle.
4. KLINISCHE ANGABEN
4.1 Anwendungsgebiete
Starke und stärkste Schmerzen.
4.2 Dosierung und Art der Anwendung
Dosierung
Initial wird die Behandlung mit einem nicht retardierten Morphin (Tablette oder Lösung) begonnen, um diejenige Dosis zu ermitteln, mit der eine angemessene Schmerzkontrolle erzielt wird. Danach wird der Patient auf die entsprechende Tagesdosis Capros 10 / 30 / 60 / 100 mg umgestellt. Weiter bestehende Schmerzen (Durchbruchschmerzen) sind mit einer unretardierten Darreichungsform von Morphin (Tablette oder Lösung) zu behandeln.
Retardiertes Morphin wird in der Regel in einem 12-Stunden-Intervall eingenommen. Dabei hängt die Dosierung von der Schwere der Schmerzen sowie vom Alter des Patienten und dessen bisherigem Analgetikabedarf ab.
Erwachsene und Jugendliche ab 12 Jahren:
1 Hartkapsel, retardiert Capros 10 mg 2-mal täglich (entsprechend 15 mg Morphin/Tag).
1 Hartkapsel, retardiert Capros 30 mg 2-mal täglich (entsprechend 45 mg Morphin/Tag).
1 Hartkapsel, retardiert Capros 60 mg 2-mal täglich (entsprechend 90 mg Morphin/Tag).
1 Hartkapsel, retardiert Capros 100 mg 2-mal täglich (entsprechend 150 mg Morphin/Tag).
Leber- oder Nierenfunktionsstörungen
Bei Patienten mit Leber- oder Nierenfunktionsstörungen sowie bei Verdacht auf verzögerte MagenDarm-Passage soll Capros 10 / 30 / 60 / 100 mg besonders vorsichtig dosiert werden.
Ältere Patienten
Patienten im höheren Lebensalter (im Regelfall ab 75 Jahren) und Patienten mit schlechtem körperlichem Allgemeinzustand können empfindlicher auf Morphin reagieren. Daher ist darauf zu achten, dass die Dosiseinstellung vorsichtiger erfolgt und/oder längere Dosisintervalle zu wählen sind. Ggf. ist auf geringere Wirkstoffstärken auszuweichen.
Kinder
Für Kinder unter 12 Jahren ist Capros 100 mg im Allgemeinen nicht geeignet, da der Wirkstoffgehalt zu hoch ist.
Darüber hinaus liegen zur Anwendung von Dosisstärken mit weniger als 100 mg Morphin bei Kindern unter 12 Jahren keine ausreichend dokumentierten Erfahrungen vor.
Besondere Hinweise zur Dosiseinstellung:
Zur ersten Dosiseinstellung sollten schnell freisetzende Morphinzubereitungen genutzt werden. Für eine Neueinstellung der Dosis kommen ggf. Darreichungsformen mit geringerem Wirkstoffgehalt zur Anwendung, eventuell auch zusätzlich zu einer bestehenden Therapie mit Retardtabletten.
Patienten, die von einer parenteralen Morphintherapie auf Morphin Retardtabletten umgestellt werden, müssen unter Berücksichtigung der individuell unterschiedlichen Empfindlichkeit vorsichtig behandelt werden, d.h. der Tagesbedarf darf nicht überschätzt werden.
Patienten mit schweren Schmerzen sollten im Regelfall mit 10 - 30 mg Morphinsulfat / Morphinhydrochlorid alle 12 Stunden beginnen, wobei Patienten mit geringem Körpergewicht (< 70 kg KG) eine niedrige Initialdosis benötigen.
Bei sich verstärkender Schmerzsymptomatik ist eine höhere Morphindosis erforderlich. Individuell optimal eingestellt ist die Dosierung dann, wenn ohne Nebenwirkungen, bzw. wenn diese zu vertreten sind, für die Dauer von 12 Stunden Schmerzlinderung erzielt wird.
Grundsätzlich sollte eine ausreichend hohe Dosis gegeben werden und gleichzeitig die im Einzelfall kleinste schmerzlindernd wirksame Dosis angestrebt werden.
Bei der Behandlung chronischer Schmerzen ist der Dosierung nach einem festen Zeitplan der Vorzug zu geben.
Bei Patienten, die einer anderen zusätzlichen Schmerztherapie (z. B. Operation, Plexusblockade) unterzogen werden, ist nach der Maßnahme die Dosis neu einzustellen.
Art der Anwendung
Die Hartkapseln, retardiert sind unzerkaut, unzerkleinert und ungeteilt mit ausreichend Flüssigkeit -unabhängig von den Mahlzeiten - einzunehmen, wobei sich die Einnahme morgens und abends empfiehlt.
Bei allen Patienten, die die Kapsel nicht schlucken können, kann der Inhalt der geöffneten Kapsel mit einer kleinen Menge Joghurt, Apfelmus, Marmelade eingerührt oder über Sonden (Durchmesser > 16 FG) verabreicht werden. Die Mischung sollte spätestens 30 Minuten nach der Zubereitung gefolgt von 30 -50 ml Wasser gegeben werden. Die Kügelchen selbst dürfen nicht gekaut oder zerdrückt werden.
Der Mund sollte ausgespült werden, um sicher zu sein, dass der gesamte Kapselinhalt geschluckt worden ist.
Über die Dauer der Behandlung entscheidet der Arzt in Abhängigkeit von den Schmerzbeschwerden. Capros 10 / 30 / 60 / 100 mg sollte auf keinen Fall länger als unbedingt notwendig angewendet werden. Wenn entsprechend Art und Schwere der Erkrankung eine länger dauernde Schmerzbehandlung mit Capros 10 / 30 / 60 / 100 mg erforderlich erscheint, sollte eine sorgfältige und in kurzen Abständen regelmäßige Überprüfung erfolgen (ggf. durch Anwendungspausen), ob und inwieweit ein medizinisches Erfordernis weiter besteht. Gegebenenfalls ist auf geeignetere Darreichungsformen auszuweichen. Bei chronischen Schmerzzuständen ist einem festen Dosierungsschema der Vorzug zu geben.
Da das Risiko des Auftretens von Entzugserscheinungen bei plötzlichem Behandlungsabbruch größer ist, sollte die Dosierung nach Absetzen der Behandlung schrittweise verringert werden.
4.3 Gegenanzeigen
• Überempfindlichkeit gegen den Wirkstoff oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile
• Ileus
• akutes Abdomen
4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung
Eine besonders sorgfältige ärztliche Überwachung und ggf. Dosisreduktion ist erforderlich bei:
• Abhängigkeit von Opioiden,
• Bewusstseinsstörungen,
• Krankheitszuständen, bei denen eine Störung des Atemzentrums und der Atemfunktion vorliegt oder vermieden werden muss,
• Cor pulmonale,
• Zuständen mit erhöhtem Himdruck, wenn nicht eine Beatmung durchgeführt wird,
• Hypotension bei Hypovolämie,
• Prostatahyperplasie mit Resthambildung (Gefahr der Blasenruptur durch Hamverhalten),
• Hamwegsverengungen oder Koliken der Hamwege,
• Gallenwegserkrankungen,
• obstruktiven und entzündlichen Darmerkrankungen,
• Phäochromozytom,
• Pankreatitis,
• Hypothyreose,
• epileptischen Anfallsleiden oder erhöhter Neigung zu Krampfanfällen.
Um die Retardierung der in den Kapseln enthaltenen Granula nicht zu beeinträchtigen, müssen die Kapseln bzw. ihr Inhalt als Ganzes geschluckt werden und dürfen nicht zerteilt, zerkaut oder zerrieben werden. Die Anwendung zerteilter, zerkauter oder zerriebener Granula führt zu einer schnellen Wirkstofffreisetzung und zur Resorption einer möglicherweise letalen Dosis von Morphin (siehe Abschnitt 4.9).
Capros 10 / 30 / 60 / 100 mg ist nur für den oralen Gebrauch bestimmt. Eine missbräuchliche parenterale Verabreichung von Capros 10 / 30 / 60 / 100 mg kann wegen der Bestandteile (insbesondere von Talkum) zu schwerwiegenden, potentiell letalen unerwünschten Ereignissen (z. B. Lungengranulomen) führen.
Eine Atemdepression ist die bedeutsamste Gefährdung einer Opioidüberdosierung.
Bei gleichzeitiger Einnahme von Alkohol und Capros 10 / 30 / 60 / 100 mg können vermehrt Nebenwirkungen von Capros 10 / 30 / 60 / 100 mg auftreten. Die gleichzeitige Einnahme sollte vermieden werden.
Die Anwendung von Morphin kann zur Entwicklung körperlicher Abhängigkeit führen. Das Absetzen nach wiederholter Anwendung oder Applikation eines Opiatantagonisten kann ein typisches Entzugsbild (Entzugssyndrom) auslösen.
Bei bestimmungsgemäßer Anwendung bei chronischen Schmerzpatienten ist das Risiko psychischer Abhängigkeit deutlich reduziert bzw. differenziert zu bewerten.
Capros 10 / 30 / 60 / 100 mg wird präoperativ und innerhalb 24 Stunden postoperativ wegen des gegenüber Nichtoperierten in der postoperativen Phase höheren Risikos eines Ileus oder einer Atemdepression nicht empfohlen.
Aufgrund der analgetischen Wirkung von Morphin können schwerwiegende intraabdominelle Komplikationen wie eine Darmperforation maskiert werden.
Bei bestehender Nebennierenrindeninsuffizienz (z. B. Morbus Addison) sollte die Plasmakortisolkonzentration kontrolliert und gegebenenfalls Kortikoide substituiert werden.
Wegen der mutagenen Eigenschaften von Morphin sollte dieser Wirkstoff Männern und Frauen im zeugungs- bzw. gebärfähigen Alter nur dann verabreicht werden, wenn eine wirksame Verhütung sichergestellt ist (siehe Abschnitt 4.6)
Die Anwendung von Capros 10 / 30 / 60 / 100 mg kann bei Dopingkontrollen zu positiven Ergebnissen führen.
Patienten mit der seltenen hereditären Fructose-Intoleranz, Glucose-Galactose-Malabsorption oder Saccharase-Isomaltase-Mangel sollten Capros 10 / 30 / 60 / 100 mg nicht einnehmen.
4.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen
Folgende Wechselwirkungen dieses Arzneimittels müssen beachtet werden:
Die gleichzeitige Anwendung von Morphin und anderen zentral dämpfend wirkenden Arzneimitteln wie Tranquilizer, Anästhetika, Hypnotika und Sedativa, Neuroleptika, Barbiturate, Antidepressiva, Antihistaminika/Antiemetika und anderer Opioide kann zu einer Verstärkung der Nebenwirkungen von Morphin bei üblicher Dosierung führen. Dies betrifft insbesondere die Möglichkeit einer Atemdepression, Sedierung, Hypotonie oder auch eines Komas.
Alkohol kann die pharmakodynamischen Effekte von Capros 10 / 30 / 60 / 100 mg verstärken. Die gleichzeitige Einnahme sollte vermieden werden. Arzneimittel mit anticholinerger Wirkung (z. B. Psychopharmaka, Antihistaminika, Antiemetika, Arzneimittel bei Morbus Parkinson) können anticholinerge Nebenwirkungen von Opioiden verstärken (z. B. Obstipation, Mundtrockenheit oder Störungen beim Wasserlassen).
Durch Cimetidin und andere den Leberstoffwechsel belastende Arzneimittel können durch Hemmung des Abbaus erhöhte Plasmakonzentrationen von Morphin auftreten.
Durch Morphin kann die Wirkung von Muskelrelaxantien verstärkt werden.
Bei Vorbehandlung von Patienten mit bestimmten Antidepressiva (MAO-Hemmstoffen) innerhalb der letzten 14 Tage vor der Opioid-Anwendung sind lebensbedrohende Wechselwirkungen auf Zentralnervensystem, Atmungs- und Kreislauffunktion mit Pethidin beobachtet worden. Dies ist auch mit Morphin nicht auszuschließen.
Bei gleichzeitiger Anwendung von Rifampicin kann es zu einer Abschwächung der Morphinwirkung kommen.
4.6 Fertilität, Schwangerschaft und Stillzeit
Schwangerschaft
Beim Menschen liegen keine ausreichenden Daten vor, die die Bewertung eines möglichen teratogenen Risikos erlauben würden. Über einen möglichen Zusammenhang mit einer erhöhten Häufigkeit von Leistenbrüchen wurde berichtet. Morphin passiert die Plazentaschranke. Untersuchungen an Tieren zeigten ein Schädigungspotential für die Nachkommen während der gesamten Dauer der Trächtigkeit (siehe Abschnitt 5.3). Morphin darf daher in der Schwangerschaft nur angewendet werden, wenn der Nutzen für die Mutter das Risiko für das Kind klar überwiegt. Wegen der mutagenen Eigenschaften von Morphin sollte es Männern und Frauen im zeugungs- und gebärfähigen Alter nur dann verabreicht werden, wenn eine wirksame Verhütung sichergestellt ist.
Bei Neugeborenen wurden Entzugserscheinungen nach längerer Morphinanwendung während der Schwangerschaft beschrieben.
Entbindung
Morphin kann die Dauer der Wehentätigkeit verlängern oder verkürzen. Neugeborene, deren Mütter während der Entbindung Opioidanalgetika erhalten, sollten auf Anzeichen einer Atemdepression oder eines Entzugssyndroms überwacht und gegebenenfalls mit einem spezifischen Opioidantagonisten behandelt werden.
Stillzeit
Morphin wird in die Muttermilch ausgeschieden und erreicht dort höhere Konzentrationen als im mütterlichen Plasma. Da beim Säugling klinisch relevante Konzentrationen erreicht werden können, ist vom Stillen abzuraten.
4.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen
Morphin kann Aufmerksamkeit und Reaktionsvermögen so weit verändern, dass die Fähigkeit zur aktiven Teilnahme am Straßenverkehr oder zum Bedienen von Maschinen beeinträchtigt oder nicht mehr gegeben ist.
Dies ist insbesondere bei Behandlungsbeginn, Dosiserhöhung und Präparatewechsel sowie im Zusammenwirken mit Alkohol oder der Einnahme von Beruhigungsmitteln zu erwarten.
Die Beurteilung der jeweils individuellen Situation ist durch den behandelnden Arzt vorzunehmen. Bei einer stabilen Therapie ist ein generelles Fahrverbot nicht zwingend erforderlich.
4.8 Nebenwirkungen
Bei der Bewertung von Nebenwirkungen werden folgende Häufigkeitsangaben zugrunde gelegt:
|
Sehr häufig |
> 1/10 |
|
Häufig |
> 1/100 bis < 1/10 |
|
Gelegentlich |
> 1/1.000 bis < 1/100 |
|
Selten |
> 1/10.000 bis < 1/1.000 |
|
Sehr selten |
< 1/10.000 |
Nicht bekannt Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar
|
Organklasse |
Häufigkeit |
|
Erkrankungen des Immunsystems |
Nicht bekannt: Anaphylaktische oder anaphylaktoide Reaktionen |
|
Endokrine Erkrankungen |
Sehr selten: Syndrom der inadäquaten ADH-Sekretion (SIADH; Leitsymptom: Hyponatriämie) |
|
Organklasse |
Häufigkeit |
|
Psychiatrische Erkrankungen |
Sehr häufig: Stimmungsveränderungen, meist Euphorie aber auch Dysphorie Häufig: Veränderungen der Aktiviertheit (meist Dämpfung, aber auch Steigerung oder Erregungszustände), Schlaflosigkeit und Veränderungen der kognitiven und sensorischen Leistungsfähigkeit (z. B. Denkstörungen, Wahrnehmungsstörungen/Halluzinationen, Verwirrtheit) Sehr selten: Abhängigkeit (siehe auch Abschnitt 4.4), Verminderung der Libido oder Potenzschwäche. |
|
Erkrankungen des Nervensystems |
Häufig: Kopfschmerzen, Schwindel Sehr selten: Tremor, unwillkürliches Muskelzucken, epileptische Krampfanfälle, Hyperalgesie oder Allodynie (dosisabhängig) Nicht bekannt: Sedierung von leichter Müdigkeit bis zur Benommenheit (dosisabhängig) |
|
Augenerkrankungen |
Sehr häufig: Pupillenverengung Sehr selten: Verschwommenes Sehen, Doppeltsehen und Augenzittern |
|
Herzerkrankungen |
Gelegentlich: Klinisch bedeutsamer Abfall als auch Anstieg von Blutdruck und Herzfrequenz Nicht bekannt: Gesichtsrötungen, Herzklopfen, allgemeine Schwäche bis hin zum Ohnmachtsanfall, Herzversagen |
|
Erkrankungen der Atemwege, des Brustraums und Mediastinums |
Selten: Bronchospasmen Sehr selten: Dyspnoe Nicht bekannt: Atemdämpfung (dosisabhängig), nicht-kardiogen bedingte Lungenödeme (bei intensivmedizinisch behandelten Patienten) |
|
Organklasse |
Häufigkeit |
|
Erkrankungen des Gastrointestinaltrakts |
Sehr häufig: Verstopfung (bei Dauerbehandlung) Häufig: Erbrechen (besonders zu Beginn der Behandlung), Appetitlosigkeit, Dyspepsie, Geschmacksveränderungen Selten: Erhöhung der Pankreasenzyme bzw. Pankreatitis Sehr selten: Darmverschluss, Bauchschmerzen Nicht bekannt: Übelkeit und Mundtrockenheit (beides dosisabhängig) |
|
Leber- und Gallenerkrankungen |
Selten: Gallenkoliken Sehr selten: Erhöhung leberspezifischer Enzyme |
|
Erkrankungen der Haut und des Unterhautzellgewebes |
Häufig: Schwitzen, Überempfindlichkeitsreaktionen wie Urticaria, Pruritus Sehr selten: Andere Hautausschläge wie Exantheme und periphere Ödeme (bilden sich nach Absetzen zurück) |
|
Skelettmuskulatur-, Bindegewebs- und Knochenerkrankungen |
Sehr selten: Muskelkrämpfe, Muskelstarre |
|
Erkrankungen der Nieren und Harnwege |
Häufig: Störungen bei der Blasenentleerung Selten: Nierenkoliken |
|
Erkrankungen der Geschlechtsorgane und der Brustdrüse |
Sehr selten: Amenorrhoe |
|
Allgemeine Erkrankungen und Beschwerden am Verabreichungsort |
Selten: Entzugserscheinungen Sehr selten: Asthenie, Unwohlsein, Schüttelfrost, Zahnveränderungen, wobei jedoch ein ursächlicher Zusammenhang zur Morphin-Therapie nicht hergestellt werden konnte Nicht bekannt: T oleranzentwicklung |
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung dem Bundesinstitut für Arzneimittel und Medizinprodukte, Abt. Pharmakovigilanz, Kurt-Georg-Kiesinger Allee 3, D-53175 Bonn, Website: www.bfarm.de anzuzeigen.
4.9 Überdosierung
Symptome der Intoxikation
Da die Empfindlichkeit auf Morphin individuell stark schwankt, können Intoxikationserscheinungen beim Erwachsenen ab Einzeldosen auftreten, die einer subkutanen und intravenösen Gabe von ca.
30 mg entsprechen. Bei Karzinompatienten werden diese Werte oft überschritten, ohne gravierende Nebenwirkungen hervorzurufen.
Die Opiatvergiftung äußert sich durch die Trias: Miosis, Atemdepression und Koma: Die Pupillen sind zunächst stecknadelkopfgroß. Bei starker Hypoxie dilatieren sie jedoch. Die Atmung ist stark reduziert (bis auf 2 - 4 Atemzüge pro Minute). Der Patient wird zyanotisch.
Überdosierung mit Morphin führt zu Benommenheit und Stupor bis hin zum Koma. Der Blutdruck bleibt zunächst normal, fällt jedoch bei fortschreitender Intoxikation rapide ab. Anhaltender Blutdruckabfall kann in einen Schockzustand übergehen. Tachykardie, Bradykardie und Rhabdomyolyse können auftreten. Die Körpertemperatur fällt ab. Die Skelettmuskulatur wird relaxiert, gelegentlich können, insbesondere bei Kindern, generalisierte Krämpfe auftreten. Der Tod tritt meist durch Ateminsuffizienz oder durch Komplikationen wie pulmonales Ödem ein.
Therapie von Intoxikationen
Bei bewusstlosen Patienten mit Atemstillstand sind Beatmung, Intubation und die intravenöse Gabe eines Opiatantagonisten (z. B. 0,4 mg Naloxon i.v.) angezeigt. Bei anhaltender Ateminsuffizienz muss die Einzeldosis 1 - 3-mal in dreiminütigen Abständen wiederholt werden, bis die Atemfrequenz normalisiert ist und der Patient auf Schmerzreize reagiert.
Strenge Überwachung (mind. 24 Stunden) ist notwendig, da die Wirkung des Opiatantagonisten kürzer ist als die des Morphins, so dass mit einem erneuten Auftreten der Ateminsuffizienz gerechnet werden muss.
Die Dosis des Opiatantagonisten beträgt bei Kindern pro Einzeldosis 0,01 mg pro kg Körpergewicht. Ferner können Maßnahmen zum Schutz vor Wärmeverlusten und zur Volumentherapie erforderlich sein.
5. PHARMAKOLOGISCHE EIGENSCHAFTEN
5.1 Pharmakodynamische Eigenschaften
Pharmakotherapeutische Gruppe: Opioide, ATC-Code: N02AA01
Morphin ist ein Phenantren-Alkaloid aus Schlafmohn (Papaver somniferum) mit opiatagonistischen Eigenschaften. Es zeigt eine ausgeprägte Affinität zu p-Rezeptoren.
Zentrale Wirkungen
Morphin wirkt analgetisch, antitussiv, sedierend, tranquillisierend, atemdepressiv, miotisch, antidiuretisch, emetisch und antiemetisch (Späteffekt) und geringgradig blutdruck- und herzfrequenzsenkend.
Periphere Wirkungen
Obstipation, Kontraktion der Sphinkteren im Bereich der Gallenwege, Steigerung des Tonus der Harnblasenmuskulatur und des Blasenschließmuskels, Verzögerung der Magenentleerung durch Pyloruskonstriktion, Hautrötung, Urtikaria und Juckreiz durch Histaminfreisetzung sowie bei Asthmatikern Bronchospasmus, Beeinflussung der hypophysär-hypothalamischen Achse und damit Beeinflussung der Hormonwirkung von Kortikoiden, Sexualhormonen, Prolactin und antidiuretischem Hormon. Eine Manifestation klinischer Symptome aufgrund dieser Hormonveränderungen kann möglich sein.
Der Wirkungseintritt nach oraler Applikation erfolgt nach 30 - 90 Minuten. Die Wirkdauer beträgt ca. 4 - 6 Stunden und ist bei retardierter Wirkstofffreisetzung erheblich verlängert.
Der Wirkungseintritt nach intramuskulärer oder subkutaner Applikation erfolgt nach 15 - 30 Minuten, nach intravenöser Gabe in wenigen Minuten. Die Wirkdauer beträgt unabhängig von diesen Applikationsarten ca. 4 - 6 Stunden. Nach epiduraler und intrathekaler Gabe sind lokal begrenzte analgetische Wirkungen bereits nach wenigen Minuten nachweisbar. Die Wirkdauer beträgt bei epiduraler Anwendung ca. 12 Stunden und geht bei intrathekaler Gabe noch darüber hinaus.
In vitro- und Tierstudien zeigen unterschiedliche Effekte natürlicher Opioide, wie Morphin, auf Komponenten des Immunsystems. Die klinische Bedeutung dieser Befunde ist nicht bekannt.
5.2 Pharmakokinetische Eigenschaften
Morphin wird nach oraler Applikation relativ rasch - vorwiegend aus dem oberen Dünndarm und geringfügig auch aus dem Magen - resorbiert. Die geringe absolute Bioverfügbarkeit (20% - 40%) ist auf einen ausgeprägten first-pass-Effekt zurückzuführen.
Cmax wird nach oraler Einnahme von einer 60 mg Retardtablette (bei Probanden) nach durchschnittlich
2.3 ± 1,1 h erreicht. Morphin wird zu ca. 20 - 35% an Plasmaproteine, bevorzugt an die Albuminfraktion, gebunden.
Das Verteilungsvolumen von Morphin wird mit 1,0 - 4,7 l/kg nach i.v. Einmalgabe von 4 - 10 mg angegeben. Hohe Gewebekonzentrationen findet man in der Leber, Niere, im Gastrointestinaltrakt und im Muskel. Morphin überwindet die Blut-Hirnschranke.
Morphin wird vorwiegend in der Leber, aber auch im Darmepithel metabolisiert. Der wesentliche Schritt ist die Glucuronidierung der phenolischen Hydroxylgruppe mittels der hepatischen UDP-Glukuronyltransferase und N-Demethylierung.
Hauptmetabolite sind vor allem Morphin-3-glucuronid und in geringerer Menge Morphin-6-glucuronid. Außerdem entstehen unter anderem Sulfatkonjugate sowie oxidative Stoffwechselprodukte wie Normorphin, Morphin-N-oxid und ein in 2-Stellung hydroxiliertes Morphin. Die Halbwertszeit der Glucuronide ist erheblich länger als die des freien Morphins. Das Morphin-6-glucuronid ist biologisch wirksam. Es ist möglich, dass eine verlängerte Wirkung bei Patienten mit Niereninsuffizienz auf diesen Metaboliten zurückzuführen ist.
Im Harn werden nach oraler oder parenteraler Applikation ca. 80 % des verabreichten Morphins wieder gefunden (10 % unverändertes Morphin, 4 % Normorphin und 65 % als Glucuronide, davon Morphin-3-glucuronid: Morphin-6-glucuronid [10 : 1]). Die Eliminationshalbwertszeit von Morphin unterliegt großen interindividuellen Schwankungen. Sie liegt nach parenteraler Gabe durchschnittlich zwischen 1,7 und 4,5 Stunden, gelegentlich wurden auch Werte um 9 Stunden gefunden. Etwa 10 % der Morphin-Glucuronide werden über die Galle mit den Faeces ausgeschieden.
5.3 Präklinische Daten zur Sicherheit
Bei fortgesetzter Anwendung von Morphin nimmt die Empfindlichkeit des ZNS gegenüber Morphin ab. Diese Gewöhnung kann so ausgeprägt sein, dass Dosen vertragen werden, die bei erstmaliger Anwendung infolge Atemdepression toxisch wirken. Aufgrund der euphorischen Wirkungskomponente des Morphins besteht Suchtgefahr (siehe auch Abschnitt 4.4).
Es liegen zur Mutagenität klar positive Befunde vor, die darauf hindeuten, dass Morphin klastogen wirkt und eine solche Wirkung auch auf Keimzellen ausübt. Daher ist Morphin als mutagen wirksame Substanz anzusehen; eine derartige Wirkung muss auch im Menschen angenommen werden.
Morphin sollte nur unter sicherem Konzeptionsschutz eingenommen werden.
Langzeituntersuchungen am Tier auf ein tumorerzeugendes Potential von Morphin liegen nicht vor. Untersuchungen an Tieren zeigten ein Schädigungspotential für die Nachkommen während der gesamten Dauer der Trächtigkeit (ZNS-Missbildungen, Wachstumsretardierung, Testisatrophie, Veränderungen bei Neurotransmittersystemen und Verhaltensweisen, Abhängigkeit). Daneben hatte Morphin bei verschiedenen Tierspezies Auswirkungen auf das männliche Sexualverhalten und die weibliche Fertilität.
5.4 Bioverfügbarkeit
Eine im Jahre 1989 durchgeführte vergleichende Bioverfügbarkeitsuntersuchung (bei Mehrfachapplikation) an 25 Krebspatienten ergab im Vergleich zum Referenzpräparat (Sirup):
Testpräparat Referenzpräparat
48,13 ± 30,67 49,52 ± 28,38
maximale Plasmakonzentration Cmax [ng/ml]
Zeitpunkt der maximalen Plasmakonzentration (tmax)h:
3,60 ± 1,95
2,70 ± 2,67
Fläche unter der Konzentrations-Zeit-Kurve 323,2 ± 201,7 308,4 ± 203,8
(AUC 0 - 12 h) [ng h/ml]_
Angabe der Werte als Mittelwerte und Streubreite.
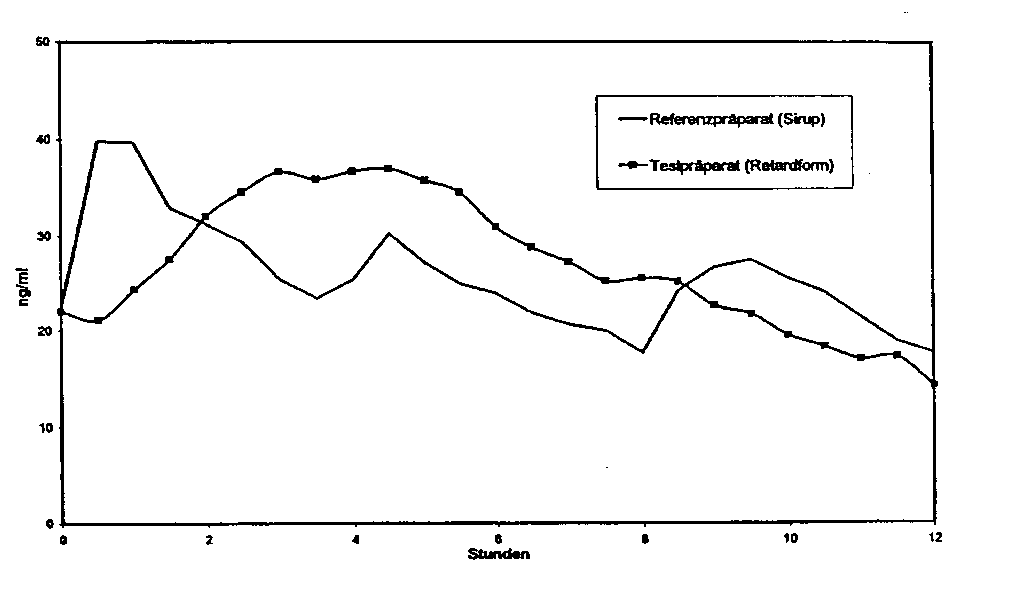
Mittlere Plasmaspiegelverläufe im Vergleich zu einem Referenzpräparat in einem KonzentrationsZeit-Diagramm:
6. PHARMAZEUTISCHE ANGABEN
6.1 Liste der sonstigen Bestandteile
Maisstärke, Macrogol 4000, Ethylcellulose, Natriumdodecylsulfat, Hexadecan-1-ol, Dibutyldecandioat, Talkum, Sucrose, Gelatine, Farbstoffe: Capros 10 mg: E 104, E 127, E 132, E 171; Capros 30 mg: E 132, E 171; Capros 60 mg:E 132, E 171; Capros 100 mg: E 132, E 171
6.2 Inkompatibilitäten
Nicht zutreffend.
6.3 Dauer der Haltbarkeit
3 Jahre.
6.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung
Nicht über 25 °C lagern.
In der Originalpackung aufbewahren, um den Inhalt vor Feuchtigkeit zu schützen.
6.5 Art und Inhalt des Behältnisses
Packungen mit 20 Hartkapseln, retardiert 50 Hartkapseln, retardiert 100 Hartkapseln, retardiert 100 Hartkapseln, retardiert (Klinikpackung)
6.6 Besondere Vorsichtsmaßnahmen für die Beseitigung
Keine besonderen Anforderungen.
7. INHABER DER ZULASSUNG
Ethypharm GmbH An den Gehren 1 12529 Schönefeld Deutschland
Telefon: +49 (0) 30 634 99 393 Telefax: +49 (0) 30 634 99 395
8. ZULASSUNGSNUMMERN
30177.00.00
30177.01.00
30177.02.00
30177.03.00
9. DATUM DER ERTEILUNG DER ZULASSUNG / VERLÄNGERUNG DER
ZULASSUNG
25.03.1993 / 17.03.2006
10. STAND DER INFORMATION
August 2015
11. VERSCHREIBUNGSSTATUS/APOTHEKENPFLICHT
Verschreibungspflichtig entsprechend der Betäubungsmittelverschreibungsverordnung.