Digimed 0,07Mg
Fachinformation
1. BEZEICHNUNG DES ARZNEIMITTELS
Digimed® 0,07 mg
Tabletten
2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Wirkstoff: Digitoxin
Vollständige Auflistung der sonstigen Bestandteile, siehe Abschnitt 6.1.
3. DARREICHUNGSFORM
Tabletten
Digimed 0,07 mg sind orangefarbene, runde Tabletten.
4. KLINISCHE ANGABEN
4.1 Anwendungsgebiete
- Manifeste chronische Herzinsuffizienz (aufgrund systolischer Dysfunktion),
- Tachyarrhythmia absoluta bei Vorhofflimmern/ Vorhofflattern,
- Paroxysmales Vorhofflimmern/Vorhofflattern.
4.2 Dosierung und Art der Anwendung Dosierung
Wegen der geringen therapeutischen Breite von Digitoxin ist eine sorgfältig überwachte Einstellung auf die individuelle therapeutische Dosis notwendig.
Die Höhe der individuellen Dosierung hängt vom Glykosidbedarf sowie von der Eliminationsgeschwindigkeit ab.
Die Dosierung sollte individuell - vor allem nach dem Behandlungserfolg - festgelegt werden. Häufig ist eine tägliche Erhaltungsdosis von 0,05 - 0,1 mg Digitoxin ausreichend, um effektive Serum-Digitoxin Konzentrationen zu erreichen. Eine tägliche Erhaltungsdosis von 1gg (= 0,001 mg) Digitoxin/kg Körpergewicht ist in der Regel ausreichend, um therapeutische Serum-Digitoxin-Konzentrationen zu erreichen.
Patienten mit einigen besonderen Krankheitsbildern müssen mit reduzierter Glykosiddosierung und unter sorgfältiger ärztlicher Überwachung behandelt werden (siehe auch entsprechende Hinweise im Abschnitt Gegenanzeigen).
Eine regelmäßige Kontrolle des klinischen Bildes bei gleichzeitigem Monitoring der Digitoxin-Serumkonzentrationen ist zu empfehlen.
Im Allgemeinen wird in Abhängigkeit vom Glykosidbedarf in der Praxis mit einer mittelschnellen Sättigungsbehandlung begonnen. Dafür wird bei Erwachsenen drei Tage lang 0,15 - 0,3 mg Digitoxin gegeben. Ab dem 4. Tag erfolgt die Erhaltungsbehandlung mit 0,05 - 0,1 mg Digitoxin.
Folgende Empfehlungen können als Anhaltspunkte für die Einleitung der Behandlung (Aufsättigung) und Dauertherapie dienen:
Im Allgemeinen wird in Abhängigkeit vom Glykosidbedarf in der Praxis mit einer mittelschnellen Sättigungsbehandlung über 3 Tage begonnen:
a) Bei Patienten über 60 Jahren, außer bei stark Muskulösen, bei denen wie unter b) dosiert wird:
1. Tag:
3mal 1 Tablette einer 0,05 mg-Formulierung bzw. 1 Tablette Digimed 0,07 mg (entsprechend 0,15-0,21 mg Digitoxin / Tag)
2. Tag:
3mal 1 Tablette einer 0,05 mg-Formulierung bzw. 1 Tablette Digimed 0,07 mg (entsprechend 0,15-0,21 mg Digitoxin / Tag)
3. Tag:
3mal 1 Tablette einer 0,05 mg-Formulierung bzw. 1 Tablette Digimed 0,07 mg (entsprechend 0,15-0,21 mg Digitoxin / Tag) ab 4. Tag:
Erhaltungsbehandlung mit 1 Tablette einer 0,05 mg-Formulierung bzw. 1 Tablette Digimed 0,07 mg täglich.
b) Bei Patienten unter 60 Jahre, außer bei Untergewichtigen, bei denen wie unter a) dosiert wird, empfiehlt sich eine höhere Dosierung:
1. Tag:
3mal 1 Tablette Digimed 0,1 mg (entsprechend 0,3 mg Digitoxin / Tag)
2. Tag:
3mal 1 Tablette Digimed 0,1 mg (entsprechend 0,3 mg Digitoxin / Tag)
3. Tag:
3mal 1 Tablette Digimed 0,1 mg (entsprechend 0,3 mg Digitoxin / Tag) ab 4. Tag:
Erhaltungsbehandlung mit 1 Tablette Digimed 0,1 mg täglich
Es stehen entsprechende Darreichungsformen mit höherem Wirkstoffgehalt zur Verfügung.
Eingeschränkte Leber- und/oder Nierenfunktion
Bei gleichzeitig bestehender schwerer Leber- und Niereninsuffizienz kann der Digitoxinbedarf vermindert sein.
Auch wird empfohlen, den Digitoxinbedarf bei Patienten mit sehr schwerer Niereninsuffizienz (GFR < 10 ml/min) insbesondere zu Beginn der Therapie zu überprüfen und ggf. die Dosierung zu vermindern.
Umstellung von Digoxin auf Digitoxin
Eine vorausgegangene Behandlung mit anderen Herzglykosiden ist bei der Gabe von Digimed 0,07 mg zu berücksichtigen. Bei vorangegangenen Gaben von Digoxin und seinen Derivaten oder anderen Herzglykosiden ist bei der Umstellung auf die obengenannten Digimed 0,07 mg-Formen bei Nierengesunden eine Behandlungspause von 2 Tagen bzw. bei Patienten mit gestörter Nierenfunktion (z. B. älteren Patienten) eine Behandlungspause von 3 Tagen oder länger einzuhalten.
Art der Anwendung
Bereits mit Herzglykosiden vorbehandelte Patienten sollten bei Umstellung auf Digitoxin besonders engmaschig kontrolliert werden.
Über die Dauer der Anwendung entscheidet der behandelnde Arzt.
Die Digitalisbedürftigkeit des Patienten sollte bei Langzeittherapie durch kontrollierte Auslassversuche überprüft werden.
Digimed 0,07 mg sollte vorzugsweise nach einer Mahlzeit unzerkaut mit ausreichend Flüssigkeit eingenommen werden.
Es ist unbedingt darauf zu achten, dass dieses Arzneimittel regelmäßig in der vom Arzt verordneten Menge eingenommen wird.
Überwachung der Serumspiegel
Die therapeutische Breite der Herzglykoside ist gering. Eine Dosis, die um ca. 60% über der therapeutischen Dosis liegt, löst mit größter Wahrscheinlichkeit Intoxikationen aus.
Digitoxin-Serum-Spiegel können mittels Radioimmunoassay bestimmt werden. Die Blutentnahme sollte vor der täglichen Gabe erfolgen. Die therapeutischen Serumkonzentrationen im steady state liegen in der Regel zwischen 10 und 30 ng/ml; höhere Werte insbesondere über 35 ng/ml können mit toxischen Erscheinungen einhergehen.
Andere Glykoside, Spironolacton und dessen Metabolite sowie die Metaboliten von Digitoxin können mit den Radioimmunoassays interferieren. Daher sollten Messwerte, die mit dem klinischen Zustand des Patienten nicht im Einklang stehen, mit Vorsicht interpretiert werden.
4.3 Gegenanzeigen
- Überempfindlichkeit gegen Digitoxin, andere herzwirksame Glykoside,
Gelborange S, Aluminiumsalz (E 110) oder einen der in Abschnitt 6.1 genannten
sonstigen Bestandteile
- Verdacht auf Digitalisintoxikation
- Kammertachykardie oder Kammerflimmern
AV-Block II. oder III. Grades, pathologischer Sinusknotenfunktion (ausgenommen bei Schrittmacher-Therapie)
vorgesehener elektrischer Kardioversion
akzessorischen, atrioventrikulären Leitungsbahnen (z. B. WPW-Syndrom) oder Verdacht auf solche
Carotissinussyndrom
Hypokaliämie
Hyperkalziämie, Hypomagnesiämie
hypertropher Kardiomyopathie mit Obstruktion (idiopathische hypertrophe Subaortenstenose)
thorakalem Aortenaneurysma
gleichzeitiger intravenöser Gabe von Kalziumsalzen (s. Wechselwirkungen)
4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung
Eine besonders sorgfältige ärztliche Überwachung ist erforderlich bei:
- Bradykardie infolge von Erregungsbildungs- und/oder -leitungsstörungen, AV-Block I. Grades.
- Hyperkaliämie, da vermehrt Erregungsbildungs- und -leitungsstörungen auftreten können
- älteren Patienten oder wenn anzunehmen ist, dass die renale Clearance von Digitoxin vermindert ist (siehe auch Dosierung, Abschnitt 4.2).
- Schilddrüsenerkrankungen (bei einer Hypothyreose sollten Aufsättigungs- und Erhaltungsdosis verringert werden. Bei einer Hyperthyreose kann eine Dosiserhöhung erforderlich sein)
- akutem Myokardinfarkt (Patienten mit akutem Myokardinfarkt sind z. B. häufig hypokaliämisch und/oder neigen zu Herzrhythmusstörungen)
- akuter Myokarditis, Cor pulmonale oder Hypoxämie infolge schwerer Atemwegserkrankung, da eine erhöhte Empfindlichkeit gegenüber DigitalisGlykosiden besteht.
- Patienten, die in den vorangegangenen 2 Wochen Herzglykoside erhalten haben. Hier kann eine verringerte Aufsättigungsdosierung nötig sein.
Hinweise:,
Es bestehen erhebliche interindividuelle Unterschiede der Glykosidempfindlichkeit.
Eine erhöhte Glykosidempfindlichkeit besteht z. B. bei Patienten höheren Lebensalters, Hypothyreose, Hypoxämie, Myokarditis, akutem Myokardinfarkt, Störungen des Säure-, Basen- und Elektrolythaushaltes. Entsprechende Patienten bzw. Krankheitsbilder sollten mit reduzierter Glykosiddosierung behandelt und sorgfältig überwacht werden.
Eine Digitoxin-Toxizität kann sich durch das Auftreten von Arrhythmien äußern, von denen einige solchen Arrhythmien ähneln können, für die das Arzneimittel therapeutisch angezeigt sein könnte. Z. B. ist besondere Vorsicht erforderlich bei Vorhoftachykardie mit wechselndem AV-Block, da der Rhythmus klinisch einem Vorhofflimmern entspricht.
Digitoxin kann ST-T Veränderungen im EKG verursachen, ohne dass gleichzeitig eine Myokardischämie vorliegt.
Für die Beurteilung, ob ein unerwünschtes Ereignis auf Digitoxin zurückzuführen ist, sollte der klinische Zustand des Patienten zusammen mit den Serum-Kalium-Spiegeln sowie der Nieren- und Schilddrüsenfunktion als wichtigste Faktoren herangezogen werden.
Bei Kaliummangel wird das Myokard für Digitoxin sensibilisiert, obwohl die DigitoxinSerumkonzentration im therapeutischen Bereich liegen kann.
Ein Kaliummangel kann z. B. auftreten durch Dialyse, Absaugen von Magen-DarmSekret, Unterernährung, Durchfall, längeres Erbrechen, sowie bei hohem Alter oder bei chronischer Herzinsuffizienz (z. B. infolge von Diuretikatherapie).
Im Allgemeinen sollten schnelle Änderungen der Serumkaliumkonzentration oder anderer Elektrolyte (z. B. Magnesium, Calcium) vermieden werden.
Eine Nierenfunktionsstörung ist einer der häufigsten Gründe für die Auslösung einer Digitalisintoxikation.
Kontrollen der Serum-Elektrolyte sowie der Nierenfunktion sollten in regelmäßigen Abständen (in Abhängigkeit vom klinischen Zustand) erfolgen.
Patienten mit der seltenen hereditären Galactose-Intoleranz, Lactase-Mangel oder Glucose-Galactose-Malabsorption sollten Digimed 0,07 mg nicht einnehmen.
4.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen
Wechselwirkungen können resultieren aus einer Beeinflussung der renalen Ausscheidung, der Bindung an Körpergewebe, der Plasmaproteinbindung, der Verteilung, der Resorptionskapazität des Darmes und der Empfindlichkeit gegenüber Digitoxin.
Als Vorsichtsmaßnahme sollte bei jeglicher zusätzlicher Therapie die Möglichkeit einer Interaktion berücksichtigt werden. Im Zweifelsfall sollten die Digitoxin-Serum-Spiegel überprüft werden.
Eine Übersicht von Wechselwirkungen geben die nachstehenden Tabellen. Wirkungsverstärkung
|
Calcium (darf nicht i.v. injiziert werden) |
Verstärkung der Glykosidtoxizität |
|
Arzneimittel, die die ElektrolytHomöostase beeinflussen, wie z. B. Diuretika (gerade im Hinblick auf Kaliuretika), Laxantien (Abusus), Benzylpenicillin, Amphotericin B, Carbenoxolon, Korticosteroide, ACTH, Salicylate, Lithiumsalze |
Verstärkung der Glykosidtoxizität durch medikamentös bedingte Hypokaliämie bzw. Hypomagnesiämie |
|
CYP3A-Inhibitoren, wie bestimmte Antibiotika (z.B. Makrolide), bestimmte Antimykotika (z.B. Itraconazol), Steroidhormone (z.B. Prednison, Danazol), bestimmte Antidepressiva (z.B. Fluoxetin), Proteaseinhibitoren (z.B. Indinavir, Ritonavir), Calciumantagonisten (z.B. Verapamil, Nifedipin, Diltiazem) oder bestimmte Antiarrhythmika (z. B. Amiodaron) |
Erhöhung der Digitoxinserumkonzentration |
|
ß-Blocker |
Verstärkung der bradykardisierenden Wirkung |
|
P-Glykoprotein-Inhibitoren, wie bestimmte Antibiotika (z.B. Makrolide, Tetrazykline) oder Chinidin. |
Erhöhung der Digitoxinserumkonzentration |
|
Antibiotika, die den Abbau von Digitoxin durch E. lentum hemmen (dies trifft nur für 10 % der Bevölkerung zu), wie Makrolide, Carbapeneme und ß-Lactamantibiotika |
Erhöhung der Digitoxinserumkonzentration |
Muskelrelaxantien (z.B. Begünstigung von
Suxamethoniumchlorid, Herzrhythmusstörungen
Pancuronium), Reserpin, trizyklische
Antidepressiva
Sympathomimetika,
Phosphodiesterasehemmer (z. B.
Theophyllin), Lithium (bei Patienten mit sinuatrialem Block)
Wirkungsabschwächung
|
Kaliumspiegelerhöhende Arzneimittel (z. B. Spironolacton, Kaliumcanrenoat, Amilorid, Triamteren, Kaliumsalze) |
Verminderung der positiv inotropen Wirkung von Digitoxin und Begünstigung von Herzrhythmusstörungen |
|
Aktivkohle, Cholestyramin, Colestipol, Kaolin-Pektin, einige Füll- oder QuellLaxantien |
Verminderung der Glykosidresorption durch Bindung - daher Digimed 0,07 mg 2 Stunden vorher einnehmen - bzw. Beschleunigung der Elimination durch Unterbrechung des enterohepatischen Kreislaufs |
|
Arzneimittel, die CYP3A oder P-Glycoprotein induzieren, wie z. B. Phenylbutazon, Phenytoin, Rifampicin, Rifabutin, Spironolacton, Barbiturate |
Erniedrigung der Digitoxinserumkonzentration |
4.6 Fertilität, Schwangerschaft und Stillzeit
Während der Schwangerschaft ist die Patientin besonders sorgfältig zu überwachen und auf eine individuelle, bedarfsgerechte Dosierung zu achten. Bisherige Erfahrungen mit Digitalis-Glykosiden in therapeutischen Dosierungen während der Schwangerschaft haben keine Hinweise auf eine Schädigung des Embryos oder Föten ergeben. Während der letzten Wochen der Schwangerschaft kann der Glykosidbedarf ansteigen.
Nach der Geburt ist dagegen häufig eine Dosisreduzierung angezeigt. Nach DigitalisVergiftungen der Mutter wurde auch beim Föten über Intoxikationserscheinungen berichtet.
Digitoxin wird in die Muttermilch abgegeben, daher sollte vorsichtshalber abgestillt werden.
4.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen
Digimed 0,07 mg hat keinen Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen.
4.8 Nebenwirkungen
Bei der Bewertung von Nebenwirkungen werden folgende Häufigkeiten zugrunde gelegt:
Sehr häufig: Häufig: Gelegentlich: Selten:
Sehr selten: Nicht bekannt:
(> 1/10 )
(> 1/100 bis < 1/10)
(> 1/1.000 bis < 1/100)
(> 1/10.000 bis < 1/1.000)
(< 1/10.000)
(Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar)
Nebenwirkungen können die Symptome einer Überdosierung sein.
Kardiale Nebenwirkungen werden am häufigsten beobachtet. Grundsätzlich ist jede Form von Herzrhythmusstörungen unter der Therapie mit Digimed 0,07 mg möglich. Das Auftreten von Herzrhythmusstörungen wird durch das zusätzliche Vorliegen von Elektrolytstörungen (Kalium, Kalzium, Magnesium) begünstigt.
|
Systemorganklasse (MedDRA) |
Sehr häufig ((> 1/10) |
Häufig (> 1/100 bis < 1/10) |
Gelegentlich (> 1/1.000 bis < 1/100) |
Selten (> 1/10.000 bis < 1/1.000) |
Sehr selten (< 1/10.000) |
|
Herzerkrank ungen |
Jede Form von Herzrhythmusstörung en, insbesondere Extraschläge, die von den Herzkammern ausgehen (Extrasystolen), Kammertachykardien (Bigeminie/Trige-minie - Doppel-/Dreifachschläge). Schnelle Schlagfolge der Vorhöfe (Vorhoftachykardien) (bei sehr hoher Dosierung). Erregungsleitungsstö rungen zwischen Herzvorhof und Herzkammer (AV-Block I.- III. Grades), Störungen der Herzschlagfolge (z.B. Verlangsamung der Herzfrequenz [Bradykardie]). |
|
Augenerkrank ungen |
Veränderung des Farbsehens (Grün-/Gelb-Bereich) bereits im therapeutischen Bereich | ||||
|
Erkrankungen des Gastrointestinaltrakts |
Appetitlosigkeit, Übelkeit (das Auftreten von Übelkeit sollte als frühes Zeichen einer übermäßig hohen Dosierung angesehen werden), Erbrechen, Abdominelle Beschwerden (z.B. Bauchschmerzen), Durchfall |
Gefäßverschluss im Bauchraum (Mesenterialinfarkt) | |||
|
Skelettmuskulatur-, Bindegewebs- und Knochenerkrankungen |
Muskelschwäche | ||||
|
Endokrine Erkrankungen |
Vergrößerung der Brustdrüse beim Mann (Gynäkomastie) (bildet sich nach Absetzen von Digimed 0,07 mg i.d.R. wieder zurück.) | ||||
|
Allgemeine Erkrankungen und Beschwerden am Verabreichungsort |
Kopfschmerzen, Müdigkeit, Schlaflosigkeit | ||||
|
Erkrankungen des Immunsystems |
Allergische Reaktionen bilden sich nach Absetzen von Digimed 0,07 mg i.d.R. wieder zurück. Nesselsuchtartige oder scharlachartige Hautausschläge mit Veränderungen im Blutbild (ausgeprägter Eosinophilie), Hautrötung (Erythem); Verminderung der Blutplättchen (Thrombozytopenie) oder Schmetterlingserythem (Lupus erythematodes) |
|
Psychiatrische Erkrankungen |
Psychische Veränderungen (z.B. Alpträume, Agitiertheit, Verwirrtheit) sowie Depressionen, Sinnestäuschungen (Halluzinationen) und Psychosen |
Sprachstörunge n (Aphasien), Schwäche, Teilnahmslosigk eit (Apathie) und Unwohlsein |
Gelborange S (E 110) kann allergische Reaktionen hervorrufen.
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-RisikoVerhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung über das
Bundesinstitut für Arzneimittel und Medizinprodukte
Abt. Pharmakovigilanz
Kurt-Georg-Kiesinger Allee 3
D-53175 Bonn
Website:
http. //www.bfarm.de anzuzeigen.
4.9 Überdosierung
a) Symptome einer Überdosierung
Bei Überdosierung können, individuell verschieden, die allgemein von Digitalisglykosiden bekannten kardialen, gastrointestinalen und zentralnervösen Nebenwirkungen auftreten. Eine typische Reihenfolge des Auftretens der Symptome gibt es nicht. Extrakardiale und kardiale Symptome können gleichzeitig oder nacheinander vorkommen, wobei die kardialen Zeichen einer Digitalisintoxikation weitaus ernster zu bewerten sind.
Glykosidintoxikationen mit letalem Ausgang sind in der Regel Folge von kardiotoxischen Wirkungen der Glykoside.
Bei digitalisierten Patienten ist das Auftreten einer Herzrhythmusstörung stets als digitalisbedingt aufzufassen, solange nicht durch einen Auslassversuch oder eine Serumspiegelbestimmung das Gegenteil erwiesen ist.
Bei einer akuten Überdosierung kann eine Hyperkaliämie auftreten, wogegen eine Hypokaliämie häufig mit chronischer Überdosierung assoziiert ist. Die toxischen Wirkungen können bis zu 12 Stunden nach einer akuten Überdosierung noch zunehmen.
b) Therapiemaßnahmen bei Überdosierung
Bei Überdosierung muss die Behandlung mit Digimed 0,07 mg sofort abgebrochen werden. Die Reihenfolge und Art der therapeutischen Maßnahmen richten sich nach dem Schweregrad der Intoxikation:
Bei nur leichter Digitoxinintoxikation reichen Absetzen von Digimed 0,07 mg und sorgfältige Überwachung des Patienten aus. Bedingungen, die zu einer Verminderung der Digitalistoleranz führen, sind zu vermeiden bzw. zu korrigieren (z. B. Störungen im Elektrolyt- und/oder Säure-Basen-Haushalt).
Bedrohliche, digitalisinduzierte Herzrhythmusstörungen
Diese Patienten sollten unter EKG-Monitoring intensivmedizinisch betreut werden. Kalium- und Digitoxinserumkonzentration sollten engmaschig kontrolliert werden.
In Abhängigkeit von der klinischen Situation können folgende Maßnahmen ergriffen werden bei:
- Hypokaliämie:
Anheben des Serumkaliumspiegels auf hochnormale Werte (Kontraindikation: retrograde AV-Blockierungen bei nicht vorhandener Schrittmacher-Therapie).
- komplexen ventrikulären Arrhythmien:
Verabreichung von Phenytoin 250 mg i.v. über 10 min, dann Therapie per os fortsetzen oder Lidocain 100 mg i.v. als Bolus, dann Infusion von 2 mg/min.
- bradykarden Herzrhythmusstörungen:
Verabreichung von Parasympatholytika (z. B. Atropin, Ipratropiumbromid), ggf. ist eine passagere transvenöse Schrittmachersonde angezeigt.
Ein eventuell vorhandenes Magnesiumdefizit ist auszugleichen.
Lebensbedrohliche Intoxikationen:
Bei Einnahme extrem hoher Dosen erfolgen Maßnahmen der primären Giftelimination:
Magenspülung, wenn die Einnahme nicht lange zurückliegt, anschließend Aktivkohle, Cholestyramin oder Colestipol.
Therapie der Wahl einer schweren Digitoxinintoxikation ist die Behandlung mit spezifischem Digitalisantikörperfragment (Digitalis-Antidot), das freies Glykosid zu unwirksamen Antikörper-Glykosid-Komplexen im Extrazellularraum bindet, die dann über die Nieren ausgeschieden werden.
Digitoxin-Serumspiegelmessungen können nach Antidotgabe - je nach Bestimmungsmethode - vorübergehend sehr hohe Werte anzeigen.
Im Rahmen schwerer Intoxikationen treten initial häufig bedrohliche Hyperkaliämien auf, zur Therapie dieser Hyperkaliämien ist die intravenöse Infusion hochprozentiger Glukose und Insulin indiziert.
Forcierte Diurese, Peritoneal- und Hämodialyse haben sich als unwirksam zur Digitoxinelimination erwiesen.
Vor allem durch die selektive Hämoperfusion mit trägergebundenen Digitoxinantikörpern, aber in geringem Umfang auch durch die Hämoperfusion mit beschichteter Aktivkohle oder Plasmapherese kann der Körperbestand von Digitoxin vermindert werden.
5. PHARMAKOLOGISCHE EIGENSCHAFTEN
5.1 Pharmakodynamische Eigenschaften
Pharmakotherapeutische Gruppe: Herzwirksames Glykosid aus Digitalis purpurea. ATC-Code: C01AA04
Digitoxin ist ein langwirkendes Glykosid (Cardenolid). Der kardiale Effekt des Digitoxins ist gekennzeichnet durch:
1. eine positiv inotrope Wirkung
(gesteigerte Kontraktionskraft und -geschwindigkeit bei verzögerter
Relaxationszeit)
2. eine negativ chronotrope Wirkung (Abnahme der Schlagfrequenz)
3. eine negativ dromotrope Wirkung (Verzögerung der Erregungsleitung) und
4. eine positiv bathmotrope Wirkung
(gesteigerte Erregbarkeit, besonders im Bereich der Kammermuskulatur)
Die pharmakodynamischen Effekte von Digitoxin sind bis zu 21 Tagen beobachtbar.
Die primäre Digitoxin-Wirkung ist die spezifische Hemmung der
Adenosintriphosphatase und damit des aktiven Transports von Natrium/Kalium-Ionen (Na+/K+). Die veränderte Ionenverteilung an der Membran bewirkt einen vermehrten Einstrom von Calcium-Ionen und damit eine Zunahme an verfügbarem Calcium zum Zeitpunkt der elektromechanischen Kopplung. Die Wirksamkeit von Digitoxin kann daher verstärkt sein, wenn die extrazelluläre Kalium-Konzentration niedrig ist; demgegenüber hat eine Hyperkalziämie den umgekehrten Effekt.
Die Hemmung des Na+/K+-Austausches führt zu einer Reduktion der Impulsüberleitungsrate im Vorhof und dem AV-Knoten und einer Sensibilisierung der Karotissinusnerven. Indirekt resultieren Veränderungen der kardialen Kontraktilität auch aus der veränderten venösen Dehnbarkeit, die durch den veränderten vegetativen Tonus und die direkte venöse Wirkung hervorgerufen wird.
5.2 Pharmakokinetische Eigenschaften
Die Bioverfügbarkeit von Digitoxin nach oraler Applikation liegt bei 98 - 100 %.
Die Plasmaproteinbindung von Digitoxin liegt bei etwa 90 - 97 %. Der Anteil der freien Digitoxinfraktion im Plasma beträgt bei der Dauerbehandlung Nierengesunder etwa 0,8 ng / ml.
Das Verteilungsvolumen variiert interindividuell zwischen 0,4 und 1 l / kg.
Digitoxin unterliegt einem enterohepatischen Kreislauf.
Etwa 2 % des Gesamtdigitoxins werden in der Leber zu Digoxin hydroxyliert, der größte Teil wird zu Digitoxigenin nach schrittweiser Abspaltung der Digitoxosen epimerisiert und anschließend sulfatiert oder glukuronidiert.
Bei leber- und nierengesunden Patienten werden ca. 60 % über die Nieren, davon die Hälfte als konjugierte Metaboliten, und ca. 40 % im Stuhl ausgeschieden. Die tägliche Abklingquote beträgt 7 - 10 %. Die Eliminationshalbwertszeit beträgt im Mittel 7 - 8 Tage.
Alleinige Störungen der Nierenfunktion haben kaum einen Einfluss auf die Elimination von Digitoxin, da die reduzierte renale Elimination durch vermehrte Metabolisierung und fäkale Elimination kompensiert wird.
Bei Leberinsuffizienz kann, bei gleichzeitiger Leber- und Niereninsuffizienz muss mit erhöhten Digitoxin-Plasmaspiegeln gerechnet werden.
Dialyse eliminiert Digitoxin nur geringfügig, da der größte Teil des Digitoxins an Plasmaproteine gebunden ist.
Digitoxin ist aus Digimed 0,07 mg nahezu vollständig biologisch verfügbar, wie aus Untersuchungen unter Steady-state-Bedingungen (Verlauf der Plasmakonzentrationen über 2 Dosierungsintervalle von je 24 Stunden jeweils nach oraler bzw. intravenöser Applikation radioimmunologisch gemessen) hervorgeht.
Bioverfügbarkeit
Eine im Jahr 1990 durchgeführte Bioverfügbarkeitsuntersuchung an 19 Probanden ergab im Vergleich zum Referenzpräparat:
Testpräparat
maximale Plasmakonzentration (Cmax) 18,2 ± 3,1
[|jg/ml]:
Zeitpunkt der maximalen Plasmakonzentration (tmax) [h]: 1,74 ± 0,81
Fläche unter der Konzentrations-ZeitKurve (AUC0-¥
[h*jg/ml]: 333,0 ± 60,0
Referenzpräparat
18,2 ± 3,8
2,35 ± 0,86
330,6 ± 69,7
Angabe der Werte als Mittelwert und Streubreite
Mittlere Plasmaspiegelverläufe im Vergleich zu einem Referenzpräparat in einem Konzentrations-Zeit-Diagramm:
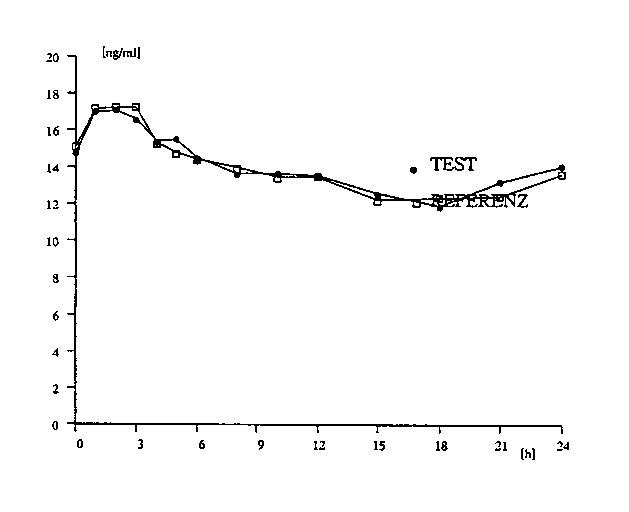
Abb. 1: Mittlere Serumkonzentration-Zeit-Kurven (n=19) von Digitoxin
a) Akute Toxizität
Siehe Punkt 4.9 Überdosierung.
b) Chronische Toxizität
Aufgrund erheblicher Speziesunterschiede im pharmakokinetischen Verhalten (Gewebeverteilung, Metabolismus) ist eine Übertragbarkeit tierexperimenteller toxischer Daten auf den Menschen ohne Bedeutung. Bei chronischer Gabe treten dieselben kardialen und extrakardialen Nebenwirkungen wie beim Menschen auf (siehe Punkt 4.8 Nebenwirkungen).
c) Mutagenes und tumorerzeugendes Potential
In vitro-Untersuchungen zum mutagenen Potential verliefen negativ. Untersuchungen auf ein tumorerzeugendes Potential liegen nicht vor.
d) Reproduktionstoxizität
In Untersuchungen mit Metildigoxin an Ratten und Kaninchen zeigten sich keine Hinweise auf teratogene Eigenschaften. Es ist nicht bekannt, ob Digitoxin die Fertilität beeinflusst. Digitoxin passiert die Plazenta, zur Konzentration im Feten liegen keine Untersuchungen vor. Es gibt jedoch Anhaltspunkte für einen Anstieg der Plazentapassage von Digitalis-Glykosiden im Verlauf der Schwangerschaft.
Sonstige Hinweise
Für die Entscheidung über eine eventuelle Dosiserhöhung kann die Bestimmung der Serum-Digitoxin-Konzentration hilfreich sein. Allerdings sollte bedacht werden, dass der Assay auch auf andere Glykoside anspricht und somit falsch positive Messergebnisse liefern kann. Eine Beobachtung des Patienten während eines vorübergehenden Absetzens der Dosierung von Digitoxin könnte daher geeigneter sein.
6. PHARMAZEUTISCHE ANGABEN
6.1 Liste der sonstigen Bestandteile
Lactose-Monohydrat Kartoffelstärke Mikrokristalline Cellulose Crospovidon
Carboxymethylstärke-Natrium (Typ A) (Ph. Eur.)
Carmellose-Natrium
Cellulosepulver
Hochdisperses Siliciumdioxid
Magnesiumstearat (Ph. Eur.) [pflanzl.]
Povidon K 25
Gelborange S, Aluminiumsalz (E 110)
6.2 Inkompatibilitäten Nicht zutreffend.
6.3 Dauer der Haltbarkeit
2 Jahre
6.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung
Nicht über 25 °C lagern!
In der Originalverpackung aufbewahren.
6.5 Art und Inhalt des Behältnisses
Blisterpackung aus Aluminiumfolie und PVC / PVDC Folie.
Originalpackung mit 50 Tabletten Originalpackung mit 100 Tabletten Unverkäufliches Muster mit 10 Tabletten
Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht.
6.6 Besondere Vorsichtsmaßnahmen für die Beseitigung
Nicht verwendetes Arzneimittel oder Abfallmaterial ist entsprechend den nationalen Anforderungen zu entsorgen.
7. INHABER DER ZULASSUNG
biomo® pharma GmbH
Josef-Dietzgen-Str. 3
53773 Hennef
Tel.: 02242/8740-0
Fax: 02242/8740-499
E-Mail: biomo@biomopharma.de
8. ZULASSUNGSNUMMER
9402.00.00
DATUM DER ERTEILUNG DER ZULASSUNG / VERLÄNGERUNG DER ZULASSUNG
06.10.1992
10.
11.
STAND DER INFORMATION
06/2013
VERKAUFSABGRENZUNG
Verschreibungspflichtig
Seite 18 von 18