Dorzo Plus T Stada 20 Mg/Ml + 5 Mg/Ml Augentropfen
GEBRAUCHSINFORMATION: Information für Anwender
Dorzo plus T STADA® 20 mg/ml + 5 mg/ml Augentropfen
Wirkstoffe: Dorzolamid und Timolol
Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
Anwendung dieses Arzneimittels beginnen, denn sie enthält wichtige
Informationen.
• Heben Sie die Packungsbeilage auf. Vielleicht möchten Sie diese später nochmals lesen.
• Wenn Sie weitere Fragen haben, wenden Sie sich bitte an Ihren Arzt oder Apotheker.
• Dieses Arzneimittel wurde Ihnen persönlich verschrieben. Geben Sie es nicht an Dritte weiter. Es kann anderen Menschen schaden, auch wenn diese die gleichen Beschwerden haben wie Sie.
• Wenn Sie Nebenwirkungen bemerken, wenden Sie sich an Ihren Arzt oder
Apotheker. Dies gilt auch für Nebenwirkungen, die nicht in dieser Packungsbeilage angegeben sind. Siehe Abschnitt 4._
Was in dieser Packungsbeilage steht
1. Was ist Dorzo plus T STADA® und wofür wird es angewendet?
2. Was sollten Sie vor der Anwendung von Dorzo plus T STADA® beachten?
3. Wie ist Dorzo plus T STADA® anzuwenden?
4. Welche Nebenwirkungen sind möglich?
5. Wie ist Dorzo plus T STADA® aufzubewahren?
6. Inhalt der Packung und weitere Informationen
1. Was ist Dorzo plus T STADA® und wofür wird es angewendet?
Dorzo plus T STADA® enthält zwei Wirkstoffe: Dorzolamid und Timolol.
• Dorzolamid gehört zur Arzneimittelgruppe der so genannten „Carboanhydrasehemmer“.
• Timolol gehört zur Arzneimittelgruppe der so genannten „Betablocker“.
Dorzo plus T STADA® wird zur Senkung des erhöhten Augeninnendrucks
bei der Glaukombehandlung verordnet, wenn Betablocker-Augentropfen allein nicht ausreichen.
2. Was sollten Sie vor der Anwendung von Dorzo plus T STADA® beachten?
Dorzo plus T STADA® darf NICHT angewendet werden • wenn Sie allergisch gegen Dorzolamid, Timolol, Betablocker oder einen der in Abschnitt 6. genannten sonstigen Bestandteile dieses Arzneimittels sind,
• wenn Sie zurzeit oder in der Vergangenheit an Atemwegserkrankungen wie Asthma oder schwerer chronisch-obstruktiver Bronchitis (einer schweren Lungenerkrankung, die zu Keuchen, Atemschwierigkeiten und/oder anhaltendem Husten führen kann) leiden oder gelitten haben,
• wenn Sie schwerwiegende Nierenprobleme oder in der Vergangenheit an Nierensteinen gelitten haben,
• wenn Sie eine Störung des Blut-pH-Wertes (Säure-Basen-Gleichgewicht) haben,
• wenn Sie unter bestimmten Herzproblemen leiden einschließlich bestimmter Herzrhythmusstörungen mit einem ungewöhnlich langsamen Herzschlag oder schwerer Herzschwäche.
Wenn Sie glauben, dass etwas davon auf Sie zutrifft, dürfen Sie Dorzo plus T STADA® nicht anwenden, bevor Sie mit Ihrem Arzt gesprochen haben.
Warnhinweise und Vorsichtsmaßnahmen
Bitte sprechen Sie mit Ihrem Arzt oder Apotheker, bevor Sie Dorzo plus T STADA® anwenden, wenn Sie an einer der folgenden Störungen leiden oder in der Vergangenheit gelitten haben:
• Erkrankung der Herzkranzgefäße (koronare Herzkrankheit; die Anzeichen können Schmerzen [auch beim Ruhen] oder Engegefühl in der Brust, Atemnot oder Erstickungsgefühl umfassen), Herzleistungsschwäche, niedriger Blutdruck,
• Atemprobleme, Asthma oder chronisch-obstruktive Lungenerkrankung
(eine Lungenerkrankung mit Verengung der Atemwege),
• Durchblutungsstörungen (wie z.B. Raynaud-Syndrom),
• Diabetes, da Timolol die Anzeichen eines niedrigen Blutzuckerspiegels verschleiern kann,
• Überfunktion der Schilddrüse, da Timolol die Anzeichen dafür verschleiern kann,
• Allergie gegen Arzneimittel.
Bevor Sie sich einer Operation unterziehen, informieren Sie bitte Ihren Arzt darüber, dass Sie Dorzo plus T STADA® anwenden, da Dorzolamid/Timolol die Wirkung einiger Arzneimittel verändern kann, die zur Narkose eingesetzt werden. Bei einer Narkose kann ein plötzlicher Blutdruckabfall auftreten.
Informieren Sie Ihren Arzt, wenn Sie Leberprobleme haben oder in der Vergangenheit hatten, wenn Sie an Muskelschwäche leiden oder bei Ihnen eine Myasthenia gravis (bestimmte Muskelerkrankung) diagnostiziert wurde.
Suchen Sie sofort Ihren Arzt auf, wenn eine Bindehautentzündung (Rötung und Reizung der Augen), eine Schwellung der Augen oder Augenlider, Hautausschlag oder Juckreiz im oder um das Auge herum auftritt. Diese Symptome können auf eine allergische Reaktion zurückzuführen oder auch eine Nebenwirkung von Dorzo plus T STADA® sein (siehe unter Abschnitt 4: Welche Nebenwirkungen sind möglich?).
Informieren Sie Ihren Arzt, wenn sich eine Augeninfektion entwickelt, Sie sich am Auge verletzen, Sie sich einer Augenoperation unterziehen müssen oder wenn Sie neue oder sich verschlimmernde Beschwerden bzw. Reaktionen bemerken.
Wenn Sie Kontaktlinsen tragen, müssen Sie diese vor der Anwendung Ihrer Augentropfen entfernen und dürfen diese frühestens 15 Minuten nach der Anwendung wieder einsetzen. Das Konservierungsmittel Benzalkoniumchlorid kann zur Verfärbung weicher Kontaktlinsen führen.
Kinder
Zur Anwendung von Dorzo plus T STADA® bei Säuglingen und Kindern sind begrenzte Erfahrungen vorhanden.
Ältere Patienten
In Studien mit Dorzolamid/Timolol-Augentropfen waren die Wirkungen dieser Augentropfen bei älteren und jüngeren Patienten gleich.
Auswirkungen bei Fehlgebrauch zu Dopingzwecken
Die Anwendung von Dorzo plus T STADA® kann bei Dopingkontrollen zu positiven Ergebnissen führen. Die gesundheitlichen Folgen der Anwendung von Dorzo plus T STADA® als Dopingmittel können nicht abgesehen werden, schwerwiegende Gesundheitsgefährdungen sind nicht auszuschließen.
Anwendung von Dorzo plus T STADA® zusammen mit anderen Arzneimitteln
Dorzo plus T STADA® kann die Wirkung anderer Arzneimittel, die Sie anwenden, beeinflussen oder von diesen beeinflusst werden, einschließlich anderer Augentropfen für die Behandlung eines Glaukoms. Informieren Sie Ihren Arzt, wenn Sie blutdrucksenkende Arzneimittel, Herzmittel oder Arzneimittel zur Behandlung eines Diabetes mellitus anwenden oder beabsichtigen anzuwenden.
Informieren Sie Ihren Arzt oder Apotheker immer, wenn Sie andere Arzneimittel anwenden, kürzlich andere Arzneimittel angewendet haben oder beabsichtigen, andere Arzneimittel anzuwenden. Dies ist besonders wichtig, wenn eine der folgenden Angaben auf Sie zutrifft:
• Sie nehmen Antihypertonika ein, die zur Senkung eines hohen Blutdrucks angewendet werden, oder Arzneimittel zur Behandlung von Herzerkrankungen, wie z.B. Calciumkanalblocker, Betablocker und Digoxin.
• Sie nehmen Arzneimittel zur Behandlung eines gestörten oder unregelmäßigen Herzschlags ein, wie z.B. Chinidin (auch zur Behandlung einiger Malaria-Arten verwendet) oder Digoxin.
• Sie verwenden weitere Augentropfen, die einen Betablocker enthalten.
• Sie nehmen einen weiteren Carboanhydrasehemmer, wie z.B. Acetazolamid ein. Dabei kann es sich um Arzneimittel zum Einnehmen, Augentropfen oder ein in einer anderen Weise anzuwendendes Arzneimittel handeln.
• Sie nehmen Monoaminoxidase-Hemmer (MAO-Hemmer) oder selektive Serotonin-Wiederaufnahmehemmer (SSRI, z.B. Fluoxetin und Paroxetin) zur Behandlung von Depressionen oder anderen Erkrankungen ein.
• Sie nehmen ein Parasympathomimetikum ein, das Ihnen zur besseren
Urinausscheidung verschrieben worden sein könnte. Parasympathomimetika gehören auch zu einer Art von Arzneimitteln, die manchmal zur Normalisierung von Darmbewegungen verwendet werden.
• Sie nehmen Betäubungsmittel, wie z.B. Morphin, die zur Behandlung mäßiger bis starker Schmerzen angewendet werden, oder hohe Dosen Acetylsalicylsäure ein. Obwohl keine Hinweise dafür vorliegen, dass Dorzolamidhydrochlorid mit Acetylsalicylsäure Wechselwirkungen eingeht, ist von einigen anderen mit Dorzolamidhydrochlorid verwandten oral einzunehmenden Arzneimitteln bekannt, dass sie mit Acetylsalicylsäure Wechselwirkungen haben.
• Sie nehmen Arzneimittel zur Behandlung von Diabetes oder hohem Blutzucker ein.
• Sie nehmen Epinephrin (Adrenalin) ein.
Schwangerschaft und Stillzeit
Wenn Sie schwanger sind oder stillen, oder wenn Sie vermuten, schwanger zu sein oder beabsichtigen, schwanger zu werden, fragen Sie vor der Anwendung dieses Arzneimittels Ihren Arzt oder Apotheker um Rat.
Schwangerschaft
Wenden Sie Dorzo plus T STADA® nicht an, wenn Sie schwanger sind, es sei denn, Ihr Arzt hält dies für erforderlich. Informieren Sie Ihren Arzt, wenn Sie schwanger sind oder eine Schwangerschaft planen.
Stillzeit ®
Wenden Sie Dorzo plus T STADA® nicht an, wenn Sie stillen. Timolol kann in die Muttermilch übergehen. Informieren Sie Ihren Arzt, wenn Sie stillen oder beabsichtigen zu stillen.
Verkehrstüchtigkeit und Fähigkeit zum Bedienen von Maschinen
Dorzo plus T STADA® kann bei einigen Patienten Nebenwirkungen wie Verschwommensehen hervorrufen. Sie dürfen sich nicht an das Steuer eines Fahrzeugs setzen oder Werkzeuge oder Maschinen bedienen, bis die Symptome abgeklungen sind.
Dorzo plus T STADA®enthält Benzalkoniumchlorid
• Benzalkoniumchlorid kann Reizungen am Auge hervorrufen.
• Vermeiden Sie den Kontakt mit weichen Kontaktlinsen. Benzalkoniumchlorid kann zur Verfärbung weicher Kontaktlinsen führen.
• Kontaktlinsen müssen Sie vor der Anwendung entfernen und dürfen diese frühestens 15 Minuten nach der Anwendung wieder einsetzen.
3. Wie ist Dorzo plus T STADA® anzuwenden?
Wenden Sie dieses Arzneimittel immer genau nach Absprache mit Ihrem Arzt oder Apotheker an. Fragen Sie bei Ihrem Arzt oder Apotheker nach, wenn Sie sich nicht sicher sind.
Die richtige Dosierung und Dauer der Behandlung wird von Ihrem Arzt festgelegt.
Erwachsene
Die empfohlene Dosis beträgt
• 2-mal täglich 1 Tropfen in die betroffenen Augen, z.B. morgens und abends.
Wenn Sie außer Dorzo plus T STADA® noch andere Arzneimittel am Auge anwenden, sollte zwischen der Verabreichung von Dorzo plus T STADA® und den anderen Augentropfen mindestens ein zeitlicher Abstand von 10 Minuten liegen.
Ändern Sie die Dosierung des Arzneimittels nicht ohne Rücksprache mit Ihrem Arzt. Wenn Sie die Behandlung abbrechen müssen, suchen Sie sofort Ihren Arzt auf.
Berühren Sie mit der Tropferspitze des Behältnisses nicht Ihre Augen oder die Umgebung der Augen. Es kann sonst zur Verunreinigung des Behältnisses mit Bakterien kommen, was Augeninfektionen verursachen und zu schweren Augenschädigungen bis hin zum Verlust des Sehvermögens führen kann.
Um eine Verunreinigung des Behältnisses zu vermeiden, müssen Sie sicherstellen, dass Sie mit der Tropferspitze keine Oberflächen berühren!
Um eine korrekte Dosierung sicherzustellen, dürfen Sie die Öffnung in der Tropferspitze nicht vergrößern.
Hinweise zur Anwendung
Es wird empfohlen, vor der Anwendung der Augentropfen die Hände zu waschen. Möglicherweise fällt Ihnen die Anwendung der Augentropfen leichter, wenn Sie dabei in einen Spiegel sehen.
1. Vergewissern Sie sich vor der ersten Anwendung des Arzneimittels, dass der Sicherheitsstreifen am Flaschenhals unversehrt ist. Ein Spalt zwischen Flasche und Schraubdeckel ist bei ungeöffneter Flasche normal.
2. Nehmen Sie den Schraubdeckel von der Flasche ab.
3. Beugen Sie den Kopf nach hinten und ziehen Sie das Unterlid leicht herab, damit sich zwischen Ihrem Augenlid und Ihrem Auge eine Tasche bildet.
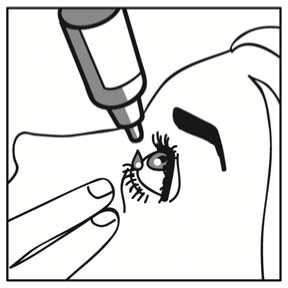
4. Kippen Sie die Flasche und drücken Sie sie leicht zusammen, bis ein einzelner Tropfen in das Auge gelangt, wie von Ihrem Arzt verordnet. Berühren Sie mit der Tropferspitze nicht Ihr Auge oder Augenlid.
5. Drücken Sie nach der Anwendung von Dorzo plus T STADA® 2 Minuten lang mit einem Finger auf den inneren Augenwinkel neben der Nase. Dies verhindert, dass Dorzolamid/Timolol von Ihrem Körper aufgenommen wird.
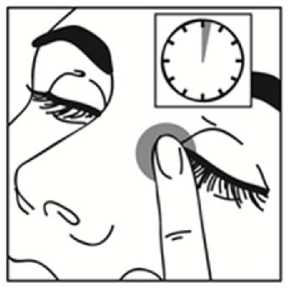
6. Falls von Ihrem Arzt angeordnet, wiederholen Sie die Schritte 3 bis 5 am anderen Auge.
7. Verschließen Sie die Flasche direkt nach der Anwendung wieder mit dem Schraubdeckel und stellen Sie die Flasche wieder in den Originalkarton zurück.
Wenn Sie eine größere Menge von Dorzo plus T STADA® angewendet haben, als Sie sollten
Es ist wichtig, dass Sie sich an die von Ihrem Arzt verschriebene Dosierung halten. Wenn Sie zu viele Tropfen in Ihr Auge einbringen oder etwas vom Inhalt der Flasche schlucken, können Sie sich unwohl fühlen, es kann Ihnen z.B. schwindelig werden und Schwierigkeiten beim Atmen können auftreten oder Sie werden bemerken, dass Ihr Herzschlag langsamer wird als gewöhnlich.
Wenn Sie eine der oben stehenden Wirkungen bemerken, müssen Sie sofort ärztlichen Rat einholen.
Wenn Sie die Anwendung von Dorzo plus T STADA® vergessen haben
Es ist wichtig, dass Sie Dorzo plus T STADA® nach der Anweisung Ihres Arztes anwenden.
Wenn Sie eine Dosis vergessen haben, holen Sie sie schnellstmöglich nach. Ist es jedoch fast Zeit für die nächste Anwendung, lassen Sie die vergessene Dosis aus und kehren Sie zu Ihrem regelmäßigen Dosierungsschema zurück.
Wenden Sie nicht die doppelte Dosis an, um eine vergessene Dosis nachzuholen.
Wenn Sie die Anwendung von Dorzo plus T STADA® abbrechen
Wenn Sie die Behandlung mit diesem Arzneimittel abbrechen möchten, sprechen Sie zuerst mit Ihrem Arzt.
Wenn Sie weitere Fragen zur Anwendung dieses Arzneimittels haben, wenden Sie sich an Ihren Arzt oder Apotheker.
4. Welche Nebenwirkungen sind möglich?
Wie alle Arzneimittel kann auch dieses Arzneimittel Nebenwirkungen haben, die aber nicht bei jedem auftreten müssen.
Sie können die Augentropfen in der Regel weiter anwenden, es sei denn, die Nebenwirkungen sind schwerwiegend. Bitte wenden Sie sich an Ihren Arzt oder Apotheker, wenn Sie beunruhigt sind. Beenden Sie die Anwendung von Dorzo plus T STADA® nicht, ohne vorher mit Ihrem Arzt zu sprechen.
Wenn bei Ihnen allergische Reaktionen mit Nesselsucht (Urtikaria), Schwellung von Gesicht, Lippen Zunge und/oder Rachen auftreten, die zu Atem- oder Schluckstörungen führen können, müssen Sie die Anwendung von Dorzo plus T STADA® sofort beenden und sofort Ihren Arzt informieren.
Sehr häufig (kann mehr als 1 von 10 Behandelten betreffen):
Brennen und Stechen in den Augen, Geschmacksstörung.
Häufig (kann bis zu 1 von 10 Behandelten betreffen):
Rötung der Augen und der Augenumgebung, Tränen und Jucken der Augen, Auswirkungen auf die Augenoberfläche, Schwellung und/oder Reizung der Augen und der Augenumgebung, Fremdkörpergefühl im Auge (Hornhauterosion), verminderte Empfindlichkeit der Hornhaut (gegenüber Fremdkörpern im Auge und Schmerzen), Augenschmerzen, trockene Augen, Verschwommensehen, Kopfschmerzen, Nasennebenhöhlenentzündung (Spannungs- oder Druckgefühl in der Nase), Übelkeit und Müdigkeit/Erschöpfung.
Gelegentlich (kann bis zu 1 von 100 Behandelten betreffen):
Schwindel, Depressionen, Entzündung der Regenbogenhaut, verschwommenes Sehen (in einigen Fällen aufgrund des Absetzens eines Arzneimittels zur Behandlung einer übermäßigen Pupillenverengung im Auge), verlangsamter Herzschlag, plötzlicher Bewusstseinsverlust, Verdauungsstörungen und Nierensteine (häufig durch plötzlich auftretende starke, krampfartige Schmerzen im unteren und/oder seitlichen Rückenbereich, in der Leistengegend oder im Bauchraum erkennbar).
Selten (kann bis zu 1 von 1.000 Behandelten betreffen):
Systemischer Lupus erythematodes (eine Immunerkrankung, die eine Entzündung innerer Organe verursachen kann), Kribbeln oder taubes Gefühl der Hände oder Füße, Schlafstörungen, Albträume, Gedächtnisverlust, Muskelschwäche, verminderter Geschlechtstrieb, Schlaganfall, vorübergehende Kurzsichtigkeit, die nach Beendigung der Behandlung zurückgehen kann, Flüssigkeitsansammlung unter der Netzhaut (Aderhautabhebung nach fistulierenden Operationen), Herabhängen der Augenlider, Doppeltsehen, Verkrustung der Augenlider, Hornhautschwellung (mit Sehstörungen als Begleiterscheinung), niedriger Augeninnendruck, Ohrgeräusche (Tinnitus), niedriger Blutdruck, unregelmäßiger Herzschlag, Schmerzen im Brustkorb, Herzklopfen (schneller und/oder unregelmäßiger Herzschlag), Herzblock/Herzstillstand, kongestive Herzinsuffizienz (eine Herzerkrankung, die mit Atemlosigkeit und geschwollenen Beinen und Füßen aufgrund von Wasserstauungen einhergeht), Ödeme (Wasserstauungen), verminderte Durchblutung des Gehirns, Schwellungen oder Kältegefühl an Händen und Füßen und Durchblutungsstörungen der Arme und Beine, schlechte Blutzirkulation, was dazu führt, dass die Zehen und Finger taub werden und sich verfärben (Raynaud-Syndrom), Krämpfe in den Beinen und/oder Schmerzen beim Gehen (Claudicatio), Kurzatmigkeit, Atemlosigkeit, laufende oder verstopfte Nase, Nasenbluten, Atemschwierigkeiten/Atemnot, Husten, Halsreizung, Mundtrockenheit, Durchfall, allergische Hautreaktion (Kontaktdermatitis), Haarausfall, Schuppenflechte (Psoriasis) oder Verschlechterung einer Schuppenflechte, Peyronie-Krankheit (kann zur Krümmung des Penis führen), Schwäche/Müdigkeit, generalisierte allergische Reaktionen inklusive Schwellungen unterhalb der Haut, die im Gesicht (Schwellung von Lippen, Augen und des Mundes) und den Gliedern auftreten können und dazu führen können, dass die Atemwege verstopft sind und Schwierigkeiten beim Schlucken oder Atmen auftreten, pfeifende Atemgeräusche/Giemen, Nesselsucht (Urtikaria), juckender Hautausschlag, generalisierter oder lokalisierter Hautausschlag, Juckreiz, schwere lebensbedrohliche allergische Reaktionen.
Wie andere Arzneimittel, die am Auge angewendet werden, wird auch Timolol in das Blut aufgenommen. Dadurch können ähnliche Nebenwirkungen auftreten wie sie bei Einnahme von Betablockern oder ihrer Verabreichung in eine Vene beobachtet werden. Das Auftreten von Nebenwirkungen nach örtlicher Anwendung am Auge ist geringer als wenn Arzneimittel z.B. eingenommen oder mit Hilfe einer Spritze gegeben werden. Aufgeführt sind solche Nebenwirkungen, die in der Klasse der Betablocker bei Anwendung zur Behandlung von Augenerkrankungen beobachtet wurden.
Nicht bekannt (Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar):
• Niedriger Blutzuckerspiegel,
• Herzversagen,
• Bauchschmerzen, Erbrechen,
• Muskelschmerzen, die nicht durch Anstrengung verursacht werden,
• sexuelle Funktionsstörungen.
Meldung von Nebenwirkungen
Wenn Sie Nebenwirkungen bemerken, wenden Sie sich an Ihren Arzt oder Apotheker. Dies gilt auch für Nebenwirkungen, die nicht in dieser Packungsbeilage angegeben sind. Sie können Nebenwirkungen auch direkt anzeigen:
Bundesinstitut für Arzneimittel und Medizinprodukte Abt. Pharmakovigilanz Kurt-Georg-Kiesinger-Allee 3 D-53175 Bonn Website: www.bfarm.de
Indem Sie Nebenwirkungen melden, können Sie dazu beitragen, dass mehr Informationen über die Sicherheit dieses Arzneimittels zur Verfügung gestellt werden.
5. Wie ist Dorzo plus T STADA® aufzubewahren?
Bewahren Sie dieses Arzneimittel für Kinder unzugänglich auf.
Sie dürfen dieses Arzneimittel nach dem auf dem Etikett und dem Umkarton nach „verwendbar bis" angegebenen Verfallsdatum nicht mehr verwenden. Das Verfallsdatum bezieht sich auf den letzten Tag des angegebenen Monats.
Für dieses Arzneimittel sind keine besonderen Lagerungsbedingungen erforderlich.
Dorzo plus T STADA® sollte nicht länger als 28 Tage nach Anbruch der Flasche verwendet werden. Das heißt, dass Sie die Flasche 4 Wochen nach Anbruch entsorgen müssen, auch wenn der Inhalt noch nicht vollständig aufgebraucht ist. Notieren Sie daher in dem dafür vorgesehenen Feld auf dem Umkarton den Tag, an dem Sie die Flasche zum ersten Mal geöffnet haben.
Entsorgen Sie Arzneimittel nicht im Abwasser oder Haushaltsabfall. Fragen Sie Ihren Apotheker, wie das Arzneimittel zu entsorgen ist, wenn Sie es nicht mehr verwenden. Sie tragen damit zum Schutz der Umwelt bei.
6. Inhalt der Packung und weitere Informationen
Was Dorzo plus T STADA® enthält
Die Wirkstoffe sind: Dorzolamid und Timolol.
1 ml enthält 20 mg Dorzolamid (als 22,6 mg Dorzolamidhydrochlorid) und 5 mg Timolol (als 6,83 mg Timololmaleat).
Die sonstigen Bestandteile sind
Mannitol (Ph. Eur.), Natriumcitrat (Ph. Eur.), Hyetellose, NatriumhydroxidLösung (zur Einstellung des pH-Wertes), Benzalkoniumchlorid-Lösung, Wasser für Injektionszwecke.
Wie Dorzo plus T STADA® aussieht und Inhalt der Packung
Dorzo plus T STADA® ist eine sterile, klare, leicht zähflüssige, farblose wässrige Augentropfenlösung.
Dorzo plus T STADA® ist in einer weißen undurchsichtigen Flasche aus MDPE mit versiegelter Tropferspitze aus LDPE und HDPE-Schraubdeckel mit Originalitätsverschluss, die 5 ml Augentropfenlösung enthält.
Dorzo plus T STADA® ist in Packungen mit 1 Flasche, 3 Flaschen oder 6 Flaschen erhältlich.
Pharmazeutischer Unternehmer
STADApharm GmbH, Stadastraße 2-18, 61118 Bad Vilbel Telefon: 06101 603-0, Telefax: 06101 603-259, Internet: www.stada.de
Hersteller
STADA Arzneimittel AG, Stadastraße 2-18, 61118 Bad Vilbel oder
Pharmathen S.A., 6 Dervenakion Str., 15351 Pallini Attikis, Griechenland oder
Famar S.A., 63 AG. Dimitriou Aven, 17456 Alimos/Athen, Griechenland oder
STADA Arzneimittel GmbH, Muthgasse 36/2, 1190 Wien, Österreich oder
Eurogenerics NV, Heizel Esplanade b 22, 1020 Brüssel, Belgien oder
PharmaCoDane ApS, Marielundvej 46A, 2730 Herlev, Dänemark
Dieses Arzneimittel ist in den Mitgliedstaaten des Europäischen Wirtschaftsraumes (EWR) unter den folgenden Bezeichnungen zugelassen:
Belgien Dorzolamide/Timolol EG 20 mg/ml + 5
Dänemark
Deutschland
Finnland
Frankreich
Irland
Italien
Luxemburg
Niederlande
Österreich
Spanien
Vereinigtes Königreich
mg/ml oogdruppels, oplossing Costad
Dorzo plus T STADA® 20 mg/ml + 5 mg/ml Augentropfen Glaukostad 20 mg/ml + 5 mg/ml silmätipat, liuos
Dorzolamide/Timolol EG 20 mg/ml + 5
mg/ml, collyre en solution
Claropt 20 mg/ml + 5 mg/ml eye drops,
solution
Dorzolamide e Timololo EG 20 mg/ml + 5
mg/ml collirio, soluzione
Doticol (20 + 5) mg/ml eye drops solution
Dorzolamide/Timolol CF 20 + 5 mg/ml
oogdruppels, oplossing
Dorzastad 20 mg/ml + 5 mg/ml
Augentropfen
Dorzolamida/Timolol STADA 20 mg/ml + 5
mg/ml colirio en solucion
Doticol 20 mg/ml + 5 mg/ml eye drops
solution
Diese Packungsbeilage wurde zuletzt überarbeitet im Mai 2014.
11