Doxazosin Al 8
Fachinformation (Zusammenfassung der Merkmale des Arzneimittels/SPC)
1. Bezeichnung des Arzneimittels
Doxazosin AL 1 Doxazosin 1 mg pro Tablette
Doxazosin AL 2 Doxazosin 2 mg pro Tablette
Doxazosin AL 4 Doxazosin 4 mg pro Tablette
Doxazosin AL 8 Doxazosin 8 mg pro Tablette
2. Qualitative und quantitative Zusammensetzung
Doxazosin AL 1
1 Tablette enthält 1,21 mg Doxazosinmesilat (entspr. 1 mg Doxazosin). Sonstiger Bestandteil mit bekannter Wirkung: 1 Tablette enthält 40 mg Lactose.
Doxazosin AL 2
1 Tablette enthält 2,43 mg Doxazosinmesilat (entspr. 2 mg Doxazosin). Sonstiger Bestandteil mit bekannter Wirkung: 1 Tablette enthält 40 mg Lactose.
Doxazosin AL 4
1 Tablette enthält 4,85 mg Doxazosinmesilat (entspr. 4 mg Doxazosin). Sonstiger Bestandteil mit bekannter Wirkung: 1 Tablette enthält 80 mg Lactose.
Doxazosin AL 8
1 Tablette enthält 9,70 mg Doxazosinmesilat (entspr. 8 mg Doxazosin). Sonstiger Bestandteil mit bekannter Wirkung: 1 Tablette enthält 80,88 mg Lactose-Monohydrat.
Vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt 6.1.
3. Darreichungsform
Tablette Doxazosin AL 1
Weiße, runde, bikonvexe Tablette mit Prägung „D1".
Doxazosin AL 2
Weiße, oblonge Tablette mit einseitiger Bruchkerbe und Prägung „D2".
Die Tablette kann in gleiche Dosen geteilt werden.
Doxazosin AL 4
Weiße, oblonge Tablette mit einseitiger Bruchkerbe und Prägung „D4".
Die Tablette kann in gleiche Dosen geteilt werden.
Doxazosin AL 8
Weiße bis fast weiße, runde, bikonvexe Tablette mit beidseitiger Kreuzbruchkerbe (Vario-Tab®) und Prägung „D", „Z", „S" und „8" auf einer Seite. Die Tablette kann in gleiche Dosen geteilt werden.
4. Klinische Angaben
4.1 Anwendungsgebiete
Essenzielle Hypertonie.
4.2 Dosierung und Art der Anwendung Dosierung
Zu Beginn der Behandlung wird 1 mg Doxazosin 1-mal täglich eingenommen. In Abhängigkeit von der Wirksamkeit kann die Dosis individuell bei Bedarf jeweils nach 1 - 2 Wochen auf 2 mg Doxazosin 1-mal täglich, dann auf 4 mg Doxazosin 1-mal täglich und schließlich auf 8 mg Doxazosin 1-mal täglich gesteigert werden.
Die durchschnittliche Tagesdosis für die Erhaltungstherapie beträgt 2 - 4 mg Doxazosin 1-mal täglich.
Die maximale Tagesdosis beträgt 16 mg Doxazosin 1-mal täglich.
Zusätzlich für Doxazosin AL 8 Hinweis:
Doxazosin AL 8 ist aufgrund des hohen Wirkstoffgehalts nicht für den Therapiebeginn geeignet.
Ältere Patienten
Da die pharmakokinetischen Eigenschaften von Doxazosin bei älteren Patienten unverändert sind, wird im Allgemeinen die Anwendung der normalen Dosierungen empfohlen.
Patienten mit Niereninsuffizienz
Da es bei Patienten mit Niereninsuffizienz keinen Hinweis darauf gibt, dass Doxazosin eine bestehende Niereninsuffizienz verschlimmert, wird allgemein die Anwendung der normalen Dosierungen empfohlen. Die Dosis sollte jedoch so niedrig wie möglich gehalten werden und eine Dosissteigerung nur unter genauer Beobachtung vorgenommen werden. Doxazosin unterliegt einer starken Proteinbindung. Daher kann es durch Dialyse nicht eliminiert werden.
Patienten mit Leberinsuffizienz
Bei Patienten mit eingeschränkter Leberfunktion sollte Doxazosin besonders vorsichtig dosiert werden.
Bei Patienten mit schwerwiegender Leberfunktionsstörung liegen keine klinischen Erfahrungen vor (siehe Abschnitt 4.4).
Kinder und Jugendliche
Mangels ausreichender klinischer Erfahrungen bei Kindern wird die Anwendung von Doxazosin bei Kindern nicht empfohlen.
Art der Anwendung
Die Einnahme von Doxazosin AL kann unabhängig von den Mahlzeiten mit ausreichend Flüssigkeit (z.B. 1 Glas Wasser) erfolgen.
Zusätzlich für Doxazosin AL 8
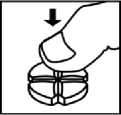
Zur Erleichterung einer individuellen Dosierung steht Doxazosin AL 8 als Tablette mit Kreuzbruchkerbe (Vario-Tab®) zur Verfügung.
Die Tablette wird mit der tieferen Bruchkerbe nach oben auf eine harte flache Unterlage gelegt. Durch leichten Daumendruck von oben wird die Tablette in vier gleich große Teile zerteilt.
4.3 Gegenanzeigen
• Überempfindlichkeit gegen den Wirkstoff, andere Chinazoline (z.B. Prazosin, Terazosin) oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile,
• anamnestisch bekannte orthostatische Hypotonie,
• benigne Prostatahyperplasie und gleichzeitig bestehende Stauung im oberen Harntrakt, chronische Harnwegsinfektion oder Blasensteine,
• Stillzeit (siehe Abschnitt 4.6).
Doxazosin ist kontraindiziert als Monotherapie bei Patienten mit Überlaufblase oder Anurie mit oder ohne progredienter Niereninsuffizienz.
4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung
Therapiebeginn
Aufgrund der alphablockierenden Eigenschaften von Doxazosin kann es bei Patienten zu einer orthostatischen Hypotonie kommen, die sich als
Schwindelgefühl und Schwäche oder selten als Ohnmacht (Synkope) äußert, insbesondere bei Therapiebeginn. Deshalb empfiehlt es sich, den Blutdruck bei Therapiebeginn zu überwachen, um das Risiko orthostatischer Effekte zu verringern. Der Patient sollte angewiesen werden, vorsichtshalber Situationen zu meiden, in denen Verletzungsgefahr bestehen könnte, falls bei Einleitung der Doxazosin-Therapie Schwindelgefühl oder Schwäche auftritt.
Anwendung bei Patienten mit akuten Herzerkrankungen Wie bei anderen gefäßerweiternden Antihypertensiva empfiehlt es sich, bei der Anwendung von Doxazosin bei Patienten mit den folgenden akuten Herzerkrankungen Vorsicht walten zu lassen:
• Lungenödem infolge einer Aorten- oder Mitralklappenstenose,
• High-Output-Herzinsuffizienz,
• Rechtsherzinsuffizienz infolge von Lungenembolie oder Perikarderguss,
• Linksherzinsuffizienz mit niedrigem Füllungsdruck.
Bei Patienten mit schwerer koronarer Herzkrankheit kann ein zu rascher oder zu starker Blutdruckabfall zu einer Verschlechterung der Angina pectoris-Beschwerden führen.
Bei Patienten, die eine salzarme Diät einhalten oder die mit Diuretika behandelt werden, ist das Risiko von Kreislaufstörungen insbesondere bei Lagewechsel erhöht.
Anwendung zusammen mit PDE-5-Inhibitoren
Die gleichzeitige Anwendung von Phosphodiesterase-5-Inhibitoren (z.B. Sildenafil, Tadalafil und Vardenafil) und Doxazosin AL kann bei einigen Patienten zu einer symptomatischen Hypotonie führen. Um das Risiko für die Entwicklung einer orthostatischen Hypotonie zu vermindern, sollten die Patienten stabil auf die Alpha-Blocker-Therapie eingestellt sein, wenn sie Phosphodiesterase-5-Inhibitoren anwenden. Weiterhin wird empfohlen, mit der niedrigsten Dosis des Phosphodiesterase-5-Inhibitors zu beginnen und diesen in einem zeitlichen Abstand zur Gabe von Doxazosin (mindestens 6 Stunden) einzunehmen.
Anwendung bei Patienten, die sich einer Kataraktoperation unterziehen Bei einigen Patienten, die gleichzeitig oder bis kurz vorher mit Tamsulosin behandelt wurden, trat während Katarakt-Operationen das sog. „Intraoperative Floppy Iris Syndrome" (IFIS, eine Variante des Syndroms der engen Pupille) auf. Da auch bei Anwendung anderer Alpha-Blocker vereinzelt das Auftreten eines IFIS gemeldet wurde, kann ein Gruppeneffekt nicht ausgeschlossen werden. IFIS kann zu Komplikationen während der Operation führen. Deshalb sollten Kataraktchirurgen und Augenärzte vor einer Kataraktoperation darüber informiert werden, ob die Patienten aktuell Alpha-Blocker anwenden oder diese früher erhielten.
Patienten mit Leberinsuffizienz
Wie alle Arzneimittel, die vollständig durch die Leber metabolisiert werden, sollte Doxazosin bei Patienten mit Anzeichen einer eingeschränkten Leberfunktion besonders vorsichtig angewendet werden. Da keine klinischen Erfahrungen bei Patienten mit schwerer Leberfunktionsstörung vorliegen, wird die Anwendung bei diesen Patienten nicht empfohlen.
Patienten mit der seltenen hereditären Galactose-Intoleranz, Lactase-Mangel oder Glucose-Galactose-Malabsorption sollten Doxazosin AL nicht einnehmen.
4.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen
Die gleichzeitige Anwendung von Phosphodiesterase-5-Inhibitoren (z.B. Sildenafil, Vardenafil, Tadalafil) kann bei manchen Patienten zu einer symptomatischen Hypotonie führen (siehe Abschnitt 4.4).
Doxazosin ist im Plasma überwiegend (zu 98%) an Proteine gebunden. Aus In-vitro-Daten im Humanplasma geht hervor, dass Doxazosin keinen Einfluss auf die Proteinbindung von Digoxin, Warfarin, Phenytoin oder Indometacin hat.
Gebräuchliches Doxazosin wurde mit Thiaziddiuretika, Furosemid,
Betablockern, Antibiotika, oralen Antidiabetika, Urikosurika und Antikoagulanzien angewendet, ohne dass in der klinischen Erfahrung Arzneimittelwechselwirkungen auftraten. Jedoch liegen keine Daten aus formalen Arzneimittelwechselwirkungsstudien vor.
Doxazosin verstärkt die blutdrucksenkende Wirkung anderer Alphablocker und anderer Antihypertensiva.
In einer offenen, randomisierten und placebokontrollierten Studie bei 22 gesunden männlichen Probanden führte die Verabreichung einer Einzeldosis von 1 mg Doxazosin an Tag 1 einer 4-tägigen Behandlung mit oralem Cimetidin (2-mal täglich 400 mg) zu einer Zunahme der mittleren AUC von Doxazosin um 10%, dagegen zu keinen statistisch signifikanten Veränderungen der mittleren Cmax und der mittleren Halbwertszeit von Doxazosin. Die Zunahme der mittleren AUC von Doxazosin um 10% bei gemeinsamer Anwendung mit Cimetidin liegt innerhalb der interindividuellen Variabilität (27%) der mittleren AUC von Doxazosin zusammen mit Plazebo.
Folgende Wechselwirkungen können bei gleichzeitiger Anwendung von Doxazosin und den nachfolgend genannten Arzneimitteln bzw. Substanzen auftreten:
Die blutdrucksenkende Wirkung von Doxazosin kann verstärkt werden durch:
• Vasodilatatoren und Nitrate.
Die blutdrucksenkende Wirkung von Doxazosin kann abgeschwächt werden durch:
• nicht-steroidale Antirheumatika und Östrogene,
• Sympathomimetika.
Doxazosin kann die Wirkung von Dopamin, Ephedrin, Epinephrin, Metaraminol, Methoxamin und Phenylephrin auf Blutdruck und Gefäße abschwächen.
Doxazosin kann die Plasma-Renin-Aktivität und die Ausscheidung der Vanillinmandelsäure im Harn erhöhen. Dies ist bei der Interpretation von Labordaten zu berücksichtigen.
4.6 Fertilität, Schwangerschaft und Stillzeit
Schwangerschaft
Da keine adäquaten und gut kontrollierten Studien bei schwangeren Frauen vorliegen, ist die Sicherheit von Doxazosin während der Schwangerschaft nicht nachgewiesen. Deshalb sollte Doxazosin während der Schwangerschaft nur angewendet werden, wenn der potenzielle Nutzen das Risiko übersteigt. Auch wenn in tierexperimentellen Untersuchungen keine teratogenen Wirkungen festgestellt wurden, wurde bei Tieren nach extrem hohen Dosen eine geringere Überlebensrate der Feten beobachtet (siehe Abschnitt 5.3).
Stillzeit
Unter einer Doxazosin-Therapie darf nicht gestillt werden, da das Arzneimittel in der Milch laktierender Ratten akkumuliert und keine Informationen zur Ausscheidung des Wirkstoffs in die Muttermilch beim Menschen vorliegen. Alternativ sollten Mütter abstillen, wenn eine Behandlung mit Doxazosin notwendig ist (siehe Abschnitt 5.3).
4.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen
Die Fähigkeit zur aktiven Teilnahme am Straßenverkehr oder zum Bedienen von Maschinen kann beeinträchtigt sein, insbesondere zu Beginn der Behandlung.
4.8 Nebenwirkungen
Unter der Therapie mit Doxazosin können die nachfolgend genannten Nebenwirkungen auftreten.
Bei den Häufigkeitsangaben zu Nebenwirkungen werden folgende Kategorien zugrunde gelegt: sehr häufig (>1/10), häufig (>1/100 bis <1/10), gelegentlich (>1/1.000 bis <1/100), selten (>1/10.000 bis <1/1.000), sehr selten (<1/10.000), nicht bekannt (Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar).
|
Systemorgankl asse |
Häufig |
Gelegentlich |
Selten |
Sehr selten |
Nicht bekannt |
|
Infektionen und parasitäre |
Atemwegsinfe ktion, |
|
Erkrankungen |
Harnwegsinfek tion | ||||
|
Erkrankungen des Blutes und des Lymphsystems |
Leukope nie, Thrombo zytopenie j Erythrozy topenie | ||||
|
Erkrankungen des Immunsystems |
Allergische Arzneimittelr eaktionen | ||||
|
Stoffwechsel- und Ernährungsstör ungen |
Gicht, gesteigerter Appetit, Anorexie, Hypokaliämie , Durstgefühl |
Hypoglyk ämie | |||
|
Psychiatrische Erkrankungen |
Agitiertheit, Depressione n, Angst, Schlaflosigke it, Nervosität, Alpträume, emotionale Labilität | ||||
|
Erkrankungen des Nervensystems |
Kopfschmerze n, Schläfrigkeit, Benommenheit , Schwindel, Apathie, Erregtheit. |
Zerebrovask uläre Ereignisse, Hypästhesie, Synkope, Tremor, Geschmacks störungen, Gedächtnisv erlust |
Parästhe sien |
Schwinde l bei Lagewec hsel | |
|
Augenerkranku ngen |
Akkommodatio nsstörungen |
Abnormer Tränenfluss, Photophobie |
Verschwo mmenes Sehen |
IFIS (Intraoper ative Floppy Iris Syndrome ) (siehe Abschnitt 4.4) | |
|
Erkrankungen des Ohrs und des Labyrinths |
Vertigo |
Tinnitus | |||
|
Herzerkrankung en |
Palpitationen, Tachykardie |
Angina pectoris, Myokardinfar kt, |
Bradykar die |
|
Arrhythmie, periphere Ischämie | |||||
|
Gefäßerkrankun gen |
Hypotonie, Blutdruckabfall bei Lagewechsel, Ödeme |
Durchblut ungsstöru ngen der Hirngefäß e |
Hitzewall ungen | ||
|
Erkrankungen der Atemwege, des Brustraums und Mediastinums |
Bronchitis, Husten, Dyspnoe, Rhinitis, verstopfte Nase |
Bronchospas mus, Pharyngitis, Epistaxis |
Kehlkopfö dem | ||
|
Erkrankungen des Gastrointestinalt rakts |
Abdominalsch merzen, Dyspepsie, Mundtrockenh eit, Übelkeit, Obstipation |
Flatulenz, Erbrechen, Gastroenteriti s, Diarrhö |
Magensc hmerzen | ||
|
Leber- und Gallenerkranku ngen |
Anomale Leberfunktion swerte, Ikterus |
Hepatitis, Cholesta se | |||
|
Erkrankungen der Haut und des Unterhautzellge webes |
Pruritus |
Hautausschla g, Haarausfall |
Purpura |
Urtikaria | |
|
Skelettmuskulat ur-, Bindegewebs- und Knochenerkran kungen |
Rückenschmer zen, Muskelschmer zen, Muskelkrämpf e |
Muskelschwä che, Gelenkschm erzen, Muskelsteifig keit | |||
|
Erkrankungen der Nieren und Harnwege |
Zystitis, Harninkontinen z, verstärkter Harndrang, häufigeres Wasserlassen |
Miktionsstöru ngen, Dysurie, Hämaturie |
Polyurie |
Verstärkt e Diurese, Nykturie, Anstieg von Harnstoff und Kreatinin im Plasma | |
|
Erkrankungen der Geschlechtsorg ane und der Brustdrüse |
Ejakulationsstö rungen |
Impotenz |
Priapismu s |
Gynäkom astie |
Retrograd e Ejakulatio n |
|
Allgemeine Erkrankungen und Beschwerden am Verabreichungs ort |
Müdigkeit,Sch wäche, Brustkorbschm erzen, grippeähnliche Symptome (Fieber, Schüttelfrost), periphere Ödeme. |
Generalisiert e Ödeme, Schmerzen, Gesichtsöde me, Flush, Blässe |
Verringert e Körperte mperatur bei älteren Patienten |
Fatigue, Unwohls ein | |
|
Untersuchunge n |
Gewichtszun ahme |
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung dem
Bundesinstitut für Arzneimittel und Medizinprodukte Abt. Pharmakovigilanz Kurt-Georg-Kiesinger-Allee 3 D-53175 Bonn
| Website: Fehler! Hyperlink-Referenz ungültig.www.bfarm.de anzuzeigen.
4.9 Überdosierung
Eine Überdosierung von Doxazosin AL führt in der Regel zu Hypotonie, unter Umständen verbunden mit Synkopen.
Bei Hypotonie infolge einer Überdosierung sollte in erster Linie das kardiovaskuläre System stabilisiert werden. Zur Normalisierung von Blutdruck und Herzfrequenz sollte der Patient auf dem Rücken in Kopftieflage gebracht werden. Falls diese Maßnahme nicht ausreicht, sollte ein Schock zuerst mit Volumenexpandern behandelt werden. Falls notwendig, kann anschließend ein Vasopressor gegeben werden. Die Nierenfunktion sollte überwacht und, falls erforderlich, unterstützt werden. Da Doxazosin im Plasma vorwiegend proteingebunden vorliegt, ist eine Dialyse als Therapiemaßnahme nicht indiziert.
5. Pharmakologische Eigenschaften
5.1 Pharmakodynamische Eigenschaften
Pharmakotherapeutische Gruppe: Antihypertensivum. ATC-Code: C02CA04
Doxazosin bewirkt durch selektive und kompetitive Blockade von postsynaptischen Alpha-1-Rezeptoren eine periphere Vasodilatation.
Die Anwendung von Doxazosin beim Hypertoniker führt zur Senkung des Blutdrucks durch Verminderung des peripheren Gefäßwiderstandes.
Bei einer einmal täglichen Dosierung ist die Wirkung noch 24 Stunden nach der Einnahme nachzuweisen. Nach Therapiebeginn kommt es zu einer allmählichen Senkung des Blutdrucks, orthostatische Reaktionen können auftreten. Die maximale Blutdrucksenkung wird normalerweise 2 - 6 Stunden nach der Tabletteneinnahme erzielt. Bei Hypertonikern sind die Blutdruckwerte unter Doxazosin-Therapie im Liegen und im Stehen ähnlich.
Eine Toleranzentwicklung bezüglich der antihypertensiven Wirkung wurde bei Langzeittherapie mit Doxazosin bisher nicht beobachtet. Gelegentlich kommt es bei fortgesetzter Anwendung zum Anstieg der Plasmareninaktivität und zu Tachykardien.
Die Zwischenauswertung der ALLHAT-Studie (Antihypertensive and Lipid Lowering Treatment to Prevent Heart Attack Trial) zeigte, dass das Risiko für eine schwerwiegende Herzinsuffizienz bei mit Doxazosin behandelten Bluthochdruckpatienten mit mindestens einem weiteren KHK-Risikofaktor im Vergleich zu den mit Chlorthalidon behandelten Patienten etwa doppelt so hoch war. Außerdem war bei diesen Patienten das Risiko für das Auftreten von schwerwiegenden kardiovaskulären Komplikationen um 25% höher als in der Gruppe der Chlorthalidon-Patienten. Aufgrund dieser Ergebnisse wurde der Doxazosin-Arm der ALLHAT-Studie abgebrochen. Unterschiede im Hinblick auf die Mortalität waren zu diesem Zeitpunkt nicht vorhanden. Die Ergebnisse sind noch nicht abschließend ausgewertet.
Unter Behandlung mit Doxazosin konnte eine Regression der linksventrikulären Hypertrophie festgestellt werden.
5.2 Pharmakokinetische Eigenschaften
Nach oraler Applikation wird Doxazosin gut resorbiert, die Plasmaspitzenkonzentrationen werden etwa nach 2 Stunden erreicht. Die absolute Bioverfügbarkeit beträgt nahezu 63%. 98,3% des Doxazosins im Plasma liegen in proteingebundener Form vor. Die Plasmaelimination verläuft biphasisch, die terminale Halbwertszeit beträgt 22 Stunden und ermöglicht somit eine tägliche Einmalgabe.
Der größte Anteil von Doxazosin wird metabolisiert (O-Demethylierung und Hydroxylierung); die Elimination erfolgt vorwiegend über die Faeces (nur 5% der verabreichten Dosis werden unverändert ausgeschieden).
6-Hydroxy-Doxazosin ist ein potenter selektiver Alpha-Blocker und entspricht beim Menschen 5% der peroral aufgenommenen Dosis. Daher trägt 6-Hydroxy-Doxazosin wenig zur antihypertensiven Wirkung von Doxazosin bei.
Studien bei älteren Personen und Patienten mit Niereninsuffizienz haben keine relevanten pharmakokinetischen Unterschiede zu Patienten mit normaler Nierenfunktion ergeben.
Über den Einsatz bei Patienten mit Leberinsuffizienz und über die Wirkung von Arzneimitteln mit bekanntem Einfluss auf den Leberstoffwechsel (z.B.
Cimetidin) liegen nur in begrenztem Umfang Daten vor. In einer klinischen Studie mit 12 Patienten mit geringgradiger Leberinsuffizienz war die Fläche unter der Kurve (AUC) um 43% erhöht und die Clearance nach oraler einmaliger Applikation um 30% vermindert.
Da Doxazosin nahezu vollständig in der Leber metabolisiert wird, sollte Doxazosin AL bei Patienten mit veränderter Leberfunktion vorsichtig angewendet werden (siehe auch Abschnitt 4.4).
5.3 Präklinische Daten zur Sicherheit
Tierversuche zur Sicherheitspharmakologie, chronischen Toxizität, Reproduktionstoxizität, Mutagenität und Kanzerogenität ergaben keine Hinweise auf ein erhöhtes Risiko für die Anwendung beim Menschen.
Obwohl tierexperimentelle Untersuchungen keinen Hinweis auf eine teratogene Wirkung ergeben haben, wurde bei Tieren mit Dosen, die etwa 300-mal höher waren als die empfohlene Höchstdosis beim Menschen, eine verringerte fetale Überlebensrate beobachtet.
Bei Versuchen mit Ratten zeigte sich nach oraler Einmalgabe von 1 mg/kg [2-14C]-Doxazosin, dass Doxazosin in der Muttermilch mit maximal dem etwa 20Fachen der mütterlichen Plasmakonzentration akkumuliert.
Für weitere Informationen siehe Abschnitt 4.6.
6. Pharmazeutische Angaben
6.1 Liste der sonstigen Bestandteile
Doxazosin AL 1 Doxazosin AL 2 Doxazosin AL 4
Carboxymethylstärke-Natrium (Typ A) (Ph.Eur.), Mikrokristalline Cellulose, Lactose, Magnesiumstearat (Ph.Eur.), Natriumdodecylsulfat, Hochdisperses Siliciumdioxid
Doxazosin AL 8
Carboxymethylstärke-Natrium (Typ A) (Ph.Eur.), Mikrokristalline Cellulose,
Lactose-Monohydrat, Magnesiumstearat (Ph.Eur.), Natriumdodecylsulfat, Hochdisperses Siliciumdioxid.
6.2 Inkompatibilitäten
Nicht zutreffend.
6.3 Dauer der Haltbarkeit
5 Jahre.
6.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung
Doxazosin AL 1 Doxazosin AL 2 Doxazosin AL 4 Nicht über 30°C lagern.
Doxazosin AL 8
Für dieses Arzneimittel sind keine besonderen Lagerungsbedingungen erforderlich.
6.5 Art und Inhalt des Behältnisses
PVC/PVDC/Aluminium-Blisterpackungen
Doxazosin AL 1
Originalpackung mit 20, 50 und 100 Tabletten Doxazosin AL 2
Originalpackung mit 20, 50 und 100 Tabletten Doxazosin AL 4
Originalpackung mit 20, 50 und 100 Tabletten Doxazosin AL 8
Originalpackung mit 20, 50 und 100 Tabletten
6.6 Besondere Vorsichtsmaßnahmen für die Beseitigung
Nicht verwendetes Arzneimittel oder Abfallmaterial ist entsprechend den nationalen Anforderungen zu beseitigen.
7. Inhaber der Zulassung
ALIUD PHARMA® GmbH Gottlieb-Daimler-Str. 19 D-89150 Laichingen Telefon: 07333 9651-0 Telefax: 07333 9651-6004 info@aliud.de
8. Zulassungsnummern
42373.00. 00
42373.01.00
42373.02.00
49260.00. 00
9. Datum der Erteilung der Zulassung/Verlängerung der Zulassung
Doxazosin AL 1 Doxazosin AL 2 Doxazosin AL 4
19. Mai 1999/06. November 2007 Doxazosin AL 8
16. Februar 2001/17. April 2008
10. Stand der Information
Juli 2014
11. Verkaufsabgrenzung
Verschreibungspflichtig
13