Eferox 25 Mikrogramm
FACHINFORMATION
1. BEZEICHNUNG DER ARZNEIMITTEL
Eferox® 25 Mikrogramm, Tabletten Eferox® 50 Mikrogramm, Tabletten Eferox® 75 Mikrogramm, Tabletten Eferox® 100 Mikrogramm, Tabletten Eferox® 125 Mikrogramm, Tabletten Eferox® 150 Mikrogramm, Tabletten
Wirkstoff: Levothyroxin-Natrium
2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Eferox® 25 Mikrogramm
1 Tablette enthält 25 Mikrogramm Levothyroxin-Natrium.
Eferox® 50 Mikrogramm
1 Tablette enthält 50 Mikrogramm Levothyroxin-Natrium.
Eferox® 75 Mikrogramm
1 Tablette enthält 75 Mikrogramm Levothyroxin-Natrium.
Eferox® 100 Mikrogramm
1 Tablette enthält 100 Mikrogramm Levothyroxin-Natrium.
Eferox® 125 Mikrogramm
1 Tablette enthält 125 Mikrogramm Levothyroxin-Natrium.
Eferox® 150 Mikrogramm
1 Tablette enthält 150 Mikrogramm Levothyroxin-Natrium.
Vollständige Auflistung der sonstigen Bestandteile siehe, Abschnitt 6.1.
3. DARREICHUNGSFORM
Tablette
Eferox® 25 Mikrogramm
weiße, runde Tabletten mit Bruchkerbe, Prägung 25 auf einer Seite
Eferox® 50 Mikrogramm
weiße, runde Tabletten mit Bruchkerbe, Prägung 50 auf einer Seite
Eferox® 75 Mikrogramm
weiße, runde Tabletten mit Bruchkerbe, Prägung 75 auf einer Seite
Eferox® 100 Mikrogramm
weiße, runde Tabletten mit Bruchkerbe, Prägung 100 auf einer Seite
Eferox® 125 Mikrogramm
weiße, runde Tabletten mit Bruchkerbe, Prägung 125 auf einer Seite
Eferox® 150 Mikrogramm
weiße, runde Tabletten mit Bruchkerbe, Prägung 150 auf einer Seite Die Tabletten können in gleiche Dosen geteilt werden.
4. KLINISCHE ANGABEN
4.1 Anwendungsgebiete
Für alle Wirkstärken Eferox® 25/50/75/100/125/150 Mikrogramm gelten die Indikationen:
- Schilddrüsenhormonsubstitution bei Hypothyreose jeglicher Genese,
- Prophylaxe einer Rezidivstruma nach Resektion einer Struma mit euthyreoter Funktionslage,
- benigne Struma mit euthyreoter Funktionslage,
Zusätzlich gilt für die Wirkstärken Eferox® 25/50/75/100 Mikrogramm:
- Begleittherapie bei thyreostatischer Behandlung einer Hyperthyreose nach Erreichen der euthyreoten Funktionslage.
Zusätzlich gilt für die Wirkstärken Eferox® 75/100/125/150 Mikrogramm:
- Suppressions- und Substitutionstherapie bei Schilddrüsenmalignom, vor allem nach Thyreoidektomie.
4.2 Dosierung und Art der Anwendung
Schilddrüsenhormontherapie/Substitution
Dosierung
Die Dosierungsangaben gelten als Richtlinien. Die individuelle Tagesdosis sollte durch labordiagnostische und klinische Untersuchungen ermittelt werden.
Bei erhaltener Restfunktion der Schilddrüse kann eine geringere Substitutionsdosis ausreichend sein.
Bei älteren Patienten, bei Patienten mit koronarer Herzkrankheit und bei Patienten mit schwerer oder lang bestehender Schilddrüsenunterfunktion ist eine Behandlung mit Schilddrüsenhormonen besonders vorsichtig zu beginnen, das heißt, eine niedrige Initialdosis ist zu wählen und diese unter häufigen Schilddrüsenhormonkontrollen langsam und in größeren Zeitabständen zu steigern. Erfahrungsgemäß ist auch bei Patienten mit niedrigem Körpergewicht und bei Patienten mit einer großen Struma eine geringere Dosis ausreichend.
Da bei einigen Patienten die T4- oder fT4-Werte erhöht sein können, ist zur Überwachung des Behandlungsschemas die Bestimmung der Serum-TSH-Konzentration besser geeignet.
|
Indikation |
Dosis (Mikrogramm Levothyroxin-Natrium/Tag) | |
|
Hypothyreose: | ||
|
Erwachsene |
initial |
25-50 |
|
(Steigerung in 2- bis 4-wöchigen Abständen um 25-50 Mikrogramm) |
danach |
100-200 |
|
Prophylaxe einer Rezidivstruma: |
75-200 | |
|
Benigne Struma mit euthyreoter Funktionslage: |
75-200 | |
|
Begleittherapie bei thyreostatischer Behandlung der Hyperthyreose: |
50-100 | |
|
Nach Thyreoidektomie wegen Schilddrüsenmalignom: |
150-300 |
Kinder
Die Erhaltungsdosis liegt bei angeborener und erworbener Hypothyreose im Allgemeinen bei 100 bis 150 Mikrogramm Levothyroxin-Natrium/m2 Körperoberfläche pro Tag.
Bei Neugeborenen und Kindern mit angeborener Hypothyreose, die eine rasche Substitution erfordert, wird eine Anfangsdosis von 10 bis 15 Mikrogramm Levothyroxin-Natrium/kg Körpergewicht pro Tag für die ersten 3 Monate empfohlen. Anschließend sollte die Dosis individuell anhand der klinischen Befunde und der Schilddrüsenhormon- und TSH-Werte angepasst werden.
Bei Kindern mit erworbener Hypothyreose wird eine Anfangsdosis von 12,5 bis 50 Mikrogramm Levothyroxin-Natrium pro Tag empfohlen. Die Dosis sollte anhand der klinischen Befunde und der Schilddrüsenhormon-und TSH-Werte schrittweise alle 2 bis 4 Wochen erhöht werden bis die zur kompletten Substitution erforderliche Dosis erreicht ist.
Art der Anwendung
Die gesamte Tagesdosis wird morgens nüchtern mindestens eine halbe Stunde vor dem Frühstück unzerkaut mit Flüssigkeit eingenommen.
Kinder erhalten die gesamte Tagesdosis mindestens eine halbe Stunde vor der ersten Tagesmahlzeit. Die Tabletten können auch in suspendierter Form verabreicht werden. Hierzu lässt man die Tablette in etwas Wasser (10 bis 15 ml) zerfallen und verabreicht die entstehende feine Verteilung (sie ist für jede Einnahme frisch zuzubereiten!) mit etwas weiterer Flüssigkeit (5 bis 10 ml).
Hinweis zur leichteren Teilbarkeit:
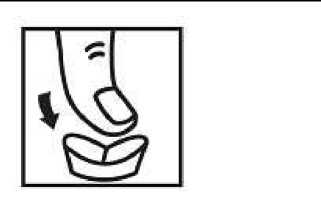
Legen Sie die Tablette mit der Bruchrille nach oben auf eine feste ebene Unterlage. Drücken Sie mit dem Daumen von oben mittig auf die Tablette, um die Tablette zu teilen.
Dauer der Anwendung
Bei Hypothyreose und Thyreoidektomie wegen Schilddrüsenmalignom meist zeitlebens, bei euthyreoter Struma und Struma-Rezidivprophylaxe einige Monate oder Jahre bis zeitlebens, bei Begleittherapie zur Behandlung der Hyperthyreose entsprechend der Dauer der thyreostatischen Medikation.
Für die Behandlung der euthyreoten Struma ist ein Behandlungszeitraum von 6 Monaten bis zu zwei Jahren notwendig. Falls die Behandlung mit Eferox® innerhalb dieser Zeit nicht den gewünschten Erfolg erbracht hat, sollten andere Therapiemöglichkeiten in Erwägung gezogen werden.
Dosierung bei älteren Menschen
Bei älteren Patienten ist im individuellen Fall, z. B. bei kardialer Problematik, einer einschleichenden Gabe von Levothyroxin-Natrium unter regelmäßiger Kontrolle des TSH-Spiegels der Vorzug zu geben.
4.3 Gegenanzeigen
- Überempfindlichkeit gegen den Wirkstoff oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile,
- unbehandelte Hyperthyreose,
- unbehandelte adrenale Insuffizienz,
- unbehandelte hypophysäre Insuffizienz (sofern diese eine therapiebedürftige adrenale Insuffizienz zur Folge hat),
- akuter Myokardinfarkt,
- akute Myokarditis,
- akute Pankarditis.
Während einer Schwangerschaft ist die gleichzeitige Einnahme von Levothyroxin und einem Thyreostatikum kontraindiziert.
Anwendung in Schwangerschaft und Stillzeit siehe Abschnitt 4.6.
4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung
Vor Beginn einer Schilddrüsenhormontherapie sind folgende Krankheiten oder Zustände auszuschließen bzw. zu behandeln:
- koronare Herzkrankheit,
- Angina Pectoris,
- Hypertonie,
- Hypophysen- und/oder Nebennierenrindeninsuffizienz,
- Schilddrüsenautonomie.
Bei koronarer Herzkrankheit, Herzinsuffizienz, tachykarden Herzrhythmusstörungen, Myokarditis mit nicht akutem Verlauf, lange bestehender Hypothyreose oder bei Patienten, die bereits einen Myokardinfarkt erlitten haben, ist auch eine leichtere medikamentös induzierte hyperthyreote Funktionslage unbedingt zu vermeiden. Bei einer Schilddrüsenhormontherapie sind bei diesen Patienten häufigere Kontrollen der Schilddrüsenhormonparameter durchzuführen (siehe Abschnitt 4.2).
Bei sekundärer Hypothyreose muss geklärt werden, ob gleichzeitig eine Nebennierenrindeninsuffizienz vorliegt. Ist das der Fall, so muss zunächst substituiert werden (Hydrocortison).
Bei Verdacht auf eine Autonomie der Schilddrüse wird empfohlen, einen TRH-Test oder ein Suppressionsszintigramm durchzuführen.
Bei der Levothyroxin-Therapie postmenopausaler Frauen, die ein erhöhtes Osteoporoserisiko aufweisen, sollte zur Vermeidung supraphysiologischer Blutspiegel von Levothyroxin die Schilddrüsenfunktion häufiger kontrolliert werden.
Schilddrüsenhormone dürfen nicht zur Gewichtsreduktion gegeben werden. In euthyreoten Patienten bewirken normale Dosen keine Gewichtsreduktion. Höhere Dosen können schwerwiegende oder sogar lebensbedrohliche Nebenwirkungen verursachen, insbesondere in Kombination mit bestimmten Mitteln zur Gewichtsreduktion.
Ist ein Levothyroxin-Behandlungsschema einmal festgelegt, sollte die Umstellung auf ein anderes schilddrüsenhormonhaltiges Arzneimittel nur unter Überwachung der labordiagnostischen und klinischen Parameter erfolgen.
Bei Diabetikern und bei Patienten mit einer Therapie mit gerinnungshemmenden Stoffen siehe Abschnitt 4.5.
4.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen
Antidiabetika:
Levothyroxin kann die blutzuckersenkende Wirkung von Antidiabetika vermindern. Bei Diabetikern ist deshalb vor allem zu Beginn einer Schilddrüsenhormontherapie der Blutzuckerspiegel regelmäßig zu kontrollieren. Die Dosierung des blutzuckersenkenden Arzneimittels ist ggf. anzupassen.
Cumarinderivate:
Levothyroxin kann die Wirkung von Cumarinderivaten durch Verdrängung aus der Plasmaeiweißbindung verstärken. Bei gleichzeitiger Behandlung sind deshalb regelmäßige Kontrollen der Blutgerinnung erforderlich, ggf. ist die Dosierung des gerinnungshemmenden Arzneimittels anzupassen (Dosisreduktion).
Ionenaustauscherharze:
Ionenaustauscherharze wie Colestyramin, Colestipol oder Calcium- und Natriumsalze der Polystyrolsulfonsäure hemmen die Resorption von Levothyroxin und sollten deshalb erst 4 bis 5 Stunden nach der Einnahme von Eferox® verabreicht werden.
Gallensäurenkomplexbildner:
Colesevelam bindet Levothyroxin und verringert so die Resorption von Levothyroxin aus dem Gastrointestinaltrakt. Wenn Levothyroxin mindestens 4 Stunden vor Colesevelam eingenommen wurde, wurde keine Interaktion beobachtet. Daher sollte Eferox® mindestens 4 Stunden vor Colesevelam eingenommen werden.
Aluminiumhaltige magensäurebindende Arzneimittel, eisenhaltige Arzneimittel, Calciumcarbonat:
Die Resorption von Levothyroxin kann durch die gleichzeitige Einnahme von aluminiumhaltigen magensäurebindenden Arzneimitteln (Antazida, Sucralfate), eisenhaltigen Arzneimitteln und Calciumcarbonat vermindert werden. Deshalb sollte die Einnahme von Eferox® mindestens zwei Stunden vor diesen erfolgen.
Propylthiouracil, Glukokortikoide und Betarezeptorenblocker:
Diese Substanzen inhibieren die Umwandlung von T4 in T3.
Amiodaron und iodhaltige Kontrastmittel können - bedingt durch ihren hohen Iodgehalt -sowohl eine Hyperthyreose als auch eine Hypothyreose auslösen. Besondere Vorsicht ist bei einer nodösen Struma mit möglicherweise unerkannten Autonomien geboten. Durch diese Wirkung von Amiodaron auf die Schilddrüsenfunktion kann eine Dosisanpassung von Eferox® notwendig werden.
Salicylate, Dicumarol, Furosemid, Clofibrat, Phenytoin:
Levothyroxin kann durch Salicylate, Dicumarol, hohe Dosen (250 mg) Furosemid, Clofibrat, Phenytoin und andere Substanzen aus der Plasmaeiweißbindung verdrängt werden. Dies führt zu einer Erhöhung des Plasmaspiegels von freiem Thyroxin (fT4).
Östrogenhaltige Kontrazeptiva, Arzneimittel zur postmenopausalen Hormonsubstitution:
Während der Einnahme von östrogenhaltigen Kontrazeptiva oder während einer postmenopausalen Hormonersatztherapie kann der Levothyroxin-Bedarf steigen.
Sertralin, Chloroquin/Proguanil:
Diese Substanzen vermindern die Wirksamkeit von Levothyroxin und erhöhen den Serum-TSH-Spiegel.
Enzyminduzierende Arzneimittel:
Barbiturate, Rifampicin, Carbamazepin und andere Arzneimittel mit leberenzyminduzierenden Eigenschaften können die hepatische Clearance von Levothyroxin erhöhen.
Protease-Inhibitoren:
Es liegen Berichte vor, dass es zu einem Verlust der therapeutischen Wirkung von Levothyroxin kommt, wenn dieses gleichzeitig mit Lopinavir/Ritonavir angewendet wird. Daher sollte bei Patienten, die gleichzeitig Levothyroxin und Protease-Inhibitoren anwenden, eine sorgfältige Kontrolle der klinischen Symptome und der Schilddrüsenfunktion erfolgen.
Sojaprodukte können die intestinale Aufnahme von Levothyroxin vermindern. Bei Kindern wurde über einen Anstieg des Serumspiegels von TSH berichtet, wenn diese eine sojahaltige Ernährung erhielten und aufgrund einer kongenitalen Hypothyreose mit Levothyroxin behandelt wurden. Ungewöhnlich hohe Dosen von Levothyroxin können erforderlich sein, um normale Serumspiegel von T4 und TSH zu erzielen. Während und nach Beendigung einer sojahaltigen Ernährung ist eine engmaschige Kontrolle der Serumspiegel von T4 und TSH notwendig, gegebenenfalls kann eine Dosisanpassung von Levothyroxin erforderlich sein.
4.6 Fertilität, Schwangerschaft und Stillzeit
Eine Behandlung mit Schilddrüsenhormonen ist insbesondere während der Schwangerschaft und Stillzeit konsequent durchzuführen. Bisher sind trotz umfangreicher Anwendungen während der Gravidität keine unerwünschten Wirkungen von Levothyroxin auf die Schwangerschaft oder die Gesundheit des Fetus/Neugeborenen bekannt geworden. Die während der Laktation selbst bei hoch dosierter Therapie mit Levothyroxin in die Muttermilch sezernierte Schilddrüsenhormonmenge reicht zur Entwicklung einer Hyperthyreose oder Suppression der TSH-Sekretion beim Säugling nicht aus.
Während der Schwangerschaft kann der Levothyroxin-Bedarf östrogenbedingt steigen. Die Schilddrüsenfunktion sollte daher sowohl während als auch nach einer Schwangerschaft kontrolliert und die Schilddrüsenhormondosis ggf. angepasst werden.
Während der Schwangerschaft ist die Anwendung von Levothyroxin als Begleittherapie bei Behandlung einer Hyperthyreose durch Thyreostatika kontraindiziert. Eine Zusatzmedikation mit Levothyroxin kann eine höhere Dosierung der Thyreostatika erforderlich machen. Im Gegensatz zu Levothyroxin können Thyreostatika die Plazentaschranke in wirksamen Dosen passieren. Dies kann eine Hypothyreose beim Fetus hervorrufen. In der Gravidität sollte aus diesem Grunde bei Vorliegen einer Hyperthyreose stets eine niedrig dosierte Monotherapie mit thyreostatisch wirksamen Substanzen erfolgen.
4.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen
Es wurden keine Studien zu den Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen durchgeführt.
4.8 Nebenwirkungen
Bei sachgemäßer Anwendung und unter Kontrolle der klinischen Befunde sowie der labordiagnostischen Werte sind Nebenwirkungen während der Behandlung mit Eferox® eher unwahrscheinlich. Wird im Einzelfall die Dosisstärke nicht vertragen oder liegt eine Überdosierung vor, so können, besonders bei zu schneller Dosissteigerung zu Beginn der Behandlung, die typischen Symptome auftreten, wie sie auch bei einer Überfunktion der Schilddrüse vorkommen, z. B. Herzklopfen, Herzrhythmusstörungen, insbesondere Tachykardie, pektanginöse Beschwerden, Muskelschwäche und Muskelkrämpfe, Hitzegefühl, Hyperhidrosis, Tremor, innere Unruhe, Schlaflosigkeit, Diarrhö, Gewichtsabnahme, Kopfschmerzen, Menstruationsstörungen. Als untypische Symptome können auch Fieber, Erbrechen sowie Pseudotumor cerebri (besonders bei Kindern) beobachtet werden. In diesen Fällen sollte die Tagesdosis reduziert oder die Medikation für mehrere Tage unterbrochen werden. Sobald die Nebenwirkung abgeklungen ist, kann die Behandlung unter vorsichtiger Dosierung wieder aufgenommen werden.
Im Falle der Überempfindlichkeit gegen Levothyroxin oder einen der sonstigen Bestandteile von Eferox® kann es zu allergischen Reaktionen an der Haut und im Bereich der Atemwege kommen.
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung dem Bundesinstitut für Arzneimittel und Medizinprodukte, Abt. Pharmakovigilanz, Kurt-Georg-Kiesinger-Allee 3, D-53175 Bonn, Website: http://www.bfarm.de, anzuzeigen.
4.9 Überdosierung
Als Hinweis auf eine Überdosierung ist ein erhöhter T3-Spiegel zuverlässiger als erhöhte T4- oder fT4-Spiegel.
Bei Überdosierung und Intoxikationen treten Symptome einer mäßigen bis schweren Stoffwechselsteigerung auf (siehe Abschnitt 4.8). Eine Unterbrechung der Einnahme und eine Kontrolluntersuchung werden in Abhängigkeit von der Höhe der Überdosierung empfohlen.
Anlässlich von Vergiftungsunfällen (Suizidversuchen) beim Menschen wurden Dosen bis 10 mg Levothyroxin komplikationslos vertragen. Mit ernsten Komplikationen wie Bedrohung der vitalen Funktionen (Atmung und Kreislauf) muss nicht gerechnet werden, es sei denn, dass eine koronare Herzkrankheit besteht. Dennoch existieren Berichte über Fälle von thyreotoxischer Krise, Krämpfen, Herzschwäche und Koma. Einzelne Fälle von plötzlichem Herztod wurden bei Patienten mit jahrelangem Levothyroxin-Abusus berichtet.
Bei akuter Überdosierung kann die gastrointestinale Absorption durch Gabe von medizinischer Kohle vermindert werden. Die Behandlung erfolgt meist symptomatisch und unterstützend. Bei starken betasympathomimetischen Wirkungen wie Tachykardie, Angstzustand, Agitation und Hyperkinesie können die Beschwerden durch Betarezeptorenblocker gemildert werden. Thyreostatika sind nicht angebracht, da die Schilddrüse bereits völlig ruhiggestellt ist.
Bei extrem hohen Dosen (Suizidversuch) kann eine Plasmapherese hilfreich sein.
Eine Levothyroxin-Überdosierung erfordert eine längere Überwachungsperiode. Durch die graduelle Umwandlung von Levothyroxin in Liothyronin können Symptome bis zu 6 Tage verzögert auftreten.
5. PHARMAKOLOGISCHE EIGENSCHAFTEN
5.1 Pharmakodynamische Eigenschaften
Pharmakotherapeutische Gruppe: Schilddrüsenhormone,
ATC-Code: H03AA01.
Das in Eferox® enthaltene synthetische Levothyroxin ist in seiner Wirkung mit dem von der Schilddrüse vorwiegend gebildeten natürlich vorkommenden Schilddrüsenhormon identisch. Der Körper kann nicht zwischen endogen gebildetem und exogenem Levothyroxin unterscheiden.
Nach partieller Umwandlung zu Liothyronin (T3), besonders in Leber und Niere, und Übertritt in die Körperzellen werden durch Aktivierung der T3-Rezeptoren die charakteristischen Schilddrüsenhormonwirkungen auf Entwicklung, Wachstum und Stoffwechsel beobachtet.
Die Substitution von Schilddrüsenhormon führt zu einer Normalisierung der Stoffwechselvorgänge.
So wird z. B. ein durch die Hypothyreose bedingter Cholesterinanstieg durch die Gabe von Levothyroxin signifikant reduziert.
5.2 Pharmakokinetische Eigenschaften
Oral appliziertes Levothyroxin wird in deutlicher Abhängigkeit von der Art der galenischen Zubereitung bis zu maximal 80% bei Nüchterneinnahme vorwiegend aus dem oberen Dünndarm resorbiert. Wird das Präparat zu einer Mahlzeit gegeben, so ist die Resorption deutlich vermindert.
Maximale Plasmaspiegel werden ca. 2 bis 3 Stunden nach der Einnahme erreicht.
Der Wirkungseintritt erfolgt bei Beginn einer oralen Therapie nach 3 bis 5 Tagen.
Das Verteilungsvolumen errechnet sich auf ca. 10 bis 12 l. Levothyroxin ist zu ca. 99,97% an spezifische Transportproteine gebunden. Diese Protein-Hormon-Bindung ist nicht kovalent, so dass ein ständiger und sehr schneller Austausch zwischen freiem und gebundenem Hormon stattfindet.
Die metabolische Clearance für Levothyroxin liegt bei ca. 1,2 l Plasma/Tag. Der Abbau erfolgt hauptsächlich in Leber, Niere, Gehirn und Muskel. Die Metaboliten werden mit Urin und Faeces ausgeschieden.
Die Halbwertszeit von Levothyroxin beträgt ca. 7 Tage; bei Hyperthyreose ist sie kürzer (3 bis 4 Tage) und bei Hypothyreose länger (ca. 9 bis 10 Tage).
Levothyroxin passiert die Plazenta nur in geringen Mengen. Unter normal dosierter Therapie werden nur geringe Mengen an Levothyroxin in die Muttermilch sezerniert.
Wegen der hohen Proteinbindung ist Levothyroxin weder der Hämodialyse noch der Hämoperfusion zugänglich.
5.3 Präklinische Daten zur Sicherheit
Akute Toxizität
Die akute Toxizität von Levothyroxin ist sehr gering.
Chronische Toxizität
Untersuchungen zur chronischen Toxizität wurden an verschiedenen Tierspezies (Ratte, Hund) durchgeführt. In hohen Dosen wurden Anzeichen einer Hepatopathie, erhöhtes Auftreten von spontanen Nephrosen sowie veränderten Organgewichten bei der Ratte gesehen. Beim Hund wurden keine wesentlichen Nebenwirkungen beobachtet.
Mutagenität
Erkenntnismaterial zum mutagenen Potenzial von Levothyroxin liegt nicht vor. Es haben sich bisher keine Verdachtsmomente oder Anhaltspunkte für eine Schädigung der Nachkommenschaft durch Veränderungen des Genoms durch Schilddrüsenhormone ergeben.
Kanzerogenität
Langzeituntersuchungen am Tier auf ein Tumor erzeugendes Potenzial von Levothyroxin wurden nicht durchgeführt.
Reproduktionstoxizität
Schilddrüsenhormone passieren die Plazenta zu einem sehr kleinen Anteil.
Erkenntnismaterial über Schädigungen der männlichen oder weiblichen Fruchtbarkeit liegt nicht vor. Es existieren keinerlei Verdachtsmomente oder Anhaltspunkte.
6. PHARMAZEUTISCHE ANGABEN
6.1 Liste der sonstigen Bestandteile
Magnesiumstearat (Ph.Eur.) [pflanzlich]; mikrokristalline Cellulose; Carboxymethylstärke-Natrium (Typ A) (Ph.Eur.); schweres Magnesiumoxid
6.2 Inkompatibilitäten
Bisher keine bekannt.
6.3 Dauer der Haltbarkeit
Eferox® 25 Mikrogramm:
Die Dauer der Haltbarkeit beträgt 18 Monate.
Eferox® 50 / 75 /100 Mikrogramm:
Die Dauer der Haltbarkeit beträgt 24 Monate.
Eferox® 125 /150 Mikrogramm:
Die Dauer der Haltbarkeit beträgt 21 Monate.
Diese Arzneimittel sollen nach Ablauf des Verfalldatums nicht mehr angewendet werden.
6.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung Nicht über 25 °C lagern.
6.5 Art und Inhalt des Behältnisses
PVC/Aluminium-Blisterpackung.
Eferox® 25 Mikrogramm
Packungen mit 50 Tabletten (N2), 98 Tabletten (N3) (Kalenderpackung) und 100 Tabletten (N3) Anstaltspackung mit 250 Tabletten (1x250 bzw. 5x50 Tabletten)
Eferox® 50 Mikrogramm
Packungen mit 50 Tabletten (N2), 98 Tabletten (N3) (Kalenderpackung) und 100 Tabletten (N3) Anstaltspackung mit 250 Tabletten (1x250 bzw. 5x50 Tabletten)
Eferox® 75 Mikrogramm
Packungen mit 50 Tabletten (N2), 98 Tabletten (N3) (Kalenderpackung) und 100 Tabletten (N3) Anstaltspackung mit 250 Tabletten (1x250 bzw. 5x50 Tabletten)
Eferox® 100 Mikrogramm
Packungen mit 50 Tabletten (N2), 98 Tabletten (N3) (Kalenderpackung) und 100 Tabletten (N3) Anstaltspackung mit 250 Tabletten (1x250 bzw. 5x50 Tabletten)
Eferox® 125 Mikrogramm
Packungen mit 50 Tabletten (N2), 98 Tabletten (N3) (Kalenderpackung) und 100 Tabletten (N3) Anstaltspackung mit 250 Tabletten (1x250 bzw. 5x50 Tabletten)
Eferox® 150 Mikrogramm
Packungen mit 50 Tabletten (N2), 98 Tabletten (N3) (Kalenderpackung) und 100 Tabletten (N3) Anstaltspackung mit 250 Tabletten (1x250 bzw. 5x50 Tabletten)
Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht.
6.6 Besondere Vorsichtsmaßnahmen für die Beseitigung
Nicht verwendetes Arzneimittel oder Abfallmaterial ist entsprechend den nationalen Anforderungen zu beseitigen.
7. PHARMAZEUTISCHER UNTERNEHMER
Aristo Pharma GmbH
Wallenroder Straße 8-10 13435 Berlin Tel.: +49 30 71094-4200 Fax: +49 30 71094-4250
8. ZULASSUNGSNUMMERN
5189.00.00
5189.01.00
5189.04.00
5189.02.00
5189.05.00
5189.03.00
Eferox® 25 Mikrogramm: Eferox® 50 Mikrogramm: Eferox® 75 Mikrogramm: Eferox® 100 Mikrogramm Eferox® 125 Mikrogramm Eferox® 150 Mikrogramm
9. DATUM DER ERTEILUNG DER ZULASSUNGEN/VERLÄNGERUNG DER ZULASSUNGEN
05.03.1985/05.02.2005
Eferox® 25 Mikrogramm: Eferox® 50 Mikrogramm : Eferox® 75 Mikrogramm : Eferox® 100 Mikrogramm Eferox® 125 Mikrogramm Eferox® 150 Mikrogramm
05.03.1985/05.02.2005
05.03.1985/05.02.2005
28.10.1991/05.02.2005
05.03.1985/05.02.2005
18.10.1991/05.02.2005
10. STAND DER INFORMATION
November 2016
11. VERKAUFSABGRENZUNG
Verschreibungspflichtig
11