Enantone Monats-Depot 3,75Mg Retardmikrokapseln Und Suspensionsmittel
FACHINFORMATION
1. BEZEICHNUNG DES ARZNEIMITTELS
Enantone® Monats-Depot 3,75 mg Retardmikrokapseln und Suspensionsmittel
2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
1 Zweikammerspritze mit 44,1 mg Retardmikrokapseln und 1 ml Suspensionsmittel enthält 3,75 mg des Wirkstoffes Leuprorelinacetat, entsprechend 3,57 mg Leuprorelin.
Sonstige Bestandteile mit bekannter Wirkung: Eine Zweikammerspritze enthält 5,0 mg Carmellose-Natrium
Vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt 6.1.
3. DARREICHUNGSFORM
Retardmikrokapseln und Suspensionsmittel
4. KLINISCHE ANGABEN
4.1 Anwendungsgebiete
Enantone Monats-Depot wird angewendet bei männlichen Erwachsenen und Kindern.
Bei Männern Diagnostik:
Prüfung der Hormonempfindlichkeit eines Prostatakarzinoms zur Beurteilung der Notwendigkeit von hormonsupprimierenden/hormonablativen Maßnahmen.
Therapie:
Zur symptomatischen Behandlung des fortgeschrittenen hormonabhängigen Prostatakarzinoms.
Zur Behandlung des lokal fortgeschrittenen, hormonabhängigen Prostatakarzinoms; begleitend zur und nach der Strahlentherapie.
Bei Kindern
Zur Behandlung der Pubertas praecox vera (bei Mädchen unter 9 Jahren und Jungen unter 10 Jahren).
4.2 Dosierung und Art der Anwendung Dosierung
Die Indikationsstellung zur Behandlung und die längerfristigen Therapiekontrollen sollten bei Kindern vorzugsweise in endokrinologisch-pädiatrischen Zentren erfolgen. Die Behandlung in der Indikation „Prostatakarzinom“ sollte von in der Geschwulsttherapie erfahrenen Ärzten vorgenommen werden.
Männer
Einmal monatlich 44,1 mg Retardmikrokapseln mit 3,75 mg Leuprorelinacetat, suspendiert in 1 ml Suspensionsmittel, s.c. applizieren.
Kinder und Jugendliche
Das Dosierschema wird individuell angepasst. Die empfohlene Anfangsdosis ist abhängig vom Körpergewicht und beträgt:
a) Kinder mit einem Körpergewicht > 20 kg:
Einmal monatlich 44,1 mg Retardmikrokapseln mit 3,75 mg Leuprorelinacetat, suspendiert in 1 ml Suspensionsmittel, s.c. applizieren.
b) Kinder mit einem Körpergewicht < 20 kg:
Für diese Einzelfälle gilt unter Berücksichtigung der klinischen Aktivität der Pubertas praecox vera:
Einmal monatlich eine gebrauchsfertige Suspension aus 44,1 mg Retardmikrokapseln mit 3,75 mg Leuprorelinacetat und 1 ml Suspensionsmittel herstellen. Von dieser Suspension sind dann 0,5 ml (22,05 mg Retardmikrokapseln mit 1,88 mg Leuprorelinacetat) subkutan zu applizieren. Der Rest der Suspension ist zu verwerfen. Die Gewichtszunahme des Kindes ist zu kontrollieren.
Je nach Aktivität der Pubertas Praecox Vera kann bei nicht ausreichender Suppression (klinische Hinweise wie z. B. Schmierblutungen bzw. im GnRH-Test keine ausreichende Suppression der Gonadotropine) eine Dosiserhöhung notwendig werden. Die minimal wirksame, monatlich zu applizierende Dosis ist dann mittels GnRH-Test zu ermitteln.
Sterile Abszesse am Injektionsort treten nach intramuskulärer und nicht bestimmungsgemäßer hoher Dosierung auf. Daher sollte in solchen Fällen subkutan injiziert werden (siehe Abschnitt 4.4).
Es wird empfohlen, bei Kindern die kleinstmöglichen Volumina einzusetzen, um unangenehme Begleiterscheinungen der intramuskulären/subkutanen Injektion zu reduzieren.
Art der Anwendung
Die Suspension von Enantone Monats-Depot ist vor der Gabe frisch zuzubereiten (Hinweise zur Vorbereitung der Zweikammerspritze vor der Anwendung, siehe Abschnitt 6.6).
Die Injektion soll subkutan erfolgen. Die Injektionsstelle ist monatlich zu wechseln. Dabei kann die subkutane Injektion in die Bauchhaut, das Gesäß oder z. B. den Oberschenkel erfolgen.
Eine versehentliche intraarterielle Injektion ist aufgrund tierexperimenteller Befunde (Thrombosierung kleiner Gefäße distal des Applikationsortes) unbedingt zu vermeiden.
Männer
In der Regel kann nach etwa 3 Monaten abgeklärt werden, ob das fortgeschrittene Prostatakarzinom androgenempfindlich ist. Führender diagnostischer Parameter ist die Serumkonzentration des prostataspezifischen Antigens (PSA), die in der Regel im fortgeschrittenen Tumorstadium über 10 ng/ml liegt. Im Test wird das Verhalten des PSA-Wertes nach Enantone Monats-Depot-induziertem Androgenentzug untersucht. Deshalb müssen zu Beginn und nach 3-monatiger Anwendung von Enantone Monats-Depot sowohl der PSA- als auch der Gesamttestosterongehalt im Serum bestimmt werden. Ein positives Testergebnis liegt vor, wenn nach 3 Monaten der Testosteronspiegel auf Kastrationsniveau liegt (< 1 ng/ml) und der PSA-Wert abgefallen ist. Ein früher, deutlicher Abfall des PSA-Wertes (in der Größenordnung von etwa 80 % gegenüber dem Ausgangswert) kann als guter prognostischer Indikator für die Langzeitantwort auf den Androgenentzug angesehen werden. Eine hormonablative Therapie (z. B. Enantone Monats-Depot) ist angezeigt.
Ein negatives Testergebnis liegt vor, wenn bei supprimiertem Testosteron der PSA-Wert unverändert bleibt oder angestiegen ist.
Sollte der Patient jedoch klinisch angesprochen haben (z. B. Besserung der Schmerzsymptomatik und der dysurischen Beschwerden, Verkleinerung der Prostata), muss ein falsch negatives Ergebnis in Betracht gezogen werden. In diesen seltenen Fällen sollte die Anwendung von Enantone MonatsDepot fortgeführt und der PSA-Wert nach 3 Monaten erneut überprüft werden; außerdem sollte der Patient mit Blick auf die klinische Symptomatik unter engmaschiger Überwachung stehen.
Die Behandlung von Patienten, die an einem Prostatakarzinom erkrankt sind, mit einem GnRH (Gonadotropin-Releasing-Hormon)-Analogon, kann auch nach Erreichen einer Kastrationsresistenz fortgeführt werden. Die relevanten Leitlinien sind hierbei zu beachten.
In der Regel ist die Therapie fortgeschrittener, hormonabhängiger Prostatakarzinome mit Enantone Monats-Depot eine Langzeitbehandlung.
Klinische Daten haben gezeigt, dass bei lokal fortgeschrittenem, hormonabhängigem Prostatakarzinom eine begleitend zur und nach der Strahlentherapie eingesetzte 3-jährige Androgenentzugstherapie einer 6-monatigen vorzuziehen ist (siehe auch Abschnitt 5.1). In medizinischen Leitlinien wird für Patienten (T3 - T4), die eine Strahlentherapie erhalten, eine Androgenentzugstherapie mit einer Behandlungsdauer von 2 - 3 Jahren empfohlen.
Kinder und Jugendliche
Die Dauer der Anwendung richtet sich nach den klinischen Parametern zu Behandlungsbeginn bzw. im Therapieverlauf (Endgrößenprognose, Wachstumsgeschwindigkeit, Knochenalter bzw. Knochenalterakzeleration) und wird vom behandelnden Pädiater zusammen mit den Sorgeberechtigten und ggf. dem erkrankten Kind festgelegt.
Das Knochenalter sollte während der Behandlung in Intervallen von 6 - 12 Monaten überwacht werden. Ein Absetzen der Therapie bei einer Knochenreifung von mehr als 12 Jahren bei Mädchen und mehr als 13 Jahren bei Jungen sollte unter Beachtung der klinischen Parameter in Betracht gezogen werden.
Bei Mädchen ist darauf zu achten, dass vor Therapiebeginn keine Schwangerschaft vorliegt. Falls das Auftreten einer Schwangerschaft während der Behandlung nicht ausgeschlossen werden kann, sollte fachmedizinischer Rat eingeholt werden.
Hinweis
Das Applikationsintervall sollte 30 ± 2 Tage betragen, um ein erneutes Auftreten von Symptomen der Pubertas praecox zu vermeiden.
4.3 Gegenanzeigen
- Überempfindlichkeit gegen Leuprorelin oder andere GnRH-Analoga, gegen Poly(glycolsäure-co-milchsäure) oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile des Suspensionsmittels.
bei Männern:
- Nachgewiesene Hormonunabhängigkeit des Karzinoms.
bei Mädchen mit Pubertas praecox vera
- Schwangerschaft und Stillzeit.
- Vaginalblutungen unbekannter Ursache
4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung
Patienten mit Bluthochdruck sollten sorgfältig überwacht werden.
Bei Patienten, die mit GnRH-Agonisten, wie Leuprorelin behandelt werden, besteht ein erhöhtes Risiko für Depressionen (die schwerwiegend sein können). Die Patienten sind über dieses Risiko aufzuklären und im Falle auftretender Symptomatik entsprechend zu behandeln.
Allergische und anaphylaktische Reaktionen wurden bei Erwachsenen und Kindern beobachtet. Diese beinhalten sowohl lokale Reaktionen an der Einstichstelle als auch systemische Symptome.
Nach der Markteinführung von Leuprorelinacetat wurden Krampfanfälle bei Kindern und Erwachsenen mit oder ohne eine Vorgeschichte von Epilepsie, Anfallsleiden oder Risikofaktoren für Krampfanfälle, beobachtet und berichtet.
Die Anwendung von Enantone Monats-Depot kann bei Dopingkontrollen zu positiven Ergebnissen führen.
Enantone Monats-Depot enthält Natrium, aber weniger als 1 mmol (23 mg) Natrium pro Zweikammerspritze.
Männer
Nach chirurgischer Kastration bewirkt Enantone Monats-Depot keine weitere Absenkung des Testosteronspiegels.
Wegen des kurzfristigen Anstiegs des Serumtestosteronspiegels zu Beginn der Therapie, der zu einer vorübergehenden Verstärkung bestimmter Krankheitssymptome führen kann, sollten Patienten mit drohenden neurologischen Komplikationen, Wirbelsäulenmetastasen sowie Harnwegsobstruktionen während der ersten Behandlungswochen unter ständiger, möglichst stationärer Überwachung stehen.
Für die Initialphase der Behandlung sollte die zusätzliche Gabe eines geeigneten Antiandrogens erwogen werden, um so die möglichen Folgeerscheinungen des anfänglichen Testosteronanstiegs und die Verschlechterung der klinischen Symptomatik abzuschwächen.
Der Therapieerfolg sollte regelmäßig (insbesondere aber bei Anzeichen für eine Progression trotz adäquater Therapie) durch klinische Untersuchungen (rektale Austastung der Prostata, Sonographie, Skelettszintigraphie, Computertomographie) und durch Überprüfung der Phosphatasen bzw. des PSA und des Serumtestosterons kontrolliert werden.
Eine Langzeit-Androgendeprivationstherapie mit GnRH-Analoga bzw. Orchiektomie ist mit einem erhöhten Risiko der Knochendemineralisierung assoziiert. Bei Risikopatienten kann dies zu einer Osteoporose und erhöhtem Frakturrisiko führen.
Metabolische Veränderungen und Kardiovaskuläres Risiko:
Epidemiologische Daten haben gezeigt, dass es unter der Therapie mit GnRH-Analoga zu einer Veränderung des Stoffwechsels (Herabsetzung der Glucosetoleranz oder Verschlechterung eines bestehenden Diabetes mellitus) kommt und dass ein erhöhtes Risiko für kardiovaskuläre Erkrankungen bestehen kann. Prospektive Daten bestätigten jedoch den Zusammenhang zwischen der Behandlung mit GnRH-Analoga und einer erhöhten kardiovaskuläre Mortalität nicht. Diabetiker und Patienten mit erhöhtem Risiko für metabolische oder kardiovaskuläre Erkrankungen sollen während der Behandlung mit Enantone Monats-Depot angemessen überwacht werden.
Eine Androgendeprivationstherapie kann die QT-Zeit verlängern.
Bei Patienten mit einer QT-Zeitverlängerung in der Vorgeschichte oder mit einem Risiko für eine QT-Zeitverlängerung und bei Patienten, die gleichzeitig QT-zeitverlängernde Arzneimittel einnehmen (siehe Abschnitt 4.5), sollte daher vor der Anwendung von Enantone Monats-Depot eine sorgfältige Nutzen-Risiko-Bewertung inklusive des Risikos für die Entstehung von Torsade de pointes durchgeführt werden.
Kinder und Jugendliche
Vor der Behandlung ist eine genaue Diagnose der idiopathischen oder neurogenen gonadotropinabhängigen Pubertas praecox notwendig.
Die individuell eingestellte Langzeitbehandlung mit Enantone Monats-Depot sollte so genau wie möglich in monatlichen Abständen erfolgen. Eine ausnahmsweise Verzögerung der Injektion von einigen Tagen (30 ± 2 Tagen) hat keinen Einfluss auf das Therapieergebnis.
Beim Auftreten von sterilen Abszessen an der Injektionsstelle (häufig berichtet bei intramuskulärer Injektion einer nicht bestimmungsgemäßen hohen Dosis) kann die Resorption von Leuprorelinacetat reduziert sein. In diesem Fall sollten die hormonellen Parameter (Testosteron, Estradiol) im Abstand von 2 Wochen überwacht werden (siehe Abschnitt 4.2).
Bei Patienten mit progredientem Gehirntumor sollte vor Beginn der Behandlung eine sorgfältige Nutzen-/Risikobewertung durchgeführt werden.
Nach der ersten Injektion kann es bei Mädchen zu Hormonentzugserscheinungen in Form von Vaginalblutungen, Schmierblutungen und Ausfluss kommen. Die Ursache für Vaginalblutungen, die über die ersten beiden Monaten andauern, muss abgeklärt werden.
Während einer Therapie der Pubertas praecox mit GnRH-Analoga kann es zu einer Abnahme der Knochendichte kommen. Nach Beendigung der Behandlung findet in aller Regel wieder eine Remineralisierung statt, so dass die Knochenmasse im jungen Erwachsenenalter nicht durch die Behandlung beeinträchtigt zu sein scheint.
Nach Abschluss der Behandlung entwickeln sich die Pubertätsmerkmale. Daten zur zukünftigen Fertilität liegen nur begrenzt vor. Bei den meisten Mädchen beginnt die Menstruation im Durchschnitt ein Jahr nach Ende der Behandlung und ist dann in den meisten Fällen regelmäßig.
Nach Beendigung der Behandlung mit Enantone Monats-Depot kann es zu einer Epiphysiolyse des Femurkopfes kommen. Der Grund dafür könnte eine Auflockerung der Epiphysenfuge aufgrund der geringen Östrogenkonzentration während der Behandlung mit GnRH-Analoga sein. Die gesteigerte Wachstumsgeschwindigkeit nach Beendigung der Behandlung resultiert in einer Verringerung der Scherkräfte, die für die Verschiebung der Epiphyse benötigt wird.
Mädchen mit Pubertas praecox vera:
Eine Therapie mit Enantone Monats-Depot kann eine Schwangerschaft nicht sicher verhindern.
4.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen
Da eine Androgendeprivationstherapie zu einer Verlängerung der QT-Zeit führen kann, sollte die gleichzeitige Anwendung von Enantone Monats-Depot mit anderen Arzneimitteln, die bekanntermaßen zu einer QT-Zeitverlängerung führen, oder Arzneimitteln, die ein Risiko zur Entstehung von Torsade de pointes haben, wie Antiarrhythmika der Klasse IA (z. B. Chinidin, Disopyramid) oder Klasse III (z. B. Amiodaron, Sotalol, Dofetilid, Ibutilid), Methadon, Moxifloxacin,
Antipsychotika usw., sorgfältig geprüft werden (siehe Abschnitt 4.4).
4.6 Fertilität, Schwangerschaft und Stillzeit
Enantone Monats-Depot ist in der Schwangerschaft und Stillzeit kontraindiziert (siehe Abschnitt 4.3). Vor Therapiebeginn ist eine Schwangerschaft auszuschließen.
4.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen
Wegen der bei wenigen Patienten insbesondere zu Therapiebeginn auftretenden Müdigkeit, welche auch durch die zugrunde liegende Tumorerkrankung bedingt sein kann, kann dieses Arzneimittel auch bei bestimmungsgemäßem Gebrauch das Reaktionsvermögen so weit verändern, dass die Fähigkeit zur aktiven Teilnahme am Straßenverkehr oder zum Bedienen von Maschinen beeinträchtigt wird.
Dies gilt in verstärktem Maße im Zusammenwirken mit Alkohol.
4.8 Nebenwirkungen
Männer
Anfangs kommt es regelmäßig zu einem kurzfristigen Anstieg des Serumtestosteronspiegels, was zu einer vorübergehenden Verstärkung bestimmter Krankheitssymptome führen kann (Auftreten oder Zunahme von Knochenschmerzen, Harnwegsobstruktion und deren Folgen, Rückenmarkskompressionen, Muskelschwäche in den Beinen, Lymphödeme). Diese Zunahme der Beschwerden geht üblicherweise spontan zurück, ohne dass Enantone Monats-Depot abgesetzt werden muss.
Aufgrund des Entzuges der Geschlechtshormone kann es zum Auftreten von Nebenwirkungen kommen. Bei den Häufigkeitsangaben zu Nebenwirkungen werden folgende Kategorien zugrunde gelegt: sehr häufig (>1/10), häufig (>1/100 bis <1/10), gelegentlich (>1/1.000 bis <1/100), selten (>1/10.000 bis <1/1.000), sehr selten (<1/10.000), nicht bekannt (Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar).
Tabelle 1. Nebenwirkungen bei Männern
|
Erkrankungen des Immunsystems | |
|
Sehr selten |
Allgemein allergische Reaktionen (Fieber, Hautausschlag, Juckreiz, Eosinophilie), anaphylaktische Reaktionen |
|
Stoffwechsel- und Ernährungsstörungen | |
|
Häufig |
Appetitzunahme |
|
Gelegentlich |
Appetitverminderung, Veränderung einer diabetischen Stoffwechsellage (Erhöhung oder Senkung von Blutzuckerwerten) |
|
Psychiatrische Erkrankungen | |
|
Häufig |
Schlafstörungen Stimmungsschwankungen, Depression |
|
Erkrankungen des Nervensystems | |
|
Häufig |
Parästhesie |
|
Gelegentlich |
Kopfschmerz, Schwindel |
|
Sehr selten |
Vorübergehende Geschmacksveränderungen. Wie auch bei anderen Arzneimitteln dieser Stoffklasse wurde in sehr seltenen Fällen über eine Apoplexie der Hypophyse nach initialer Verabreichung von Enantone Monats-Depot bei Patienten mit Hypophysenadenom berichtet. |
|
Nicht bekannt |
Krampfanfälle |
|
Herzerkrankungen | |
|
Nicht bekannt |
Verlängerung der QT-Zeit (siehe Abschnitt 4.4 und 4.5) |
|
Gefäßerkrankungen | |
|
Sehr häufig |
Hitzewallungen mit Schweißausbrüchen |
|
Gelegentlich |
Blutdruckveränderungen (Hypertonie oder Hypotonie) |
|
Erkrankungen der Atemwege, des Brustraums und Mediastinums | |
|
Gelegentlich |
Atembeschwerden |
|
Erkrankungen des Gastrointestinaltrakts | |
|
Gelegentlich |
Durchfall |
|
Sehr selten |
Übelkeit/Erbrechen |
|
Erkrankungen der Haut und des Unterhautzellgewebes | |
|
Gelegentlich |
Haarausfall, trockene Haut bzw. Schleimhaut, Nachtschweiß |
|
Skelettmuskulatur-, Bindegewebs- und Knochenerkrankungen | |
|
Sehr häufig |
Knochenschmerzen |
|
Sehr selten |
Gelenk- bzw. Rückenschmerzen und Muskelbeschwerden |
|
Nicht bekannt: |
Knochendemineralisierung (siehe Abschnitt 4.4) |
|
Erkrankungen der Niere und der Harnwege | |
|
Häufig |
Nykturie, Dysurie, Pollakisurie |
|
Gelegentlich |
Harnverhaltung |
|
Erkrankungen der Geschlechtsorgane und Brustdrüse | |
|
Sehr häufig |
Verminderung der Libido und der Potenz |
|
Gelegentlich |
Verkleinerung der Hoden, testikuläre Schmerzen, Gynäkomastie |
|
Allgemeine Erkrankungen und Beschwerden am Verabreichungsort | |
|
Sehr häufig |
Vermehrtes Schwitzen |
|
Sehr selten |
Ödeme, Müdigkeit; lokale Hautreaktionen, z. B. Rötungen oder Verhärtungen an der Injektionsstelle, die sich in der Regel auch bei fortgesetzter Behandlung zurückbilden. |
|
Nicht bekannt |
In Einzelfallen trat ein Abszess an der Injektionsstelle auf. |
|
Untersuchungen | |
|
Gelegentlich |
Gewichtszunahme, Gewichtsabnahme, Anstieg von Enzymen wie Lactatdehydrogenase (LDH), alkalischer Phosphatase (AP) oder Transaminasen wie ALT (SGPT), AST (SGOT) oder y-GT |
Nach Zulassung wurde überwiegend in Japan über das Auftreten interstitieller Pneumonien berichtet. In einem Einzelfall trat eine Thrombose der Arteria centralis retinae auf.
Hinweise:
Die Reaktion auf die Enantone Monats-Depot-Therapie kann durch Messung der Serumspiegel von Testosteron, saurer Phosphatase und PSA kontrolliert werden. So steigt der Testosteronspiegel bei Behandlungsbeginn zunächst an und sinkt dann während eines Zeitraumes von zwei Wochen wieder ab. Nach zwei bis vier Wochen werden Testosteronspiegel erreicht, wie sie nach einer beidseitigen Orchiektomie beobachtet werden, und die über den gesamten Behandlungszeitraum bestehen bleiben.
Ein Anstieg saurer Phosphatasespiegel kann in der Anfangsphase der Therapie erfolgen und ist vorübergehender Natur. Gewöhnlich werden nach einigen Wochen wieder Normalwerte bzw. annähernde Normalwerte erreicht.
Kinder und Jugendliche
In der Initialphase der Therapie kommt es zu einem kurzfristigen Anstieg der Sexualhormonspiegel mit nachfolgendem Abfall auf Werte in den präpubertären Bereich. Aufgrund dieser pharmakologischen Wirkung können insbesondere zu Therapiebeginn Nebenwirkungen auftreten, deren Häufigkeiten bereits zu Beginn des Abschnitts 4.8 definiert wurden.
Tabelle 2. Nebenwirkungen bei Kindern und Jugendlichen
|
Erkrankungen des Immunsystems | |
|
Sehr selten |
Allgemein allergische Reaktionen (Fieber, Hautausschlag, Juckreiz), anaphylaktische Reaktionen |
|
Psychiatrische Erkrankungen | |
|
Häufig |
Emotionale Labilität |
|
Erkrankungen des Nervensystems | |
|
Häufig |
Kopfschmerz |
|
Sehr selten |
Wie auch bei anderen Arzneimitteln dieser Stoffklasse wurde in sehr seltenen Fällen über eine Apoplexie der Hypophyse nach initialer Verabreichung von Enantone Monats-Depot bei Patienten mit Hypophysenadenom berichtet. |
|
Nicht bekannt |
Krampfanfälle |
|
Erkrankungen des Gastrointestinaltrakts | |
|
Häufig |
Bauchschmerzen/Bauchkrämpfe, Übelkeit/Erbrechen |
|
Erkrankungen der Haut und des Unterhautzellgewebes | |
|
Häufig |
Akne |
|
Allgemeine Erkrankungen und Beschwerden am Verabreichungsort | |
|
Häufig |
Reaktionen an der Injektionsstelle |
|
Erkrankungen der Geschlechtsorgane und der Brustdrüse | |
|
Häufig |
Vaginale Blutungen, Schmierblutungen, Ausfluss |
Hinweise:
Im Allgemeinen ist das Auftreten von vaginalen Schmierblutungen im weiteren Behandlungsverlauf (nach einer möglichen Entzugsblutung im ersten Behandlungsmonat) als Zeichen einer möglichen Unterdosierung zu werten. Das Ausmaß der hypophysären Suppression sollte dann mittels GnRH-Test abgeklärt werden.
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung dem
Bundesinstitut für Arzneimittel und Medizinprodukte Abt. Pharmakovigilanz Kurt-Georg-Kiesinger-Allee 3 53175 Bonn
Website: www.bfarm.de anzuzeigen.
4.9 Überdosierung
Intoxikationssymptome wurden bisher nicht beobachtet.
Männer
Selbst bei Verabreichung von Dosen bis zu 20 mg Leuprorelinacetat pro Tag über zwei Jahre, die bei
ersten klinischen Studien Anwendung fanden, konnten keine anderen bzw. neuen Nebenwirkungen, die sich von denen nach täglicher Applikation von 1 mg oder monatlicher Applikation von 3,75 mg unterschieden, gefunden werden.
Kinder und Jugendliche
In den USA kamen in klinischen Studien Dosierungen von 7,5 mg bis 22,5 mg Leuprorelinacetat als Depot pro Monat zum Einsatz. Andere bzw. neue systemische Nebenwirkungen, die sich von denen nach monatlicher Applikation von 3,75 mg Leuprorelinacetat als Depot unterschieden, wurden nicht gefunden.
5. PHARMAKOLOGISCHE EIGENSCHAFTEN
5.1 Pharmakodynamische Eigenschaften
Pharmakotherapeutische Gruppe: GnRH-Analoga ATC-Code: L02AE
Leuprorelinacetat, der Wirkstoff von Enantone Monats-Depot, ist ein synthetisches Analogon des natürlich vorkommenden hypothalamischen "Releasing-Faktors" GnRH, der die Freisetzung der gonadotropen Hormone LH (luteinisierendes Hormon) und FSH (follikelstimulierendes Hormon) aus dem Hypophysenvorderlappen kontrolliert. Diese Hormone stimulieren ihrerseits die gonadale Steroidsynthese.
Im Gegensatz zum physiologischen GnRH, das pulsatil vom Hypothalamus freigesetzt wird, blockiert das auch als GnRH-Agonist bezeichnete Leuprorelinacetat bei therapeutischer Daueranwendung die GnRH-Rezeptoren der Hypophyse kontinuierlich und verursacht nach einer initialen, kurzfristigen Stimulation deren Desensibilisierung ("down regulation"). Als Folge kommt es zu einer reversiblen hypophysären Suppression der Gonadotropin-Freisetzung mit nachfolgendem Abfall der Estradiol (E2)- bzw. Testosteron-Spiegel.
Männer
Es kommt zu einer Senkung des Testosteronspiegels und damit zu einer Beeinflussung des Wachstums des karzinomatös veränderten Prostatagewebes, das durch Dihydrotestosteron - gebildet durch Reduktion von Testosteron in den Prostatazellen - normalerweise stimuliert wird.
Die kontinuierliche Applikation von Leuprorelinacetat führt zu einer Abnahme der Anzahl und/oder der Empfindlichkeit (sogenannte "down regulation") der in der Hypophyse vorhandenen Rezeptoren und in der Folge zum Abfall der LH-, FSH- und DHT-Spiegel. Der Testosteronspiegel wird dabei in den Kastrationsbereich abgesenkt.
Auch in Tierversuchen konnte die antiandrogene Wirkung und Wachstumshemmung von Prostatakarzinomen nachgewiesen werden.
Den experimentellen und klinischen Studien zufolge bewirkt die monatliche Behandlung mit Enantone Monats-Depot nach anfänglicher Stimulation eine Hemmung der Gonadotropinfreisetzung.
Beim Mann bewirkt die subkutane Verabreichung von Enantone Monats-Depot einen anfänglichen Anstieg von LH (luteinisierendes Hormon) und FSH (follikelstimulierendes Hormon), gekennzeichnet durch einen passageren Spiegelanstieg von Testosteron und Dihydrotestosteron.
Da in Einzelfällen in den ersten drei Wochen eine damit zusammenhängende kurzfristige symptomatische Verschlechterung des Krankheitsbildes beobachtet wurde, ist bei Männern mit
Prostatakarzinom die zusätzliche Gabe von Antiandrogenen zu erwägen.
Die Langzeittherapie mit Enantone Monats-Depot bewirkt dagegen bei allen Patienten eine Erniedrigung der LH- und FSH-Spiegel; es werden beim Mann Androgenspiegel erreicht, wie sie nach einer beidseitigen Orchiektomie vorliegen. Diese Veränderungen treten meist zwei bis drei Wochen nach Therapiebeginn auf und sind über den gesamten Behandlungszeitraum manifest. Aus diesem Grund kann auch mit Enantone Monats-Depot die Hormonempfindlichkeit eines Prostatakarzinoms und der mögliche therapeutische Wert einer Orchiektomie geprüft werden. Gegebenenfalls kann die Orchiektomie durch die monatliche Gabe von Enantone Monats-Depot ersetzt werden. Kastrationsspiegel für Testosteron konnten bisher nach kontinuierlicher Gabe von Leuprorelinacetat über fünf Jahre gehalten werden.
Klinische Wirksamkeit
In einer multizentrischen, randomisierten Phase III Studie mit Leuprorelinacetat wurden 263 Patienten mit lokal fortgeschrittenem Prostatakarzinom der Stadien T3 - T4 oder pT3, N0, M0 ausgewertet. Eine Kombination aus Radiotherapie mit einer Langzeit-Androgenentzugstherapie über 3 Jahre erhielten 133 Patienten und eine alleinige dreijährige Androgenentzugstherapie mit Leuprorelinacetat 130 Patienten.
Basierend auf den ASTRO (Phoenix) Kriterien lag das 5-Jahres-Progressionsfreie Überleben bei
60,9 % (64,7 %) in der Kombinationstherapie im Vergleich zu 8,5 % (15,4 %) in der Gruppe mit alleiniger Hormontherapie [p = 0,0001; (p = 0.0005)]. Entsprechend den ASTRO Kriterien lag das Progressionsrisiko 3,8 mal höher in der Gruppe mit alleiniger Hormontherapie (95 % CI [2,17; 6,49]). Die mediane klinische oder biochemische progressionsfreie Überlebenszeit nach ASTRO Definition lag bei 641 Tagen (95 % CI [626; 812]) in der Gruppe mit alleiniger Androgenentzugstherapie und bei 2.804 Tagen (95 % CI [2.090; -]; p < 0,0001) in der Gruppe mit Kombinationstherapie. Es ergaben sich weitere statistisch signifikante Unterschiede hinsichtlich einer lokoregionalen Progression [HR 3,6 (95 % CI [1,9; 6,8]; p < 0,0001)], metastatischer Progression (p < 0,018) und metastasenfreiem Überleben (p = 0,018) für die Gruppe mit Kombinationstherapie im Vergleich zur alleinigen Androgenentzugstherapie.
Die Ergebnisse dieser Studie konnten zeigen, dass eine 3-jährige Androgenentzugstherapie mit Leuprorelinacetat in Kombination mit Strahlentherapie der alleinigen 3-jährigen Androgenentzugstherapie mit Leuprorelinacetat überlegen ist.
In klinischen Studien konnte bei Patienten mit metastasiertem, kastrationsresistentem Prostatakarzinom der Nutzen einer zusätzlichen Wirkstoffgabe, wie etwa Inhibitoren der Androgensynthese (z. B. Abirateronacetat), Antiandrogene (z. B. Enzalutamid), Taxane (z. B. Docetaxel oder Cabazitaxel) oder Radiotherapeutika (z. B. Radium-223) zusätzlich zu GnRH-Agonisten, wie Leuprorelinacetat gezeigt werden.
Kinder und Jugendliche
Es kommt zu einer reversiblen Suppression der hypophysären Gonadotropin-Freisetzung mit nachfolgendem Abfall der Estradiol (E2)- bzw. Testosteronspiegel auf Werte in den präpubertären Bereich. Bei Patientinnen, die bereits vor Therapiebeginn postmenarchal sind, kommt es nach Behandlungsbeginn zu einer Entzugsblutung und im weiteren Verlauf der Therapie sistieren die Blutungen.
Es lassen sich die folgenden therapeutischen Wirkungen zeigen:
- Suppression der basalen und stimulierten Gonadotropinspiegel auf präpubertäres Niveau.
- Suppression erhöhter Sexualhormonspiegel auf präpubertäres Niveau, prämature Menstruationen werden gestoppt.
- Stopp oder Verminderung der somatischen Pubertätsentwicklung (Tanner-Stadien).
- Angleichung/Normalisierung des Verhältnisses von tatsächlichem Alter zu Knochenalter.
- Prävention einer beschleunigten Zunahme des Knochenalters.
- Abnahme bis zur Normalisierung der pathologisch erhöhten Wachstums-Geschwindigkeit.
- Zunahme der finalen Körpergröße.
Das Ergebnis der Behandlung ist eine Unterdrückung der pathologisch vorzeitig aktivierten Hypothalamus-Hypophysen-Gonadenachse entsprechend einer altersgemäßen pubertären Entwicklung.
Klinische Wirksamkeit
In einer klinischen Langzeitstudie an Kindern, die mit Leuprorelinacetat in Dosen bis zu 15 mg pro Monat über > 4 Jahre behandelt wurden, wurde bei Behandlungsende eine Wiederaufnahme der pubertären Entwicklung beobachtet. Follow-up Untersuchungen an 20 weiblichen Probanden zeigten bei 80 % eine normale Zyklustätigkeit im Erwachsenenalter und 12 Schwangerschaften in 7 von 20 Probanden einschließlich Mehrlingsschwangerschaften bei 4 Probandinnen.
5.2 Pharmakokinetische Eigenschaften
Freisetzung
Der Wirkstoff Leuprorelinacetat wird nach Injektion der Depotsuspension Enantone Monats-Depot kontinuierlich aus dem Copolymer, bestehend aus Glycolsäure und Milchsäure im Verhältnis 1:3, über den Zeitraum von einem Monat freigesetzt. Das Copolymer wird dabei wie chirurgisches Nahtmaterial resorbiert.
Männer
Resorption
Die Abbildung 1 zeigt die Leuprorelinspiegel im Serum nach einmaliger s.c. Applikation von Enantone Monats-Depot. Innerhalb von 1 Stunde werden Serumspiegel von 13 ng/ml gemessen. Nachweisbare Spiegel im Serum liegen bis 35 Tage nach der letzten Applikation vor.
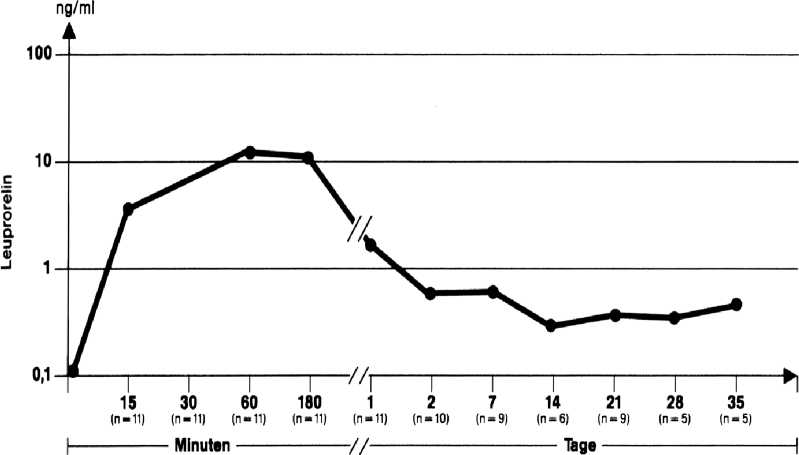
Abb.1: Leuprorelinspiegel im Serum nach einmaliger s.c. Applikation von 3,75mg Leuprorelinacetat als Enantone Monats-Depot
Verteilung und Elimination
Das Verteilungsvolumen von Leuprorelin beträgt bei Männern 36 l, die totale Clearance liegt bei 139,6 ml/min. (bestimmt unter Anwendung von Enantone Monats-Depot).
Bei wiederholter Gabe kommt es zu einer anhaltenden Senkung des Testosteronspiegels in den
Kastrationsbereich, ohne dass der Testosteronspiegel wie nach erstmaliger Injektion einen vorübergehenden Anstieg zeigt.
Patienten mit eingeschränkter Nierenfunktion/Leberfunktion
Bei Patienten mit eingeschränkter Nierenfunktion wurden nach Gabe von Enantone Monats-Depot teilweise höhere Leuprorelinserumspiegel gemessen, bei Patienten mit eingeschränkter Leberfunktion dagegen verminderte Werte. Klinisch scheint diese Beobachtung jedoch ohne Relevanz.
Kinder und Jugendliche
Die Abbildung 2 zeigt die Leuprorelinspiegel nach einmaliger s.c. Applikation von Leuprorelinacetat Depot in einer Dosierung von 30 pg/kg Körpergewicht. 60 Minuten nach der Applikation werden die maximalen Serumspiegel erreicht. Sie liegen bei 7,81 ± 3,59 ng/ml. Die AUC0-672 beträgt 105,78 ± 52,40 ng x h/ml.
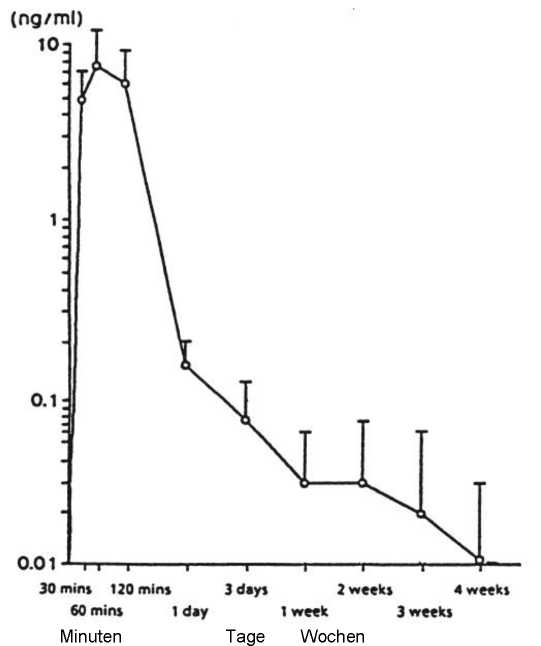
Abb.2: Leuprorelinspiegel im Serum nach einmaliger s.c. Applikation von 30 pg/kg Körpergewicht Leuprorelinacetat als Depot (n=6, Mittelwert ± SD)
Bioverfügbarkeit
Die Bioverfügbarkeit, berechnet durch Vergleich mit der AUC einer i.v. Gabe von 1 mg Leuprorelinacetat, beträgt nach 28 Tagen für die Depotformulierung von Leuprorelinacetat 98 %, gemessen bei Männern.
5.3 Präklinische Daten zur Sicherheit
Akute Toxizität (LD50)
Die akute Toxizität der Depotzubereitung wurde bei männlichen und weiblichen Mäusen und Ratten in vier Applikationsformen (i.p., i.m., s.c., p.o.) untersucht.
Bis zu Dosen von 2.000 bzw. 5.000 mg Leuprorelinacetat Depot wurden keine Todesfälle beobachtet. Toxizität bei wiederholter Gabe
Studien zur chronischen Toxizität wurden an Ratten und Hunden über 13 Wochen (subkutane oder intramuskuläre Injektion von bis zu 8 mg Leuprorelinacetat/kg KG pro Woche) und über 12 Monate (subkutane Applikation bis zu 32 mg Leuprorelinacetat/kg KG pro Monat) durchgeführt.
Bei allen Dosierungen (die niedrigste getestete Dosis betrug 0,8 mg Leuprorelinacetat/kg KG pro Monat) kam es zu lokalen Hautläsionen an der Injektionsstelle und zu atrophischen Veränderungen an den Reproduktionsorganen. Bei der Ratte traten bei allen Dosierungen Vakuolen in Leberzellen und in den tubulären Epithelzellen der Niere auf. Die Veränderungen an den Reproduktionsorganen sind aufgrund der endokrinologischen Wirkungen der Substanz zu erklären.
Karzinogenität, Mutagenität, Beeinflussung der Fertilität
Karzinogenität
Karzinogenitätsstudien wurden über zwei Jahre an Ratten und Mäusen durchgeführt. Bei Ratten zeigte sich eine dosisabhängige Zunahme von Hypophysenadenomen. Diese Befunde traten nach täglicher subkutaner Applikation bei Dosierungen von 0,6 bis 4 mg bei der Ratte während 24 Monaten auf.
Bei Mäusen traten Hypophysenadenome bei Dosierungen von 60 mg/kg/Tag über zwei Jahre nicht auf.
Mutagenität
In vitro und in vivo Untersuchungen mit Leuprorelinacetat zum Nachweis von Gen- und Chromosomenmutationen ergaben keine Hinweise auf ein mutagenes Potential.
Fertilität
Untersuchungen an geschlechtsreifen weiblichen Ratten, die Leuprorelinacetat jeweils 2-mal täglich 10 ^g s.c. über 14 Tage bzw. 40 ^g s.c. über 13 Tage erhielten, zeigten nach Absetzen der Substanz eine Zunahme der Organgewichte von Uterus und Ovarien, einen Anstieg der Hormonspiegel sowie ein Auftreten von frischen Corpora lutea.
Untersuchungen an weiblichen und männlichen unreifen Ratten über 3 Monate bei fortgesetzter (200 ^g/kg KG/Tag) bzw. intermittierender (0,8 bzw. 2,4 mg/kg KG/Monat) Applikation haben gezeigt, dass in der anschließenden Erholungsphase ein normales Reproduktionsverhalten vorliegt.
Die F1-Generation zeigte keine Anomalitäten. Das Reproduktionsverhalten der F1-Generation wurde nicht untersucht.
Männer:
Klinische und pharmakologische Studien haben gezeigt, dass die Unterdrückung der Fertilität spätestens 24 Wochen nach Absetzen einer kontinuierlichen Leuprorelinacetat-Applikation voll reversibel war.
Reproduktionstoxizität
Untersuchungen an Ratten und Kaninchen haben keine Hinweise auf ein teratogenes Potential ergeben. Embryotoxische/embryoletale Wirkungen wurden beim Kaninchen bei Dosen über 0,24 ^g/kg beobachtet.
6. PHARMAZEUTISCHE ANGABEN 6.1 Liste der sonstigen Bestandteile
Retardmikrokapseln:
33,75 mg Poly(glycolsäure-co-milchsäure) 1:3
Mannitol (Ph.Eur.)
Suspensionsmittel:
Mannitol (Ph.Eur.)
Carmellose-Natrium Polysorbat 80
Essigsäure 99 % (zur Einstellung des pH-Wertes)
Wasser für Injektionszwecke
6.2 Inkompatibilitäten
Nicht zutreffend.
6.3 Dauer der Haltbarkeit
Die Retardmikrokapseln und das Suspensionsmittel sind 36 Monate haltbar.
Bei Auftreten einer Verfärbung der Retardmikrokapseln und/oder Trübung des klaren Suspensionsmittels vor der Suspendierung darf die Zweikammerspritze nicht mehr verwendet werden. Nach der Zubereitung entsteht eine milchig-trübe Suspension.
Die chemische und physikalische Stabilität der gebrauchsfertigen Zubereitung wurde für 24 Stunden bei 25 °C nachgewiesen. Aus mikrobiologischer Sicht sollte die gebrauchsfertige Zubereitung sofort verwendet werden. Wenn die gebrauchsfertige Zubereitung nicht sofort verwendet wird, ist der Anwender für die Dauer und die Bedingungen der Aufbewahrung verantwortlich.
Vor der Injektion ist die Suspension erneut aufzuschütteln. Nach Anbruch Rest verwerfen.
6.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung
Nicht über 25 °C lagern. Zweikammerspritze im Umkarton aufbewahren, um den Inhalt vor Licht zu schützen.
6.5 Art und Inhalt des Behältnisses
1 Zweikammerspritze enthält 44,1 mg Retardmikrokapseln und 1 ml Suspensionsmittel.
Folgende Packungsgrößen sind erhältlich:
1 Zweikammerspritze 3 Zweikammerspritzen Klinikpackung mit 1 Zweikammerspritze
Die Zweikammerspritze (Glas EP Typ I) mit Luer-Lock-Verschluss (Polypropylen) und Stopfensystem (Chlorbutyl-Gummi) ist versiegelt in einer Blisterpackung.
6.6 Besondere Vorsichtsmaßnahmen für die Beseitigung und sonstige Hinweise zur Handhabung
Keine besonderen Anforderungen.
Anleitung zur Herstellung der Enantone Monats-Depot Suspension
1. Spritzenstempel bis zum Anschlag eindrehen.
2. Spritze mit der Kanüle senkrecht nach oben halten.
3. Das Stopfensystem langsam bis zur blauen Markierung vorschieben.
Dabei gelangt das Suspensionsmittel über den Bypass in die vordere Wirkstoffkammer.
4. Der Spritzenstempel darf jetzt nicht mehr zurückgezogen werden.
5. Spritze zur Herstellung einer milchigen Suspension mit der Kanüle senkrecht nach oben halten und durch Bewegung nach links und rechts oder Aufklopfen auf das Zeigefingergrundgelenk gut aufschütteln (nicht waagerecht oder nach unten halten, da sonst Suspensionsmittel austreten kann).
6. Vor der Injektion die Schutzkappe von der Injektionsnadel abziehen, nicht abdrehen! Dann die Luft über der Suspension vorsichtig herausdrücken.
Die Spritze ist jetzt injektionsbereit.
Eine Aspiration ist bei subkutan liegender Injektionsnadel möglich.
Handhabung nach der Injektion
7. Sicherheitsvorrichtung an der Kanüle bis zum fühlbaren/hörbaren Einrasten entsprechend der Pfeilmarkierung ganz nach vorne schieben.
8. Spritze bitte ordnungsgemäß entsorgen.
7. INHABER DER ZULASSUNG
Takeda GmbH Byk-Gulden-Str. 2 78467 Konstanz Tel.: 0800 8253325 Fax: 0800 8253329 E-Mail: medinfo@takeda.de
8. ZULASSUNGSNUMMER
34204.00.00
9. DATUM DER ERTEILUNG DER ZULASSUNG/VERLÄNGERUNG DER ZULASSUNG
Datum der Erteilung der Zulassung: 20. Januar 1998 Datum der letzten Verlängerung der Zulassung: 26. Juli 2010
10. STAND DER INFORMATION
März 2016
11. VERKAUFSABGRENZUNG
V erschreibungspflichtig.
15