Fanhdi 250 I.e.
Gebrauchsinformation: Information für Anwender
Fanhdi® 250 I.E., 500 I.E., 1000 I.E. und 1500 I.E. Trockensubstanz und Lösungsmittel zur Herstellung einer Injektionslösung
Wirkstoff: Blutgerinnungsfaktor VIII vom Menschen
Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses
Arzneimittels beginnen, denn sie enthält wichtige Informationen.
- Heben Sie die Packungsbeilage auf. Vielleicht möchten Sie diese später nochmals lesen.
- Wenn Sie weitere Fragen haben, wenden Sie sich bitte an Ihren Arzt, Apotheker oder das medizinische Fachpersonal.
- Dieses Arzneimittel wurde Ihnen persönlich verschrieben. Geben Sie es nicht an Dritte weiter. Es kann anderen Menschen schaden, auch wenn diese die gleichen Beschwerden haben wie Sie.
- Wenn Sie Nebenwirkungen bemerken, wenden Sie sich an Ihren Arzt, Apotheker oder das medizinische Fachpersonal. Dies gilt auch für Nebenwirkungen, die nicht in dieser Packungsbeilage angegeben sind. Siehe Abschnitt 4.
Was in dieser Packungsbeilage steht
1. Was ist Fanhdi® und wofür wird es angewendet?
2. Was sollten Sie vor der Anwendung von Fanhdi® beachten?
3. Wie ist Fanhdi® anzuwenden?
4. Welche Nebenwirkungen sind möglich?
5. Wie ist Fanhdi® aufzubewahren?
6. Inhalt der Packung und weitere Informationen
1. Was ist Fanhdi® und wofür wird es angewendet?
Fanhdi® ist ein Mittel zur Blutstillung (Antihämorrhagikum).
Fanhdi® wird angewendet zur Behandlung und Prophylaxe von Blutungen bei Patienten mit Hämophilie A (angeborener Faktor-VIII-Mangel).
Fanhdi® kann zur Behandlung von erworbenem Faktor-VIII-Mangel eingesetzt werden.
2. Was sollten Sie vor der Anwendung von Fanhdi® beachten?
Fanhdi® darf nicht angewendet werden,
- wenn Sie allergisch gegen Blutgerinnungsfaktor VIII vom Menschen, Heparin (theoretisch in Spuren aus dem Herstellungsprozess enthalten) oder einen der in Abschnitt 6. genannten sonstigen Bestandteile dieses Arzneimittels sind.
Warnhinweise und Vorsichtsmaßnahmen
Bitte sprechen Sie mit Ihrem Arzt, Apotheker oder dem medizinischen Fachpersonal, bevor Sie
Fanhdi® anwenden.
Besondere Vorsicht bei der Anwendung von Fanhdi® ist erforderlich,
- da es in seltenen Fällen zu einer anaphylaktischen Reaktion (plötzliche schwere allergische Reaktion) kommen kann. Wenn Sie Ausschlag oder generalisierte Nesselsucht, Engegefühl in der Brust, Schwindel, Übelkeit oder ein Absinken des Blutdrucks, was sich durch Schwindelgefühle beim Stehen bemerkbar macht, bei sich beobachten, können dies Anzeichen für eine anaphylaktische Reaktion gegenüber Fanhdi® sein. Sollten diese Symptome auftreten, müssen Sie die Anwendung des Produktes sofort abbrechen und sich mit Ihrem Arzt in Verbindung setzen.
- wenn sich Ihre Blutung mit Fanhdi® nicht kontrollieren lässt. Setzen Sie sich sofort mit Ihrem Arzt in Verbindung. Sie haben wahrscheinlich Hemmkörper gegen Faktor VIII entwickelt und Ihr Arzt wird einige Tests durchführen, um dies abzuklären. Faktor-VIII-Hemmkörper sind im Blut vorkommende Antikörper, die gegen den Faktor VIII, den Sie verwenden, gerichtet sind. Dies führt zu einer geringeren Wirksamkeit von Faktor VIII bei der Kontrolle der Blutung.
Bei der Herstellung von Arzneimitteln aus menschlichem Blut oder Plasma erfolgen bestimmte Maßnahmen, um die Übertragung von Infektionen auf Patienten zu verhindern. Diese beinhalten:
• die sorgfältige Auswahl von Blut- und Plasmaspendern, um sicherzustellen, dass Infektionsträger ausgeschlossen werden,
• die Testung der einzelnen Spende und der Plasmapools auf Anzeichen von Viren/Infektionen,
• die Aufnahme bestimmter Schritte in die Weiterverarbeitung von Blut oder Plasma, die Viren inaktivieren oder entfernen können.
Trotz dieser Maßnahmen kann bei der Anwendung von Arzneimitteln, die aus menschlichem Blut oder Plasma hergestellt werden, die Möglichkeit der Übertragung einer Infektion nicht vollständig ausgeschlossen werden. Dies trifft auch für alle unbekannten oder neu auftauchenden Viren oder anderen Infektionstypen zu.
Die durchgeführten Maßnahmen werden bei umhüllten Viren wie dem Human Immunodeficiency Virus (HIV), dem Hepatitis-B-Virus und dem Hepatitis-C-Virus sowie bei dem nicht-umhüllten Hepatitis A-Virus als wirksam erachtet. Sie können von begrenzter Wirksamkeit gegen nicht-umhüllte Viren wie Parvovirus B19 sein. Parvovirus-B19-Infektionen können schwerwiegende Folgen für schwangere Frauen ( Infektion des Ungeborenen) haben und für Patienten, deren Immunsystem geschwächt ist oder die bestimmte Formen der Anämie (z.B. Sichelzellen-Anämie oder hämolytische Anämie) haben.
Möglicherweise empfiehlt Ihnen Ihr Arzt über eine Impfung gegen Hepatitis A oder Hepatitis B nachzudenken, wenn Sie regelmäßig/wiederholt Faktor-VIII-Produkte aus menschlichem Plasma erhalten.
Jedes Mal, wenn Sie Fanhdi® erhalten, sollte der Produktname und die Chargenbezeichnung aufgeschrieben werden, um eine Dokumentation der verwendeten Chargen zu erhalten.
Siehe auch Abschnitt 4. Welche Nebenwirkungen sind möglich?
Anwendung von Fanhdi® zusammen mit anderen Arzneimitteln
Informieren Sie Ihren Arzt oder Apotheker, wenn Sie andere Arzneimittel einnehmen/anwenden, kürzlich andere Arzneimittel eingenommen/angewendet haben oder beabsichtigen andere Arzneimittel einzunehmen/anzuwenden.
Es sind keine Wechselwirkungen von Blutgerinnungsfaktor VIII vom Menschen mit anderen Arzneimitteln bekannt.
Schwangerschaft und Stillzeit
Aufgrund des seltenen Auftretens von Hämophilie A bei Frauen, liegen keine Erfahrungen hinsichtlich der Anwendung von Fanhdi® während der Schwangerschaft und Stillzeit vor.
Fragen Sie vor der Einnahme/Anwendung von allen Arzneimitteln Ihren Arzt oder Apotheker um Rat.
Verkehrstüchtigkeit und Fähigkeit zum Bedienen von Maschinen
Fanhdi® hat keinen oder nur vernachlässigbaren Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen.
Wie ist Fanhdi® anzuwenden?
3.
Wenden Sie Fanhdi® immer genau nach der Anweisung des Arztes an. Bitte fragen Sie bei Ihrem
Arzt oder Apotheker nach, wenn Sie sich nicht ganz sicher sind.
Fanhdi® ist nur intravenös zu verabreichen.
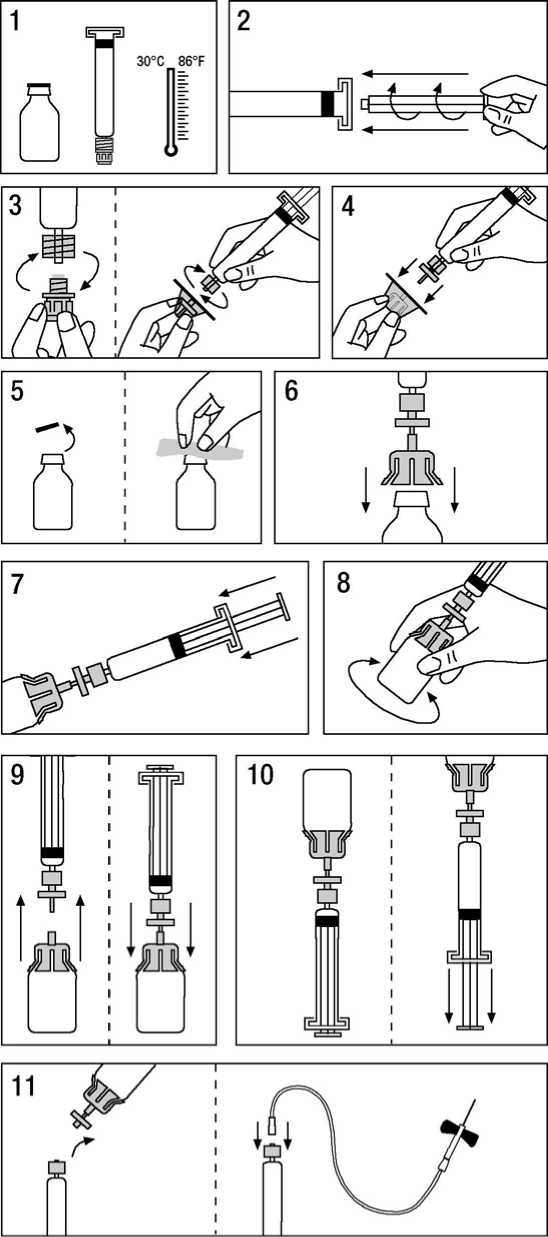
Herstellung der Injektionslösung:
1. Produktflasche und Spritze auf Raumtemperatur bringen.
2. Kolben in die Spritze mit dem Lösungsmittel eindrehen, wobei die Plastikmanschette in diesem Bereich unter keinen Umständen entfernt werden darf.
3. Folie von der Filterverpackung abziehen. Verschlusskappe von der Spritzenspitze entfernen und Spritze auf den Filter drehen.
4. Transferadapter aus der Verpackung nehmen und auf die Spritze mit dem Filter setzen.
5. Kunststoffdeckel von der Produktflasche entfernen und den Gummistopfen mit dem beigepackten Alkoholtupfer desinfizieren.
6. Gummistopfen der Produktflasche mit der Kanüle des Transferadapters durchstechen.
7. Das gesamte Lösungsmittel wird nun aus der Spritze in die Produktflasche überführt.
8. Spritze mit Produktflasche vorsichtig schwenken bis das Lyophilisat vollständig gelöst ist. Wie für jede parenterale Lösung gilt, dass sie nicht verwendet werden darf, wenn das Lyophilisat nicht vollständig aufgelöst ist oder Partikel sichtbar sind.
9. Spritze mit Filter kurz von der Produktflasche mit Transferadapter trennen, um das Vakuum zu entfernen.
10. Produktflasche mit aufgesetzter Spritze umdrehen und Lösung in die Spritze aufziehen.
11. Injektionsstelle vorbereiten. Spritze (ohne Filter!) abnehmen, beigepackte Butterfly-Kanüle aufsetzen, entlüften und Lösung intravenös injizieren. Die Infusionsgeschwindigkeit sollte 3 ml/min. betragen. Um vasomotorische Reaktionen zu vermeiden sollte sie 10 ml/min. nie überschreiten.
Das Infusionsbesteck darf nicht wieder verwendet werden.
Nicht verwendetes Produkt oder Abfallmaterial muss gemäß den geltenden Bestimmungen entsorgt
werden.
Die zu verabreichende Dosis an Fanhdi® sowie die Häufigkeit der Anwendung hängt von vielen Faktoren wie z.B. Gewicht, Schwere der Hämophilie, Blutungsort und -ausmaß, Höhe der evtl. vorhandenen Faktor-VIII-Hemmkörper sowie dem erforderlichen Faktor-VIII-Spiegel ab.
Ihr Arzt wird die Dosierung und Anwendungshäufigkeit von Fanhdi® berechnen, um die notwendige Faktor-VIII-Aktivität in Ihrem Blut zu erreichen.
Die erforderliche Dosis lässt sich durch folgende Formel ermitteln:
Erforderliche Einheiten an FVIII (I.E.) = Körpergewicht (kg) x erwünschter Anstieg der Faktor VIII-Aktivität (%) (I.E./dl) x 0,5
Die zu verabreichende Dosis und Häufigkeit der Anwendung sollte sich stets an der klinischen Wirksamkeit im Einzelfall orientieren.
Bei den im Folgenden aufgeführten Blutungsereignissen sollte die angegebene Faktor-VIII-Aktivität im Plasma (in % des Normalwertes oder in I.E./dl) im betreffenden Zeitraum nicht unterschritten werden.
Die folgende Tabelle dient zur Orientierung für die Dosierung bei Blutungsereignissen und chirurgischen Eingriffen:
|
Schwere der Blutung / Art des chirurgischen Eingriffs |
Erforderlicher F VIII-Plasmaspiegel (%) (I.E./dl) |
Häufigkeit der Dosierung (Stunden) / Behandlungsdauer (Tage) |
|
Blutungen | ||
|
Gelenkblutungen im Frühstadium, Muskelblutungen, Blutungen im Mundbereich |
20 - 40 |
Injektion alle 12 bis 24 Stunden; mindestens 1 Tag, bis die (durch Schmerzen erkennbare) Blutung sistiert bzw. Wundheilung erreicht ist. |
|
Ausgeprägte Gelenkblutungen, Muskelblutungen oder Hämatome |
30 - 60 |
Injektion alle 12 bis 24 Stunden für 3 bis 4 Tage oder länger wiederholen, bis die Schmerzen und Behinderungen beseitigt sind. |
|
Lebensbedrohliche Blutungen |
60 - 100 |
Injektion alle 8 bis 24 Stunden wiederholen, bis die Gefahr für den Patienten vorüber ist. |
|
Chirurgische Eingriffe | ||
|
Kleinere Eingriffe, einschließlich Zahnextraktionen |
30 - 60 |
Injektion alle 24 Stunden; mindestens 1 Tag, bis Wundheilung erreicht ist. |
|
Größere Eingriffe |
80 - 100 (prä- und postoperativ) |
Injektion alle 8 bis 24 Stunden wiederholen, bis ausreichende Wundheilung erreicht ist; dann für mindestens weitere 7 Tage einen Faktor VIII-Spiegel von 30 % bis 60 % (I.E./dl) aufrechterhalten. |
Ihr Arzt wird die Dosis und Anwendungshäufigkeit von Fanhdi® immer an die klinische Wirksamkeit im Einzelfall anpassen. Manchmal werden die benötigten Mengen höher sein als die vorher berechneten, insbesondere bei der ersten Dosis.
Verwenden Sie Fanhdi® um Blutungen zu verhindern (Prophylaxe), so wird Ihr Arzt die geeignete Dosierung berechnen. Die übliche Dosierung liegt bei 20 bis 40 I.E. Faktor VIII pro kg Körpergewicht im Abstand von 2-3 Tagen. In manchen Fällen, besonders bei jüngeren Patienten, können kürzere Dosierungsintervalle oder höhere Dosen erforderlich sein.
Obwohl die Dosierung mittels der oben aufgeführten Formel berechnet werden kann, ist es empfehlenswert in angemessenen Abständen geeignete Tests im Plasma durchzuführen, um sicherzustellen, dass passende Faktor-VIII-Spiegel erreicht und aufrechterhalten werden. Im Falle größerer operativer
Eingriffe ist eine genaue Überwachung der Substitutionstherapie mittels Gerinnungsanalysen unverzichtbar.
Werden die erwarteten Faktor-VIII-Spiegel nicht erreicht oder kann die Blutung mit einer offenbar angemessenen Dosis nicht kontrolliert werden, so muss vermutet werden, dass Hemmkörper gegen Faktor VIII vorhanden sind. Die Anwesenheit und Menge von Faktor-VIII-Hemmkörpern wird von Spezialisten mittels geeigneter Labormethoden bestimmt.
Bitte sprechen Sie mit Ihrem Arzt, wenn Sie den Eindruck haben, dass die Wirkung von Fanhdi® zu stark oder zu schwach ist.
Hemmkörperpatienten
Wenn Ihr Arzt Ihnen mitteilt, dass Sie Hemmkörper gegen Faktor VIII entwickelt haben, werden Sie wahrscheinlich größere Mengen Fanhdi® benötigen, um Blutungen zu kontrollieren. Wenn diese Dosierung Ihre Blutung nicht kontrolliert, sollten andere therapeutische Möglichkeiten erwogen werden. Erhöhen Sie nicht die verordnete Fanhdi®-Dosierung um die Blutung zu stillen, ohne Ihren Arzt zu konsultieren. Sollten Sie weitere Informationen benötigen, so fragen Sie Ihren Arzt. Diese Behandlungen sollten nur von Ärzten, die über Erfahrung in der Therapie der Hämophilie A verfügen, durchgeführt werden.
Siehe auch Abschnitt 2. Was müssen Sie vor der Anwendung von Fanhdi® beachten?
Anwendung bei Kindern und Jugendlichen
Es liegen nicht genügend Daten aus klinischen Studien über die Behandlung von Kindern unter 6 Jahren vor.
Wenn Sie eine größere Menge von Fanhdi® verabreicht haben, als Sie sollten
Symptome von Überdosierung mit Blutgerinnungsfaktor VIII vom Menschen wurden nicht berichtet.
Dennoch sollten Sie sich sofort mit Ihrem Arzt oder Apotheker in Verbindung setzen, wenn Sie mehr Fanhdi® infudiert haben als notwendig.
Wenn Sie die Anwendung von Fanhdi® vergessen haben
Applizieren Sie sofort die nächste Anwendung und fahren Sie danach in regelmäßigen Intervallen gemäß den Anweisungen des Arztes fort.
Infundieren Sie nicht die doppelte Dosis, wenn Sie die vorherige Gabe vergessen haben.
Wenn Sie weitere Fragen zur Anwendung dieses Arzneimittels haben, wenden Sie sich an Ihren Arzt, Apotheker oder das medizinische Fachpersonal.
4. Welche Nebenwirkungen sind möglich?
Wie alle Arzneimittel kann auch dieses Arzneimittel Nebenwirkungen haben, die aber nicht bei jedem auftreten müssen.
In seltenen Fällen können folgende Nebenwirkungen nach der Verabreichung von Fanhdi® auftreten:
- Juckreiz, lokale Reaktionen an der Injektionsstelle (z.B. Brennen und vorübergehende Rötung)
- Allergische Reaktionen (z.B. Engegefühl in der Brust, Unwohlsein, Schwindel, Übelkeit und leichtes Absinken des Blutdrucks, was zu Schwindelgefühlen beim Stehen führen kann)
- Eigenartiger Geschmack in Ihrem Mund
- Fieber
- Herzjagen
Gelegentlich kann ein anaphylaktischer Schock auftreten. Beobachten Sie während der Injekti-on/Perfusion Symptome wie,
- Engegefühl in der Brust, Unwohlsein,
- Schwindel,
- leichtes Absinken des Blutdrucks (was zu Schwindelgefühlen beim Stehen führen kann) oder
- Übelkeit,
so kann dies ein erstes Anzeichen von Überempfindlichkeit und einer anaphylaktischen Reaktion sein.
Im Fall einer anaphylaktischen oder allergischen Reaktion, unterbrechen Sie die Injekti-on/Perfusion und benachrichtigen Sie sofort Ihren Arzt.
Allergische Reaktionen gegen Bestandteile des Produkts können nicht vollständig ausgeschlossen werden. Die Bildung neutralisierender Antikörper gegen Faktor VIII (Hemmkörper/Inhibitoren) ist eine bekannte Komplikation bei der Behandlung von Patienten mit Hämophilie A. Gemäß Studien, die mit Faktor-VIII-Produkten menschlichen Ursprungs durchgeführt wurden, kommt es insbesondere bei Patienten, die vorher noch nicht behandelt wurden, zur Entwicklung von Hemmkörpern. Sie müssen deshalb sorgfältig anhand geeigneter klinischer Beobachtungen sowie mittels Laboruntersuchungen auf Bildung von Hemmkörpern überwacht werden.
Heparin, welches in Fanhdi® theoretisch in Spuren aus dem Herstellungsprozess enthalten sein kann, kann allergische Reaktionen hervorrufen und die Blutplättchenzahl vermindern mit der Folge einer Blutgerinnungsstörung. Wenn bei Ihnen früher durch Heparin bedingte allergische Reaktionen aufgetreten sind, sollten Sie Fanhdi® nicht anwenden.
Meldung von Nebenwirkungen
Wenn Sie Nebenwirkungen bemerken, wenden Sie sich an Ihren Arzt, Apotheker oder das medizinische Fachpersonal. Dies gilt auch für Nebenwirkungen, die nicht in dieser Packungsbeilage angegeben sind. Sie können Nebenwirkungen auch direkt dem Bundesinstitut für Impfstoffe und biomedizinische Arzneimittel, Paul-Ehrlich-Institut, Paul-Ehrlich-Straße 51-59, 63225 Langen, Tel: +49 6103 77 0, Fax: +49 6103 77 1234, Website: www.pei.de anzeigen.
Indem Sie Nebenwirkungen melden, können Sie dazu beitragen, dass mehr Informationen über die Sicherheit dieses Arzneimittels zur Verfügung gestellt werden.
5. Wie ist Fanhdi® aufzubewahren?
Bewahren Sie dieses Arzneimittel für Kinder unzugänglich auf.
Sie dürfen dieses Arzneimittel nach dem auf dem Etikett angegebenen Verfalldatum nicht mehr verwenden.
Aufbewahrungsbedingungen
Nicht über 30 °C lagern. Nicht einfrieren. Die Flasche im Umkarton aufbewahren, um den Inhalt vor Licht zu schützen.
Sie dürfen Fanhdi® nicht verwenden, wenn die hergestellte Lösung trüb ist oder einen Bodensatz aufweist. Generell ist die Lösung klar oder leicht opaleszent.
Weist die Lösung nach der Rekonstitution sichtbare Partikel oder Verfärbung auf, so muss sie verworfen werden.
Hinweis auf Haltbarkeit nach Anbruch oder Zubereitung
Nach der Herstellung der Lösung ist Fanhdi® innerhalb von 3 Stunden unter Verwendung der beigepackten Spritze zu verwenden.
Nicht verwendete Lösung darf nicht zur späteren Anwendung aufbewahrt werden bzw. darf nicht im Kühlschrank gelagert werden.
Entsorgen Sie Arzneimittel nicht im Abwasser oder Haushaltsabfall. Fragen Sie Ihren Arzt oder Apotheker, wie das Arzneimittel zu entsorgen ist, wenn Sie es nicht mehr verwenden. Sie tragen damit zum Schutz der Umwelt bei.
6. Inhalt der Packung und weitere Informationen Was Fanhdi® enthält
Trockensubstanz: Der Wirkstoff ist Blutgerinnungsfaktor VIII vom Menschen, welcher in Fanhdi® als Komplex mit dem von-Willebrand-Faktor vorliegt.
Die sonstigen Bestandteile sind Arginin, Albumin vom Menschen und Histidin.
Lösungsmittel: Wasser für Injektionszwecke.
Fanhdi® 250 I.E. enthält nach Rekonstitution in 10 ml Wasser für Injektionszwecke ungefähr 25 I.E. Blutgerinnungsfaktor VIII vom Menschen pro ml.
Fanhdi® 500 I.E. enthält nach Rekonstitution in 10 ml Wasser für Injektionszwecke ungefähr 50 I.E. Blutgerinnungsfaktor VIII vom Menschen pro ml.
Fanhdi® 1000 I.E. enthält nach Rekonstitution in 10 ml Wasser für Injektionszwecke ungefähr 100 I.E. Blutgerinnungsfaktor VIII vom Menschen pro ml.
Fanhdi® 1500 I.E. enthält nach Rekonstitution in 15 ml Wasser für Injektionszwecke ungefähr 100 I.E. Blutgerinnungsfaktor VIII vom Menschen pro ml.
Wie Fanhdi® aussieht und Inhalt der Packung
Glasflasche mit weißer oder schwach gelblicher Trockensubstanz und Spritze mit Wasser für Injektionszwecke (Lösungsmittel).
Stärken:
Fanhdi® 250 I.E.
Fanhdi® 500 I.E.
Fanhdi® 1000 I.E.
Fanhdi® 1500 I.E.
Eine Packung Fanhdi® enthält: 1 Fläschchen mit Trockensubstanz, 1 vorgefüllte Spritze mit Lösungsmittel und Set zur Applikation (Transferadapter, Microfilter, 2 Alkoholtupfer, Butterfly-Kanüle).
Es werden möglicherweise nicht alle Stärken in den Verkehr gebracht.
Pharmazeutischer Unternehmer
Grifols Deutschland GmbH Lyoner Straße 15 60528 Frankfurt Tel.: 069/660 593 100 Fax: 069/660 593 110
Hersteller, der für die Chargenfreigabe verantwortlich ist
Instituto Grifols, S.A.
Can Guasc, 2 - Parets del Valles E-08150 Barcelona
Diese Packungsbeilage wurde zuletzt überarbeitet im Juli 2014 Herkunftsland des Blutplasmas
Das zur Herstellung von Fanhdi® verwendete Blutplasma stammt aus den USA, Tschechien oder der Slowakei.
8