Fem7 Sequi 50 Mikrogramm + 50 Mikrogramm/10 Mikrogramm/24 Stunden Transdermale Pflaster
1
GEBRAUCHSINFORMATION: INFORMATION FÜR DIE ANWENDERIN
Fem7® Sequi 50 Mikrogramm + 50 Mikrogramm/10 Mikrogramm/24 Stunden Transdermale Pflaster
Estradiol, Levonorgestrel
Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung
dieses Arzneimittels beginnen.
• Heben Sie die Packungsbeilage auf. Vielleicht möchten Sie diese später nochmals lesen.
• Wenn Sie weitere Fragen haben, wenden Sie sich bitte an Ihren Arzt oder Apotheker.
• Dieses Arzneimittel wurde Ihnen persönlich verschrieben. Geben Sie es nicht an Dritte weiter. Es kann anderen Menschen schaden, auch wenn diese dieselben Symptome haben wie Sie.
• Wenn Sie Nebenwirkungen bemerken, wenden Sie sich an Ihren Arzt oder Apotheker. Dies gilt auch für Nebenwirkungen, die nicht in dieser Packungsbeilage angegeben sind. Siehe Abschnitt 4.
Diese Packungsbeilage beinhaltet:
1. Was ist Fem7 Sequi und wofür wird es angewendet?
2. Was sollten Sie vor der Anwendung von Fem7 Sequi beachten?
3. Wie ist Fem7 Sequi anzuwenden?
4. Welche Nebenwirkungen sind möglich?
5. Wie ist Fem7 Sequi aufzubewahren?
6. Weitere Informationen
1. Was ist Fem7 Sequi und wofür wird es angewendet?
Fem7 Sequi ist ein Arzneimittel zur sequenziell kombinierten Hormonersatztherapie (HRT). Es enthält ein Estrogen (Estradiol) und ein Gelbkörperhormon (Levonorgestrel). Fem7 Sequi ist bei postmenopausalen Frauen anwendbar.
Während der Menopause nimmt die Menge an Estrogen ab, die vom Körper der Frau produziert wird. Bei einigen Frauen kann dies zu Symptomen wie z. B. Hitzegefühl in Gesicht, Nacken, Brustkorb (Hitzewallungen) führen. Die Anwendung von Fem7 Sequi mildert diese Symptome nach der Menopause.
Es liegen nur begrenzte Erfahrungen bei der Behandlung von Frauen über 65 Jahren vor.
2. Was sollten Sie vor der Anwendung von Fem7 Sequi beachten?
Sie sollten Ihren Arzt über alle wichtigen Krankheiten in Ihrer Vorgeschichte und in der Vorgeschichte Ihrer nächsten Verwandten informieren, ehe Sie mit einer Hormonersatztherapie (HRT) beginnen.
Medizinische Untersuchung und Kontrolluntersuchungen:
Ihr Arzt wird vor Beginn der Therapie und dann regelmäßig während der Therapie (mindestens einmal jährlich) eine medizinische Untersuchung veranlassen, um zu überprüfen, ob Ihr Körper die Medikation verträgt.
Ihre Brüste werden regelmäßig von Ihrem Arzt untersucht, insbesondere wenn Sie Knoten (Zysten oder Knötchen) haben oder jemand in Ihrer Familie bereits Brustkrebs hatte. Ihr Arzt wird Sie eventuell bitten, eine Mammographie durchführen zu lassen.
Von Zeit zu Zeit, mindestens einmal im Jahr, sollten Risiken und Nutzen der HRT sorgfältig neu bewertet werden, um zu entscheiden, ob die Behandlung fortgesetzt werden sollte.
Fem7 Sequi darf nicht angewendet werden,
• wenn Sie überempfindlich (allergisch) gegen einen der Wirkstoffe (Estradiol oder Levonorgestrel) oder einen der sonstigen Bestandteile von Fem7 Sequi sind (siehe auch Abschnitt 6)
• wenn Sie Brustkrebs haben oder hatten oder Ihr Arzt den Verdacht hat, dass Sie an einer Brustkrebserkrankung leiden könnten
• wenn bei Ihnen Blutgerinnselbildungen in einer Ihrer Venen in den Beinen oder der Lunge (tiefe Venenthrombose oder Lungenembolie) aufgetreten sind oder im Moment vorliegen
• wenn Sie an einer mit Thromboseneigung einhergehenden Blutgerinnungsstörung leiden (Thrombophilie, wie z.B. Protein-C-, Protein-S- oder Antithrombin-Mangel)
• wenn bei Ihnen eine durch Blutgerinnselbildung in den Arterien ausgelöste Erkrankung, wie z. B. anfallsartig auftretende Brustschmerzen mit Brustenge (Angina pectoris) oder ein Herzinfarkt oder ein Schlaganfall vorliegt oder erst kurze Zeit zurückliegt
• wenn Sie Brustkrebs, Gebärmutterkrebs oder einen anderen bösartigen Tumor haben, dessen Wachstum durch Zufuhr bestimmter weiblicher Geschlechtshormone angeregt wird (Estrogen-abhängiger Krebs), oder Ihr Arzt den Verdacht auf eine solche Erkrankung bei Ihnen hat
• wenn bei Ihnen eine übermäßige Verdickung der Gebärmutterschleimhaut (Endometriumhyperplasie) vorliegt, die noch nicht behandelt wurde;
• wenn Sie unter Blutungen aus der Scheide leiden, deren Ursache vom Arzt nicht geklärt ist
• wenn Sie eine Lebererkrankung haben oder hatten; in diesem Fall dürfen Sie Fem7 Sequi nicht anwenden, solange sich wichtige Leberwerte nicht normalisiert haben
• wenn Sie eine (erblich bedingte) Störung des Aufbaus des roten Blutfarbstoffes haben (Porphyrie)
Besondere Vorsicht bei der Anwendung von Fem7 Sequi ist erforderlich
Informieren Sie Ihren Arzt, wenn bei Ihnen eine der folgenden Situationen oder Erkrankungen vorliegt oder früher einmal vorlag und/oder wenn diese sich während einer Schwangerschaft oder einer vorhergehenden Hormonbehandlung verschlechtert hat, bevor Sie mit der Anwendung von Fem7 Sequi beginnen:
• wenn Sie hohen Blutdruck haben
• wenn Sie ein erhöhtes Risiko für die Bildung von Blutgerinnseln haben (siehe „HRT und die Auswirkungen auf das Herz und den Blutkreislauf“)
• wenn Sie einen hohen Blutzuckerspiegel (Diabetes) mit oder ohne Gefäßveränderungen haben
• wenn bei Ihnen eine Ansiedlung von Gebärmutterschleimhaut außerhalb der Gebärmutter (Endometriose) vorliegt, die Schmerzen und Blutungen verursacht
• wenn Sie einen gutartigen Tumor in Ihrer Gebärmutter haben (Gebärmutterfibrom)
• wenn Sie eine übermäßige Verdickung der Gebärmutterschleimhaut (Endometriumhyperplasie) in der Vorgeschichte haben
• wenn Sie ein erhöhtes Risiko für die Entwicklung von Tumorerkrankungen haben, die vom Estrogenspiegel im Blut abhängen (wie das Auftreten von Brustkrebs bei nahen Blutsverwandten)
• wenn Sie eine Leber- oder Gallenblasenerkrankung haben (Leberadenom, Gallensteine)
• wenn Sie unter Krampfanfällen (Epilepsie) leiden
• wenn Sie schwere Kopfschmerzen oder Migräne haben
• wenn Sie Asthma haben
• wenn Sie eine schwere Autoimmunerkrankung haben, die im Besonderen Ihre Haut betrifft (systemischer Lupus erythematodes)
• wenn Sie an einer Krankheit leiden, die einen Hörverlust bewirkt (Otosklerose)
Beenden Sie die Anwendung von Fem7 Sequi sofort
wenn einer der Punkte auftritt, die unter „Fem7 Sequi darf nicht angewendet werden" aufgelistet sind, oder wenn eine der folgenden Situationen eintritt:
• Sie entwickeln eine Gelbfärbung der Haut (Gelbsucht) oder Ihre Leberfunktion verschlechtert sich
• Ihr Blutdruck steigt plötzlich deutlich an
• Sie leiden erstmals unter migräneartigen Kopfschmerzen
• Sie sind schwanger
Bitte beachten Sie: Fem7 Sequi ist kein transdermales Kontrazeptivum und schützt Sie nicht davor, schwanger zu werden.
Sie müssen Ihren Arzt auch informieren, wenn
• Sie sich einer Operation zu unterziehen haben
• Sie für einen längeren Zeitraum immobilisiert sind
• Sie an einer anderen Krankheit erkrankt sind
Welche Risiken sind mit der Anwendung von Fem7 Sequi assoziiert?
HRT und die Auswirkungen auf das Herz und den Blutkreislauf
Blutgerinnsel (Thrombose)
Informieren Sie umgehend Ihren Arzt, wenn Sie unter der Anwendung von Fem7 Sequi eine schmerzhafte Schwellung eines Beines, plötzlichen Schmerz in der Brust oder Kurzatmigkeit bemerken. Dies könnten Anzeichen einer venösen Thrombose oder einer Lungenembolie sein. In diesem Fall müssen Sie die Anwendung von Fem7 Sequi sofort abbrechen.
Eine HRT erhöht das Risiko für Blutgerinnsel in den Venen um das 1,3 bis 3fache, insbesondere im ersten Jahr der Anwendung.
Zum Vergleich
Betrachtet man Frauen im Alter zwischen 50 und 59 Jahren, die keine Hormonersatztherapie anwenden, so würde erwartet werden, dass im Durchschnitt 4 von 1.000 Frauen über einen Zeitraum von 5 Jahren ein Blutgerinnsel bekommen.
Für Frauen zwischen 50 und 59 Jahren, die über einen Zeitraum von 5 Jahren eine Hormonersatztherapie anwenden, wird die Zahl der zusätzlichen Fälle 5 von 1.000 Anwenderinnen betragen.
Ihr Risiko, eine venöse Thrombose zu entwickeln, ist im Allgemeinen höher, wenn
• Sie Estrogene anwenden
• Sie älter sind
• Sie Krebs haben
• Sie schwanger sind oder kürzlich ein Kind geboren haben
• einer Ihrer nahen Blutsverwandten eine venöse Thrombose in der Vorgeschichte hat
• Sie ausgeprägtes Übergewicht haben
• Sie systemischen Lupus erythematodes (eine Autoimmunkrankheit) haben
• Sie an einem Blutgerinnungsproblem leiden, welches eine Langzeittherapie mit einem Blutverdünner erfordert
• Sie für eine längere Zeit immobilisiert sind (z. B., wenn Sie Bettruhe verordnet bekommen haben), einen Unfall oder eine größere Operation hatten. Unter diesen Umständen könnte es notwendig sein, die Anwendung der Fem7 Sequi Pflaster temporär auszusetzen. Vor einer geplanten Operation könnte es notwendig sein, die Anwendung 4 bis 6 Wochen vorher auszusetzen.
Es ist unklar, ob Krampfadern zu einem erhöhten Risiko für venöse Thrombosen führen.
Wenn eine der genannten Situationen auf Sie zutrifft, informieren Sie bitte Ihren Arzt. Falls Sie ein Antikoagulans einnehmen, müssen Risiko und Nutzen einer HRT-Anwendung sorgfältig gegeneinander abgewogen werden.
Koronare Herzkrankheit (KHK)
Unterbrechen Sie die Anwendung von Fem7 Sequi sofort und kontaktieren Sie umgehend Ihren Arzt, wenn Sie Schmerzen in der Brust entwickeln, die in den Arm oder den Hals ausstrahlen. Diese Schmerzen können ein Zeichen für eine Herzerkrankung sein.
Es gibt keinen Hinweis darauf, dass eine HRT vor einer Herzerkrankung schützt. Frauen, die eine Estrogen-Gestagen-HRT anwenden, weisen ein geringfügig höheres Risiko für eine Herzerkrankung auf als Frauen, die keine HRT-Medikamente anwenden. Da das Risiko für koronare Herzerkrankung sehr stark altersabhängig ist, ist die Anzahl der zusätzlichen Fälle von koronarer Herzerkrankung auf Grund einer Estrogen-Gestagen-Anwendung bei gesunden Frauen kurz nach der Menopause sehr niedrig, wird jedoch mit dem Alter ansteigen.
Schlaganfallrisiko
Unterbrechen Sie die Anwendung von Fem7 Sequi sofort und kontaktieren Sie umgehend Ihren Arzt, wenn sie unerklärliche migräneartige Kopfschmerzen mit oder ohne Sehstörungen bekommen. Solche Kopfschmerzen können ein frühes Zeichen für einen Schlaganfall sein.
Kombinierte Estrogen-Gestagen-HRT und Estrogen-Monotherapie erhöhen das Risiko für einen Schlaganfall bis zu 1,5-fach. Das Risiko von Anwenderinnen im Vergleich zu dem von NichtAnwenderinnen ändert sich nicht mit dem Alter oder dem zeitlichen Abstand zur Menopause.
Da jedoch das Risiko für Schlaganfall stark altersabhängig ist, wird in der Gesamtschau das Risiko für einen Schlaganfall bei Frauen, die eine HRT anwenden, mit dem Alter ansteigen.
Zum Vergleich
Betrachtet man Frauen im Alter zwischen 50 und 59 Jahren, die keine Hormonersatztherapie anwenden, so würde erwartet werden, dass im Durchschnitt 8 von 1.000 Frauen über einen Zeitraum von 5 Jahren einen Schlaganfall erleiden.
Für Frauen im Alter zwischen 50 und 59 Jahren, die über einen Zeitraum von 5 Jahren eine Hormonersatztherapie anwenden, wird die Zahl der zusätzlichen Fälle 3 von 1.000 Anwenderinnen betragen.
HRT und das Risiko für die Entwicklung einer Krebserkrankung
Übermäßige Verdickung der Gebärmutterschleimhaut (Endometriumhyperplasie) und Krebs der Gebärmutterschleimhaut (Endometriumkarzinom)
Bei Frauen mit Gebärmutter ist das Risiko einer übermäßigen Verdickung der Gebärmutterschleimhaut (Endometriumhyperplasie) und eines Endometriumkarzinoms erhöht, wenn Estrogene über einen längeren Zeitraum angewendet werden. Um dieses Risiko zu verringern ist es notwendig, Estrogene für mindestens 12 Tage im Monat kombiniert mit einem Gestagen anzuwenden.
In den ersten Monaten der Behandlung können außerplanmäßige Blutungen auftreten. Kontaktieren Sie Ihren Arzt, wenn diese Blutungen • über die ersten Behandlungsmonate hinaus bestehen bleiben;
• erst nach einer längeren Behandlungszeit auftreten;
• nach Beendigung der Fem7 Sequi Anwendung anhalten.
Ihr Arzt wird die Ursache hierfür untersuchen. Dies kann eine Biopsie der Gebärmutterschleimhaut beinhalten, um herauszufinden, ob Sie einen Krebs der Gebärmutterschleimhaut haben.
Zum Vergleich
Betrachtet man Frauen, die eine Gebärmutter haben und keine Hormonersatztherapie anwenden, so wird im Durchschnitt bei 5 von 1.000 Frauen ein Krebs der Gebärmutterschleimhaut diagnostiziert werden.
Bei 1.000 Frauen im Alter zwischen 50 und 65 Jahren, die eine Estrogen-Monotherapie anwenden, erhöht sich diese Anzahl in Abhängigkeit von Estrogendosis und Therapiedauer um 5 bis 55 zusätzliche Fälle.
Durch die zusätzliche Gabe eines Gestagens zur Estrogen-Monotherapie wird das Risiko für einen Krebs der Gebärmutterschleimhaut erheblich verringert.
Brustkrebs
Es gibt Hinweise darauf, dass die Anwendung einer kombinierten Estrogen-Gestagen-HRT und möglicherweise auch einer Estrogen-Monotherapie das Risiko für Brustkrebs erhöht. Dies hängt davon ab, wie lange Sie die HRT anwenden. Das zusätzliche Risiko ist nach etwa 3 Jahren Therapiedauer sichtbar. Allerdings sinkt das Risiko innerhalb einiger (spätestens fünf) Jahre nach Therapieende wieder auf das Risiko vor Therapiebeginn ab.
Kontaktieren Sie Ihren Arzt, wenn Sie Veränderungen an Ihren Brüsten feststellen, wie z.
B. Dellen in der Haut, Hautveränderungen im Bereich der Brustwarzen, Knoten, die Sie sehen oder tasten können.
Ihr Arzt wird Ihnen möglicherweise empfehlen, eine Untersuchung durchführen zu lassen, die auch eine Mammographie beinhalteten kann.
Zum Vergleich
Betrachtet man Frauen im Alter zwischen 50 und 65 Jahren, die keine Hormonersatztherapie anwenden, so wird über einen Zeitraum von 5 Jahren im Durchschnitt bei 9 bis 12 von 1.000 Frauen ein Brustkrebs diagnostiziert werden.
Für Frauen im Alter zwischen 50 und 65 Jahren, die über einen Zeitraum von 5 Jahren eine kombinierte Estrogen-Gestagen-Hormonersatztherapie anwenden, wird die Zahl der zusätzlichen Fälle 6 von 1.000 Anwenderinnen betragen.
Betrachtet man Frauen im Alter zwischen 50 und 79 Jahren, die keine Hormonersatztherapie anwenden, so wird über einen Zeitraum von 5 Jahren im Durchschnitt bei 14 von 1.000 Frauen ein Brustkrebs diagnostiziert werden.
Für Frauen im Alter zwischen 50 und 79 Jahren, die über einen Zeitraum von 5 Jahren eine kombinierte Estrogen-Gestagen-Hormonersatztherapie anwenden, wird die Zahl der zusätzlichen Fälle 4 von 1.000 Anwenderinnen betragen.
Falls Sie die Möglichkeit haben, am Programm zur Früherkennung von Brustkrebs (Mammographie-Screening-Programm) teilzunehmen, sollten Sie dieses Angebot nutzen. Informieren Sie die Fachkraft, die die Mammographie durchführt, dass Sie ein Arzneimittel zur Hormonersatzbehandlung anwenden. Arzneimittel, die zur Hormonersatzbehandlung angewendet werden, können das Brustgewebe dichter machen und dadurch das Ergebnis der Mammographie beeinflussen. Wenn die Dichte des Brustgewebes erhöht ist, können möglicherweise nicht alle Veränderungen erkannt werden.
Eierstockkrebs
Eierstockkrebs ist selten - viel seltener als Brustkrebs. Die Anwendung von Estrogen-Monoarzneimitteln oder kombinierten Estrogen-Gestagen-Arzneimitteln zur Hormonersatzbehandlung ist mit einem leicht erhöhten Risiko, Eierstockkrebs zu entwickeln, verbunden.
Das Risiko, Eierstockkrebs zu entwickeln, ändert sich mit dem Alter. Zum Beispiel werden bei Frauen im Alter zwischen 50 und 54 Jahren, die keine Hormonersatzbehandlung anwenden, über einen 5-Jahres-Zeitraum etwa 2 Fälle von Eierstockkrebs pro 2000 Frauen diagnostiziert. Bei Frauen, die eine Hormonersatzbehandlung 5 Jahre lang anwenden, treten etwa 3 Fälle pro 2000 Anwenderinnen auf (d. h. etwa 1 zusätzlicher Fall).
HRT und sonstige Erkrankungszustände
• Wenn Sie an einer Funktionsstörung des Herzens oder der Nieren leiden, ist unter der Anwendung von Fem7 Sequi eine engmaschige Überwachung Ihres Gesundheitszustandes erforderlich.
• Wenn Sie einen sehr hohen Triglyceridspiegel in Ihrem Blut haben (Hypertriglyceridämie), ist unter der Anwendung von Fem7 Sequi eine engmaschige Überwachung Ihres Gesundheitszustandes erforderlich.
Eine HRT verbessert die geistigen Fähigkeiten nicht. Es gibt Hinweise auf ein erhöhtes Risiko einer möglichen Demenz bei Frauen, die nach dem 65. Lebensjahr mit einer HRT beginnen.
Bitte konsultieren Sie Ihren Arzt, wenn bei Ihnen eine der oben genannten Situationen vorliegt oder vorgelegen hat.
Bei Anwendung von Fem7 Sequi mit anderen Arzneimitteln
Die Wirkung von Fem7 Sequi kann bei gleichzeitiger Anwendung anderer Arzneimittel abgeschwächt werden. Dazu zählen insbesondere Arzneimittel, die
• eingesetzt werden bei der Behandlung von Krampfanfällen [Epilepsie] (Carbamazepin, Phenobarbital, Phenytoin)
• eingesetzt werden bei der Behandlung von Tuberkulose oder anderen Infektionskrankheiten (Rifampicin, Rifabutin)
• eingesetzt werden bei der Behandlung der HIV-Infektion [AIDS] (Ritonavir, Nelfinavir, Nevirapin, Efavirenz)
• Johanniskraut (Hypericum perforatum) enthalten
Bitte informieren Sie Ihren Arzt oder Apotheker, wenn Sie andere Arzneimittel einnehmen/anwenden bzw. vor kurzem eingenommen/angewendet haben, auch wenn es sich um nicht verschreibungspflichtige Arzneimittel handelt.
Schwangerschaft und Stillzeit
Sie dürfen Fem7 Sequi nicht anwenden, wenn Sie schwanger sind oder stillen. Wenn Sie während der Behandlung mit Fem7 Sequi schwanger werden, sollte die Behandlung abgebrochen und die Situation mit Ihrem Arzt besprochen werden.
Fragen Sie Ihren Arzt oder Apotheker vor Einnahme/Anwendung jeglicher Arzneimittel um Rat.
Verkehrstüchtigkeit und das Bedienen von Maschinen
Eine Beeinflussung wird nicht erwartet.
3. Wie ist Fem7 Sequi anzuwenden?
Wenden Sie Fem7 Sequi immer genau nach Anweisung des Arztes an. Bitte fragen Sie bei Ihrem Arzt oder Apotheker nach, wenn Sie sich nicht ganz sicher sind.
Sie sollten Fem7 Sequi einmal wöchentlich anwenden, d. h. Sie ersetzen nach jeweils 7 Tagen das verbrauchte Pflaster durch ein neues ohne die Therapie zu unterbrechen: Wenn Sie ein Pflaster entfernen, sollten Sie sofort ein neues auf Ihre Haut aufkleben.
Die Packung enthält 2 Pflastersorten, je nach Anwendungsphase:
• Phase-1-Pflaster (erste und zweite Woche des Anwendungszyklus): Diese enthalten nur einen Wirkstoff (Estradiol).
• Phase-2-Pflaster (dritte und vierte Woche des Anwendungszyklus): Diese enthalten beide Wirkstoffe (Estradiol und Levonorgestrel).
Wenn Sie bisher keine HRT erhalten haben oder von einer kontinuierlich kombinierten HRT wechseln, kann die Behandlung mit Fem7 Sequi an jedem beliebigen Tag begonnen werden. Wenn Sie von einer sequenziellen HRT wechseln, sollte die Behandlung mit Fem7 Sequi am Tag nach Beendigung des vorherigen Behandlungszyklus beginnen.
Häufigkeit der Anwendung:
• Kleben Sie in den ersten zwei Wochen des Behandlungszyklus‘ einmal wöchentlich ein Phase-1-Pflaster auf;
• Entfernen Sie anschließend das letzte Phase-1-Pflaster und kleben stattdessen in den beiden folgenden Wochen einmal wöchentlich ein Phase-2-Pflaster auf.
Sie müssen die Pflaster in der richtigen Reihenfolge anwenden.
Am Ende der Anwendungsphase der Phase-2-Pflaster tritt normalerweise eine der Periodenblutung ähnliche Blutung auf. Diese Blutung ist leicht und dauert im Durchschnitt 4 bis 5 Tage.
Wenn schwere oder außerplanmäßige Blutungen auftreten, konsultieren Sie bitte Ihren Arzt. Art der Anwendung:
Dieses Arzneimittel sollte auf die Haut aufgebracht werden.
Wie wird ein Pflaster aufgebracht?
Jedes Fem7 Sequi Pflaster ist einzeln in einem Siegelbeutel verpackt und muss sofort nach Entnahme aufgeklebt werden.
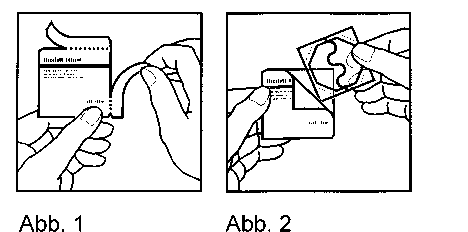
Reißen Sie den Siegelbeutel an den seitlichen Schnitten in Pfeilrichtung ein und entnehmen Sie das Pflaster (Abb. 1 und 2). Ein Pflaster besteht aus 2 Abschnitten: dem Pflaster selbst und der Schutzfolie.
Beginnend am S-förmigen Einschnitt entfernen Sie nun die eine Hälfte der zweigeteilten Schutzfolie. Vermeiden Sie dabei, die klebende Innenseite des Pflasters mit Ihren Fingern zu berühren. Sollten Sie diese versehentlich doch berühren, klebt das Pflaster möglicherweise nicht mehr richtig und Sie könnten die wirksamen Bestandteile verändern. Kleben Sie das Pflaster mit der Handinnenfläche sofort auf eine trockene, saubere Stelle Ihrer Haut (Abb. 3 und 4). Diese sollte nicht gerötet oder eingecremt sein. Die Hautstelle sollte keine größeren Falten aufweisen und nicht durch Kleidung gerieben werden (vermeiden Sie den Taillenbereich und tragen Sie keine allzu enge Kleidung). Das Pflaster kann z. B. auf Gesäß, Oberschenkel oder Bauch aufgeklebt werden.
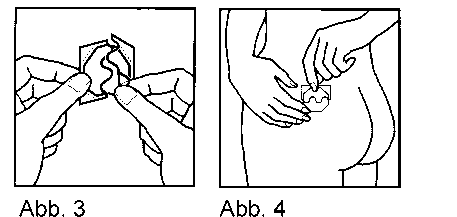
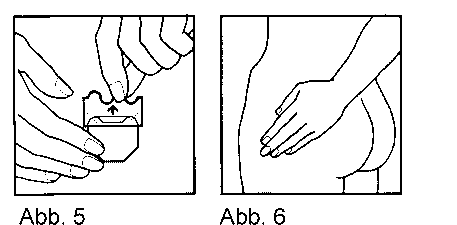
Ziehen Sie dann die zweite Hälfte der Schutzfolie ab und drücken Sie auch diese Hälfte des Pflasters mit der Handinnenfläche fest an die Haut an. Halten Sie den Druck auf das Pflaster mit der Handinnenfläche mindestens 30 Sekunden lang aufrecht, um sicherzustellen, dass das Pflaster richtig klebt. Besonders die Randstellen sollten dabei gut anliegen. Druck und Wärme der Hand sind entscheidend, um eine maximale Haftwirkung des Pflasters zu gewährleisten (Abb. 5 und 6).
Wie wird das Pflaster entfernt?
Um das Fem7 Sequi Pflaster zu entfernen, heben Sie eine Ecke an und ziehen es vorsichtig ab, um Hautirritationen zu vermeiden. Für den Fall, dass Klebstoffreste auf der Haut zurückbleiben, können diese durch vorsichtiges Abrubbeln mit einer Creme oder öligen Körperlotion entfernt werden.
Nach dem Gebrauch enthält das Pflaster noch wirksame Substanzen, jedoch in zu geringen Mengen, um weiterhin wirksam zu sein. Falten Sie das Pflaster in der Mitte (mit der Klebefläche nach innen), bevor Sie es entsorgen.
Vorsichtsmaßnahmen bei der Anwendung
Kleben Sie Fem7 Sequi Pflaster
• nicht auf oder in die Nähe Ihrer Brüste.
• nicht 2x auf die gleiche Stelle: Lassen Sie mindestens eine Woche verstreichen, bevor Sie Fem7 Sequi ein zweites Mal auf die gleiche Hautstelle kleben.
Während der Behandlung:
• Sie sollten das aufgeklebte Pflaster nicht dem direkten Sonnenlicht aussetzen.
• Sie können mit dem aufgeklebten Pflaster duschen oder baden.
• Wenn sich das Pflaster vor Ablauf der sieben Tage löst (z. B. wenn Sie intensive körperliche Anstrengungen unternommen haben oder übermäßig schwitzen oder die Haut durch Kleidung gerieben wird), entfernen Sie das alte Pflaster vollständig und verwenden Sie ein neues Pflaster (der gleichen Phase). Wechseln Sie dieses dann am ursprünglich geplanten Tag.
Dauer der Behandlung
Ihr Arzt wird über die Behandlungsdauer entscheiden.
Bitte kontaktieren Sie Ihren Arzt, wenn Sie die Behandlung beenden wollen.
Wenn Sie eine größere Menge von Fem7 Sequi angewendet haben, als Sie sollten
Eine Überdosierung ist unwahrscheinlich, kann aber folgende Symptome aufweisen:
• Brustschmerzen
• Aufblähungen im Bauch, Blähungen, Übelkeit und Erbrechen
• Reizbarkeit, Ängstlichkeit/Unruhe
• Vaginalblutungen
Eine spezielle Therapie ist nicht notwendig. Die Symptome verschwinden, wenn das Pflaster
entfernt wird.
Wenn Sie die Anwendung von Fem7 Sequi vergessen haben
• Wenn Sie vergessen haben, das Pflaster am vorgesehenen Tag zu wechseln, nehmen Sie den Wechsel bitte unverzüglich vor und folgen dann dem normalen Behandlungsschema. Den Pflasterwechsel nehmen Sie dabei am ursprünglich dafür vorgesehenen Tag vor.
• Verwenden Sie nicht zwei Pflaster gleichzeitig, wenn Sie einmal eins vergessen haben.
• Wenn Sie Fem7 Sequi über mehrere aufeinander folgende Tage nicht angewendet haben, könnte eine Entzugsblutung eintreten. Wenn Sie nicht sicher sind, fragen Sie Ihren Arzt.
Wenn Sie die Behandlung mit Fem7 Sequi abbrechen
Eine Unterbrechung oder Beendigung der Behandlung kann zum Wiederauftreten der
Wechseljahresbeschwerden, die aus einem Mangel an Estrogen resultieren, führen. Sollten Sie
weitere Fragen haben, sprechen Sie mit Ihrem Arzt.
4. Welche Nebenwirkungen sind möglich?
Wie alle Arzneimittel kann Fem7 Sequi Nebenwirkungen haben, die aber nicht bei jedem auftreten müssen.
Die folgenden Nebenwirkungen treten am häufigsten auf (bei mehr als 1 von 10 Behandelten):
• Hautreaktionen (Juckreiz, Hautirritationen, Rötungen) an der Stelle, an der das Pflaster angebracht wird. Diese Erscheinungen sind nicht schwerwiegend und verschwinden normalerweise zwei oder drei Tage nach Entfernen des Pflasters. Sollten die Symptome anhalten, kleben Sie das Pflaster an eine andere Stelle.
Die folgenden Nebenwirkungen treten häufig auf (bei 1 bis 10 Behandelten von 100):
• Spannungsgefühl oder Schmerzen in der Brust
• Kopfschmerzen
• Übelkeit, Erbrechen
• irreguläre Blutungen, Schmierblutungen
• Zu- oder Abnahme der Libido
Die folgenden Nebenwirkungen treten gelegentlich auf (bei 1 bis 10 Behandelten von 1000):
• gutartige Brusttumore
• schmerzhafte Regelblutung
• übermäßige Verdickung der Gebärmutterschleimhaut (Endometriumhyperplasie)
• hoher Blutdruck
• Aufblähungen oder Schmerzen im Bauch
• Müdigkeit
• Gewichtszunahme oder -abnahme
• Migräne
• Schwindel
• Wadenkrämpfe
• Schwellungen (Wassereinlagerungen, Ödeme)
Die folgenden Nebenwirkungen können auftreten, sind aber selten (bei 1 bis 10 Behandelten von 10.000):
• Gelbfärbung der Haut und des Augenweißes (Gelbsucht)
• gutartige Tumore in der Gebärmutter (Gebärmutterfibrom)
• Gallensteine
• Depression
Die folgenden Nebenwirkungen können ebenfalls auftreten:
• Brustkrebs, Krebs der Gebärmutterschleimhaut (Endometriumkarzinom)
• Bildung eines Blutgerinnsels in der Vene eines Beins (Thrombose) oder der Lunge (Lungenembolie)
• Bildung eines Blutgerinnsels im Gehirn (Schlaganfall) oder im Herzen (Herzinfarkt);
• Erkrankungen der Gallenblase
• Hirnleistungsstörung (Demenz)
• Erkrankungen der Haut oder des Unterhautgewebes so wie:
• Ausbildung von bräunlichen Flecken im Gesicht nach Sonnenlichteinstrahlung, auch bekannt als „Schwangerschaftsmaske“ (Chloasma)
• Hautkrankheit mit roten Flecken und flüssigkeitsgefüllten Blasen (Erythema multiforme)
• Hautkrankheit mit der Bildung von Knoten unter der Haut, die rot und schmerzhaft sind (Erythema nodosum)
• kleinere Hauteinblutungen (Purpura Schönlein-Henoch)
Informieren Sie bitte Ihren Arzt oder Apotheker, wenn eine der aufgeführten Nebenwirkungen Sie erheblich beeinträchtigt oder Sie Nebenwirkungen bemerken, die nicht in dieser Gebrauchsinformation angegeben sind.
Meldung von Nebenwirkungen
Wenn Sie Nebenwirkungen bemerken, wenden Sie sich an Ihren Arzt oder Apotheker oder das medizinische Fachpersonal. Dies gilt auch für Nebenwirkungen, die nicht in dieser Packungsbeilage angegeben sind. Sie können Nebenwirkungen auch direkt dem
Bundesinstitut für Arzneimittel und Medizinprodukte
Abt. Pharmakovigilanz
Kurt-Georg-Kiesinger Allee 3
D-53175 Bonn
anzeigen.
Indem Sie Nebenwirkungen melden, können Sie dazu beitragen, dass mehr Informationen über die Sicherheit dieses Arzneimittels zur Verfügung gestellt werden.
5. Wie ist Fem7 Sequi aufzubewahren?
Arzneimittel für Kinder unzugänglich aufbewahren.
Sie dürfen das Arzneimittel nach dem auf dem Umkarton angegebenen Verfalldatum nicht mehr verwenden.
Das Verfalldatum bezieht sich auf den letzten Tag des Monats.
Nicht über 30° C lagern.
Verwenden Sie Fem7 Sequi nicht, wenn Sie sichtbare Verfallserscheinungen des Pflasters feststellen.
Das Arzneimittel darf nicht im Abwasser oder Haushaltsabfall entsorgt werden. Fragen Sie Ihren Apotheker wie das Arzneimittel zu entsorgen ist, wenn Sie es nicht mehr benötigen. Diese Maßnahme hilft die Umwelt zu schützen.
6. Weitere Informationen Was Fem7 Sequi enthält:
Die Wirkstoffe sind:
Phase 1:
Estradiol-Hemihydrat (1,50 mg). Die Größe des Pflasters ist 15 cm2 und die Wirkstofffreisetzung beträgt 50 Mikrogramm Estradiol in 24 Stunden.
Phase 2:
Estradiol-Hemihydrat (1,50 mg) und Levonorgestrel (1,50 mg). Die Größe des Pflasters ist 15 cm2 und die Wirkstofffreisetzung beträgt 50 Mikrogramm Estradiol und 10 Mikrogramm Levonorgestrel in 24 Stunden.
Die sonstigen Bestandteile sind:
Trägerfolie: Transparente Poly(ethylenterephthalat) (PET) Folie Klebematrix: Poly(isopren-co-styrol)
Hydrierter Kolophoniumglycerolesther
Schutzfolie: transparente siliconisierte Poly(ethylenterephthalat) (PET) Folie
Wie Fem7 Sequi aussieht und Inhalt der Packung
Achteckiges, transparentes, flexibles Pflaster mit abgerundeten Ecken, befestigt an einer etwas größeren, abziehbaren Schutzfolie.
Fem7 Sequi ist in Packungen mit
• 4 Pflastern (2x Phase 1, 2x Phase 2)
• 12 Pflastern (6x Phase 1, 6x Phase 2)
jedes einzeln verpackt, erhältlich.
Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht.
Pharmazeutischer Unternehmer:
Mylan Healthcare GmbH Freundallee 9A 30173 Hannover
E-Mail: mylan.healthcare@mylan.com Hersteller:
LTS - Lohmann Therapie-Systeme AG Lohmannstraße 2 D-56626 Andernach
oder
Teva Pharmaceutical Europe B.V. Swensweg 5 2031 GA Haarlem Niederlande
Dieses Arzneimittel ist in den Mitgliedstaaten des Europäischen Wirtschaftsraumes (EWR) unter den folgenden Bezeichnungen zugelassen:
Frankreich
Vereinigtes Königreich
Österreich
Belgien
Portugal
Italien
FEMSEPTCOMBI FEMSEVEN SEQUI FEMSEVEN COMBI FEMINOVA PLUS FEMSETE COMBI COMBISEVEN
Diese Gebrauchsinformation wurde zuletzt überarbeitet: 07/2016