Fentanyl-Hexal Sublingual 67 Mikrogramm Sublingualtabletten
FACHINFORMATION
1. BEZEICHNUNG DER ARZNEIMITTEL
Fentanyl-HEXAL sublingual 67 Mikrogramm Sublingualtabletten Fentanyl-HEXAL sublingual 133 Mikrogramm Sublingualtabletten Fentanyl-HEXAL sublingual 267 Mikrogramm Sublingualtabletten Fentanyl-HEXAL sublingual 400 Mikrogramm Sublingualtabletten Fentanyl-HEXAL sublingual 533 Mikrogramm Sublingualtabletten Fentanyl-HEXAL sublingual 800 Mikrogramm Sublingualtabletten
2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Fentanyl-HEXAL sublingual 67 Mikrogramm Sublingualtabletten:
Jede Tablette enthält 110 Mikrogramm Fentanylcitrat, entsprechend 67 Mikrogramm Fentanyl.
Fentanyl-HEXAL sublingual 133 Mikrogramm Sublingualtabletten:
Jede Tablette enthält 210 Mikrogramm Fentanylcitrat, entsprechend 133 Mikrogramm Fentanyl.
Fentanyl-HEXAL sublingual 267 Mikrogramm Sublingualtabletten:
Jede Tablette enthält 420 Mikrogramm Fentanylcitrat, entsprechend 267 Mikrogramm Fentanyl.
Fentanyl-HEXAL sublingual 400 Mikrogramm Sublingualtabletten:
Jede Tablette enthält 630 Mikrogramm Fentanylcitrat, entsprechend 400 Mikrogramm Fentanyl.
Fentanyl-HEXAL sublingual 533 Mikrogramm Sublingualtabletten:
Jede Tablette enthält 840 Mikrogramm Fentanylcitrat, entsprechend 533 Mikrogramm Fentanyl.
Fentanyl-HEXAL sublingual 800 Mikrogramm Sublingualtabletten:
Jede Tablette enthält 1260 Mikrogramm Fentanylcitrat, entsprechend 800 Mikrogramm Fentanyl.
Sonstiger Bestandteil mit bekannter Wirkung:
Jede Tablette enthält 0,651 mg Natrium.
Vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt 6.1.
Sublingualtablette
Fentanyl-HEXAL sublingual 67 Mikrogramm Sublingualtabletten:
Weiße, dreieckige, konvexe Tablette mit einer Höhe von 5,6 mm und dem Aufdruck „0".
Fentanyl-HEXAL sublingual 133 Mikrogramm Sublingualtabletten:
Weiße, dreieckige, konvexe Tablette mit einer Höhe von 5,6 mm und dem Aufdruck „1".
Fentanyl-HEXAL sublingual 267 Mikrogramm Sublingualtabletten:
Weiße, dreieckige, konvexe Tablette mit einer Höhe von 5,6 mm und dem Aufdruck „2".
Fentanyl-HEXAL sublingual 400 Mikrogramm Sublingualtabletten:
Weiße, dreieckige, konvexe Tablette mit einer Höhe von 5,6 mm und dem Aufdruck „4".
Fentanyl-HEXAL sublingual 533 Mikrogramm Sublingualtabletten:
Weiße, dreieckige, konvexe Tablette mit einer Höhe von 5,6 mm und dem Aufdruck „5".
Fentanyl-HEXAL sublingual 800 Mikrogramm Sublingualtabletten:
Weiße, dreieckige, konvexe Tablette mit einer Höhe von 5,6 mm und dem Aufdruck „8".
4. KLINISCHE ANGABEN
4.1 Anwendungsgebiete
Fentanyl-HEXAL sublingual ist angezeigt für die Behandlung von Durchbruchschmerzen bei erwachsenen Krebspatienten, die bereits eine OpioidErhaltungstherapie gegen ihre chronischen Tumorschmerzen erhalten.
Bei Durchbruchschmerzen handelt es sich um eine vorübergehende Verschlimmerung der Schmerzen, die trotz anderweitig kontrollierter Dauerschmerzen auftritt.
Zu den Patienten, die eine Opioid-Erhaltungstherapie erhalten, werden diejenigen gezählt, die mindestens 60 mg orales Morphin täglich, mindestens 25 Mikrogramm transdermales Fentanyl pro Stunde, mindestens 30 mg Oxycodon täglich, mindestens 8 mg orales Hydromorphon täglich oder eine analgetisch gleichwertige Dosis eines anderen Opioids über eine Woche oder länger erhalten.
4.2 Dosierung und Art der Anwendung
Dosierung
Die Behandlung sollte von einem Arzt begonnen und überwacht werden, der Erfahrung mit einer Opioid-Therapie bei Krebspatienten hat. Der Arzt sollte das Missbrauchspotenzial von Fentanyl bedenken. Die Patienten sollten angewiesen werden, nicht gleichzeitig zwei verschiedene Formulierungen von Fentanyl für die Behandlung von Durchbruchschmerzen anzuwenden. Andere Fentanyl-Präparate zur Behandlung von Durchbruchschmerzen sollten abgesetzt werden, wenn die Behandlung auf Fentanyl-HEXAL sublingual umgestellt wird. Die Anzahl verschiedener Wirkstärken, die einem Patienten gleichzeitig zur Verfügung stehen, sollte so gering wie möglich sein, um eine Verwechselung und mögliche Überdosierung zu verhindern.
Art der Anwendung
Fentanyl-HEXAL sublingual sollte an der tiefsten Stelle direkt unter die Zunge gelegt werden.
Fentanyl-HEXAL sublingual sollte nicht geschluckt werden. Die Tablette sollte sich vollständig unter der Zunge auflösen, ohne gekaut oder gelutscht zu werden. Die Patienten sollten angewiesen werden, nichts zu essen oder zu trinken, bevor sich die Sublingualtablette vollständig aufgelöst hat.
Wenn nach 30 Minuten noch Bruchstücke der Fentanyl-HEXAL sublingualTablette vorhanden sind, können diese geschluckt werden.
Patienten mit Mundtrockenheit können die Mundschleimhaut vor der Anwendung von Fentanyl-HEXAL sublingual mit Wasser befeuchten.
Die Tablette sollte nach der Entnahme aus der Blisterpackung nicht weiter aufbewahrt werden, da ansonsten die Unversehrtheit der Tablette nicht mehr garantiert werden kann und das Risiko einer unbeabsichtigten Exposition besteht.
Dosistitration
Bevor die Patienten auf Fentanyl-HEXAL sublingual eingestellt werden, wird davon ausgegangen, dass die vorbestehenden chronischen Schmerzen durch eine Opioid-Therapie unter Kontrolle gebracht sind und dass in der Regel höchstens vier Episoden mit Durchbruchschmerzen pro Tag auftreten.
Das Ziel der Dosistitration ist die Bestimmung einer optimalen Erhaltungsdosis für die laufende Behandlung von Durchbruchschmerz-Episoden. Diese optimale Dosis sollte eine adäquate Schmerzlinderung bei akzeptablen Nebenwirkungen ermöglichen.
Die optimale Dosierung von Fentanyl-HEXAL sublingual wird individuell durch eine aufsteigende Titration ermittelt. Für die Titrationsphase sind mehrere Stärken verfügbar. Die Anfangsdosis von Fentanyl-HEXAL sublingual sollte 133 Mikrogramm betragen und kann bei Bedarf mit den verfügbaren Wirkstärken auftitriert werden.
Die Patienten sollten sorgfältig überwacht werden, bis eine optimale Dosis erreicht ist.
Die Umstellung von anderen Arzneimitteln mit dem Wirkstoff Fentanyl auf Fentanyl-HEXAL sublingual darf aufgrund der unterschiedlichen Resorptionsprofile nicht im Verhältnis 1:1 erfolgen. Bei einer Umstellung von einem anderen Fentanyl-haltigen Arzneimittel muss eine neue Dosistitration mit Fentanyl-HEXAL sublingual durchgeführt werden.
Zur Titration wird das nachfolgende Dosierungsschema empfohlen. Allerdings muss der Arzt in allen Fällen die klinische Situation des Patienten, das Alter und vorhandene Begleiterkrankungen berücksichtigen.
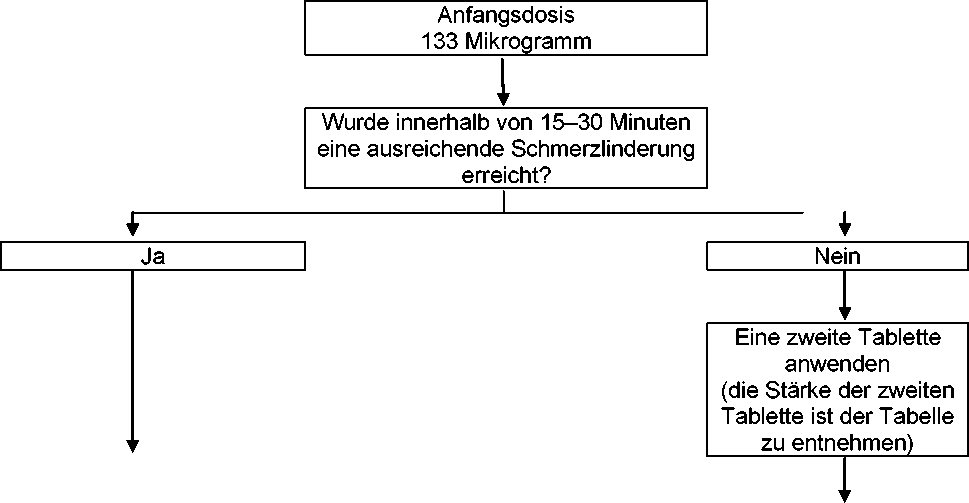
Bei allen Patienten muss die Therapie mit einer einzigen 133 Mikrogramm Sublingualtablette begonnen werden. Wird innerhalb von 15-30 Minuten nach der Anwendung einer einzelnen Tablette keine adäquate Analgesie erreicht, kann eine zusätzliche (zweite) 133 Mikrogramm Tablette angewendet werden. Wenn für die Behandlung einer Durchbruchschmerz-Episode mehr als eine Dosiereinheit notwendig ist, sollte eine Erhöhung der Dosis auf die nächst höhere verfügbare Tablettenstärke in Betracht gezogen werden (siehe Abbildung unten). Eine weitere Erhöhung der Dosis sollte schrittweise erfolgen, bis eine adäquate Analgesie erreicht wird. Die Wirkstärke der zusätzlichen (zweiten) Sublingualtablette sollte bei Dosierungen von 533 Mikrogramm von 133 auf 267 Mikrogramm erhöht werden. Dieses Schema ist nachfolgend dargestellt.
Während dieser Titrationsphase sollten bei jeder einzelnen Episode von Durchbruchschmerzen nicht mehr als zwei (2) Tabletten angewendet werden.
Titration von Fentanyl-HEXAL sublingual
|
Diese Dosis für |
Bei der nächsten | |
|
nachfolgende |
Durchbruchschmerz- | |
|
Durchbruchschmerz- |
Episode Dosis der | |
|
Episoden |
ersten | |
|
anwenden |
Tablette auf die nächst höhere Stärke erhöhen |
|
Wirkstärke (Mikrogramm) der ersten T ablette bei einer Durchbruchschmerz-Episode |
Wirkstärke (Mikrogramm) der zusätzlichen (zweiten) Sublingualtablette, die bei Bedarf 15-30 Minuten nach der ersten Tablette angewendet wird |
|
133 |
133 |
|
267 |
133 |
|
400 |
133 |
|
533 |
267 |
|
800 |
- |
Falls mit einer höheren Wirkstärke eine ausreichende Analgesie erreicht wird, aber die auftretenden Nebenwirkungen nicht akzeptabel sind, kann eine dazwischen liegende Wirkstärke gegeben werden (gegebenenfalls unter Verwendung der 67 Mikrogramm oder 133 Mikrogramm Tablette).
Dosierungen von mehr als 800 Mikrogramm wurden in klinischen Studien nicht untersucht.
Um das Risiko Opioid-bedingter Nebenwirkungen zu minimieren, und um die angemessene Dosis zu bestimmen, ist eine engmaschige ärztliche Kontrolle der Patienten während der Titrationsphase unbedingt erforderlich.
Erhaltungstherapie
Sobald eine geeignete Dosis gefunden wurde, die auch aus mehr als einer Tablette bestehen kann, sollten die Patienten auf dieser Dosis gehalten werden, und die Anwendung sollte auf eine Höchstmenge von vier Dosen Fentanyl-HEXAL sublingual pro Tag beschränkt werden.
Erneute Dosisanpassung
Falls sich das Ansprechen des Patienten auf die eingestellte Fentanyl-Dosis hinsichtlich Analgesie oder Nebenwirkungen deutlich verändert, muss die Dosis möglicherweise angepasst werden, damit eine optimale Dosierung weiterhin gewährleistet bleibt.
Wenn durchgängig mehr als vier Durchbruchschmerz-Episoden pro Tag auftreten, sollte die Dosis des zur Behandlung der chronischen Schmerzen verwendeten langwirksamen Opioids überprüft werden. Wird das langwirksame Opioid oder dessen Dosierung verändert, sollte auch die angewendete Fentanyl-HEXAL sublingual-Dosis überprüft und gegebenenfalls erneut titriert werden, um sicherzustellen, dass der Patient die optimale Dosis erhält.
Es ist zwingend erforderlich, dass jede erneute Dosisanpassung eines Analgetikums unter ärztlicher Aufsicht erfolgt.
Beendigung der Therapie
Fentanyl-HEXAL sublingual sollte sofort abgesetzt werden, wenn es nicht mehr benötigt wird.
Anwendung bei älteren Patienten
Die Dosistitration muss bei älteren Patienten mit besonderer Sorgfalt erfolgen, und die Patienten sollten insbesondere auf Anzeichen einer Fentanyl-Toxizität hin beobachtet werden.
Anwendung bei Patienten mit eingeschränkter Nieren- und/oder Leberfunktion Patienten mit eingeschränkter Nieren- und/oder Leberfunktion sollten während der Titrationsphase sorgfältig auf Anzeichen einer Fentanyl-Toxizität hin beobachtet werden (siehe Abschnitt 4.4).
Anwendung bei Kindern und Jugendlichen
Die Anwendung von Fentanyl-HEXAL sublingual ist bei Kindern und Jugendlichen unter 18 Jahren nicht indiziert, da keine Daten zur Sicherheit und Wirksamkeit vorliegen.
4.3 Gegenanzeigen
• Überempfindlichkeit gegen den Wirkstoff oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile
• Patienten ohne Opioid-Basistherapie, da ein erhöhtes Risiko für eine Atemdepression besteht
• Behandlung akuter Schmerzen, welche keine Durchbruchschmerzen darstellen
• gleichzeitige Anwendung von Monoaminoxidase-(MAO-)Hemmern oder innerhalb von 2 Wochen nach Beendigung der Anwendung von MAOHemmern
• schwere Atemdepression oder schwere obstruktive Lungenerkrankungen
4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung
Patienten und ihre Betreuer müssen darauf hingewiesen werden, dass Fentanyl-HEXAL sublingual einen Wirkstoff in einer Menge enthält, die für Kinder tödlich sein kann, und dass die Tabletten daher für Kinder unzugänglich aufbewahrt werden müssen.
Um das Risiko Opioid-bedingter Nebenwirkungen zu minimieren und um die wirksame Dosis zu bestimmen, ist eine engmaschige ärztliche Kontrolle der Patienten während der Titrationsphase unbedingt erforderlich.
Es ist wichtig, dass die Therapie mit langwirksamen Opioiden zur Behandlung der Dauerschmerzen stabil eingestellt ist, bevor mit der Therapie mit Fentanyl-HEXAL sublingual begonnen wird, und dass der Patient die Therapie mit langwirksamen Opioiden weiterführt, während er Fentanyl-HEXAL sublingual einnimmt.
Wie bei allen Opioiden besteht auch bei Anwendung von von Fentanyl-HEXAL sublingual ein Risiko für eine klinisch relevante Atemdepression. Besondere
Vorsicht ist bei der Titration von Fentanyl-HEXAL sublingual bei Patienten mit nicht-schwerwiegender chronisch obstruktiver Lungenerkrankung oder anderen Erkrankungen geboten, die für eine Atemdepression prädisponieren, da es hier sogar bei den üblichen therapeutischen Dosen von Fentanyl-HEXAL sublingual zur Verringerung des Atemantriebes bis hin zur respiratorischen Insuffizienz kommen kann.
Fentanyl-HEXAL sublingual sollte nur mit äußerster Vorsicht bei Patienten zur Anwendung kommen, die besonders anfällig für intrakranielle Wirkungen einer CO2-Retention sein können, wie z.B. Patienten mit Anzeichen eines erhöhten intrakraniellen Drucks oder einer Bewusstseinseinschränkung. Opioide können den klinischen Verlauf bei Patienten mit Kopfverletzungen verschleiern und sollten nur dann zum Einsatz kommen, wenn dies klinisch gerechtfertigt ist.
Fentanyl kann eine Bradykardie hervorrufen. Bei der Anwendung von Fentanyl bei Patienten mit früherer oder vorbestehender Bradyarrhythmie ist Vorsicht geboten.
Ebenfalls mit Vorsicht sollte Fentanyl-HEXAL sublingual bei Patienten mit Leberoder Nierenfunktionseinschränkung angewendet werden. Der Einfluss einer eingeschränkten Leber- und Nierenfunktion auf die Pharmakokinetik des Arzneimittels wurde nicht untersucht. Es konnte jedoch gezeigt werden, dass die Clearance von Fentanyl nach intravenöser Anwendung bei Vorliegen einer Leberund Nierenfunktionseinschränkung aufgrund der Veränderungen von metabolischer Clearance und Plasmaproteinen anders verläuft. Nach der Anwendung von Fentanyl-HEXAL sublingual kann eine eingeschränkte Leberund Nierenfunktion sowohl die Bioverfügbarkeit des eingenommenen Fentanyls erhöhen als auch dessen systemische Clearance herabsetzen, was verstärkte und verlängerte Opioid-Effekte zur Folge haben kann. Daher ist während des Titrationsvorgangs bei Patienten mit mittelschwerer oder schwerer Leber- oder Nierenfunktionseinschränkung besondere Sorgfalt geboten.
Besondere Aufmerksamkeit erfordern Patienten mit Hypovolämie und Hypotonie.
Fentanyl-HEXAL sublingual wurde nicht bei Patienten mit Wunden im Mund oder Mukositis untersucht. Bei diesen Patienten kann das Risiko erhöhter systemischer Wirkstoffspiegel bestehen. Daher ist hier in der Titrationsphase besondere Vorsicht geboten.
Serotonin-Syndrom
Vorsicht ist geboten, wenn Fentanyl-HEXAL sublingual gleichzeitig mit Arzneimitteln verabreicht wird, die das serotonerge Neurotransmittersystem beeinflussen.
Bei gleichzeitiger Verwendung von serotonergen Arzneimitteln wie selektiven Serotonin-Wiederaufnahmehemmern (SSRIs) und Serotonin-Noradrenalin-Wiederaufnahmehemmern (SNRIs) sowie von Arzneimitteln, die den Serotoninstoffwechsel beeinträchtigen (einschließlich Monoaminooxidase-[MAO-]Hemmer), kann sich ein möglicherweise lebensbedrohliches Serotonin-Syndrom ausbilden. Dieses kann auch innerhalb der empfohlenen Dosierung auftreten.
Das Serotonin-Syndrom kann Veränderungen der psychischen Verfassung (z. B. Agitiertheit, Halluzinationen, Koma), autonome Instabilität (z. B. Tachykardie, labiler Blutdruck, Hyperthermie), neuromuskuläre Auffälligkeiten (z. B.
Hyperreflexie, Koordinationsmangel, Rigidität) und/oder gastrointestinale Symptome (z. B. Übelkeit, Erbrechen, Diarrhö) einschließen.
Bei Verdacht auf ein Serotonin-Syndrom ist die Behandlung mit Fentanyl-HEXAL sublingual abzubrechen.
Unter der wiederholten Anwendung von Opioiden wie Fentanyl kann sich eine Gewöhnung und physische und/oder psychische Abhängigkeit entwickeln. Allerdings ist eine iatrogen hervorgerufene Abhängigkeit nach therapeutischer Anwendung von Opioiden selten.
Dieses Arzneimittel enthält 0,651 mg Natrium / Tablette. Dies ist zu berücksichtigen bei Personen unter Natrium kontrollierter (natriumarmer/-kochsalzarmer) Diät.
Auswirkungen bei Fehlgebrauch zu Dopingzwecken
Die Anwendung von Fentanyl-HEXAL sublingual kann bei Dopingkontrollen zu positiven Ergebnissen führen. Eine missbräuchliche Anwendung von Fentanyl-HEXAL sublingual als Dopingmittel kann zu einer Gefährdung der Gesundheit führen.
4.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen
Fentanyl wird vorwiegend über das humane Cytochrom-P450 3A4 IsoenzymSystem (CYP3A4) metabolisiert. Es können also Wechselwirkungen auftreten, wenn Fentanyl-HEXAL sublingual zusammen mit Substanzen angewendet wird, die die CYP3A4-Aktivität beeinflussen. Die gleichzeitige Anwendung mit Substanzen, die eine CYP3A4-Aktivität induzieren, kann die Wirksamkeit von Fentanyl-HEXAL sublingual herabsetzen. Die gleichzeitige Anwendung von Fentanyl-HEXAL sublingual mit starken CYP3A4-Inhibitoren (z.B. Ritonavir, Ketoconazol, Itraconazol, Troleandomycin, Clarithromycin und Nelfinavir) oder mittelstarken CYP3A4-Inhibitoren (z.B. Amprenavir, Aprepitant, Diltiazem, Erythromycin, Fluconazol, Fosamprenavir, Grapefruitsaft und Verapamil) kann erhöhte Plasmakonzentrationen von Fentanyl zur Folge haben, was möglicherweise zu schweren Arzneimittelnebenwirkungen einschließlich einer tödlichen Atemdepression führen kann. Patienten, die Fentanyl-HEXAL sublingual zusammen mit mittelstarken oder starken CYP3A4-Inhibitoren erhalten, sollten über längere Zeit sorgfältig überwacht werden. Bei Dosiserhöhungen ist Vorsicht geboten.
Die gleichzeitige Anwendung von anderen zentral-dämpfenden Substanzen, wie anderen Opioiden, Sedativa oder Hypnotika, Allgemeinanästhetika, Phenothiazinen, Tranquilizern, Muskelrelaxantien, sedierenden Antihistaminika und Alkohol kann additive dämpfende Effekte ergeben.
Serotonerge Arzneimittel
Die gleichzeitige Verabreichung von Fentanyl zusammen mit einem serotonergen Arzneimittel wie einem selektiven Serotonin-Wiederaufnahmehemmer (SSRI), einem Serotonin-Noradrenalin-Wiederaufnahmehemmer (SNRI) oder einem Monoaminooxidase-(MAO-)Hemmer kann das Risiko für ein möglicherweise lebensbedrohliches Serotonin-Syndrom erhöhen.
Die Anwendung von Fentanyl-HEXAL sublingual ist bei Patienten, die in den letzten 14 Tagen Monoaminoxidase-(MAO-)Hemmer erhalten haben, kontraindiziert, da für Opioid-Analgetika eine starke und unvorhersagbare Potenzierung der Wirkstärke durch MAO-Hemmer berichtet wurde.
Die gleichzeitige Anwendung von partiellen Opioid-Agonisten/Antagonisten (z.B. Buprenorphin, Nalbuphin, Pentazocin) wird nicht empfohlen. Diese weisen eine hohe Affinität zu Opioid-Rezeptoren mit relativ niedriger intrinsischer Aktivität auf. Sie antagonisieren daher teilweise die analgetische Wirkung von Fentanyl und können Entzugssymptome bei Opioid-abhängigen Patienten auslösen.
4.6 Fertilität, Schwangerschaft und Stillzeit
Schwangerschaft
Es liegen keine ausreichenden Daten für die Anwendung von Fentanyl bei Schwangeren vor. Tierexperimentelle Studien haben eine Reproduktionstoxizität
gezeigt (siehe Abschnitt 5.3). Das potenzielle Risiko für den Menschen ist nicht bekannt. Fentanyl-HEXAL sublingual darf während der Schwangerschaft nicht angewendet werden, es sei denn, es ist unbedingt erforderlich.
Nach einer Langzeitanwendung kann Fentanyl beim Neugeborenen eine Entzugssymptomatik hervorrufen.
Es wird davon abgeraten, Fentanyl während der Wehen und der Geburt (einschließlich Kaiserschnitt) anzuwenden, da Fentanyl plazentagängig ist und beim Fetus oder Neugeborenen eine Atemdepression hervorrufen kann. Wenn Fentanyl-HEXAL sublingual dennoch angewendet wird, sollte ein Antidot für das Kind unmittelbar bereitgehalten werden.
Stillzeit
Fentanyl geht in die Muttermilch über und kann beim gestillten Kind eine Sedierung und Atemdepression hervorrufen. Fentanyl soll von stillenden Frauen nicht angewendet werden. Mit dem Stillen soll erst wieder begonnen werden, wenn die letzte Anwendung von Fentanyl mindestens 48 Stunden zurückliegt.
4.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen
Es wurden keine Studien zu den Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen durchgeführt.
Allerdings beeinträchtigen Opioid-Analgetika die geistige und/oder körperliche Fähigkeit zur Ausübung potenziell gefährlicher Aufgaben (wie z.B. das Führen eines Fahrzeugs oder das Bedienen von Maschinen). Die Patienten sollten angewiesen werden, kein Fahrzeug zu führen und keine Maschinen zu bedienen, wenn sie unter der Anwendung von Fentanyl-HEXAL sublingual Somnolenz, Schwindel oder Sehstörungen bemerken und das Führen von Fahrzeugen und das Bedienen von Maschinen zu unterlassen, solange nicht bekannt ist, wie sie auf die Behandlung mit Fentanyl-HEXAL sublingual reagieren.
4.8 Nebenwirkungen
Bei der Anwendung von Fentanyl-HEXAL sublingual sind die für Opioide typischen Nebenwirkungen zu erwarten. Häufig verschwinden diese bei fortgesetzter Anwendung des Präparats oder verlieren an Intensität, während der Patient auf die am besten geeignete Dosis eingestellt wird. Zu den schwerwiegendsten Nebenwirkungen zählen Atemdepression (die potenziell zu einer Apnoe oder einem Atemstillstand führen kann), Kreislaufdepression, Hypotonie und Schock. Alle Patienten müssen sorgfältig auf diese Nebenwirkungen hin überwacht werden.
Zu den sehr häufig gemeldeten Nebenwirkungen zählen Übelkeit, Erbrechen, Obstipation, Kopfschmerzen, Somnolenz/Fatigue und Schwindel.
Die folgenden Nebenwirkungen wurden bei der Therapie mit Fentanyl-HEXAL sublingual und/oder anderen Fentanyl-haltigen Präparaten während klinischer Studien und nach der Markteinführung beobachtet. In der Praxis wurden bei der Behandlung von Durchbruchschmerzen alle Patienten gleichzeitig mit Opioiden gegen ihre Dauerschmerzen behandelt. Daher ist es nicht möglich, die alleinigen Wirkungen von Fentanyl eindeutig abzugrenzen.
Die in klinischen Studien mit Fentanyl-HEXAL sublingual berichteten Nebenwirkungen entsprachen den Erwartungen und waren typisch für andere oromukosale Fentanyl-Formulierungen.
Die Nebenwirkungen sind im Folgenden in der bevorzugten Bezeichnung gemäß MedDRA-Konvention nach Systemorganklassen und Häufigkeit aufgelistet. Die Häufigkeiten sind definiert als sehr häufig (>1/10), häufig (>1/100, <1/10), gelegentlich (>1/1.000, <1/100), selten (>1/10.000, <1/1.000), sehr selten (<1/10.000), nicht bekannt (Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar).
|
MedDRA- Systemorgan klasse |
Sehr häufig |
Häufig |
Gelegentlich |
Nicht bekannt |
|
Stoffwechsel- und Ernährungs störungen |
Anorexie | |||
|
Psychiatrische Erkrankungen |
Verwirrtheit, Angst, Halluzinationen, anormales Denken |
abnorme Träume, Depersonalisation, Depression, emotionale Labilität, Euphorie | ||
|
Erkrankungen des Nervensystems |
Somnolenz, Sedierung, Schwindel |
Bewusstseinsverlust, Vertigo, Kopfschmerzen, Myoklonus, Geschmacksstörungen |
Koma, Konvulsion, Parästhesie (einschließlich Hyperästhesie/ periorale Parästhesie), anormaler Gang/Koordinations- mangel | |
|
Augen erkrankungen |
anormales Sehen (Verschwommenoder Doppeltsehen) | |||
|
Gefäß erkrankungen |
Vasodilatation |
Flush und Hitzewallun gen | ||
|
Erkrankungen der Atemwege, des Brustraums und Mediastinums |
Dyspnoe |
Atemdepres sion | ||
|
Erkrankungen des Gastrointestinaltrakts |
Übelkeit, Obstipation |
Erbrechen, Mundtrockenheit, Bauchschmerzen, Dyspepsie |
Ileus, Flatulenz, vergrößertes Abdomen |
Zahnfleisch schwund, Diarrhö |
|
Erkrankungen der Haut und des Unterhautzell gewebes |
Pruritus, Schwitzen |
Ausschlag | ||
|
Erkrankungen der Nieren und |
Harnretention |
|
Harnwege |
|
Allgemeine Erkrankungen und Beschwerden am Verabreichungsort |
Asthenie |
Unwohlsein |
Fatigue, periphere Ödeme | |
|
Verletzung, Vergiftung und durch Eingriffe bedingte Komplikationen |
versehentliche Verletzungen |
Stürze |
Nach Beendigung der Behandlung können mögliche Entzugssymptome auftreten, beispielsweise Angst, Tremor, Schwitzen, Reizbarkeit, Übelkeit und Erbrechen, Diarrhö.
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des NutzenRisiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung dem Bundesinstitut für Arzneimittel und Medizinprodukte, Abt. Pharmakovigilanz, Kurt-Georg-Kiesinger-Allee 3, D-53175 Bonn, Website: www.bfarm.de anzuzeigen.
4.9 Überdosierung
Es ist zu erwarten, dass die Symptome einer Fentanyl-Überdosierung mit denen von intravenös angewendetem Fentanyl und anderen Opioiden vergleichbar sind und eine Verstärkung der pharmakologischen Wirkungen darstellen. Die schwerwiegendsten unerwünschten Wirkungen sind dabei ein veränderter Bewusstseinszustand, Bewusstlosigkeit, Koma, Herz-Kreislauf-Versagen, Atemdepression, Atemnot und Atemstillstand, die tödlich enden können.
Das unmittelbare Vorgehen bei einer Opioid-Überdosierung beinhaltet die Entfernung der Fentanyl-HEXAL sublingual Tabletten, wenn diese sich noch im Mund befindet, die Sicherstellung von freien Atemwegen, körperliche und verbale Stimulierung des Patienten, die Beurteilung der Bewusstseinslage, des Atem-und Kreislaufstatus sowie, falls erforderlich, eine mechanische Beatmung (assistierte Beatmung).
Zur Behandlung einer Überdosierung (versehentliche Einnahme) bei einer Opioid-naiven Person sollte ein intravenöser Zugang gelegt und je nach klinischer Indikationsstellung Naloxon oder andere Opioid-Antagonisten gegeben werden. Eine Atemdepression als Folge einer Überdosierung kann länger anhalten als die Wirkungsdauer des Opioid-Antagonisten (so liegt z.B. die Halbwertzeit von Naloxon im Bereich von 30 bis 81 Minuten), sodass eine wiederholte Gabe erforderlich sein kann. Einzelheiten zur Anwendung sind der Fachinformation des jeweiligen Opioid-Antagonisten zu entnehmen.
Zur Behandlung einer Überdosierung bei Patienten, die eine OpioidErhaltungstherapie erhalten, sollte ein intravenöser Zugang gelegt werden. Der adäquate Einsatz von Naloxon oder eines anderen Opioid-Antagonisten kann in manchen Fällen gerechtfertigt sein, ist allerdings mit dem Risiko der Auslösung einer akuten Entzugssymptomatik assoziiert.
Bei Auftreten einer schweren oder andauernden Hypotonie kann eine Hypovolämie die Ursache dafür sein. Diese sollte mit bedarfsorientiertem parenteralem Volumenersatz behandelt werden.
Nach der Gabe von Fentanyl und anderen Opioiden kann eine die Atmung beeinträchtigende Muskelrigidität auftreten. In diesem Fall können eine Endotrachealintubation, eine assistierte Beatmung und die Gabe eines OpioidAntagonisten sowie eines Muskelrelaxans erforderlich sein.
5. PHARMAKOLOGISCHE EIGENSCHAFTEN
5.1 Pharmakodynamische Eigenschaften
Pharmakotherapeutische Gruppe: Phenylpiperidin-Derivate ATC-Code: N02AB03
Fentanyl ist ein Opioid-Analgetikum, das vorwiegend mit dem Opioid-^-Rezeptor interagiert. Seine primären therapeutischen Wirkungen sind Analgesie und Sedierung. Die sekundären pharmakologischen Wirkungen sind Atemdepression, Bradykardie, Hypothermie, Obstipation, Miosis, physische Abhängigkeit und Euphorie.
Die analgetischen Wirkungen von Fentanyl sind plasmaspiegelabhängig. Im Allgemeinen erhöhen sich die wirksame Konzentration und die Konzentration, bei der eine Toxizität auftritt, mit zunehmender Gewöhnung gegenüber Opioiden.
Wie schnell sich eine Toleranz entwickelt, ist individuell sehr verschieden.
Folglich sollte die Dosistitration für Fentanyl-HEXAL sublingual bis zum Erreichen des gewünschten Effekts individuell erfolgen (siehe Abschnitt 4.2).
Die Wirksamkeit und Sicherheit von Fentanyl-HEXAL sublingual wurden in einer doppelblinden, randomisierten, placebokontrollierten Crossover-Studie bei 91 Opioid-behandelten erwachsenen Krebspatienten untersucht, die 1 bis 4 Durchbruchschmerz-Episoden pro Tag erlitten. Der primäre Endpunkt war die aufsummierte Schmerzintensitätsdifferenz 30 Minuten (SPID30) nach der Dosisverabreichung, welche im Vergleich zu Placebo statistisch signifikant ausfiel
(p < 0,0001).
Auch die aufsummierte Schmerzintensitätsdifferenz (PID) ab 6 Minuten und bis zu 60 Minuten nach der Dosisverabreichung war im Vergleich zu Placebo statistisch signifikant (p = 0,02 nach 6 Minuten und p < 0,0001 nach 60 Minuten) (siehe nachstehende Abbildung).
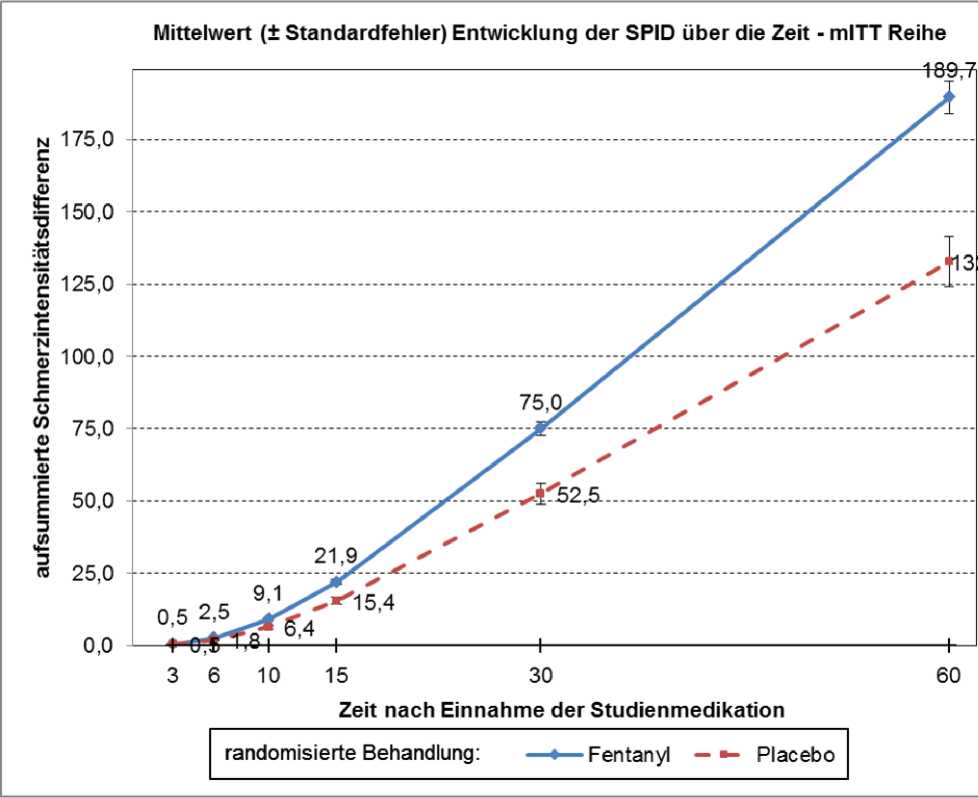
Die überlegene Wirksamkeit von Fentanyl-HEXAL sublingual gegenüber Placebo wurde durch Daten zu sekundären Endpunkten belegt:
• Bei Durchbruchschmerz-Episoden, die mit Fentanyl behandelt wurden, war die mittlere Schmerzintensitätsdifferenz ab 6 Minuten und bis zu 60 Minuten nach der Dosierung signifikant höher als bei Anwendung von Placebo (p = 0,003 bzw. p < 0,0001) (siehe nachstehende Abbildung);
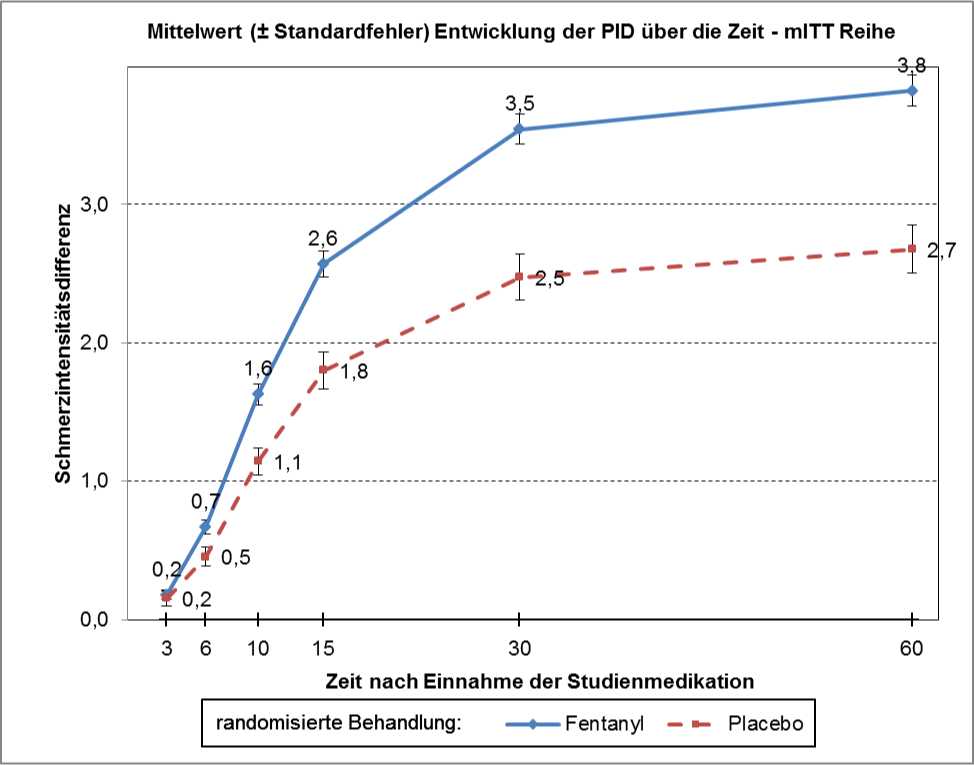
• bei Durchbruchschmerz-Episoden, die mit Fentanyl behandelt wurden, war auch die mittlere Schmerzlinderung ab 6 Minuten und bis zu 60 Minuten nach der Dosierung signifikant höher als bei Anwendung von Placebo
(p = 0,002 bzw. p < 0,0001);
• bei der Anwendung von Fentanyl-HEXAL sublingual zur Behandlung von Durchbruchschmerz-Episoden war signifikant seltener eine Notfallmedikation erforderlich als bei der Anwendung von Placebo;
• bei den mit Fentanyl-HEXAL sublingual behandelten DurchbruchschmerzEpisoden wurde nach 15 und 30 Minuten eine signifikante Verbesserung der Schmerzbeurteilung (Verringerung um > 33 % bzw. > 50 %) festgestellt.
Sämtliche Opioid-p-Rezeptor-Agonisten, einschließlich Fentanyl, rufen dosisabhängig eine Atemdepression hervor. Das Risiko einer Atemdepression ist geringer bei Patienten, die eine langfristige Opioid-Therapie erhalten, da diese Patienten eine Toleranz gegenüber den atemdepressiven Effekten entwickeln.
Während Opioide im Allgemeinen den Tonus der glatten Muskulatur des Harntrakts erhöhen, schwankt die Gesamtwirkung, wobei in manchen Fällen Harndrang und in anderen Fällen Schwierigkeiten beim Harnlassen ausgelöst werden.
Opioide erhöhen den Tonus und vermindern die propulsiven Kontraktionen der glatten Muskulatur des Gastrointestinaltraktes, wodurch sich die Durchgangszeit im Magen-Darm-Trakt verlängert, was möglicherweise für die obstipierende Wirkung von Fentanyl verantwortlich sein könnte.
5.2 Pharmakokinetische Eigenschaften
Fentanyl ist stark lipophil und kann sehr rasch über die Mundschleimhaut und langsamer über den Gastrointestinaltrakt resorbiert werden. Nach oraler Gabe unterliegt Fentanyl einem ausgeprägten First-Pass-Metabolismus in der Leber und dem Darm. Die Metaboliten haben keinen Anteil an den therapeutischen Wirkungen von Fentanyl.
Bei Fentanyl-HEXAL sublingual kommt eine Technologie zum Einsatz, die eine rasche Freisetzung von Fentanyl ermöglicht und den Anteil und die Menge des über die Mundschleimhaut aufgenommenen Fentanyls steigert. Die absolute Bioverfügbarkeit von Fentanyl-HEXAL sublingual wurde nicht bestimmt, wird aber auf etwa 70 % geschätzt.
Resorption
Die mittlere maximale Plasmakonzentration liegt bei 360 bis 2.070 pg/ml (nach der Anwendung von 133 bis 800 Mikrogramm Fentanyl-HEXAL sublingual) und wird nach 50 bis 90 Minuten erreicht.
Verteilung
Fentanyl ist in hohem Maße lipophil und verteilt sich mit einem großen scheinbaren Verteilungsvolumen gut über das Gefäßsystem. Nach sublingualer Anwendung von Fentanyl-HEXAL sublingual erfährt Fentanyl initial eine rasche Verteilung, die ein Gleichgewicht von Fentanyl zwischen Plasma und stark durchbluteten Geweben (Hirn, Herz und Lungen) darstellt. Anschließend erfolgt eine Umverteilung von Fentanyl zwischen tiefem Gewebekompartiment (Muskeln und Fett) und Plasma.
Die Plasmaproteinbindung von Fentanyl beträgt 80 % bis 85 %. Das Hauptbindungsprotein ist alpha-1-saures Glykoprotein, aber auch Albumin und Lipoproteine haben einen gewissen Anteil. Der freie Anteil von Fentanyl erhöht sich bei Vorliegen einer Azidose.
Biotransformation und Elimination
Fentanyl wird in der Leber und in der Darmschleimhaut über die CYP3A4-Isoform zu Norfentanyl metabolisiert. In Tierstudien ist Norfentanyl pharmakologisch nicht aktiv. Mehr als 90 % der verabreichten Fentanyl-Dosis wird durch Biotransformation zu N-dealkylierten und hydroxylierten inaktiven Metaboliten eliminiert.
Nach intravenöser Gabe von Fentanyl werden weniger als 7 % der verabreichten Dosis unverändert im Urin ausgeschieden und nur etwa 1 % findet sich unverändert in den Fäzes wieder. Die Metaboliten werden vorwiegend über den Urin ausgeschieden, während die fäkale Ausscheidung weniger wichtig ist.
Die terminale Eliminationsphase von Fentanyl ist das Ergebnis der Umverteilung zwischen Plasma und tiefem Gewebekompartiment. Nach Anwendung von
Fentanyl-HEXAL sublingual beträgt die terminale Eliminationshalbwertszeit ungefähr 12 Stunden.
Linearität/Nicht-Linearität
Es konnte eine Dosisproportionalität von 133 Mikrogramm bis 800 Mikrogramm gezeigt werden.
Nieren-/Leberfunktionsstörung
Eine Leber- oder Nierenfunktionsstörung kann die Serumkonzentrationen erhöhen. Ältere, kachektische oder allgemein geschwächte Patienten können eine niedrigere Fentanyl-Clearance aufweisen, was zu einer längeren terminalen Halbwertszeit des Wirkstoffs führen kann (siehe Abschnitte 4.2 und 4.4).
5.3 Präklinische Daten zur Sicherheit
Basierend auf den konventionellen Studien zur Sicherheitspharmakologie, Toxizität bei wiederholter Gabe, Genotoxizität und zum kanzerogenen Potential lassen die präklinischen Daten keine besonderen Gefahren für den Menschen erkennen.
Studien zur embryo-fetalen Entwicklung an Ratten und Kaninchen zeigten keine substanzinduzierten Missbildungen oder Entwicklungsstörungen bei Verabreichung während der Organogenese.
In einer Studie zur Fertilität und frühen embryonalen Entwicklung an Ratten wurde bei hohen Dosierungen (300 Mikrogramm/kg/Tag, s.c.) ein durch die männlichen Tiere vermittelter Effekt beobachtet. Dieser Effekt ist vermutlich eine Folge der sedierenden Auswirkungen von Fentanyl im Tierversuch.
In Studien zur prä- und postnatalen Entwicklung an Ratten war bei ausgeprägt maternal toxischen Dosierungen die Überlebensrate der Nachkommen signifikant herabgesetzt. Weitere Befunde nach Gabe von maternal toxischen Dosen waren bei F1-Jungtieren eine Verzögerung der physischen Entwicklung, der sensorischen Funktionen, der Reflexe und des Verhaltens. Diese Effekte könnten entweder indirekt durch ein verändertes Pflegeverhalten der Mutter und/oder eine verminderte Milchproduktion oder durch eine direkte Wirkung von Fentanyl auf die Jungtiere ausgelöst worden sein.
Kanzerogenitätsstudien ergaben keine Hinweise auf ein krebsauslösendes Potenzial (26-wöchiger alternativer Haut-Bioassay an transgenen Tg.AC-Mäusen; 2-jährige Studie an Ratten mit subkutaner Applikation). Bei der Untersuchung von Hirnschnitten aus der Kanzerogenitätsstudie an Ratten wurden bei Tieren, die hohe Dosen Fentanylcitrat erhalten hatten, Hirnläsionen festgestellt. Die Bedeutung dieser Befunde für den Menschen ist nicht bekannt.
6.
PHARMAZEUTISCHE ANGABEN
Calciumhydrogenphosphat mikrokristalline Cellulose Magnesiumstearat (Ph.Eur)
Hypromellose
Dinatriumhydrogenphosphat Macrogol 6000 Titandioxid (E 171)
Maltodextrin Triacetin Macrogol 8000
Drucktinte (enthält Schellack, Eisen(N,NI)-oxid [E 172])
6.2 Inkompatibilitäten
Nicht zutreffend
6.3 Dauer der Haltbarkeit
3 Jahre
6.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung
Für dieses Arzneimittel sind hinsichtlich der Temperatur keine besonderen Lagerungsbedingungen erforderlich.
In der Originalverpackung aufbewahren, um den Inhalt vor Licht zu schützen. Fentanyl-HEXAL sublingual sollte unter Verschluss aufbewahrt werden.
6.5 Art und Inhalt des Behältnisses
Abziehbare, kindergesicherte Blisterpackungen aus
• Polyamid-Aluminium-PVC/Aluminiumfolie
• Polyamid-Aluminium-PVC/Aluminium-PET-Folie
Packungsgrößen: 3 oder 30 Sublingualtabletten
6.6 Besondere Vorsichtsmaßnahmen für die Beseitigung
Nicht verwendetes Arzneimittel oder Abfallmaterial ist entsprechend den nationalen Anforderungen zu beseitigen.
7. INHABER DER ZULASSUNGEN
Hexal AG Industriestraße 25 83607 Holzkirchen Telefon: (08024) 908-0 Telefax: (08024) 908-1290 E-Mail: medwiss@hexal.com
8. ZULASSUNGSNUMMERN
88927.00. 00
88928.00. 00
88929.00. 00
88930.00. 00
88931.00. 00
88932.00. 00
9. DATUM DER ERTEILUNG DER ZULASSUNGEN
06. November 2013
10. STAND DER INFORMATION
Juli 2014
11. VERKAUFSABGRENZUNG
Verschreibungspflichtig
Betäubungsmittel