Fluarix
Gebrauchsinformation Informationen für den Anwender
Fluarix 2015/2016 Injektionssuspension in Fertigspritze
Influenza-Spaltimpfstoff (inaktiviert)
Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie bzw. Ihr Kind mit diesem Impfstoff geimpft werden, denn sie enthält wichtige Informationen.
Heben Sie die Packungsbeilage auf. Vielleicht möchten Sie diese später nochmals lesen.
Wenn Sie weitere Fragen haben, wenden Sie sich bitte an Ihren Arzt oder Apotheker. Dieser Impfstoff wurde Ihnen bzw. Ihrem Kind persönlich verschrieben.
Geben Sie ihn nicht an Dritte weiter.
Wenn Sie bzw. Ihr Kind Nebenwirkungen bemerken, wenden Sie sich an Ihren Arzt oder Apotheker. Dies gilt auch für Nebenwirkungen, die nicht in dieser Packungsbeilage angegeben sind. Siehe Abschnitt 4.
Was in dieser Packungsbeilage steht:
1. Was ist Fluarix und wofür wird es angewendet?
2. Was sollten Sie vor der Anwendung von Fluarix beachten?
3. Wie ist Fluarix anzuwenden?
4. Welche Nebenwirkungen sind möglich?
5. Wie ist Fluarix aufzubewahren?
6. Inhalt der Packung und weitere Informationen
1. Was ist Fluarix und wofür wird es angewendet?
Fluarix ist ein Impfstoff: Impfstoffe werden zum Schutz vor Infektionskrankheiten angewendet.
Dieser Impfstoff wird empfohlen, um Sie bzw. Ihr Kind vor der echten Virusgrippe (Influenza) zu schützen, insbesondere wenn ein erhöhtes Risiko für influenzabedingte Komplikationen besteht.
Nach der Verabreichung von Fluarix werden die natürlichen Abwehrmechanismen des Körpers einen Schutz vor einer Ansteckung mit der echten Virusgrippe aufbauen. Kein Bestandteil des Impfstoffes kann eine Virusgrippe verursachen.
Die echte Virusgrippe verbreitet sich sehr schnell, sie wird durch verschiedene Virustypen ausgelöst, die sich jedes Jahr ändern können. Deshalb sollten Sie bzw. Ihr Kind sich jedes Jahr impfen lassen. Die größte Gefahr einer Ansteckung mit der echten Virusgrippe besteht in der kalten Jahreszeit zwischen Oktober und März. Wenn Sie bzw. Ihr Kind nicht im Herbst geimpft wurden, kann eine Impfung auch noch bis zum Frühjahr ratsam sein, wenn für Sie bzw. Ihr Kind weiterhin Ansteckungsgefahr besteht. Ihr Arzt wird Sie beraten, wann die Impfung am besten durchgeführt wird.
Fluarix schützt Sie bzw. Ihr Kind etwa 2-3 Wochen nach Verabreichung gegen die drei im Impfstoff enthaltenen Virusstämme oder diesen Stämmen ähnliche Varianten.
Da die Inkubationszeit einer Virusgrippe einige Tage beträgt, kann Fluarix Sie bzw. Ihr Kind nicht vor einer echten Virusgrippe schützen, wenn Sie bzw. Ihr Kind sich zum Zeitpunkt der Impfung bereits angesteckt haben oder wenn die Erkrankung durch ein anderes Virus ausgelöst wurde.
Sie sollten auch beachten, dass viele Krankheitserreger grippeähnliche Erkrankungen (Erkältungskrankheiten) auslösen und Sie bzw. Ihr Kind durch Fluarix nicht vor diesen Erkrankungen geschützt werden.
2. Was sollten Sie vor der Anwendung von Fluarix beachten?
Um sicher zu sein, dass Fluarix für Sie bzw. Ihr Kind geeignet ist, ist es wichtig, dass Sie Ihren Arzt oder Apotheker darüber informieren, wenn einer der unten aufgeführten Punkte auf Sie bzw. Ihr Kind zutrifft. Fragen Sie Ihren Arzt oder Apotheker nach weiteren Erklärungen, wenn Sie etwas nicht verstehen.
Fluarix darf nicht verabreicht werden,
wenn Sie bzw. Ihr Kind überempfindlich (allergisch) sind gegen:
• die Wirkstoffe, oder
• einen der Hilfsstoffe von Fluarix, siehe Abschnitt 6, weitere Informationen, oder
• einen der in Spuren vorhandenen Bestandteile: z. B. Eier- (Ovalbumin oder Hühnerproteine) , Formaldehyd, Gentamicinsulfat oder Natriumdesoxycholat.
wenn Sie bzw. Ihr Kind an einer Erkrankung mit hohem Fieber oder an einer sonstigen akuten Erkrankung leiden. In diesem Fall sollte die Impfung verschoben werden, bis Sie bzw. Ihr Kind wieder gesund sind.
Warnhinweise und Vorsichtsmaßnahmen
Bitte sprechen Sie mit Ihrem Arzt oder Apotheker bevor Sie oder Ihr Kind mit
Fluarix geimpft werden,
• wenn Ihr Immunsystem oder das Ihres Kindes geschwächt ist (Immunsuppression).
• Wenn bei Ihnen bzw. Ihrem Kind aus irgendeinem Grund in den Tagen unmittelbar nach Gabe des Impfstoffs eine Blutuntersuchung durchgeführt werden soll, informieren Sie bitte Ihren Arzt. Bei einer kleinen Anzahl von Patienten zeigten sich bei einer Blutuntersuchung unmittelbar nach der Impfung falsch-positive Ergebnisse.
Ihr Arzt wird dann entscheiden, ob Sie bzw. Ihr Kind geimpft werden sollen.
Nach oder sogar vor einer Nadelinjektion kann es (meist bei Jugendlichen) zu einer
Ohnmacht kommen. Informieren Sie daher den Arzt oder das medizinische Fachpersonal,
wenn Sie bzw. Ihr Kind bei einer früheren Injektion schon einmal ohnmächtig geworden sind.
Wie bei allen anderen Impfstoffen auch kann es vorkommen, dass nicht alle mit
Fluarix geimpften Personen vollständig geschützt sind.
Anwendung von Fluarix zusammen mit anderen Arzneimitteln
• Bitte informieren Sie Ihren Arzt oder Apotheker, wenn Sie bzw. Ihr Kind andere Arzneimittel anwenden, kürzlich andere Arzneimittel angewendet haben oder beabsichtigen andere Arzneimittel anzuwenden.
• Fluarix kann zeitgleich mit anderen Impfstoffen in unterschiedliche Gliedmaßen verabreicht werden. Bei zeitgleicher Verabreichung kann es zu verstärkten Nebenwirkungen kommen.
• Die Immunantwort kann möglicherweise eingeschränkt sein, wenn Sie bzw. Ihr Kind sich einer Behandlung unterziehen, die das körpereigene Abwehrsystem unterdrückt wie beispielsweise eine Bestrahlung oder die Einnahme von Kortikosteroiden oder zellschädigenden Arzneimitteln (z.B. Chemotherapie).
Schwangerschaft und Stillzeit
Wenn Sie schwanger sind oder stillen, oder wenn Sie vermuten, schwanger zu sein oder beabsichtigen, schwanger zu werden, fragen Sie vor der Anwendung dieses Arzneimittels Ihren Arzt oder Apotheker um Rat.
Influenza Impfstoffe können in allen Phasen der Schwangerschaft gegeben werden. Verglichen mit dem 1. Trimester sind für das 2. und 3. Trimester größere Datenmengen über die Sicherheit von Grippeimpfungen verfügbar. Auf jeden Fall zeigen die Daten nach weltweiter Anwendung von Influenza Impfstoffen keine gesundheitsgefährdende Einflüsse auf die Schwangere oder das Baby.
Der Impfstoff (Fluarix) kann während der Stillzeit verabreicht werden.
Ihr Arzt wird entscheiden, ob Sie bzw. Ihr Kind mit Fluarix geimpft werden sollen. Fragen Sie vor der Anwendung von allen Arzneimitteln Ihren Arzt oder Apotheker um Rat.
Verkehrstüchtigkeit und das Bedienen von Maschinen
Der Impfstoff hat keine oder unwesentliche Auswirkungen auf die Verkehrstüchtigkeit oder die Fähigkeit zum Bedienen von Maschinen.
Fluarix enthält Natrium
Dieses Arzneimittel enthält weniger als 1mmol Natrium (23 mg) pro Dosis, d.h. es ist nahezu „natriumfrei“.
Fluarix enthält Kalium
Dieses Arzneimittel enthält weniger als 1 mmol Kalium (39 mg) pro Dosis, d.h. es ist nahezu „kaliumfrei“.
Fluarix enthält Ethanol
Dieses Arzneimittel enthält geringe Mengen Ethanol (Alkohol), weniger als 100 mg pro Dosis.
3. Wie ist Fluarix anzuwenden?
Dosierung
Erwachsene erhalten 1 x 0,5 ml.
Anwendung bei Kindern:
Kinder im Alter von 36 Monaten und älter erhalten 1 x 0,5 ml.
Kinder im Alter von 6 Monaten bis 35 Monaten erhalten 1 x 0,25 ml.
Kinder bis zum vollendeten 9. Lebensjahr, die noch nie gegen Grippe geimpft wurden, sollten frühestens 4 Wochen nach der ersten Impfung eine zweite Dosis erhalten.
Art der Anwendung
Ihr Arzt wird die entsprechende Dosis des Impfstoffes als Injektion in den Muskel oder tief unter die Haut verabreichen.
Wenn Sie weitere Fragen zur Anwendung des Impfstoffes haben, fragen Sie Ihren Arzt oder Apotheker.
4. Welche Nebenwirkungen sind möglich?
Wie alle Arzneimittel kann dieser Impfstoff Nebenwirkungen verursachen, die aber nicht bei jedem auftreten müssen.
In klinischen Studien mit trivalenten inaktivierten Influenza-Impfstoffen wurden die folgenden Nebenwirkungen häufig beobachtet (berichtet bei weniger als 1 von 10, aber mehr als 1 von 100 Geimpften):
• Kopfschmerzen
• Schweißausbruch
• Muskelschmerzen (Myalgien), Gelenkschmerzen (Arthralgien)
• Fieber, Unwohlsein, Schüttelfrost, Erschöpfung
• Lokale Reaktionen: Rötung, Schwellung, Schmerzen, Bluterguss, (Ekchymose), Verhärtung (Induration) an der Injektionsstelle.
Diese Nebenwirkungen klingen gewöhnlich nach 1 bis 2 Tagen ohne Behandlung wieder folgenlos ab.
Folgende Nebenwirkungen wurden bei Kindern und Jugendlichen im Alter von 6 Monaten bis 17 Jahren während der klinischen Prüfungen mit Fluarix berichtet:
Sehr häufig (Nebenwirkungen, die bei mehr als 1 von 10 Impfstoffdosen auftreten können):
• Reizbarkeit2
• Appetitlosigkeit2
• Benommenheit2
• Kopfschmerzen3
• Gelenkschmerzen3
• Muskelschmerzen3
• Fieber2
• Erschöpfung3
• Lokale Reaktionen: Rötung1, Schwellung1, Schmerzen1
Häufig (Nebenwirkungen, die bei bis zu 1 von 10 Impfstoffdosen auftreten können):
• Magen-Darm-Beschwerden3
• Schüttelfrost3
• Fieber3
1 berichtet bei Kindern im Alter von 6 Monaten bis 17 Jahren
2 berichtet bei Kindern im Alter von 6 Monaten bis <6 Jahren
3
berichtet bei Kindern im Alter von 6 Jahren bis 17 Jahren
Während der breiten Anwendung von trivalenten inaktivierten Influenza-Impfstoffen wurden zusätzlich die folgenden Nebenwirkungen beobachtet:
• allergische Reaktionen:
- Tränende und juckende Augen und verkrustete Augenlider (Konjunktivitis)
- in seltenen Fällen können diese zu einem medizinischen Notfall führen, wenn es zum Versagen des Blutkreislaufs kommt (Schock), der die ausreichende Versorgung in den verschiedenen Organen mit Blut aufrechterhält
- in sehr seltenen Fällen kann es zu Schwellungen, meistens im Bereich von Kopf, Hals oder Nacken einschließlich des Gesichts, der Lippen, der Zunge, der Kehle oder an anderen Körperstellen (Angioödeme) kommen
• Hautreaktionen, die sich nicht über den ganzen Körper ausbreiten können, einschließlich Hautjucken (Juckreiz, Nesselsucht) und Ausschlag
• Entzündung der Gefäße (Vaskulitis), die zu Hautausschlag und in sehr seltenen Fällen zu vorübergehenden Nierenproblemen führen kann.
• Schmerzen entlang der Nervenbahnen (Neuralgie), abnormale Empfindungen bei Berührung, Schmerz, Hitze oder Kälte (Parästhesien), Krämpfe in Verbindung mit Fieber, neurologische Störungen, die zu Nackensteife, Verwirrung, Taubheitsgefühl, Schmerz und Schwäche in den Gliedmaßen, Verlust des Gleichgewichts, Verlust der Reflexe, Lähmungserscheinungen an Teilen des Körpers oder am gesamten Körper (Encephalomyelitis, Neuritis, Guillain-Barre-Syndrom) führen können
• eine vorübergehende Verringerung bestimmter Blutbestandteile, die Blutplättchen genannt werden; eine zu geringe Anzahl an Blutplättchen (vorübergehende Thrombozytopenie) kann zu übermäßigen Blutergüssen oder Blutungen führen; vorübergehende Schwellung der Lymphdrüsen im Hals-, Achsel- oder Leistenbereich (vorübergehende Lymphadenopathie)
Meldung von Nebenwirkungen
Wenn Sie bzw. Ihr Kind Nebenwirkungen bemerken, wenden Sie sich an Ihren Arzt, Apotheker oder das medizinische Fachpersonal. Dies gilt auch für Nebenwirkungen, die nicht in dieser Packungsbeilage angegeben sind. Sie können Nebenwirkungen auch direkt dem Bundesinstitut für Impfstoffe und biomedizinische Arzneimittel, Paul-Ehrlich-Institut, Paul-Ehrlich-Straße 51 - 59, 63225 Langen, Telefon: +49 6 10 37 70, Telefax: +49 61 03 77 12 34, Website: www.pei.de, anzeigen. Indem Sie Nebenwirkungen melden, können Sie dazu beitragen, dass mehr Informationen über die Sicherheit dieses Arzneimittels zur Verfügung gestellt werden.
5. Wie ist Fluarix aufzubewahren?
Bewahren Sie diesen Impfstoff für Kinder unzugänglich auf.
Das Verfalldatum des Impfstoffs ist auf der Faltschachtel nach „Verwendbar bis: "mit Monat und Jahr aufgedruckt. Nach Ablauf des angegebenen Monats darf der Impfstoff nicht mehr verwendet werden.
Im Kühlschrank lagern (2° bis 8°C).
Nicht einfrieren! Impfstoffe, die versehentlich falsch gelagert oder eingefroren wurden, sind zu verwerfen.
In der Originalverpackung aufbewahren, um den Inhalt vor Licht zu schützen.
Das Arzneimittel darf nicht im Abwasser oder Haushaltsabfall entsorgt werden.
Fragen Sie Ihren Apotheker wie das Arzneimittel zu entsorgen ist, wenn Sie es nicht mehr benötigen. Diese Maßnahme hilft die Umwelt zu schützen.
6. Inhalt der Packung und weitere Informationen Was enthält Fluarix?
• Die Wirkstoffe sind: Influenza Virus (inaktiviert, Spaltantigene) der folgenden Stämme*: A/California/7/2009 (H1N1)pdm09 - ähnlich
(A/Christchurch/16/2010, NIB-74xp) 15 Mikrogramm HA**
A/Switzerland/9715293/2013 (H3N2) - ähnlich
(A/Switzerland/9715293/2013, NIB-88) 15 Mikrogramm HA**
15 Mikrogramm HA**
B/Phuket/3073/2013
pro Dosis (0,5 ml)
* gezüchtet in befruchteten Hühnereiern von gesunden Hühnerherden ** Hämagglutinin
Dieser Impfstoff entspricht den Empfehlungen der WHO (Weltgesundheitsorganisation) für die nördliche Hemisphäre und der EU-Entscheidung für die Saison 2015/2016.
• Die sonstigen Bestandteile sind: Natriumchlorid, Natriummonohydrogenphosphat x 12H2O, Kaliumdihydrogenphosphat, Kaliumchlorid, Magnesiumchlorid x 6H2O, RRR - a -Tocopherolhydrogensuccinat, Polysorbat 80 (Tween 80), Octoxinol 10 (Triton X-100) sowie Wasser für Injektionszwecke
Wie sieht Fluarix aus und welche Packungsgrößen gibt es?
Fluarix ist eine farblose bis leicht opaleszierende Suspension in einer Fertigspritze mit oder ohne Kanüle (0,5 ml).
Fluarix Packungsgrößen zu 1, 10, 20 Fertigspritzen sind zugelassen.
Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht.
Pharmazeutischer Unternehmer und Hersteller
PHARMAZEUTISCHER UNTERNEHMER GlaxoSmithKline GmbH & Co. KG
80700 München
Service Tel.: +49 (0)89 36044 8701 Service Fax: 0800 1 22 33 66 e-mail: produkt.info@gsk.com
HERSTELLER
GlaxoSmithKline Biologicals
NL der SmithKline Beecham Pharma GmbH & Co. KG
Zirkusstr. 40, 01069 Dresden
Telefon : 0049-351-4561 0
Telefax : 0049-351-4561 5211
Dieses Arzneimittel ist in den Mitgliedstaaten der Europäischen Union im Rahmen des Verfahrens der gegenseitigen Anerkennung unter den folgenden Bezeichnungen zugelassen:
|
Mitgliedsland |
Handelsname |
|
Bulgarien, Dänemark, Deutschland, Estland, Finnland, Frankreich, Griechenland, Großbritannien, Irland, Island, Italien, Kroatien, Lettland, Litauen, Malta, Niederlande, Norwegen, Österreich, Polen, Portugal, Rumänien, Schweden, Slowakische Republik, Slowenien, Spanien, Tschechische Republik, Ungarn, Zypern |
Fluarix |
|
Belgien, Luxemburg |
a-RIX |
Diese Gebrauchsinformation wurde zuletzt überarbeitet im August 2015.
Wie bei allen injizierbaren Impfstoffen sollten für den seltenen Fall einer anaphylaktischen Reaktion nach der Gabe des Impfstoffes entsprechende Möglichkeiten der medizinischen Behandlung und Überwachung stets sofort verfügbar sein (Adrenalin, Kortikosteroide, Antihistaminika).
Die Immunisierung mit Fluarix sollte intramuskulär oder durch tief subkutane Injektion erfolgen.
Der Impfstoff (Fluarix) sollte auf keinen Fall intravasal verabreicht werden.
Bei gleichzeitiger Verabreichung eines anderen Impfstoffes sollten verschiedene Injektionsstellen (kontralateral) gewählt werden.
Der Impfstoff sollte bei der Verabreichung Zimmertemperatur haben.
Vor Gebrauch ist die Spritze mit dem Impfstoff zu schütteln. Überprüfen Sie den Impfstoff optisch vor der Anwendung.
Wenn eine Dosis von 0,5 ml appliziert werden soll, ist der gesamte Inhalt der Spritze zu verabreichen.
Abbildung 1
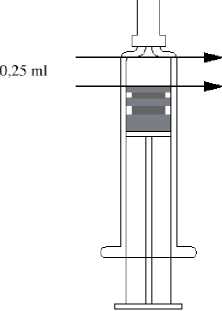
Anleitung für die Verabreichung von 0.25 ml des Impfstoffes für die Anwendung bei Kindern im Alter von 6 bis 35 Monaten:
Wenn eine Dosis von 0,25 ml appliziert werden soll, ist die Spritze in aufrechter Position zu halten und die Hälfte des Volumens abzuspritzen. Dazu wird der Stopfen bis zur Markierung auf der Spritze gedrückt. Bei Spritzen ohne Markierung kann Bild 1 als Dosierungshilfe benutzt werden. Man legt den oberen Rand der Spritze an die obere Pfeilspitze an und drückt den Stopfen bis zur unteren Pfeilspitze. Es verbleiben 0,25 ml Impfstoff in der Spritze (siehe Abbildung 1). Dann ist nach Möglichkeit die Kanüle zu wechseln, um das Impfen mit nasser Kanüle zu vermeiden. Der verbleibende Impfstoff von 0,25 ml ist zu verabreichen.
Anleitung für die Verabreichung des Impfstoffes in einer Fertigspritze ohne Nadel Um die Kanüle/Nadel an der Spritze anzubringen, folgen Sie der Anleitung in Abbildung 2.
Nadel
Spritzenzylinder
Abbildung 2
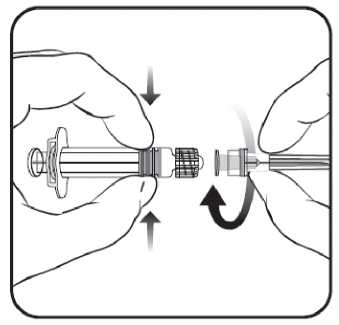
1. Halten Sie den Spritzenzylinder in einer Hand (vermeiden Sie, die Spritze am Kolben zu halten), drehen Sie die Spritzenkappe entgegen dem Uhrzeigersinn ab.
2. Um die Nadel an der Spritze anzubringen, drehen Sie die Nadel im Uhrzeigersinn in die Spritze bis sie fest sitzt (siehe Abbildung 2).
3. Entfernen Sie den Nadelschutz, der gelegentlich ein wenig fest sitzen kann.
4. Verabreichen Sie den Impfstoff.
Nicht verwendeter Arzneimittel oder Abfallmaterial ist gemäß den lokalen Vorschriften zu entsorgen.
Sonstige Hinweise
Gemäß § 22 Infektionsschutzgesetz müssen alle Schutzimpfungen vom Impfarzt mit dem Impfdatum, Handelsnamen, der Chargen-Bezeichnung sowie der Angabe der Krankheit, gegen die geimpft wurde, in einen Impfausweis eingetragen werden.
Häufig unterbleiben indizierte Impfungen, weil bestimmte Situationen irrtümlicherweise als Impfhindernisse angesehen werden. Einzelheiten hierzu finden Sie in den jeweils aktuellen STIKO-Empfehlungen (Ständige Impfkommission am Robert-Koch-Institut, aktuell abrufbar über www.rki.de)
8