Gabrielle-30 0,15 Mg/0,03 Mg Tabletten
Wortlaut der für die Fachinformation vorgesehenen Angaben
Fachinformation
1. Bezeichnung der Arzneimittel
Gabrielle-20 0,15 mg/0,02 mg Tabletten Gabrielle-30 0,15 mg/0,03 mg Tabletten
2. Qualitative und quantitative Zusammensetzung
Gabrielle-20 0,15 mg/0,02 mg Tabletten:
Jede Tablette enthält 0,15 mg Desogestrel und 0,02 mg Ethinylestradiol.
Sonstiger Bestandteil mit bekannter Wirkung: Jede unbeschichtete Tablette enthält 58 mg Lactose.
Gabrielle-30 0,15 mg/0,03 mg Tabletten:
Jede Tablette enthält 0,15 mg Desogestrel und 0,03 mg Ethinylestradiol.
Sonstiger Bestandteil mit bekannter Wirkung: Jede unbeschichtete Tablette enthält 58 mg Lactose.
Vollständige Auflistung der sonstigen Bestandteile, siehe Abschnitt 6.1.
3. Darreichungsform
Tablette.
Gabrielle-20 0,15 mg/0,02 mg Tabletten:
Jede Tablette ist rund, weiß bis cremefarben, mit einem Durchmesser von
5.00 mm, unbeschichtet, bikonvex und der Prägung „141" auf der einen Seite und glatt auf der anderen Seite.
Gabrielle-30 0,15 mg/0,03 mg Tabletten:
Jede Tablette ist rund, weiß bis cremefarben, mit einem Durchmesser von
5.00 mm, unbeschichtet, bikonvex und der Prägung „142" auf der einen Seite und glatt auf der anderen Seite.
4. Klinische Angaben
4.1 Anwendungsgebiete
Orale Kontrazeption.
Bei der Entscheidung, Gabrielle zu verschreiben, sollten die aktuellen, individuellen Risikofaktoren der einzelnen Frauen, insbesondere im Hinblick auf venöse Thromboembolien (VTE), berücksichtigt werden. Auch sollte das Risiko für eine VTE bei Anwendung von Gabrielle mit dem anderer kombinierter hormonaler Kontrazeptiva (KHK) verglichen werden (siehe Abschnitte 4.3 und 4.4).
4.2 Dosierung und Art der Anwendung
Dosierung
Wie soll Gabrielle eingenommen werden:
Die Tabletten sind in der auf der Blisterpackung angegebenen Reihenfolge jeden Tag möglichst zur gleichen Tageszeit, falls erforderlich, mit etwas Flüssigkeit einzunehmen. Hierbei wird an 21 aufeinanderfolgenden Tagen täglich eine Tablette eingenommen. Vor jeder weiteren Packung ist ein 7-tägiges einnahmefreies Intervall einzulegen, in dem es üblicherweise zu einer Entzugsblutung kommt. Diese beginnt normalerweise 2 bis 3 Tage nach der letzten Tabletteneinnahme und kann noch andauern, wenn bereits mit der nächsten Packung begonnen wird.
Beginn der Einnahme von Gabrielle:
• Keine vorangegangene Einnahme von hormonalen Kontrazeptiva (im letzten Monat)
Mit der Einnahme wird am 1. Tag des natürlichen weiblichen Zyklus (d. h. am 1. Tag der Monatsblutung) begonnen. Die Tabletteneinnahme kann auch zwischen Tag 2 und 5 begonnen werden. Während des ersten Zyklus wird dann aber die Anwendung einer zusätzlichen Barrieremethode während der ersten 7 Tage der Tabletteneinnahme empfohlen.
• Wechsel von einem kombinierten hormonalen Kontrazeptivum (kombiniertes orales Kontrazeptivum (KOK), Vaginalring oder transdermales Pflaster)
Die Frau sollte mit Gabrielle vorzugsweise am Tag nach der Einnahme der letzten aktiven Tablette (der letzten Tablette mit Wirkstoffen) ihres bisherigen KOK beginnen, spätestens jedoch am Tag nach der üblichen Einnahmepause oder Placebo-Intervalls ihres früheren KOK. Wurde zuvor ein Vaginalring oder ein transdermales Pflaster verwendet, sollte die Frau mit der Einnahme von Gabrielle vorzugsweise am Tag nach der Entfernung, spätestens aber wenn die nächste Applikation fällig gewesen wäre, beginnen. Das hormonfreie Intervall der bisherigen Methode sollte niemals über den empfohlenen Zeitraum hinaus ausgedehnt werden.
Wenn die Anwenderin ihr bisheriges kombiniertes hormonales Kontrazeptivum konsequent und korrekt während der vorhergehenden 7 Tage angewendet hat und wenn eine Schwangerschaft mit Sicherheit ausgeschlossen werden kann, kann sie auch an jedem beliebigen Zyklustag von ihrem bisher angewandten kombinierten hormonalen Kontrazeptivum zu Gabrielle wechseln.
Es könnte sein, dass nicht alle beschriebenen kontrazeptiven Methoden (z. B. Vaginalring, transdermales Pflaster) in jedem Land der Europäischen Union vermarktet werden.
• Wechsel von einem Gestagenmonopräparat (Minipille, Injektionspräparat, Implantat), oder von einem Gestagen-freisetzenden Intrauterin-System (IUS)
Die Frau kann von der Minipille an jedem Tag (von einem Implantat oder IUS am Tag der Entfernung und von einem injizierbaren Präparat am Tag, an dem die nächste Injektion fällig wäre) wechseln. In all diesen Fällen ist während der ersten 7 Tage der Tabletteneinnahme zusätzlich eine Barrieremethode anzuwenden.
• Nach einem Abort im ersten Trimenon
Die Frau kann sofort mit der Einnahme von Gabrielle beginnen. In diesem Fall sind keine zusätzlichen empfängnisverhütenden Maßnahmen erforderlich.
• Nach einer Geburt oder einem Abort im zweiten Trimenon
Den Frauen sollte geraten werden, die Einnahme am Tag 21 bis 28 nach einer Geburt oder nach einem Abort im zweiten Trimenon zu beginnen. Wenn der Beginn der Einnahme später erfolgt, soll den Frauen geraten werden, während der ersten 7 Einnahmetage zusätzlich eine Barrieremethode anzuwenden. Wenn bereits Geschlechtsverkehr stattgefunden hat, muss vor Beginn der Einnahme von KOK eine Schwangerschaft ausgeschlossen werden oder die erste Menstruationsblutung abgewartet werden.
Zur Anwendung in der Stillzeit - siehe Abschnitt 4.6.
Vorgehen bei vergessener Einnahme:
Wird die Einnahme innerhalb von 12 Stunden nach dem üblichen
Einnahmezeitpunkt nachgeholt, ist der Konzeptionsschutz nicht eingeschränkt.
Die Frau sollte die Tabletteneinnahme sobald sie sich erinnert nachholen und alle
darauf folgenden Tabletten wieder zur gewohnten Zeit einnehmen.
Wenn der Einnahmezeitpunkt um mehr als 12 Stunden überschritten wird, ist der
Konzeptionsschutz nicht mehr voll gewährleistet.
Für das Vorgehen bei vergessener Einnahme gelten die folgenden zwei
Grundregeln:
1. Die Einnahme der T abletten darf nicht länger als 7 T age unterbrochen werden.
2. Eine regelmäßige Einnahme der Tabletten über mindestens 7 Tage ist erforderlich, um wirkungsvoll die Hypothalamus-Hypophysen-Ovar-Achse zu unterdrücken.
Daraus ergibt sich folgendes Vorgehen in der täglichen Praxis:
• Woche 1
Die Anwenderin sollte die Einnahme der letzten vergessenen Tablette nachholen, sobald sie sich daran erinnert, auch wenn dadurch 2 Tabletten zur gleichen Zeit eingenommen werden müssen. Die weitere Tabletteneinnahme erfolgt dann zur gewohnten Zeit. Zusätzlich soll während der nächsten 7 Tage eine Barrieremethode wie z. B. ein Kondom angewendet werden. Wenn während der vorangegangenen 7 Tage Geschlechtsverkehr stattgefunden hat, sollte die Möglichkeit einer Schwangerschaft in Betracht gezogen werden. Die Wahrscheinlichkeit einer Schwangerschaft ist umso höher, je mehr Tabletten vergessen wurden einzunehmen und je näher die vergessenen Tabletten an dem einnahmefreien Intervall liegen.
• Woche 2
Die Anwenderin sollte die Einnahme der letzten vergessenen Tablette nachholen, sobald sie sich daran erinnert, auch wenn dadurch 2 Tabletten zur gleichen Zeit eingenommen werden müssen. Die weitere Einnahme der Tabletten erfolgt dann zur gewohnten Zeit. Vorausgesetzt, dass die Einnahme der Tabletten an den 7 Tagen vor der vergessenen Tablette korrekt erfolgt ist, besteht keine Notwendigkeit, zusätzliche kontrazeptive Schutzmaßnahmen zu treffen. Wenn mehr als 1 Tablette vergessen wurde einzunehmen, sollen während der nächsten 7 Tage zusätzliche kontrazeptive Schutzmaßnahmen ergriffen werden.
• Woche 3
Aufgrund des bevorstehenden 7-tägigen einnahmefreien Intervalls kann ein voller Konzeptionsschutz nicht mehr gewährleistet werden. Durch eine Anpassung des Einnahmeschemas lässt sich eine Herabsetzung der empfängnisverhütenden Wirkung dennoch verhindern. Bei Einhalten einer der beiden folgenden Vorgehensweisen besteht keine Notwendigkeit, zusätzliche kontrazeptive Maßnahmen zu treffen, vorausgesetzt, die Einnahme der Tabletten an den 7 Tagen vor der ersten vergessenen Tablette erfolgte korrekt. Wenn dies nicht der Fall ist, sollte die Frau wie unter Punkt 1 beschrieben vorgehen und außerdem in den nächsten 7 Tagen zusätzliche kontrazeptive Schutzmaßnahmen ergreifen.
1. Die Anwenderin soll die Einnahme der letzten vergessenen Tablette nachholen, sobald sie sich daran erinnert, auch wenn dies bedeutet, dass zwei Tabletten zur gleichen Zeit eingenommen werden müssen. Die Einnahme der restlichen Tabletten erfolgt dann wieder zur gewohnten Zeit. Mit der Einnahme aus der nächsten Blisterpackung wird direkt nach Aufbrauchen der aktuellen Blisterpackung begonnen, d. h., zwischen den beiden Packungen soll kein einnahmefreies Intervall liegen. Es ist unwahrscheinlich, dass es bei der Anwenderin vor Aufbrauchen der zweiten Packung zu einer Abbruchblutung kommt, allerdings können noch während der Einnahme Schmier- oder Durchbruchblutungen auftreten.
2. Es kann auch ein Abbruch der Einnahme aus der aktuellen Blisterpackung empfohlen werden, an den sich ein einnahmefreies Intervall von bis zu
7 Tagen, die Tage der vergessenen Tabletten-Einnahme eingerechnet, anschließen sollte. Danach wird mit der Tabletten-Einnahme aus der neuen Packung begonnen.
Bei vergessener Tabletten-Einnahme und anschließendem Ausbleiben einer Abbruchblutung im ersten einnahmefreien Intervall sollte die Möglichkeit einer Schwangerschaft erwogen werden.
Verhalten bei Magen-Darm-Störungen:
Bei schweren Magen-Darm-Störungen (z. B. Erbrechen oder Durchfall) kann die Resorption unvollständig erfolgen und zusätzliche kontrazeptive Maßnahmen notwendig machen. Bei Erbrechen innerhalb von 3-4 Stunden nach Tabletteneinnahme sollte so schnell wie möglich eine neue (Ersatz-)Tablette eingenommen werden. Wenn möglich sollte die neue Tablette innerhalb von 12 Stunden des normalen Einnahmeschemas eingenommen werden. Wenn mehr als 12 Stunden vergangen sind, gelten dieselben Anwendungshinweise wie bei vergessener Tabletten-Einnahme, Abschnitt „Vorgehen bei vergessener Einnahme". Wenn das gewohnte Einnahmeschema beibehalten werden soll, muss die zusätzlich einzunehmende Tablette aus einer anderen Blisterpackung genommen werden.
Verschieben der Entzugsblutung:
Die Verschiebung der Entzugsblutung ist keine Indikation für dieses Präparat. Um jedoch die Entzugsblutung in Ausnahmefällen hinauszuschieben, kann die Anwenderin direkt ohne Einnahmepause mit der Tabletteneinnahme aus der nächsten Packung Gabrielle fortfahren. Die Entzugsblutung kann so lange hinausgeschoben werden wie gewünscht, aber nicht länger als bis die zweite Packung aufgebraucht ist. Während dieser Zeit kann es zu Durchbruch- oder Schmierblutungen kommen. Nach der darauf folgenden regulären 7-tägigen Einnahmepause kann die Einnahme von Gabrielle wie üblich fortgesetzt werden. Zur Verschiebung der Entzugsblutung auf einen anderen Wochentag als nach dem bisherigen Einnahmeschema üblich, kann das bevorstehende einnahmefreie Intervall um die gewünschte Zahl von Tagen verkürzt werden. Je kürzer das einnahmefreie Intervall, desto höher ist die Wahrscheinlichkeit einer ausbleibenden Entzugsblutung und während der Einnahme aus der folgenden Packung einsetzender Durchbruch- bzw. Schmierblutungen (wie beim Verschieben der Entzugsblutung).
Kinder und Jugendliche
Die Sicherheit und Wirksamkeit von Desogestrel/Ethinylestradiol bei Jugendlichen unter 18 Jahren ist bisher noch nicht erwiesen. Es liegen keine Daten vor.
Art der Anwendung Zum Einnehmen.
4.3 Gegenanzeigen
Kombinierte hormonale Kontrazeptiva (KHK) dürfen unter den folgenden Bedingungen nicht angewendet werden und müssen bei erstmaligem Auftreten einer der folgenden Erkrankungen während der KHK-Anwendung sofort abgesetzt werden:
• Vorliegen einer oder Risiko für eine venöse Thromboembolie (VTE)
o Venöse Thromboembolie - bestehende VTE (auch unter Therapie mit Antikoagulanzien) oder VTE in der Vorgeschichte (z. B. tiefe Venenthrombose [TVT] oder Lungenembolie [LE]) o Bekannte erbliche oder erworbene Prädisposition für eine venöse Thromboembolie, wie z. B. APC-Resistenz (einschließlich Faktor-V-Leiden), Antithrombin-III-Mangel, Protein-C-Mangel oder Protein-S-Mangel
o Größere Operationen mit längerer Immobilisierung (siehe Abschnitt 4.4) o Hohes Risiko für eine venöse Thromboembolie aufgrund mehrerer Risikofaktoren (siehe Abschnitt 4.4)
• Vorliegen einer oder Risiko für eine arterielle Thromboembolie (ATE) o Arterielle Thromboembolie - bestehende ATE, ATE in der
Vorgeschichte (z. B. Myokardinfarkt) oder Erkrankung im Prodromalstadium (z. B. Angina pectoris) o Zerebrovaskuläre Erkrankung - bestehender Schlaganfall, Schlaganfall oder prodromale Erkrankung (z. B. transitorische ischämische Attacke [TIA]) in der Vorgeschichte
o Bekannte erbliche oder erworbene Prädisposition für eine arterielle Thromboembolie, wie z. B. Hyperhomocysteinämie und Antiphospholipid-Antikörper (Anticardiolipin-Antikörper, Lupus antikoagulans)
o Migräne mit fokalen neurologischen Symptomen in der Vorgeschichte o Hohes Risiko für eine arterielle Thromboembolie aufgrund mehrerer Risikofaktoren (siehe Abschnitt 4.4) oder eines schwerwiegenden Risikofaktors wie:
• Diabetes mellitus mit Gefäßschädigung
• Schwere Hypertonie
• Schwere Dyslipoproteinämie
• bestehende oder vorausgegangene Pankreatitis in Zusammenhang mit schwerer Hypertriglyzeridämie
• bestehende oder vorausgegangene schwere Lebererkrankung, solange sich die Leberfunktionswerte nicht normalisiert haben
• bestehende oder vorausgegangene Lebertumoren (benigne oder maligne)
• bekannte oder vermutete sexualhormonabhängige Malignome (z. B. der Genitalorgane oder der Brüste)
• diagnostisch nicht abgeklärte vaginale Blutungen
• Endometriumhyperplasie
• Überempfindlichkeit gegen die Wirkstoffe oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile.
4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung
Warnhinweise:
Die Eignung von Gabrielle sollte mit der Frau besprochen werden, falls eine der im Folgenden aufgeführten Erkrankungen oder Risikofaktoren vorliegt. Bei einer
Verschlechterung oder dem ersten Auftreten einer dieser Erkrankungen oder Risikofaktoren ist der Anwenderin anzuraten, sich an ihren Arzt zu wenden, um zu entscheiden, ob die Anwendung von Gabrielle beendet werden sollte.
Risiko für eine venöse Thromboembolie (VTE):
Die Anwendung jedes kombinierten hormonalen Kontrazeptivums (KHK) erhöht das Risiko für eine venöse Thromboembolie (VTE) im Vergleich zur Nichtanwendung. Arzneimittel, die Levonorgestrel, Norgestimat oder Norethisteron enthalten, sind mit dem geringsten Risiko für eine VTE verbunden. Andere Arzneimittel, wie Gabrielle, können ein bis zu doppelt so hohes Risiko aufweisen. Die Entscheidung, ein Arzneimittel anzuwenden, das nicht zu denen mit dem geringsten VTE-Risiko gehört, sollte nur nach einem Gespräch mit der Frau getroffen werden, bei dem sicherzustellen ist, dass sie Folgendes versteht: das Risiko für eine VTE bei Anwendung von Gabrielle, wie ihre vorliegenden individuellen Risikofaktoren dieses Risiko beeinflussen, und dass ihr Risiko für VTE in ihrem allerersten Anwendungsjahr am höchsten ist. Es gibt zudem Hinweise, dass das Risiko erhöht ist, wenn die Anwendung eines KHK nach einer Unterbrechung von 4 oder mehr Wochen wieder aufgenommen wird.
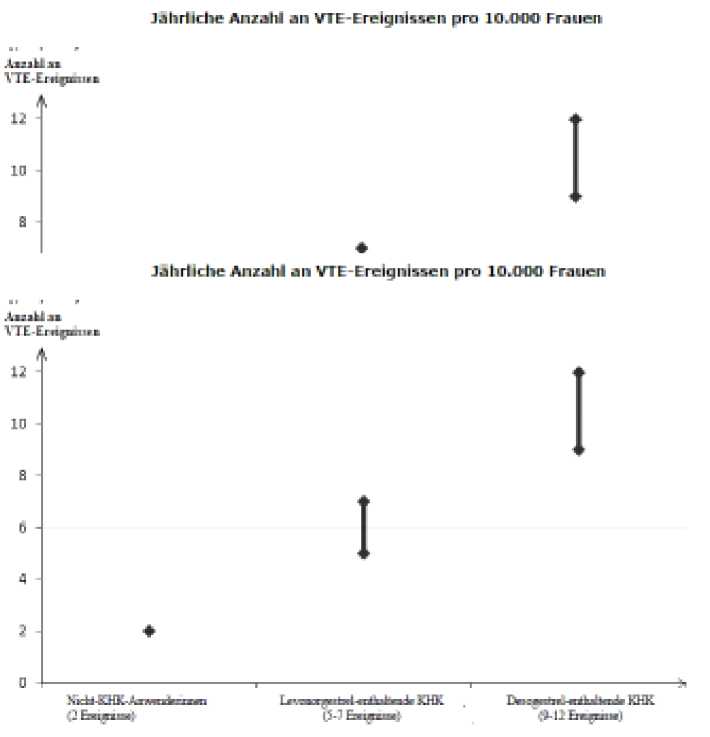
Ungefähr 2 von 10.000 Frauen, die kein KHK anwenden und nicht schwanger sind, erleiden im Verlauf eines Jahres eine VTE. Bei einer einzelnen Frau kann das Risiko jedoch in Abhängigkeit von ihren zugrunde liegenden Risikofaktoren bedeutend höher sein (siehe unten).
Es wird geschätzt1, dass im Verlauf eines Jahres 9 bis 12 von 10.000 Frauen, die ein Drospirenon-haltiges KHK anwenden, eine VTE erleiden; im Vergleich hierzu kommt es pro Jahr bei ungefähr 62 von 10.000 Frauen, die ein Levonorgestrel-haltiges KHK anwenden, zu einer VTE.
In beiden Fällen ist die Anzahl an VTE pro Jahr geringer als die erwartete Anzahl während der Schwangerschaft oder in der Zeit nach der Geburt.
VTE verlaufen in 1-2 % der Fälle tödlich.
Äußerst selten wurde bei Anwenderinnen von KHK über eine Thrombose in anderen Blutgefäßen berichtet, wie z. B. in Venen und Arterien von Leber, Mesenterium, Nieren oder Retina.
Risikofaktoren für VTE
Das Risiko für venöse thromboembolische Komplikationen bei Anwenderinnen von KHK kann deutlich ansteigen, wenn bei der Anwenderin zusätzliche Risikofaktoren bestehen, insbesondere wenn mehrere Risikofaktoren vorliegen (siehe Tabelle).
Gabrielle ist kontraindiziert, wenn bei einer Frau mehrere Risikofaktoren gleichzeitig bestehen, die insgesamt zu einem hohen Risiko für eine Venenthrombose führen (siehe Abschnitt 4.3). Weist eine Frau mehr als einen Risikofaktor auf, ist es möglich, dass der Anstieg des Risikos das Risiko der Summe der einzelnen Faktoren übersteigt - in diesem Fall muss ihr Gesamtrisiko für eine VTE in Betracht gezogen werden. Wenn das Nutzen/Risiko-Verhältnis als ungünstig erachtet wird, darf ein KHK nicht verschrieben werden (siehe Abschnitt 4.3).
Tabelle: Risikofaktoren für VTE
|
Risikofaktor |
Anmerkung |
|
Adipositas (Body-Mass-Index über 30 kg/m2) |
Das Risiko nimmt mit steigendem BMI deutlich zu. Besonders wichtig, wenn weitere Risikofaktoren vorliegen. |
|
Längere Immobilisierung, größere Operationen, jede Operation an Beinen oder Hüfte, neurochirurgische Operation oder schweres Trauma Hinweis: Eine vorübergehende Immobilisierung einschließlich einer Flugreise von > 4 Stunden Dauer kann ebenfalls einen Risikofaktor für eine VTE darstellen, insbesondere bei Frauen mit weiteren Risikofaktoren. |
In diesen Fällen ist es ratsam, die Anwendung des Pflasters/der Tablette/des Rings (bei einer geplanten Operation mindestens vier Wochen vorher) zu unterbrechen und erst zwei Wochen nach der kompletten Mobilisierung wieder aufzunehmen. Es ist eine andere Verhütungsmethode anzuwenden, um eine ungewollte Schwangerschaft zu verhindern. Eine antithrombotische Therapie muss erwogen werden, wenn Gabrielle nicht vorab abgesetzt wurde. |
|
Familiäre Vorbelastung (jede venöse Thromboembolie bei einem Geschwister oder Elternteil, insbesondere in relativ jungen Jahren, z. B. jünger als 50 Jahre). |
Bei Verdacht auf eine genetische Prädisposition ist die Frau zur Beratung an einen Spezialisten zu überweisen, bevor eine Entscheidung über die Anwendung eines KHKs getroffen wird. |
|
Andere Erkrankungen, die mit einer VTE verknüpft sind. |
Krebs, systemischer Lupus erythematodes, hämolytisches urämisches Syndrom, chronisch entzündliche Darmerkrankung (Morbus Crohn oder Colitis ulcerosa) und Sichelzellkrankheit. |
|
Zunehmendes Alter |
Insbesondere älter als 35 Jahre |
Es besteht kein Konsens über die mögliche Rolle von Varizen und oberflächlicher Thrombophlebitis bezüglich des Beginns oder Fortschreitens einer Venenthrombose.
Das erhöhte Risiko einer Thromboembolie in der Schwangerschaft und insbesondere während der 6-wöchigen Dauer des Wochenbetts muss berücksichtigt werden (Informationen zur „Schwangerschaft und Stillzeit“ siehe Abschnitt 4.6).
Symptome einer VTE (tiefe Beinvenenthrombose und Lungenembolie)
Beim Auftreten von Symptomen ist den Anwenderinnen anzuraten, unverzüglich ärztliche Hilfe in Anspruch zu nehmen und das medizinische Fachpersonal darüber zu informieren, dass sie ein KHK anwenden.
Bei einer tiefen Beinvenenthrombose (TVT) können folgende Symptome auftreten:
- unilaterale Schwellung des Beins und/oder Fußes oder entlang einer Beinvene;
- Schmerz oder Druckschmerz im Bein, der möglicherweise nur beim Stehen oder Gehen bemerkt wird;
- Erwärmung des betroffenen Beins; gerötete oder entfärbte Haut am Bein.
Bei einer Lungenembolie (LE) können folgende Symptome auftreten:
- plötzliches Auftreten unerklärlicher Kurzatmigkeit oder schnellen Atmens;
- plötzlich auftretender Husten möglicherweise in Verbindung mit Hämoptyse;
- stechender Brustschmerz;
- starke Benommenheit oder Schwindelgefühl;
- schneller oder unregelmäßiger Herzschlag.
Einige dieser Symptome (z. B. „Kurzatmigkeit“, „Husten“) sind unspezifisch und können als häufiger vorkommende und weniger schwerwiegende Ereignisse fehlinterpretiert werden (z. B. als Atemwegsinfektionen).
Andere Anzeichen für einen Gefäßverschluss können plötzlicher Schmerz sowie Schwellung und leicht bläuliche Verfärbung einer Extremität sein.
Tritt der Gefäßverschluss im Auge auf, können die Symptome von einem schmerzlosen verschwommenen Sehen bis zu einem Verlust des Sehvermögens reichen. In manchen Fällen tritt der Verlust des Sehvermögens sehr plötzlich auf.
Das Auftreten von einem oder mehrerer dieser Symptome kann ein Grund für einen sofortigen Abbruch der Einnahme von Gabrielle sein.
Risiko für eine arterielle Thromboembolie (ATE)
Epidemiologische Studien haben die Anwendung von KHK mit einem erhöhten Risiko für arterielle Thromboembolie (Myokardinfarkt) oder apoplektischen Insult (z. B. transitorische ischämische Attacke, Schlaganfall) in Verbindung gebracht. Arterielle thromboembolische Ereignisse können tödlich verlaufen.
Risikofaktoren für ATE
Das Risiko für arterielle thromboembolische Komplikationen oder einen apoplektischen Insult bei Anwenderinnen von KHK erhöht sich bei Frauen, die Risikofaktoren aufweisen (siehe Tabelle). Gabrielle ist kontraindiziert bei Frauen, die einen schwerwiegenden oder mehrere Risikofaktoren für eine ATE haben, die sie einem hohen Risiko für eine Arterienthrombose aussetzen (siehe Abschnitt 4.3). Weist eine Frau mehr als einen Risikofaktor auf, ist es möglich, dass der Anstieg des Risikos das Risiko der Summe der einzelnen Faktoren übersteigt - in diesem Fall muss ihr Gesamtrisiko betrachtet werden. Bei
Vorliegen eines ungünstigen Nutzen/Risiko-Verhältnis darf ein KHK nicht verschrieben werden (siehe Abschnitt 4.3).
Tabelle: Risikofaktoren für ATE
|
Risikofaktor |
Anmerkung |
|
Zunehmendes Alter |
Insbesondere älter als 35 Jahre |
|
Rauchen |
Frauen ist anzuraten, nicht zu rauchen, wenn sie ein KHK anwenden möchten. Frauen über 35 Jahren, die weiterhin rauchen, ist dringend zu empfehlen, eine andere Verhütungsmethode anzuwenden. |
|
Hypertonie | |
|
Adipositas (Body-Mass-Index über 30 kg/m2) |
Das Risiko nimmt mit steigendem BMI deutlich zu. Besonders wichtig bei Frauen mit zusätzlichen Risikofaktoren. |
|
Familiäre Vorbelastung (jede arterielle Thromboembolie bei einem Geschwister oder Elternteil, insbesondere in relativ jungen Jahren, d. h. jünger als 50 Jahre). |
Bei Verdacht auf eine genetische Prädisposition ist die Frau zur Beratung an einen Spezialisten zu überweisen, bevor eine Entscheidung über die Anwendung eines KHKs getroffen wird. |
|
Migräne |
Ein Anstieg der Häufigkeit oder des Schweregrads der Migräne während der Anwendung von KHK (die einem zerebrovaskulären Ereignis vorausgehen kann) kann ein Grund für ein sofortiges Absetzen sein. |
|
Andere Erkrankungen, die mit unerwünschten Gefäßereignissen verknüpft sind. |
Diabetes mellitus, Hyperhomocysteinämie, Erkrankung der Herzklappen und Vorhofflimmern, Dyslipoproteinämie und systemischer Lupus erythematodes. |
Symptome einer ATE
Beim Auftreten von Symptomen ist den Frauen anzuraten, unverzüglich ärztliche Hilfe in Anspruch zu nehmen und das medizinische Fachpersonal darüber zu informieren, dass sie ein KHK anwenden.
Bei einem apoplektischen Insult können folgende Symptome auftreten:
- plötzliches Taubheitsgefühl oder Schwäche in Gesicht, Arm oder Bein, besonders auf einer Köperseite;
- plötzliche Gehschwierigkeiten, Schwindelgefühl, Gleichgewichtsverlust oder Koordinationsstörungen;
- plötzliche Verwirrtheit, Sprech- oder Verständnisschwierigkeiten;
- plötzliche Sehstörungen in einem oder beiden Augen;
- plötzliche, schwere oder länger anhaltende Kopfschmerzen unbekannter Ursache;
- Verlust des Bewusstseins oder Ohnmacht mit oder ohne Krampfanfall.
Vorübergehende Symptome deuten auf eine transitorische ischämische Attacke (TIA) hin.
Bei einem Myokardinfarkt (MI) können folgende Symptome auftreten:
- Schmerz, Unbehagen, Druck, Schweregefühl, Enge- oder Völlegefühl in Brust, Arm oder unterhalb des Sternums;
- in den Rücken, Kiefer, Hals, Arm, Magen ausstrahlende Beschwerden;
- Völlegefühl, Indigestion oder Erstickungsgefühl;
- Schwitzen, Übelkeit, Erbrechen oder Schwindelgefühl;
- extreme Schwäche, Angst oder Kurzatmigkeit;
- schnelle oder unregelmäßige Herzschläge.
Das Vorliegen eines schweren Risikofaktors oder mehrerer Risikofaktoren für venöse oder arterielle Gefäßerkrankungen kann ebenfalls eine Gegenanzeige darstellen. Die Möglichkeit einer antikoagulatorischen Therapie soll ebenfalls in Betracht gezogen werden. Anwenderinnen von KOK sind besonders darauf hinzuweisen, bei möglichen Anzeichen einer Thrombose ihren Arzt aufzusuchen. Bei vermuteter oder bestätigter Thrombose ist das KOK abzusetzen. Wegen der Teratogenität der antikoagulatorischen Therapie (Cumarine) ist auf geeignete alternative Empfängnisverhütung umzusteigen.
Tumoren:
Epidemiologische Studien deuten darauf hin, dass die Langzeiteinnahme oraler Kontrazeptiva für Frauen, die mit dem humanen Papillomavirus (HPV) infiziert sind, das Risiko in sich birgt, ein Zervixkarzinom zu entwickeln. Es ist allerdings noch ungewiss, inwieweit dieser Befund durch andere Faktoren (wie z. B.
Anzahl der Sexualpartner oder Verwendung von mechanischen Verhütungsmitteln) beeinflusst wird.
Eine Metaanalyse von 54 epidemiologischen Studien hat ein leicht erhöhtes Brustkrebs-Risiko (RR = 1,24) für Frauen ergeben, die aktuell kombinierte orale Kontrazeptiva (KOK) anwenden. Dieses erhöhte Risiko geht innerhalb von 10 Jahren nach Absetzen der KOK allmählich wieder auf das altersentsprechende Grundrisiko zurück. Da Brustkrebs bei Frauen unter 40 Jahren selten auftritt, ist die Anzahl zusätzlicher Brustkrebserkrankungen bei Anwenderinnen von KOK oder solchen, die früher KOK eingenommen haben, gering im Vergleich zum Gesamtrisiko an Brustkrebs zu erkranken. Diese Studien liefern keine Hinweise auf Kausalität. Das beobachtete Muster eines erhöhten Risikos kann bei Anwenderinnen kombinierter oraler Kontrazeptiva auf eine frühere Diagnose von Brustkrebs, die biologischen Wirkungen von KOK oder auf eine Kombination aus beidem zurückgeführt werden. Der diagnostizierte Brustkrebs wird bei Dauer-Anwenderinnen als tendenziell geringer fortgeschritten eingestuft als bei Nicht-Anwenderinnen.
Bei Anwendung von KOK wurde selten über benigne und noch seltener über maligne Lebertumore berichtet. In Einzelfällen führten diese Tumoren zu lebensbedrohlichen intraabdominalen Blutungen. Differentialdiagnostisch sollte an einen Lebertumor gedacht werden, wenn bei Frauen, die kombinierte orale Kontrazeptiva anwenden, starke Schmerzen im Oberbauch, Lebervergrößerung oder Zeichen intraabdominaler Blutungen auftreten.
Sonstige Erkrankungen:
Frauen mit einer Hypertriglyceridämie oder einer diesbezüglich positiven Familienanamnese können ein erhöhtes Risiko für die Entwicklung einer Pankreatitis haben, wenn sie KHK einnehmen.
Obwohl bei vielen Frauen, die KOK einnehmen, ein geringer Blutdruckanstieg berichtet wurde, sind klinisch relevante Blutdruckerhöhungen selten. Nur in diesen seltenen Fällen ist eine sofortige Unterbrechung der Einnahme des KOK gerechtfertigt. Ein systematischer Zusammenhang zwischen der Anwendung von KOK und klinischer Hypertonie wurde nicht nachgewiesen. Kommt es jedoch unter Einnahme von kombinierten oralen Kontrazeptiva zu einer deutlichen Blutdruckerhöhung, sollten diese abgesetzt und eine antihypertensive Behandlung eingeleitet werden. Wenn es angemessen erscheint, kann die Einnahme des KOK wieder begonnen werden, sobald sich die Blutdruckwerte unter der antihypertensiven Therapie normalisiert haben.
Die folgenden Erkrankungen sollen Berichten zufolge sowohl in der Schwangerschaft als auch unter Anwendung eines KOK auftreten bzw. sich verschlechtern. Jedoch konnte ein Zusammenhang mit der Anwendung von KOK nicht bewiesen werden: cholestatischer Ikterus und/oder cholestasebedingter Pruritus; Gallensteinbildung; Porphyrie; systemischer Lupus erythematodes; hämolytisch-urämisches Syndrom; Sydenham-Chorea; Herpes gestationis; otosklerosebedingter Hörverlust.
Bei Frauen mit angeborenem Angioödem können exogene Östrogene Symptome eines Angioödems auslösen oder verschlimmern.
Akute oder chronische Leberfunktionsstörungen können eine Unterbrechung der Anwendung des KOKs erforderlich machen, bis sich die Leberfunktionswerte wieder normalisiert haben. Auch ein Rezidiv eines erstmals in einer vorausgegangenen Schwangerschaft aufgetretenen cholestatischen Ikterus und/oder eines in einer vorausgegangenen Schwangerschaft oder während einer früheren Anwendung von steroidalen Geschlechtshormonen cholestasebedingten Pruritus macht das Absetzen von KOK erforderlich.
Obwohl KOK einen Einfluss auf die periphere Insulinresistenz und Glucosetoleranz haben können, liegen keine Hinweise auf die Notwendigkeit einer Änderung der Therapieregime bei Diabetikerinnen vor, die KOK anwenden. Diabetikerinnen müssen jedoch während der Anwendung kombinierter oraler Kontrazeptiva sorgfältig überwacht werden, insbesondere in der frühen Phase der Anwendung kombinierter oraler Kontrazeptiva.
In Zusammenhang mit der Anwendung von KOK wurde über eine Verschlechterung von endogener Depression, Epilepsie, Morbus Crohn und Colitis ulcerosa berichtet.
Chloasmen können gelegentlich auftreten, insbesondere bei Frauen mit Chloasma gravidarum in der Anamnese. Frauen mit dieser Veranlagung sollten sich daher während der Einnahme von KOK nicht direkt der Sonne oder ultraviolettem Licht aussetzen.
Alle oben aufgeführten Informationen müssen bei der Abwägung und Auswahl einer geeigneten kontrazeptiven Methode Berücksichtigung finden.
Ärztliche Untersuchung/Beratung:
Vor der Einleitung oder Wiederaufnahme der Behandlung mit Gabrielle muss eine vollständige Anamnese (mit Erhebung der Familienanamnese) erfolgen und eine Schwangerschaft ausgeschlossen werden. Der Blutdruck sollte gemessen und eine körperliche Untersuchung durchgeführt werden, die sich an den Gegenanzeigen (siehe Abschnitt 4.3) und Warnhinweisen (siehe Abschnitt 4.4) orientiert. Es ist wichtig, die Frau auf die Informationen zu venösen und arteriellen Thrombosen hinzuweisen, einschließlich des Risikos von Gabrielle im Vergleich zu anderen KHK, die Symptome einer VTE und ATE, die bekannten Risikofaktoren und darauf, was im Falle einer vermuteten Thrombose zu tun ist.
Die Anwenderin ist zudem anzuweisen, die Packungsbeilage sorgfältig zu lesen und die darin gegebenen Ratschläge zu befolgen. Die Häufigkeit und Art der Untersuchungen sollte den gängigen Untersuchungsleitlinien entsprechen und individuell auf die Frau abgestimmt werden.
Die Anwenderinnen sind darüber aufzuklären, dass hormonale Kontrazeptiva nicht vor HIV-Infektionen (AIDS) und anderen sexuell übertragbaren Krankheiten schützen.
Verminderte Wirksamkeit:
Die Wirksamkeit von KHK kann beeinträchtigt sein, wenn z. B. Tabletten vergessen wurden (siehe Abschnitt 4.2 „Vorgehen bei vergessener Einnahme"), bei gastrointestinalen Beschwerden (siehe Abschnitt 4.2 „Verhalten bei MagenDarm-Störungen") oder wenn gleichzeitig bestimmte andere Arzneimittel eingenommen werden (siehe Abschnitt 4.5).
Pflanzliche Arzneimittel, die Johanniskraut (Hypericum perforatum) enthalten, sollten nicht gleichzeitig mit Gabrielle angewendet werden, da das Risiko besteht, dass die Plasmakonzentrationen erniedrigt werden und die Wirksamkeit von Gabrielle eingeschränkt wird (siehe Abschnitt 4.5).
Unregelmäßige Blutungen:
Bei der Anwendung von allen KOK können unregelmäßige Blutungen (Schmierund Durchbruchblutungen) auftreten, insbesondere in den ersten Monaten der Einnahme. Eine Beurteilung dieser Zwischenblutungen ist deshalb erst nach einer Einnahmedauer von ungefähr drei Monaten sinnvoll.
Bei anhaltenden Blutungsunregelmäßigkeiten oder erneutem Auftreten nach zuvor regelmäßigen Zyklen, sollten nicht-hormonale Ursachen in Betracht gezogen und geeignete diagnostische Maßnahmen zum Ausschluss einer malignen Erkrankung oder einer Schwangerschaft ergriffen werden, die auch eine Kürettage beinhalten können.
Bei einigen Anwenderinnen kann die Entzugsblutung während der Einnahmepause ausbleiben. Wenn das KOK gemäß den Anweisungen im Abschnitt 4.2 eingenommen wurde, ist es unwahrscheinlich, dass die Frau schwanger ist. Wenn das KOK jedoch vor der ersten ausbleibenden Entzugsblutung nicht gemäß diesen Anweisungen eingenommen wurde oder die Entzugsblutung in zwei aufeinanderfolgenden Zyklen ausbleibt, muss vor der weiteren Anwendung des KOK eine Schwangerschaft ausgeschlossen werden.
Gabrielle enthält Lactose. Anwenderinnen mit der seltenen hereditären Galactose-Intoleranz, Lactase-Mangel oder Glucose-Galactose-Malabsorption sollten dieses Arzneimittel nicht einnehmen.
4.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen
Hinweis: Die Fachinformationen gleichzeitig verabreichter Arzneimittel sollten auf mögliche Wechselwirkungen überprüft werden.
Wechselwirkungen
Wechselwirkungen zwischen oralen Kontrazeptiva und anderen Arzneimitteln können zu Durchbruchblutungen und/oder Versagen der Kontrazeption führen. Die folgenden Wechselwirkungen wurden in der Literatur berichtet.
Leberstoffwechsel:
Wechselwirkungen können bei gleichzeitiger Gabe von Arzneimitteln mit leberenzyminduzierenden Eigenschaften auftreten, die eine erhöhte Clearance von Sexualhormonen bewirken (z. B. Hydantoine, Barbiturate, Primidon, Carbamazepin, Rifampicin, Bosentan, Rifabutin sowie möglicherweise auch Oxcarbazepin, Modafinil, Topiramat, Felbamat, Griseofulvin und Produkte, die das pflanzliche Arzneimittel Johanniskraut (Hypericum perforatum) enthalten). Zudem können HIV-Proteaseinhibitoren mit induzierendem Potenzial (z. B. Ritonavir und Nelfinavir) sowie nichtnukleosidische Reverse-Transkriptase-Inhibitoren (z. B. Nevirapin und Efavirenz) den Leberstoffwechsel beeinflussen.
Vorgehen:
Eine Enzyminduktion kann bereits nach wenigen Behandlungstagen beobachtet werden. Die maximale Enzyminduktion tritt üblicherweise innerhalb weniger Wochen auf. Nach Beendigung der Arzneimitteltherapie kann die Enzyminduktion für ca. 4 Wochen anhalten.
Kurzzeitbehandlung:
Frauen, die mit einem enzyminduzierenden Arzneimittel behandelt werden, sollten zusätzlich zu dem KOK vorübergehend eine Barrieremethode oder eine andere Verhütungsmethode anwenden.
Die Barrieremethode muss während der gesamten Dauer der gleichzeitigen medikamentösen Therapie und weitere 28 Tage nach Beendigung der Therapie angewendet werden.
Falls die medikamentöse Behandlung länger dauert, als Tabletten in der aktuellen KOK-Packung enthalten sind, sollte mit der nächsten KOK-Packung unmittelbar nach der Vorherigen ohne die übliche Einnahmepause begonnen werden.
Langzeitbehandlung:
Für Frauen, die eine Langzeitbehandlung mit enzyminduzierenden Wirkstoffen durchführen, wird eine andere zuverlässige, nicht-hormonale Verhütungsmethode empfohlen.
Einfluss von Gabrielle auf andere Arzneimittel
Orale Kontrazeptiva können den Metabolismus bestimmter anderer Wirkstoffe beeinflussen. Dementsprechend können Plasma- und Gewebekonzentrationen ansteigen (z. B. Ciclosporin) oder abnehmen (z. B. Lamotrigin).
Labortests:
Die Anwendung von steroidalen Kontrazeptiva kann die Ergebnisse bestimmter Labortests beeinflussen, u. a. die biochemischen Parameter der Leber-, Schilddrüsen-, Nebennieren- und Nierenfunktion sowie die Plasmaspiegel von (Träger-)Proteinen, z. B. des corticosteroidbindenden Globulins und der Lipid/Lipoprotein-Fraktionen, der Parameter des Kohlenhydratstoffwechsels sowie der Gerinnungs- und Fibrinolyseparameter. Im Allgemeinen bleiben diese Veränderungen jedoch innerhalb des Normbereichs.
4.6 Fertilität, Schwangerschaft und Stillzeit
Schwangerschaft
Gabrielle ist während der Schwangerschaft nicht indiziert.
Falls während der Anwendung von Gabrielle eine Schwangerschaft eintritt, ist das Arzneimittel abzusetzen. In den meisten epidemiologischen Untersuchungen fand sich jedoch weder ein erhöhtes Risiko für Missbildungen bei Kindern, deren Mütter vor der Schwangerschaft KOK eingenommen hatten, noch eine teratogene Wirkung bei versehentlicher Einnahme von KOK in der Frühschwangerschaft.
Das erhöhte VTE-Risiko in der Zeit nach der Geburt sollte vor der erneuten Anwendung von Gabrielle nach einer Anwendungspause bedacht werden (siehe Abschnitte 4.2 und 4.4).
Stillzeit
KOK können die Laktation beeinflussen, da sie die Menge der Muttermilch vermindern und ihre Zusammensetzung verändern können. Daher wird die
Anwendung von KOK generell nicht empfohlen, solange die stillende Mutter ihr Kind nicht vollständig abgestillt hat. Geringe Mengen der kontrazeptiven Steroide und/oder ihrer Metaboliten können zwar in die Muttermilch ausgeschieden werden, Hinweise auf nachteilige Auswirkungen auf die Gesundheit des Kindes liegen jedoch nicht vor.
4.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen
Es wurden keine Studien zu den Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen durchgeführt. Bei Anwenderinnen von KOK wurden keine Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen beobachtet.
4.8 Nebenwirkungen
Wie bei allen KOK können Veränderungen des vaginalen Blutungsmusters auftreten, insbesondere während der ersten Monate der Anwendung. Dies kann Änderungen der Häufigkeit (ausbleibend, seltener, häufiger oder kontinuierlich), Intensität (erhöht oder vermindert) oder Dauer der Blutung beinhalten.
Nebenwirkungen, die möglicherweise mit der Anwendung von Desogestrel/Ethinylestradiol oder anderen KOK in Zusammenhang stehen, sind in der nachfolgenden Tabelle aufgelistet1. Alle Nebenwirkungen sind nach Systemorganklasse und Häufigkeit aufgeführt: Sehr häufig (>1/10), häufig (>1/100 bis <1/10), gelegentlich (>1/1.000 bis <1/100) und selten (>1/10.000 bis <1/1.000).
|
Systemorgan klasse |
Sehr häufig |
Häufig |
Gelegentlich |
Selten |
|
Infektionen und parasitäre Erkrankungen |
Vaginale Candidiasis | |||
|
Erkrankungen des Immunsystems |
Überempfindli chkeit | |||
|
Stoffwechsel-und Ernährungsstörungen |
Flüssigkeitsret ention | |||
|
Psychiatrische Erkrankungen |
depressive Verstimmung, Stimmungssc hwankungen |
verminderte Libido |
erhöhte Libido | |
|
Erkrankungen des Nervensystems |
Kopfschmerze n, Schwindel, Nervosität |
Migräne | ||
|
Augenerkran kungen |
Kontaktlinsen unverträglichk eit | |||
|
Erkrankungen des Ohrs und des Labyrinths |
Otosklerose | |||
|
Gefäßerkran kungen |
Hypertonie |
Thromboemb olie (VTE oder ATE) | ||
|
Erkrankungen des Gastrointestinaltrakts |
Übelkeit, Bauchschmer zen |
Erbrechen, Durchfall |
|
Erkrankungen der Haut und des Unterhautzellgewebes |
Akne |
Hautaus schlag, Urtikaria |
Erythema nodosum, Erythema multiforme, Pruritus, Alopezie | |
|
Erkrankungen der Geschlechtsorgane und der Brustdrüse |
Unregelmäßig e Blutungen |
Brustschmerz en, Empfindlichkei t der Brüste, Amenorrhoe, Metrorrhagie |
Brust vergrößerung |
Genitaler Ausfluss, Sekretion aus der Brustdrüse |
|
Untersuchungen |
Gewichtszuna hme |
Gewichtsabna hme |
1 In der Tabelle ist der passendste MedDRA Terminus zur Beschreibung einer bestimmten unerwünschten Arzneimittelwirkung aufgeführt. Synonyme oder ähnliche Erkrankungsbilder sind nicht aufgeführt, sollten jedoch ebenfalls in Betracht gezogen werden.
Beschreibung ausgewählter Nebenwirkungen
Bei Anwenderinnen von KHK wurde ein erhöhtes Risiko für arterielle und venöse thrombotische und thromboembolische Ereignisse einschließlich Myokardinfarkt, Schlaganfall, transitorische ischämische Attacken, Venenthrombose und Lungenembolie beobachtet, die in Abschnitt 4.4 eingehender behandelt werden.
Bei Anwenderinnen von KHK wird über folgende schwerwiegende Nebenwirkungen berichtet, die ebenfalls im Abschnitt 4.4. erläutert werden:
- Hypertonie;
- Hormonabhängige Tumore (z. B. Lebertumor, Brustkrebs, Gebärmutterhalskrebs);
- Auftreten oder Verschlechterung von Erkrankungen, für die ein Zusammenhang mit der Anwendung von oralen Kontrazeptiva nicht schlüssig ist: Morbus Crohn, Colitis ulcerosa, Epilepsie, Migräne, Endometriose, Uterusmyome, Porphyrie, systemischer Lupus erythematodes, Herpes gestationis, Sydenham-Chorea, hämolytischurämisches Syndrom, cholestatischer Ikterus;
- Chloasma;
- Akute oder chronische Leberfunktionsstörungen können das Absetzen der KOK notwendig machen bis sich die Leberfunktionswerte wieder normalisiert haben;
- Bei Frauen mit angeborenem Angioödem können exogene Östrogene die Symptome eines Angioödems auslösen oder verschlimmern.
Bei Anwenderinnen von oralen Kontrazeptiva ist die Häufigkeit einer Brustkrebsdiagnose sehr leicht erhöht. Da Brustkrebs bei Frauen unter 40 Jahren selten auftritt, ist die Anzahl zusätzlicher Brustkrebserkrankungen gering im Vergleich zum Gesamtrisiko, an Brustkrebs zu erkranken. Eine Kausalität mit der Anwendung kombinierter oraler Kontrazeptiva ist nicht bekannt. Für weitere Informationen, siehe Abschnitte 4.3 und 4.4.
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des NutzenRisiko-Verhältnisses des Arzneimittels.
Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung dem Bundesinstitut für Arzneimittel und Medizinprodukte, Abt. Pharmakovigilanz, Kurt-Georg-Kiesinger-Allee 3, D-53175 Bonn, Website: www.bfarm.de anzuzeigen.
4.9 Überdosierung
Es liegen keine Meldungen über schwerwiegende Folgen bei Überdosierung vor. Symptome einer Überdosierung sind: Übelkeit, Erbrechen und, bei jungen Mädchen, leichte vaginale Blutungen. Es gibt kein Antidot und die weitere Behandlung sollte symptomatisch erfolgen.
5. Pharmakologische Eigenschaften
5.1 Pharmakodynamische Eigenschaften
Pharmakotherapeutische Gruppe: Gestagene und Östrogene, fixe Kombinationen, ATC-Code: G03A A09
Die empfängnisverhütende Wirkung von KOK beruht auf einer Interaktion verschiedener Faktoren, wobei die Ovulationshemmung und die Veränderungen der zervikalen Sekretion als die wichtigsten Faktoren anzusehen sind. Neben dem Schutz vor einer Schwangerschaft haben KOK verschiedene positive Eigenschaften, die abgesehen von den negativen Eigenschaften (siehe Abschnitte 4.4 und 4.8), bei der Entscheidung über die Methode der Geburtenkontrolle nützlich sein können. Der Zyklus wird regelmäßiger, die Menstruation oft weniger schmerzhaft und die Blutungen leichter. Letzteres kann zu einem Rückgang des Vorkommens von Eisenmangel führen. In der größten multizentrischen Studie (n=23.258 Zyklen) wird der unkorrigierte Pearl-Index auf 0,1 (95 % Konfidenzintervall 0,0-0,3) geschätzt. Darüber hinaus berichteten 4,5 % der Frauen über ein Ausbleiben der Entzugsblutungen und 9,2 % berichteten über unregelmäßige Blutungen nach 6 Behandlungszyklen.
Gabrielle ist ein kombiniertes orales Kontrazeptivum mit Ethinylestradiol und dem Gestagen Desogestrel. Ethinylestradiol ist ein gut bekanntes synthetisches Östrogen. Desogestrel ist ein synthetisches Progestogen. Nach oraler Verabreichung ist es stark ovulationshemmend.
Die Anwendung von höher dosierten KOK (50 ^g Ethinylestradiol) verringert das Risiko für Endometrium- und Ovarialkarzinom. Ob dies auch für niedriger dosierte KOK gilt, muss noch bestätigt werden.
Kinder und Jugendliche
Es liegen keine klinischen Daten zur Sicherheit und Wirksamkeit bei Kindern und Jugendlichen unter 18 Jahren vor.
5.2 Pharmakokinetische Eigenschaften
Desogestrel
Resorption
Nach oraler Verabreichung von Gabrielle wird Desogestrel rasch und vollständig resorbiert und in Etonogestrel umgewandelt. Maximale Plasmaspiegel von ca. 2 ng/ml werden nach 1,5 Stunden erreicht. Die Bioverfügbarkeitbeträgt 62-81 %.
Verteilung
Etonogestrel bindet an Plasmaproteine, im Wesentlichen an Serumalbumin und sexualhormonbindendes Globulin (SHBG). Nur 2 bis 4 % der Gesamtkonzentration im Serum sind freies Steroid, 40 bis 70 % sind spezifisch an SHBG gebunden. Die Ethinylestradiol-bedingte Zunahme der SHbG-Konzentration beeinflusst die relative Bindung an Serumproteine, was zu einem Anstieg der SHBG-Bindung und zu einer Abnahme der Albumin-Bindung führt. Das Verteilungsvolumen von Desogestrel beträgt 1,5 l/kg.
Biotransformation
Etonogestrel wird vollständig über die bekannten Wege des Steroidabbaus metabolisiert. Etonogestrel wird reduziert und seine Abbauprodukte werden zu Sulfat und Glucuroniden konjugiert. Die metabolische Clearance von Etonogestrel aus dem Serum beträgt ca. 2 ml/min/kg. Aus Tierstudien ergeben sich Hinweise, dass der enterohepatische Kreislauf für die gestagene Aktivität von Desogestrel irrelevant ist. Es wurden keine Interaktionen bei gleichzeitiger Verabreichung von Ethinylestradiol gefunden.
Elimination
Die Etonogestrel-Serumspiegel nehmen zweiphasig ab. Die terminale Eliminationsphase ist charakterisiert durch eine Halbwertszeit von ca. 30 Stunden und die Plasma-Clearance liegt zwischen 5,0 und 9,5 l Stunde. Desogestrel und seine Metaboliten werden mit dem Harn und der Galle in einem Verhältnis von ca. 6 : 4 ausgeschieden.
Steady-State-Bedingungen
Die Pharmakokinetik von Etonogestrel wird durch die SHBG-Spiegel beeinflusst, die durch Ethinylestradiol um das Dreifache erhöht werden. Bei täglicher Einnahme nehmen die Serumspiegel um etwa das Zwei- bis Dreifache zu, wobei der Steady-State in der zweiten Hälfte des Verabreichungszyklus erreicht wird.
Ethinylestradiol
Resorption
Ethinylestradiol wird nach oraler Verabreichung rasch und vollständig resorbiert. Nach der Einnahme einer Einzeldosis werden maximale Plasmaspiegel von ca. 80 pg/ml nach 1 bis 2 Stunden erreicht. Die absolute Bioverfügbarkeit beträgt infolge präsystemischer Konjugatbildung und des First-Pass-Effekts ca. 60 %.
Verteilung
Ethinylestradiol ist zu einem Großteil, aber unspezifisch, an Serumalbumin gebunden (ca. 98,5 %) und verursacht eine Zunahme der Serumkonzentration von SHBG. Das Verteilungsvolumen beträgt ca. 5 l/kg.
Biotransformation
Ethinylestradiol wird präsystemisch sowohl in der Schleimhaut des Dünndarms als auch in der Leber konjugiert. Ethinylestradiol wird primär durch aromatische Hydroxylierung verstoffwechselt und in eine Vielzahl von hydroxylierten und methylierten Metaboliten umgewandelt, die sowohl in freier Form als auch als Glucuronide und Sulfate vorliegen. Die metabolische Clearance von Ethinylestradiol aus dem Serum beträgt ca. 5 ml/min/kg.
Elimination
Der Ethinylestradiol-Serumspiegel nehmen zweiphasig ab; die terminale Dispositionsphase ist charakterisiert durch eine Halbwertszeit von ca. 24 Stunden. Ethinylestradiol wird nicht in unveränderter Form ausgeschieden. Die Metaboliten von Ethinylestradiol werden mit dem Harn und der Galle im Verhältnis von 4 : 6 mit einer Halbwertszeit von ca. 1 Tag eliminiert.
Steady-State Bedingungen
Der Steady-State wird nach 3 bis 4 Tagen erreicht, wobei die Serumkonzentration ca. 30 bis 40 % höher als nach der Verabreichung einer Einzeldosis ist.
5.3 Präklinische Daten zur Sicherheit
Präklinische Daten zeigen kein spezielles Risiko für den Menschen, wenn KHK wie empfohlen angewendet werden. Diese Aussage stützt sich auf konventionelle Studien zur chronischen Toxizität, zur Genotoxizität, zum kanzerogenen Potenzial und zur Reproduktionstoxizität. Jedoch muss berücksichtigt werden, dass Sexualsteroide das Wachstum gewisser hormonabhängiger Gewebe und Tumoren fördern können.
6. Pharmazeutische Angaben
6.1 Liste der sonstigen Bestandteile
all-rac-alpha-T ocopherol Kartoffelstärke Povidon K30
Stearinsäure (Ph.Eur.) [pflanzlich]
Hochdisperses Siliciumdioxid Lactose
6.2 Inkompatibilitäten
Nicht zutreffend.
6.3 Dauer der Haltbarkeit
2 Jahre
6.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung
Nicht über 25°C lagern. In der Originalverpackung aufbewahren, um den Inhalt vor Feuchtigkeit und Licht zu schützen.
6.5 Art und Inhalt des Behältnisses
Klar-transparente PVC/PVdC-Aluminium-Blisterpackungen mit 21 Tabletten pro Kalender-Blisterpackung in Packungen mit 1x21, 3x21 oder 6x21 Tabletten.
Jede Blisterpackung ist in einem 3-fach laminierten Beutel verpackt.
Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht.
6.6 Besondere Vorsichtsmaßnahmen für die Beseitigung und sonstige Hinweise zur Handhabung
Keine besonderen Anforderungen.
Nicht verwendetes Arzneimittel oder Abfallmaterial ist entsprechend den nationalen Anforderungen zu entsorgen.
7. Inhaber der Zulassung
Mylan dura GmbH Postfach 10 06 35 64206 Darmstadt
8. Zulassungsnummern
Gabrielle-20 0,15 mg/0,02 mg Tabletten: Zul.-Nr.: 83176.00.00 Gabrielle-30 0,15 mg/0,03 mg Tabletten: Zul.-Nr.: 83177.00.00
9. Datum der Erteilung der Zulassung
Datum der Erteilung der Zulassung: 18. April 2012
10. Stand der Information
August 2016
11 Verkaufsabgrenzung
Verschreibungspflichtig
Diese Inzidenzen wurden aus der Gesamtheit der epidemiologischen Studiendaten abgeleitet, wobei relative Risiken der verschiedenen Arzneimittel im Vergleich zu Levonorgestrel-haltigen KHK verwendet wurden.
Mittelwert der Spannweite 5-7 pro 10.000 Frauenjahre, auf der Grundlage eines relativen Risikos für Levonorgestrel-haltige KHK versus Nichtanwendung von ungefähr 2,3 bis 3,6