Ingelvac Mycoflex
GEBRAUCHSINFORMATION
Ingelvac MycoFLEX Injektionssuspension für Schweine
1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN
UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE VERANTWORTLICH IST
Zulassungsinhaber und Hersteller, der für die Chargenfreigabe verantwortlich ist Boehringer Ingelheim Vetmedica GmbH 55216 Ingelheim/Rhein Deutschland
2. BEZEICHNUNG DES TIERARZNEIMITTELS
Ingelvac MycoFLEX Injektionssuspension für Schweine
3. WIRKSTOFF UND SONSTIGE BESTANDTEILE
Mycoplasma hyopneumoniae, J Stamm, Isolat B-3745 inaktiviert.
Eine Dosis (1 ml) des inaktivierten Impfstoffes enthält:
Mycoplasma hyopneumoniae: > 1 RP*
* Relative Wirksamkeit (ELISA-Test) im Vergleich mit einer Referenzvakzine
Adjuvans: Carbomer
Klare bis leicht opalisierende, rosafarbene bis braune Injektionssuspension.
4. ANWENDUNGSGEBIET
Zur aktiven Immunisierung von Schweinen ab einem Alter von 3 Wochen zur Reduktion von Lungenläsionen infolge einer Infektion mit Mycoplasma hyopneumoniae.
Beginn der Immunität: 2 Wochen nach Impfung
Dauer der Immunität: mindestens 26 Wochen
5. GEGENANZEIGEN
Keine.
6. NEBENWIRKUNGEN
Nebenwirkungen sind sehr selten (weniger als 1 von 10.000 behandelten Tieren, einschließlich Einzelfallberichte):
- Anaphylaktische oder anaphylaktoide Reaktionen können auftreten und sollten symptomatisch behandelt werden (z.B. Epinephrin).
- An der Injektionsstelle können vorübergehend Schwellungen bis zu vier Zentimeter Durchmesser, gelegentlich auch Hautrötungen beobachtet werden. Diese Schwellungen können bis zu 5 Tage anhalten.
- Nach der Impfung kann ein vorübergehender Anstieg der rektalen Körpertemperatur von durchschnittlich etwa 0,8°C beobachtet werden, der bis zu 20 Stunden anhält.
Die Angaben zur Häufigkeit von Nebenwirkungen sind folgendermaßen definiert:
- Sehr häufig (mehr als 1 von 10 behandelten Tieren zeigen Nebenwirkungen während der Behandlung)
- Häufig (mehr als 1 aber weniger als 10 von 100 behandelten Tieren)
- Gelegentlich (mehr als 1 aber weniger als 10 von 1000 behandelten Tieren)
- Selten (mehr als 1 aber weniger als 10 von 10.000 behandelten Tieren)
- Sehr selten (weniger als 1 von 10.000 behandelten Tieren, einschließlich Einzelfallberichte).
Falls Sie Nebenwirkungen insbesondere solche, die nicht in der Packungsbeilage aufgeführt sind, bei
Ihrem Tier feststellen, teilen Sie diese Ihrem Tierarzt mit.
7. ZIELTIERART
Schweine (Mastschweine oder zukünftige Zuchtschweine bis zur ersten Belegung).
8. DOSIERUNG FÜR JEDE ZIELTIERART, ART UND DAUER DER ANWENDUNG
Schweine ab einem Alter von 3 Wochen: einmalige intramuskuläre (i.m.) Injektion einer Dosis (1 ml), vorzugsweise in den Nacken.
9. HINWEISE FÜR DIE RICHTIGE ANWENDUNG
Vor Gebrauch gut schütteln.
Verunreinigungen (Kontaminationen) während der Entnahme und Anwendung des Impfstoffes sind zu vermeiden.
Mehrmaliges Anstechen des Impfstoffbehältnisses ist zu vermeiden.
Impfgeräte sind gemäß der Bedienungsanleitung des Herstellers der Impfgeräte zu benutzen.
Benutzen Sie Impfgeräte mit einer Rückflusssperre für das Tierarzneimittel.
Beim Mischen mit Ingelvac CircoFLEX:
• nur Schweine ab einem Alter von drei Wochen impfen.
Beim Mischen mit Ingelvac CircoFLEX sollten folgende Materialien benutzt werden:
• Verwenden Sie dieselben Volumina von Ingelvac CircoFLEX und Ingelvac MycoFLEX.
• Verwenden Sie eine sterilisierte Transfernadel. Sterilisierte Transfernadeln (CE zertifiziert) sind im Medizingeräte-Handel erhältlich.
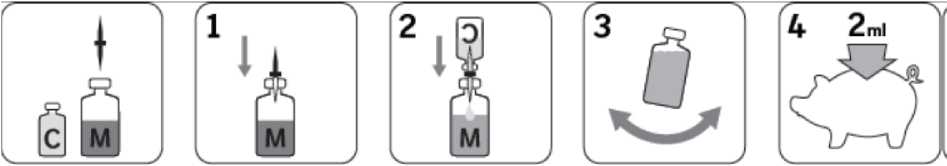
Um korrekt zu mischen, folgen Sie den unten beschriebenen Schritten:
1. Stechen Sie das eine Ende der Transfernadel in die Ingelvac MycoFLEX Impfstoffflasche.
2. - Stechen Sie das andere Ende der Transfernadel in die Ingelvac CircoFLEX
Impfstoffflasche.
- Überführen Sie den Impfstoff Ingelvac CircoFLEX in die Ingelvac MycoFLEX Impfstoffflasche. Falls nötig, drücken Sie die Ingelvac CircoFLEX Impfstoffflasche behutsam, um die Überführung zu erleichtern.
- Nach dem Transfer des gesamten Inhalts von Ingelvac CircoFLEX entfernen und entsorgen Sie die Transfernadel und die leere Ingelvac CircoFLEX Impfstoffflasche.
3. Um eine homogene Mischung der Impfstoffe sicherzustellen, schwenken Sie die Ingelvac MycoFLEX Impfstoffflasche vorsichtig, bis die Mischung eine einheitliche orange bis rötliche Färbung aufweist. Während der Impfung ist die einheitliche Färbung der Mischung zu überwachen und durch ständige Bewegung aufrecht zu erhalten.
4. Verabreichen Sie eine Impfdosis (2 ml) der Mischung pro Schwein intramuskulär, unabhängig vom Körpergewicht. Bei der Anwendung sind Impfgeräte gemäß der Bedienungsanleitung des Herstellers der Impfgeräte zu benutzen.
Die komplette Impfstoffmischung ist sofort nach dem Mischen anzuwenden. Nicht verwendete Reste der Mischung oder Abfallmaterialien sind entsprechend den nationalen Vorschriften zu entsorgen.
Vor der Anwendung der Impfstoffmischung sollte auch die Packungsbeilage von Ingelvac CircoFLEX zu Rate gezogen werden.
Falls weitere Informationen gewünscht werden, setzen Sie sich bitte mit dem örtlichen Vertreter des Zulassungsinhabers in Verbindung.
10. WARTEZEIT
Null Tage.
11. BESONDERE LAGERUNGSHINWEISE
Arzneimittel unzugänglich für Kinder aufbewahren.
Kühl lagern und transportieren (2°C - 8°C).
Nicht einfrieren.
Vor Licht schützen.
Sie dürfen das Tierarzneimittel nach dem auf der Faltschachtel und der Flasche angegebenen Verfalldatum nicht mehr anwenden.
Haltbarkeit nach Anbruch des Behältnisses: 10 Stunden.
12. BESONDERE WARNHINWEISE
Besondere Vorsichtsmaßnahmen für die Anwendung bei Tieren:
Nur klinisch gesunde Tiere impfen.
Bei Auftreten anaphylaktischer oder anaphylaktoider Reaktionen wird die Verabreichung von Epinephrin empfohlen.
Anwendung während der Trächtigkeit und Laktation:
Nicht zutreffend.
Wechselwirkungen mit anderen Arzneimitteln und andere Wechselwirkungen:
Daten zur Unschädlichkeit und Wirksamkeit belegen, dass dieser Impfstoff mit dem Impfstoff Ingelvac CircoFLEX von Boehringer Ingelheim gemischt und verabreicht werden kann.
Es liegen keine Informationen zur Unschädlichkeit und Wirksamkeit des Impfstoffes bei gleichzeitiger Anwendung eines anderen veterinärmedizinischen Produktes mit Ausnahme des oben genannten vor. Ob der Impfstoff vor oder nach Verabreichung eines anderen veterinärmedizinischen Produktes verwendet werden sollte, muss daher fallweise entschieden werden.
Überdosierung (Symptome, Notfallmaßnahmen. Gegenmittel):
Nach Verabreichung der vierfachen Dosis des Impfstoffes wurden keine anderen als die beschriebenen Nebenwirkungen beobachtet.
Inkompatibilitäten:
Nicht mit anderen Tierarzneimitteln mischen. außer mit Ingelvac CircoFLEX von Boehringer Ingelheim.
13. BESONDERE VORSICHTSMAßNAHMEN FÜR DIE ENTSORGUNG VON NICHT VERWENDETEM ARZNEIMITTEL ODER VON ABFALLMATERIAL, SOFERN ERFORDERLICH
Nicht verwendete Tierarzneimittel oder davon stammende Abfallmaterialien sind entsprechend den nationalen Vorschriften zu entsorgen.
14. GENEHMIGUNGSDATUM DER GEBRAUCHSINFORMATION
Februar 2014
15. WEITERE ANGABEN
Der Impfstoff ist dazu bestimmt. eine aktive Immunantwort gegen Mycoplasma hyopneumoniae zu induzieren.
1 oder 12 Flaschen mit 10 ml Impfstoff (10 Dosen in 30 ml Nennvolumen). 50 ml (50 Dosen in 120 ml Nennvolumen). 100 ml (100 Dosen in 250 ml Nennvolumen) oder 250 ml (250 Dosen in 500 ml Nennvolumen). in einer Pappschachtel verpackt.
Es werden möglicherweise nicht alle Packungsgrößen in Verkehr gebracht.
Österreich: Z. Nr.: 8-20319. Rezept- und apothekenpflichtig.
Deutschland: Zul.-Nr. PEI.V.04758.01.1. Verschreibungspflichtig.
Falls weitere Informationen über das Tierarzneimittel gewünscht werden. setzen Sie sich bitte mit dem örtlichen Vertreter des Zulassungsinhabers in Verbindung.
Österreich: Deutschland:
Boehringer Ingelheim RCV GmbH & Co KG Boehringer Ingelheim Vetmedica GmbH
Animal Health Binger Str. 173
Dr. Boehringer-Gasse 5-11 55216 Ingelheim/Rhein
1121 Wien Tel. +49-(0) 6132 77 92 999
Tel. +43- (0) 1 80 105 0