Leona Hexal 0,10 Mg/0,02 Mg Überzogene Tabletten
Fachinformation
1. BEZEICHNUNG DES ARZNEIMITTELS
Leona HEXAL 0,10 mg/0,02 mg überzogene Tabletten
2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
1 überzogene Tablette enthält 0,10 mg Levonorgestrel und 0,02 mg Ethinylestradiol.
Sonstige Bestandteile mit bekannter Wirkung: 1 überzogene Tablette enthält 30,17 mg Lactose (als Lactose-Monohydrat) und 19,66 mg Sucrose.
Vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt 6.1.
3. DARREICHUNGSFORM
Überzogene Tablette
Weiße, runde, bikonvexe und überzogene Tablette
4. KLINISCHE ANGABEN
4.1 Anwendungsgebiete
Orale Kontrazeption
Bei der Entscheidung, Leona HEXAL zu verschreiben, sollten die aktuellen, individuellen Risikofaktoren der einzelnen Frauen, insbesondere im Hinblick auf venöse Thromboembolien (VTE), berücksichtigt werden. Auch sollte das Risiko für eine VTE bei Anwendung von Leona HEXAL mit dem anderer kombinierter hormonaler Kontrazeptiva (KHK) verglichen werden (siehe Abschnitte 4.3 und 4.4).
4.2 Dosierung und Art der Anwendung
Dosierung
Die Tabletten müssen jeden Tag etwa zur gleichen Zeit, falls erforderlich mit etwas Flüssigkeit, in der auf der Blisterpackung angegebenen Reihenfolge eingenommen werden. An 21 aufeinander folgenden Tagen muss jeweils 1 Tablette täglich eingenommen werden. Mit der Einnahme der Tabletten aus der nächsten Blisterpackung wird nach einer 7-tägigen Einnahmepause begonnen, in der es üblicherweise zu einer Abbruchblutung kommt. Diese beginnt in der Regel 2-3 Tage nach Einnahme der letzten Tablette und kann noch andauern, wenn mit der Einnahme aus der nächsten Blisterpackung begonnen wird.
Beginn der Einnahme von Leona HEXAL
Keine vorherige Einnahme hormonaler Kontrazeptiva im letzten Monat
Mit der Tabletteneinnahme ist am 1. Tag des natürlichen Zyklus (d. h. am 1. Tag
der Menstruationsblutung) zu beginnen. Wenn die Einnahme zwischen Tag 2 und 5 begonnen wird, ist während der ersten 7 Tage des Einnahmezyklus eine zusätzliche nicht-hormonale Verhütungsmethode erforderlich.
Wechsel von einem anderen kombinierten hormonalen Kontrazeptivum (kombiniertes orales Kontrazeptivum [KOK], Vaginalring, transdermales Pflaster) Mit der Einnahme von Leona HEXAL wird am Tag nach dem üblichen tablettenfreien (ringfreien, pflasterfreien) Intervall beziehungsweise am Tag nach der Einnahme der letzten wirkstofffreien Tablette des zuvor eingenommenen Kombinationspräparates begonnen.
Wechsel von einem Gestagenmonopräparat (Minipille, Injektion, Implantat) oder von einem Intrauterinsystem (IUS)
Bei vorheriger Einnahme der Minipille kann an jedem beliebigen Tag gewechselt werden. Die Umstellung von einem Implantat oder Intrauterinsystem muss am Tag der Entfernung erfolgen, die von einem Injektionspräparat zu dem Zeitpunkt, an dem die nächste Injektion fällig wäre. Jedoch ist in allen Fällen während der ersten 7 Tage der Einnahme von Leona HEXAL eine zusätzliche nicht-hormonale Verhütungsmethode erforderlich.
Nach einem Abort im 1. Trimenon
Es kann sofort mit der Einnahme von Leona HEXAL begonnen werden. In diesem Fall sind keine zusätzlichen empfängnisverhütenden Maßnahmen erforderlich.
Nach einer Geburt oder einem Abort im 2. Trimenon Anwendung in der Stillzeit siehe Abschnitt 4.6
Die Einnahme sollte an den Tagen 21-28 nach einer Geburt oder nach einem Abort im 2. Trimenon begonnen werden. Bei einem späteren Einnahmebeginn muss während der ersten 7 Tage der Tabletteneinnahme zusätzlich eine Barrieremethode angewendet werden. Wenn jedoch bereits Geschlechtsverkehr stattgefunden hat, muss vor Beginn der Einnahme eine Schwangerschaft ausgeschlossen oder die erste Menstruationsblutung abgewartet werden.
Vorgehen bei vergessener Tabletteneinnahme
Leona HEXAL enthält eine sehr niedrige Dosierung der beiden Hormone und demzufolge ist die Spanne der kontrazeptiven Wirkung sehr eng, wenn 1 Tablette vergessen wurde.
Wird die Tablette innerhalb von 12 Stunden nach dem üblichen Einnahmezeitpunkt eingenommen, ist der kontrazeptive Schutz nicht eingeschränkt. Die Einnahme der vergessenen Tablette soll in diesem Fall sofort nachgeholt werden. Alle darauf folgenden Tabletten sind dann wieder zur gewohnten Zeit einzunehmen.
Wenn der Einnahmezeitpunkt um mehr als 12 Stunden überschritten wurde, kann der Konzeptionsschutz vermindert sein. Die Wahrscheinlichkeit einer Schwangerschaft ist umso höher, je näher die vergessene Tablette an dem einnahmefreien Intervall liegt.
Bei vergessenen Tabletteneinnahmen sind grundsätzlich 2 Punkte zu beachten:
1. Die Tabletteneinnahme darf nicht länger als 7 Tage unterbrochen werden.
2. Um eine ausreichende Suppression des Hypothalamus-Hypophysen-Ovarialsystems zu erreichen, ist eine Tabletteneinnahme über mindestens 7 Tage erforderlich.
Daraus ergibt sich folgendes Vorgehen:
1. Woche
Die Anwenderin sollte die letzte vergessene Tablette einnehmen, sobald sie merkt, dass sie diese vergessen hat, selbst wenn dies bedeutet, dass sie 2 Tabletten zur gleichen Zeit einnimmt. Die weitere Tabletteneinnahme erfolgt dann zur gewohnten Zeit. In den nächsten 7 Tagen soll jedoch zusätzlich eine Barrieremethode, z. B. ein Kondom, angewendet werden. Wenn in den vorausgegangenen 7 Tagen Geschlechtsverkehr stattgefunden hat, sollte die Möglichkeit einer Schwangerschaft in Betracht gezogen werden. Das Risiko einer Schwangerschaft ist umso höher, je mehr Tabletten vergessen wurden und je näher dies zeitlich am regulären einnahmefreien Intervall liegt.
2. Woche
Die Anwenderin sollte die letzte vergessene Tablette einnehmen, sobald sie bemerkt, dass sie diese vergessen hat, auch wenn dies bedeutet, dass 2 Tabletten zur gleichen Zeit einzunehmen sind. Die weitere Einnahme der Tabletten erfolgt dann zur üblichen Zeit. Vorausgesetzt, dass die Einnahme der Tabletten an den 7 Tagen vor der ersten vergessenen Tablette korrekt erfolgt ist, besteht keine Notwendigkeit, zusätzliche Maßnahmen zur Empfängnisverhütung anzuwenden. War dies nicht der Fall, soll die Anwendung zusätzlicher kontrazeptiver Maßnahmen über 7 Tage empfohlen werden.
3. Woche
Aufgrund des bevorstehenden 7-tägigen einnahmefreien Intervalls ist ein voller Konzeptionsschutz nicht mehr gewährleistet. Jedoch lässt sich eine Herabsetzung der empfängnisverhütenden Wirkung durch eine Anpassung des Einnahmeschemas verhindern. Bei Einhalten einer der beiden folgenden Vorgehensweisen besteht daher keine Notwendigkeit zusätzlicher kontrazeptiver Maßnahmen, vorausgesetzt, die Tabletteneinnahme an den 7 Tagen vor der ersten vergessenen Tablette erfolgte korrekt. Wenn dies nicht der Fall ist, soll die Anwenderin wie unter Punkt 1 beschrieben vorgehen und außerdem in den nächsten 7 Tagen zusätzliche Maßnahmen zur Empfängnisverhütung anwenden.
1. Die Anwenderin soll die Einnahme der letzten vergessenen Tablette so schnell wie möglich nachholen, auch wenn dies bedeutet, dass 2 Tabletten zur gleichen Zeit eingenommen werden. Die Einnahme der restlichen Tabletten erfolgt dann wieder zur üblichen Zeit. Mit der Einnahme aus der nächsten Blisterpackung wird direkt nach Aufbrauchen der aktuellen Blisterpackung begonnen, d. h. zwischen den beiden Blisterpackungen liegt kein einnahmefreies Intervall. Es ist unwahrscheinlich, dass es bei der Anwenderin vor Aufbrauchen der zweiten Blisterpackung zu einer Abbruchblutung kommt, allerdings können noch während der Einnahme Schmier- oder Durchbruchblutungen auftreten.
2. Es ist auch möglich, die Einnahme der Tabletten aus der angebrochenen Blisterpackung abzubrechen. Die Anwenderin muss dann eine tablettenfreie Zeitspanne von 7 Tagen (einschließlich der Tage, an denen sie die Tabletten vergessen hat) einhalten und anschließend mit einer neuen Packung fortfahren.
Wenn die Anwenderin mehr als 1 Tablette vergessen hat, sollte bis zur nächsten üblichen Entzugsblutung eine nicht-hormonale Verhütungsmethode angewendet werden.
Wenn nach vergessener Einnahme die übliche Entzugsblutung ausbleibt, muss eine Schwangerschaft ausgeschlossen werden, bevor mit einer neuen Blisterpackung begonnen wird.
Verhalten bei Erbrechen oder Durchfall
Bei Erbrechen oder schwerem Durchfall innerhalb der ersten 3-4 Stunden nach der Einnahme von Leona HEXAL werden die Wirkstoffe möglicherweise nicht vollständig aufgenommen und es sollten zusätzliche empfängnisverhütende
Maßnahmen angewendet werden. Weiterhin gelten dieselben Anwendungshinweise wie bei vergessener Tabletteneinnahme. Wenn das gewohnte Einnahmeschema beibehalten werden soll, muss die zusätzlich einzunehmende Tablette aus einer anderen Blisterpackung eingenommen werden. Bei anhaltenden oder wiederkehrenden gastrointestinalen Störungen sollten zusätzlich nicht-hormonale Verhütungsmethoden angewendet werden.
Verschieben des Termins der Menstruation und Veränderung des Wochentags des Menstruationsbeginns
Um die Entzugsblutung hinauszuschieben, soll nach Aufbrauchen einer Blisterpackung Leona HEXAL direkt ohne einnahmefreies Intervall mit der Einnahme aus der nächsten Blisterpackung begonnen werden. Die Entzugsblutung kann so lange wie gewünscht verzögert werden, maximal bis zum Ende der zweiten Blisterpackung. Während dieser Zeit kann es zu Durchbruchoder Schmierblutungen kommen. Nach der regulären 7-tägigen Einnahmepause kann die Einnahme von Leona HEXAL wie üblich fortgesetzt werden.
Zur Verschiebung des Beginns der Menstruation auf einen anderen Wochentag kann das nächste einnahmefreie Intervall um die gewünschte Zahl von Tagen verkürzt werden. Je kürzer das einnahmefreie Intervall, desto höher ist die Wahrscheinlichkeit, dass die Abbruchblutung ausbleibt und während der Einnahme aus der folgenden Packung Durchbruch- bzw. Schmierblutungen auftreten (genau wie beim Hinauszögern der Menstruation).
4.3 Gegenanzeigen
Kombinierte hormonale Kontrazeptiva (KHK) dürfen unter folgenden Bedingungen nicht angewendet werden. Wenn eine dieser Erkrankungen während der Anwendung des KHK zum ersten Mal auftritt, muss das Arzneimittel sofort abgesetzt werden.
• Vorliegen einer oder Risiko für eine venöse Thromboembolie (VTE)
- venöse Thromboembolie - bestehende VTE (auch unter Therapie mit Antikoagulanzien) oder VTE in der Vorgeschichte (z. B. tiefe Venenthrombose [TVT] oder Lungenembolie [LE])
- bekannte erbliche oder erworbene Prädisposition für eine venöse Thromboembolie wie z. B. APC-Resistenz (einschließlich Faktor-V-Leiden) Antithrombin-III-Mangel, Protein-C-Mangel oder Protein-S-Mangel
- größere Operationen mit längerer Immobilisierung (siehe Abschnitt 4.4)
- hohes Risiko für eine venöse Thromboembolie aufgrund mehrerer Risikofaktoren (siehe Abschnitt 4.4)
• Vorliegen einer oder Risiko für eine arterielle Thromboembolie (ATE)
- arterielle Thromboembolie - bestehende ATE, ATE in der Vorgeschichte (z. B. Myokardinfarkt) oder Erkrankungen im Prodromalstadium (z. B. Angina pectoris)
- zerebrovaskuläre Erkrankung - bestehender Schlaganfall, Schlaganfall oder prodromale Erkrankungen (z. B. transitorische ischämische Attacke [TIA]) in der Vorgeschichte
- bekannte erbliche oder erworbene Prädisposition für eine arterielle Thromboembolie wie z. B. Hyperhomocysteinämie und AntiphospholipidAntikörper (Anticardiolipin-Antikörper, Lupusantikoagulans)
- Migräne mit fokalen neurologischen Symptomen in der Vorgeschichte
- hohes Risiko für eine arterielle Thromboembolie aufgrund mehrerer Risikofaktoren (siehe Abschnitt 4.4) oder eines schwerwiegenden Risikofaktors wie:
o Diabetes mellitus mit Gefäßschäden o schwere Hypertonie
o schwere Dyslipoproteinämie
• bestehende oder vorausgegangene Pankreatitis, wenn diese mit schwerer Hypertriglyceridämie einhergeht
• bestehende oder vorausgegangene schwerwiegende Lebererkrankung, solange sich die Leberfunktion nicht normalisiert hat (auch Dubin-Johnson- und RotorSyndrom)
• bestehende oder vorausgegangene Lebertumoren (gutartig oder bösartig)
• bekannte oder vermutete sexualhormonabhängige maligne Tumoren (z. B. der Genitalorgane oder der Brust)
• diagnostisch nicht abgeklärte vaginale Blutungen
• Amenorrhö unbekannter Ursache
• Überempfindlichkeit gegen die Wirkstoffe oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile
4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung
Warnhinweise
Die Eignung von Leona HEXAL sollte mit der Frau besprochen werden, falls eine der im Folgenden aufgeführten Erkrankungen oder Risikofaktoren vorliegt.
Bei einer Verschlechterung oder dem ersten Auftreten einer dieser Erkrankungen oder Risikofaktoren ist der Anwenderin anzuraten, sich an ihren Arzt zu wenden, um zu entscheiden, ob die Anwendung von Leona HEXAL beendet werden sollte.
Gefäßerkrankungen
Risiko für eine venöse Thromboembolie (VTE)
Die Anwendung jedes kombinierten hormonalen Kontrazeptivums (KHK) erhöht das Risiko für eine venöse Thromboembolie (VTE) im Vergleich zur Nichtanwendung. Die Entscheidung, Leona HEXAL anzuwenden, sollte nur nach einem Gespräch mit der Frau getroffen werden, bei dem sicherzustellen ist, dass sie Folgendes versteht: das Risiko für eine VTE bei Anwendung von Leona HEXAL, wie ihre vorliegenden individuellen Risikofaktoren dieses Risiko beeinflussen, und dass ihr Risiko für VTE in ihrem allerersten Anwendungsjahr am höchsten ist. Es gibt zudem Hinweise, dass das Risiko erhöht ist, wenn die Anwendung eines KHK nach einer Unterbrechung von 4 oder mehr Wochen wieder aufgenommen wird.
Ungefähr 2 von 10.000 Frauen, die kein KHK anwenden und nicht schwanger sind, erleiden im Verlauf eines Jahres eine VTE. Bei einer einzelnen Frau kann das Risiko jedoch in Abhängigkeit von ihren zugrunde liegenden Risikofaktoren bedeutend höher sein (siehe unten).
Ungefähr 61 von 10.000 Frauen, die ein Levonorgestrel-haltiges KHK anwenden, erleiden im Verlauf eines Jahres eine VTE.
Diese Anzahl an VTE pro Jahr ist geringer als die erwartete Anzahl während der Schwangerschaft oder in der Zeit nach der Geburt.
VTE verlaufen in 1-2% der Fälle tödlich.
1 Mittelwert der Spannweite 5-7 pro 10.000 Frauenjahre, auf der Grundlage eines relativen Risikos für Levonorgestrel-haltige KHK versus Nichtanwendung von ungefähr 2,3-3,6.
Anzahl an VTE Ereignissen
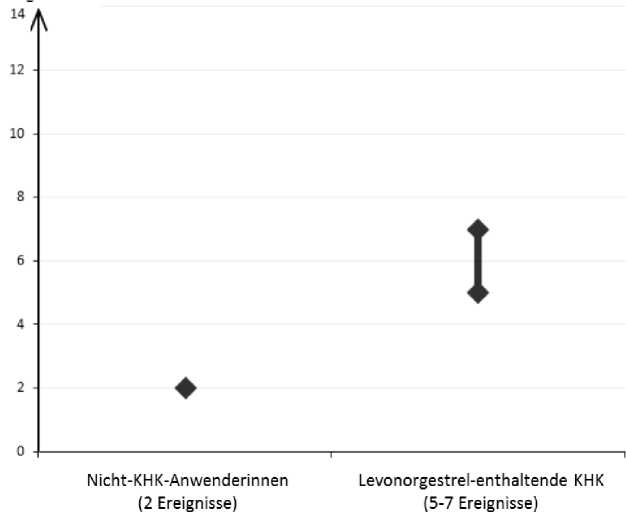
Äußerst selten wurde bei Anwenderinnen von KHK über eine Thrombose in anderen Blutgefäßen berichtet, wie z. B. in Venen und Arterien von Leber, Mesenterium, Nieren oder Retina.
Risikofaktoren für VTE Das Risiko für venöse thromboembolische Komplikationen bei Anwenderinnen von KHK kann deutlich ansteigen, wenn bei der Anwenderin zusätzliche Risikofaktoren bestehen, insbesondere wenn mehrere Risikofaktoren vorliegen (siehe Tabelle).
Leona HEXAL ist kontraindiziert, wenn bei einer Frau mehrere Risikofaktoren gleichzeitig bestehen, die insgesamt zu einem hohen Risiko für eine Venenthrombose führen (siehe Abschnitt 4.3). Weist eine Frau mehr als einen Risikofaktor auf, ist es möglich, dass der Anstieg des Risikos das Risiko der Summe der einzelnen Faktoren übersteigt - in diesem Fall muss ihr Gesamtrisiko für eine VTE in Betracht gezogen werden. Wenn das Nutzen/Risiko-Verhältnis als ungünstig erachtet wird, darf ein KHK nicht verschrieben werden (siehe Abschnitt 4.3).
Tabelle: Risikofaktoren für VTE
|
Risikofaktor |
Anmerkung |
|
Adipositas (Body-Mass-Index über 30 kg/m2) |
Das Risiko nimmt mit steigendem BMI deutlich zu. Besonders wichtig, wenn weitere Risikofaktoren vorliegen. |
|
Längere Immobilisierung, größere Operationen, jede Operation an Beinen oder Hüfte, neurochirurgische Operation oder schweres Trauma |
In diesen Fällen ist es ratsam, die Anwendung der Tablette (bei einer geplanten Operation mindestens 4 Wochen vorher) zu unterbrechen und erst 2 Wochen nach der kompletten Mobilisierung wieder aufzunehmen. Es ist eine andere |
|
Hinweis: Eine vorübergehende Immobilisierung einschließlich einer Flugreise von > 4 Stunden Dauer kann ebenfalls einen Risikofaktor für eine VTE darstellen, insbesondere bei Frauen mit weiteren Risikofaktoren. |
Verhütungsmethode anzuwenden, um eine ungewollte Schwangerschaft zu verhindern. Eine antithrombotische Therapie muss erwogen werden, wenn Leona HEXAL nicht vorab abgesetzt wurde. |
|
familiäre Vorbelastung (jede venöse Thromboembolie bei einem Geschwister oder Elternteil, insbesondere in relativ jungen Jahren, z. B. jünger als 50 Jahre) |
Bei Verdacht auf eine genetische Prädisposition ist die Frau zur Beratung an einen Spezialisten zu überweisen, bevor eine Entscheidung über die Anwendung eines KHKs getroffen wird. |
|
andere Erkrankungen, die mit einer VTE verknüpft sind |
Krebs, systemischer Lupus erythematodes, hämolytischurämisches Syndrom, chronisch entzündliche Darmerkrankung (Morbus Crohn oder Colitis ulcerosa) und Sichelzellkrankheit |
|
zunehmendes Alter |
insbesondere älter als 35 Jahre |
Es besteht kein Konsens über die mögliche Rolle von Varizen und oberflächlicher Thrombophlebitis bezüglich des Beginns oder Fortschreitens einer Venenthrombose.
Das erhöhte Risiko einer Thromboembolie in der Schwangerschaft und insbesondere während der 6-wöchigen Dauer des Wochenbetts muss berücksichtigt werden (Informationen zu Schwangerschaft und Stillzeit siehe Abschnitt 4.6).
Symptome einer VTE (tiefe Beinvenenthrombose und Lungenembolie)
Beim Auftreten von Symptomen ist den Anwenderinnen anzuraten, unverzüglich ärztliche Hilfe in Anspruch zu nehmen und das medizinische Fachpersonal darüber zu informieren, dass sie ein KHK anwenden.
Bei einer tiefen Beinvenenthrombose (TVT) können folgende Symptome auftreten:
• unilaterale Schwellung des Beins und/oder Fußes oder entlang einer Beinvene
• Schmerz oder Druckschmerz im Bein, der möglicherweise nur beim Stehen oder Gehen bemerkt wird
• Erwärmung des betroffenen Beins; gerötete oder entfärbte Haut am Bein
Bei einer Lungenembolie (LE) können folgende Symptome auftreten:
• plötzliches Auftreten unerklärlicher Kurzatmigkeit oder schnellen Atmens
• plötzlich auftretender Husten möglicherweise in Verbindung mit Hämoptyse
• stechender Brustschmerz
• starke Benommenheit oder Schwindelgefühl
schneller oder unregelmäßiger Herzschlag
Einige dieser Symptome (z. B. „Kurzatmigkeit“, „Husten") sind unspezifisch und können als häufiger vorkommende und weniger schwerwiegende Ereignisse fehlinterpretiert werden (z. B. als Atemwegsinfektionen).
Andere Anzeichen für einen Gefäßverschluss können plötzlicher Schmerz sowie Schwellung und leicht bläuliche Verfärbung einer Extremität sein.
Tritt der Gefäßverschluss im Auge auf, können die Symptome von einem schmerzlosen verschwommenen Sehen bis zu einem Verlust des Sehvermögens reichen. In manchen Fällen tritt der Verlust des Sehvermögens sehr plötzlich auf.
Risiko für eine arterielle Thromboembolie (ATE)
Epidemiologische Studien haben die Anwendung von KHK mit einem erhöhten Risiko für arterielle Thromboembolie (Myokardinfarkt) oder apoplektischen Insult (z. B. transitorische ischämische Attacke, Schlaganfall) in Verbindung gebracht. Arterielle thromboembolische Ereignisse können tödlich verlaufen.
Risikofaktoren für ATE
Das Risiko für arterielle thromboembolische Komplikationen oder einen apoplektischen Insult bei Anwenderinnen von KHK erhöht sich bei Frauen, die Risikofaktoren aufweisen (siehe Tabelle). Leona HEXAL ist kontraindiziert bei Frauen, die einen schwerwiegenden oder mehrere Risikofaktoren für eine ATE haben, die sie einem hohen Risiko für eine Arterienthrombose aussetzen (siehe Abschnitt 4.3). Weist eine Frau mehr als einen Risikofaktor auf, ist es möglich, dass der Anstieg des Risikos das Risiko der Summe der einzelnen Faktoren übersteigt - in diesem Fall muss ihr Gesamtrisiko betrachtet werden. Bei Vorliegen eines ungünstigen Nutzen/Risiko-Verhältnis darf ein KHK nicht verschrieben werden (siehe Abschnitt 4.3).
Tabelle: Risikofaktoren für ATE
|
Risikofaktor |
Anmerkung |
|
zunehmendes Alter |
insbesondere älter als 35 Jahre |
|
Rauchen |
Frauen ist anzuraten, nicht zu rauchen, wenn Sie ein KHK anwenden möchten. Frauen über 35 Jahren, die weiterhin rauchen, ist dringend zu empfehlen, eine andere Verhütungsmethode anzuwenden. |
|
Hypertonie | |
|
Adipositas (Body-Mass-Index über 30 kg/m2) |
Das Risiko nimmt mit steigendem BMI deutlich zu. Besonders wichtig bei Frauen mit zusätzlichen Risikofaktoren. |
|
familiäre Vorbelastung (jede arterielle Thromboembolie bei einem Geschwister oder Elternteil, insbesondere in relativ jungen Jahren, d. h. jünger als 50 Jahre) |
Bei Verdacht auf eine genetische Prädisposition ist die Frau zur Beratung an einen Spezialisten zu überweisen, bevor eine Entscheidung über die Anwendung eines KHKs getroffen wird. |
|
Migräne |
Ein Anstieg der Häufigkeit oder des Schweregrads der Migräne während der Anwendung von KHK (die einem zerebrovaskulären Ereignis vorausgehen kann) kann ein Grund für ein sofortiges Absetzen sein. |
|
andere Erkrankungen, die mit unerwünschten Gefäßereignissen verknüpft sind |
Diabetes mellitus, Hyperhomocysteinämie, Erkrankung der Herzklappen und Vorhofflimmern, Dyslipoproteinämie und systemischer Lupus erythematodes |
Symptome einer ATE
Beim Auftreten von Symptomen ist den Frauen anzuraten, unverzüglich ärztliche Hilfe in Anspruch zu nehmen und das medizinische Fachpersonal darüber zu informieren, dass sie ein KHK anwenden.
Bei einem apoplektischen Insult können folgende Symptome auftreten:
• plötzliches Taubheitsgefühl oder Schwäche in Gesicht, Arm oder Bein, besonders auf einer Körperseite
• plötzliche Gehschwierigkeiten, Schwindelgefühl, Gleichgewichtsverlust oder Koordinationsstörungen
• plötzliche Verwirrtheit, Sprech- oder Verständnisschwierigkeiten
• plötzliche Sehstörungen in einem oder beiden Augen
• plötzliche, schwere oder länger anhaltende Kopfschmerzen unbekannter Ursache
• Verlust des Bewusstseins oder Ohnmacht mit oder ohne Krampfanfall Vorübergehende Symptome deuten auf eine transitorische ischämische Attacke (TIA) hin.
Bei einem Myokardinfarkt (MI) können folgende Symptome auftreten:
• Schmerz, Unbehagen, Druck, Schweregefühl, Enge- oder Völlegefühl in Brust, Arm oder unterhalb des Sternums
• in den Rücken, Kiefer, Hals, Arm, Magen ausstrahlende Beschwerden
• Völlegefühl, Indigestion oder Erstickungsgefühl
• Schwitzen, Übelkeit, Erbrechen oder Schwindelgefühl
• extreme Schwäche, Angst oder Kurzatmigkeit
• schnelle oder unregelmäßige Herzschläge
Die Möglichkeit einer Antikoagulanzientherapie sollte auch in Betracht gezogen werden. Wegen der Teratogenität der Antikoagulanzientherapie (Cumarine) ist auf eine geeignete alternative Empfängnisverhütung umzusteigen.
Tumoren
Einige epidemiologische Studien weisen darauf hin, dass die langfristige Anwendung von KOK mit einem erhöhten Risiko für Gebärmutterhalskrebs verbunden ist. Es besteht aber immer noch Uneinigkeit darüber, in welchem Ausmaß dieser Befund auch auf das Sexualverhalten und auf andere Faktoren, wie z. B. das humane Papillomavirus (HPV), zurückzuführen ist.
Eine Meta-Analyse, basierend auf 54 epidemiologischen Studien, ergab, dass Frauen, die derzeit KOK einnehmen, ein geringfügig erhöhtes relatives Brustkrebsrisiko (RR = 1,24) aufweisen. Dieses erhöhte Risiko geht innerhalb von 10 Jahren nach Absetzen der kombinierten oralen Kontrazeptiva allmählich zurück. Da Brustkrebs bei Frauen unter 40 Jahren relativ selten auftritt, ist die Anzahl zusätzlicher Brustkrebsfälle bei ehemaligen oder momentanen Anwenderinnen kombinierter oraler Kontrazeptiva klein im Vergleich zum Gesamtrisiko für Brustkrebs. Ein Kausalzusammenhang wurde mit diesen Studien nicht bewiesen. Das beobachtete Muster eines erhöhten Risikos kann an einer früheren Diagnose des Brustkrebses bei Anwenderinnen kombinierter oraler Kontrazeptiva, den biologischen Wirkungen kombinierter oraler Kontrazeptiva oder einer Kombination beider Faktoren liegen. Brustkrebs, der bei Frauen diagnostiziert wird, die irgendwann einmal ein orales Kontrazeptivum verwendet haben, scheint klinisch weit weniger fortgeschritten zu sein als Krebs bei Frauen, die noch nie ein orales Kontrazeptivum verwendet haben.
Alle Frauen, besonders wenn sie über 35 Jahre alt sind, sollten während der Einnahme der „Pille" regelmäßige Brustuntersuchungen durchführen lassen.
In seltenen Fällen sind bei Anwenderinnen von KOK gutartige und noch seltener bösartige Lebertumoren beobachtet worden. In Einzelfällen führten diese Tumoren zu lebensbedrohlichen intraabdominellen Blutungen. Wenn starke Oberbauchbeschwerden, eine Lebervergrößerung oder Anzeichen einer intraabdominellen Blutung bei Anwenderinnen oraler Kontrazeptiva auftreten, soll ein Lebertumor in die differenzialdiagnostischen Überlegungen einbezogen werden.
Sonstige Erkrankungen
Frauen mit einer Hypertriglyceridämie oder einer diesbezüglich positiven Familienanamnese können ein erhöhtes Risiko für die Entwicklung einer Pankreatitis unter der Einnahme von KOK haben.
Obwohl bei vielen Frauen, die kombinierte orale Kontrazeptiva anwenden, ein geringer Blutdruckanstieg berichtet wurde, sind klinisch relevante Blutdruckerhöhungen selten. Nur in diesen seltenen Fällen ist der sofortige Abbruch der KOK-Einnahme gerechtfertigt. Bisher konnte kein systemischer Zusammenhang zwischen der Einnahme von KOK und einer klinischen Hypertonie begründet werden. Wenn es bei einer bereits existierenden Hypertonie und der gleichzeitigen Einnahme eines oralen Kontrazeptivums zu ständig erhöhten Blutdruckwerten oder einer signifikanten Erhöhung des Blutdrucks kommt und in diesen Fällen eine antihypertensive Therapie keine Wirkung zeigt, muss das KOK abgesetzt werden. Wenn es angemessen erscheint, kann die Anwendung des KOKs wieder begonnen werden, sobald sich die Blutdruckwerte unter der antihypertensiven Therapie normalisiert haben.
Die folgenden Erkrankungen sollen Berichten zufolge sowohl in der Schwangerschaft als auch unter der Anwendung eines KOK auftreten bzw. sich verschlechtern. Jedoch konnte der Zusammenhang mit der Anwendung von KOK nicht bewiesen werden: cholestatischer Ikterus und/oder Pruritus, Gallensteine, Porphyrie, systemischer Lupus erythematodes, hämolytisch-urämisches Syndrom, Sydenham-Chorea, Herpes gestationis, Otosklerose-bedingte Schwerhörigkeit, depressive Verstimmungen.
Die Gabe von Estrogenen kann bei Frauen mit hereditärem Angioödem Symptome eines Angioödems auslösen oder verschlimmern.
Akute oder chronische Störungen der Leberfunktion können eine Unterbrechung der KOK-Anwendung bis zur Normalisierung der Leberfunktionswerte erfordern.
Ein Rezidiv eines in einer vorausgegangen Schwangerschaft oder während einer früheren Anwendung steroidaler Geschlechtshormone aufgetretenen cholestatischen Ikterus und/oder eines Cholestase-bedingten Pruritus macht das Absetzen des KOK erforderlich.
Obwohl KOK einen Einfluss auf die periphere Insulinresistenz und Glucosetoleranz haben können, liegen keinerlei Hinweise auf die Notwendigkeit einer Änderung der Therapieregime bei Diabetikerinnen vor, die niedrig dosierte KOK anwenden. Diabetikerinnen müssen jedoch sorgfältig überwacht werden, insbesondere in der ersten Zeit der Anwendung eines KOKs.
Bei Anwendung von KOK wurde über eine Verschlechterung endogener Depressionen, Epilepsie, Morbus Crohn und Colitis ulcerosa berichtet.
Chloasmen können gelegentlich auftreten, insbesondere bei Frauen mit Chloasma gravidarum in der Anamnese. Anwenderinnen mit dieser Veranlagung sollten sich daher während der Einnahme von KOK nicht direkt der Sonne oder ultraviolettem Licht aussetzen.
Dieses Arzneimittel enthält Lactose. Patienten mit der seltenen hereditären Galactose-Intoleranz, Lactase-Mangel oder Glucose-Galactose-Malabsorption sollten Leona HEXAL nicht einnehmen.
Dieses Arzneimittel enthält auch Saccharose (Sucrose). Patienten mit der seltenen hereditären Fructose-Intoleranz, Glucose-Galactose-Malabsorption oder Saccharase-Isomaltase-Mangel sollten Leona HEXAL nicht einnehmen.
Ärztliche Untersuchung/Beratung
Vor der Einleitung oder Wiederaufnahme der Behandlung mit Leona HEXAL muss eine vollständige Anamnese (mit Erhebung der Familienanamnese) erfolgen und eine Schwangerschaft ausgeschlossen werden. Der Blutdruck sollte gemessen und eine körperliche Untersuchung durchgeführt werden, die sich an den Gegenanzeigen (siehe Abschnitt 4.3) und Warnhinweisen (siehe Abschnitt 4.4) orientiert.
Es ist wichtig, die Frau auf die Informationen zu venösen und arteriellen Thrombosen hinzuweisen, einschließlich des Risikos von Leona HEXAL im Vergleich zu anderen KHK, die Symptome einer VTE und ATE, die bekannten Risikofaktoren und darauf, was im Falle einer vermuteten Thrombose zu tun ist.
Die Anwenderin ist zudem anzuweisen die Packungsbeilage sorgfältig zu lesen und die darin gegebenen Ratschläge zu befolgen. Die Häufigkeit und Art der Untersuchungen sollte den gängigen Untersuchungsleitlinien entsprechen und individuell auf die Frau abgestimmt werden.
Die Anwenderinnen sind darüber aufzuklären, dass hormonale Kontrazeptiva nicht vor HIV-Infektionen (AIDS) und anderen sexuell übertragbaren Krankheiten schützen.
Verminderte Wirksamkeit
Die Wirksamkeit von KOK kann beeinträchtigt sein, wenn Tabletten vergessen werden, bei Erbrechen oder Durchfall oder wenn gleichzeitig bestimmte andere Arzneimittel eingenommen werden.
Unregelmäßige Blutungen
Bei allen KOK kann es, insbesondere in den ersten Monaten der Anwendung, zu unregelmäßigen Blutungen (Schmier- oder Durchbruchblutungen) kommen. Eine Beurteilung dieser unregelmäßigen Blutungen ist deshalb erst nach einer Umstellungsphase von ungefähr 3 Zyklen sinnvoll. Bei mehr als 50 % der
Anwenderinnen von Levonorgestrel/Ethinylestradiol wurden während der ersten 6 Einnahmezyklen Blutungen (Schmier- oder Durchbruchblutungen) berichtet.
Wenn diese unregelmäßigen Blutungen bestehen bleiben oder nach vormals regelmäßigen Zyklen auftreten, sollten nicht-hormonale Ursachen in Betracht gezogen werden und angemessene diagnostische Maßnahmen zum Ausschluss von Malignität oder Schwangerschaft eingeleitet werden. Eine Ausschabung kann notwendig sein.
Es ist möglich, dass es bei einigen Anwenderinnen im einnahmefreien Intervall zu keiner Abbruchblutung kommt. Wenn das KOK wie in Abschnitt 4.2 beschrieben eingenommen wurde, ist eine Schwangerschaft unwahrscheinlich. Wenn die Einnahme jedoch vor der ersten ausgebliebenen Abbruchblutung nicht vorschriftsmäßig erfolgt ist oder bereits zum zweiten Mal die Abbruchblutung ausbleibt, muss eine Schwangerschaft ausgeschlossen werden, bevor die Anwendung des KOKs fortgesetzt wird.
Beendigung der Einnahme bei Kinderwunsch
Frauen, die die Einnahme von Leona HEXAL wegen eines Kinderwunsches beenden, sollten darüber aufgeklärt werden, dass Folsäuremangel zu Neuralrohrdefekten beim Ungeborenen führen kann, und dass daher eine perikonzeptionelle Folsäure-Supplementierung empfohlen wird.
4.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige
Wechselwirkungen
Hinweis: Die Fachinformationen der gleichzeitig verordneten Arzneimittel sollten auf mögliche Wechselwirkungen hin überprüft werden.
Einfluss anderer Arzneimittel auf Leona HEXAL
Wechselwirkungen können mit Arzneimitteln auftreten, die mikrosomale Enzyme induzieren. Dies kann eine erhöhte Clearance von Sexualhormonen zur Folge haben und zu Durchbruchblutungen und/oder kontrazeptivem Versagen führen.
Vorgehen
Eine Enzyminduktion kann bereits nach wenigen Tagen der Behandlung beobachtet werden. Eine maximale Enzyminduktion tritt gewöhnlich innerhalb von wenigen Wochen auf und kann bis zu 4 Wochen nach Absetzen der Therapie anhalten.
Kurzzeittherapie
Frauen, die mit Enzym-induzierenden Arzneimitteln behandelt werden, sollten vorübergehend eine Barrieremethode oder eine andere Verhütungsmethode zusätzlich zu dem KOK anwenden. Die Barrieremethode muss während der gesamten Dauer der gleichzeitigen Anwendung der Arzneimittel und bis zu 28 Tage nach Absetzen der Behandlung verwendet werden. Wenn eines dieser Arzneimittel auch dann noch weiter eingenommen werden muss, wenn die Blisterpackung des KOK aufgebraucht ist, sollte direkt ohne das übliche einnahmefreie Intervall mit der Einnahme aus der nächsten Blisterpackung des KOK begonnen werden.
Langzeittherapie
Bei Frauen unter einer Langzeittherapie mit Arzneimitteln, die die Leberenzyme induzieren, wird eine andere zuverlässige nicht-hormonale Verhütungsmethode empfohlen.
Die folgenden Interaktionen wurden in der Literatur beschrieben.
Substanzen, die die Clearance von KOK erhöhen (verminderte Wirksamkeit von KOK durch Enzyminduktion) wie z. B.:
Barbiturate, Bosentan, Carbamazepin, Phenytoin, Primidon, Rifampicin und HIV-Arzneimittel, wie Ritonavir, Nevirapin und Efavirenz und möglicherweise auch Felbamat, Griseofulvin, Oxcarbazepin, Topiramat und pflanzliche Präparate, die Johanniskraut (Hypericum perforatum) enthalten.
Substanzen mit unterschiedlicher Wirkung auf die Clearance von KOK:
Viele Kombinationen von HIV-Proteaseinhibitoren und nicht-nukleosidalen Reverse-Transkriptase-Hemmern, einschließlich Kombinationen mit HCV-Inhibitoren, können bei gleichzeitiger Verabreichung mit KOK die Plasmakonzentrationen von Estrogenen und Gestagenen erhöhen oder senken. Diese Veränderungen können in einigen Fällen klinisch relevant sein.
Daher sollten die Fachinformationen der gleichzeitig verordneten HIV/HCV-Arzneimittel auf mögliche Wechselwirkungen und damit verbundene Empfehlungen überprüft werden. Im Zweifel sollte von Frauen unter einer Therapie mit Proteaseinhibitoren oder nicht-nukleosidalen Reverse-Transkriptase-Hemmern eine zusätzliche Barrieremethode zur Empfängnisverhütung verwendet werden.
Verminderte Resorption
Arzneimittel, die die gastrointestinale Motilität erhöhen, z. B. Metoclopramid, können die Hormonresorption vermindern.
Einfluss von Leona HEXAL auf andere Arzneimittel
Orale Kontrazeptiva können mit dem Metabolismus verschiedener Arzneimittel interagieren. Ansteigende Plasma-Konzentrationen von Ciclosporin wurden bei gleichzeitiger Anwendung mit KOK beschrieben. Für KOK hat sich gezeigt, dass der Metabolismus von Lamotrigin induziert wird, mit dem Ergebnis subtherapeutischer Plasmakonzentrationen von Lamotrigin.
Troleandomycin kann bei gleichzeitiger Gabe mit KOK das Risiko einer intrahepatischen Cholestase erhöhen.
Der Bedarf an Insulin oder oralen Antidiabetika kann infolge einer Beeinflussung der Glucosetoleranz verändert sein.
Labortests
Die Anwendung von kontrazeptiven Steroiden kann die Ergebnisse bestimmter Labortests beeinflussen, einschließlich der biochemischen Parameter der Leber-, Schilddrüsen-, Nebennieren- und Nierenfunktion, Plasmaspiegel von Trägerproteinen, z. B. kortikosteroidbindendes Globulin und Lipid/Lipoprotein-Fraktionen, Parameter des Kohlenhydratstoffwechsels und Parameter der Blutgerinnung und der Fibrinolyse. Im Allgemeinen bleiben diese Veränderungen innerhalb des Normbereichs.
4.6 Fertilität, Schwangerschaft und Stillzeit
Schwangerschaft
Leona HEXAL ist während der Schwangerschaft nicht indiziert.
Vor Beginn der Anwendung von Leona HEXAL ist eine Schwangerschaft auszuschließen. Falls unter der Anwendung von Leona HEXAL eine Schwangerschaft eintritt, ist das Arzneimittel sofort abzusetzen.
In den meisten epidemiologischen Untersuchungen fand sich jedoch weder ein erhöhtes Risiko für Missbildungen bei Kindern, deren Mütter vor der Schwangerschaft kombinierte orale Kontrazeptiva eingenommen hatten, noch eine teratogene Wirkung bei versehentlicher Einnahme von kombinierten oralen Kontrazeptiva in der Frühschwangerschaft.
Das erhöhte VTE-Risiko in der Zeit nach der Geburt sollte vor der erneuten Anwendung nach einer Anwendungspause bedacht werden (siehe Abschnitte
4.2 und 4.4).
Stillzeit
Kontrazeptiva können die Laktation beeinflussen, da sie die Menge der Muttermilch vermindern und ihre Zusammensetzung verändern können. Daher wird die Anwendung von KOK nicht empfohlen, solange eine Mutter ihr Kind nicht vollständig abgestillt hat. Kleine Mengen der kontrazeptiven Steroide und/oder ihrer Metaboliten könnten in die Muttermilch ausgeschieden werden. Diese Mengen könnten das Kind beeinträchtigen.
4.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum
Bedienen von Maschinen
Leona HEXAL hat keinen Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen.
4.8 Nebenwirkungen
Die häufigsten (> 10 %) mit der Anwendung von Levonorgestrel/Ethinylestradiol verbundenen Nebenwirkungen sind Kopfschmerzen (einschließlich Migräne), Schmier- und Zwischenblutungen.
|
Organsystem |
Nebenwirkungshäufigkeit | |||
|
Häufig 01/100 bis <1/10) |
Gelegentlich (>1/1.000 bis <1/100) |
Selten (>1/10.000 bis <1/1.000) |
Sehr selten (<1/10.000) | |
|
Infektionen und parasitäre Erkrankungen |
Vaginitis, einschließlich Candidose | |||
|
Erkrankungen des Immunsystems |
allergische Reaktionen, Überempfindlic hkeit |
Angioödem, schwere anaphylaktische Reaktionen mit Atem-und Kreis-lauf-Symptomen | ||
|
Stoffwechsel- und Ernährungsstörun gen |
Appetitveränderungen (Zu- oder Abnahme), Flüssigkeitsretention |
beeinträchtigte Glucosetoleran z | ||
|
psychiatrische Erkrankungen |
depressive Verstimmung Stimmungs schwankungen, |
verminderte Libido |
gesteigerte Libido | |
|
Erkrankungen |
Nervosität, |
Migräne | ||
|
des Nervensystems |
Benommenheit, Schwindel, Kopfschmerzen | |||
|
Augenerkrankung en |
Sehstörungen |
Kontaktlinsen unverträglich keit | ||
|
Gefäßerkrankung en |
arterielle Thromboembolie (ATE) venöse Thromboembolie (VTE) | |||
|
Erkrankungen des Gastrointestinaltrakts |
Übelkeit, Bauchschmerzen |
Durchfall, Erbrechen, Bauchkrämpfe, Blähungen | ||
|
Leber- und Gallenerkrankungen |
cholestatischer Ikterus | |||
|
Erkrankungen der Haut und des Unterhautzellgewebes |
Akne |
Ausschlag, Chloasma (Melasma) möglicherweise persistierend, Hirsutismus, Alopezie, Hautausschlag, Urtikaria |
Erythema nodosum, Erythema multiforme | |
|
Erkrankungen der Geschlechtsorga ne und der Brustdrüse |
Brustschmerzen, Empfindlichkeit der Brüste, Dysmenorrhö, Änderungen des Menstruationsflusses, Änderungen der zervikalen Umwandlungszone und Sekretion, Amenorrhö |
Brustvergrößerung |
Brustdrüsen sekretion, vaginaler Ausfluss | |
|
Untersuchungen |
Gewichtszunahme |
Blutdruckerhöhung, Veränderungen der Serumlipidspiegel, einschließlich Hypertriglyceridämie |
Gewichtsabna hme, Abnahme der Serumfolsäurespiegel |
Beschreibung ausgewählter Nebenwirkungen
Bei Anwenderinnen von KHK wurde ein erhöhtes Risiko für arterielle und venöse thrombotische und thromboembolische Ereignisse einschließlich Myokardinfarkt, Schlaganfall, transitorische ischämische Attacken, Venenthrombose und Lungenembolie beobachtet, die in Abschnitt 4.4 eingehender behandelt werden.
Die folgenden schwerwiegenden Nebenwirkungen sind bei KOK-Anwenderinnen berichtet worden; diese werden unter Abschnitt 4.4 Warnhinweise und Vorsichtmaßnahmen beschrieben:
• venöse thromboembolische Erkrankungen
• arterielle thromboembolische Erkrankungen
• Bluthochdruck
• Lebertumoren
• Morbus Crohn, Colitis ulcerosa, Porphyrie, systemischer Lupus erythematodes, Herpes gestationis, Sydenham-Chorea, hämolytischurämisches Syndrom, cholestatische Gelbsucht
Weiterhin wurden unter Anwendung von KOK folgende Nebenwirkungen berichtet (die Häufigkeit dieser Nebenwirkungen lässt sich aus den vorhandenen Daten nicht berechnen):
• Sehnervenentzündung (kann zu teilweisem oder vollständigem Verlust des Sehvermögens führen)
• Verschlechterung einer Varikosis
• Pankreatitis bei gleichzeitig bestehender, schwerer Hypertriglyceridämie
• Gallenblasenerkrankung, einschließlich Gallensteine (KOK können zum Auftreten einer Gallenblasenerkrankung führen oder eine vorbestehende Gallenblasenerkrankung verschlechtern)
• hämolytisch-urämisches Syndrom
• Herpes gestationis
• Otosklerose
• Verschlechterung eines systemischen Lupus erythematodes
• Verschlechterung einer Porphyrie
• Verschlechterung einer Sydenham- Chorea
• Verschlechterung einer Depression
• Verschlechterung chronisch-entzündlicher Darmerkrankungen (Morbus Crohn und Colitis ulcerosa)
Die Diagnosehäufigkeit von Brustkrebs unter Anwenderinnen von KOK ist geringfügig erhöht. Da bei Frauen unter 40 Jahren Brustkrebs selten auftritt, ist das zusätzliche Risiko, an Brustkrebs zu erkranken, im Verhältnis zum Gesamtrisiko gering. Die Kausalität mit der Anwendung von KOK ist nicht bekannt. Für weitere Informationen siehe Abschnitte 4.3 und 4.4.
Die Gabe von Estrogenen kann bei Frauen mit hereditärem Angioödem Symptome eines Angioödems auslösen oder verschlimmern.
Wechselwirkungen
Durchbruchblutungen und/oder kontrazeptives Versagen können durch Wechselwirkungen mit anderen Arzneimitteln (Enzyminduktoren) und oralen Kontrazeptiva verursacht werden (siehe Abschnitt 4.5).
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung dem
Bundesinstitut für Arzneimittel und Medizinprodukte Abt. Pharmakovigilanz Kurt-Georg-Kiesinger-Allee 3 D-53175 Bonn Website: www.bfarm.de
anzuzeigen.
4.9
Überdosierung
Es gibt keine Berichte über schwerwiegende Auswirkungen einer Überdosierung. Symptome einer Überdosierung mit oralen Kontrazeptiva bei Erwachsenen und Kindern können umfassen: Übelkeit, Erbrechen, Brustspannen, Benommenheit, Bauchschmerzen, Schläfrigkeit/Müdigkeit. Bei Frauen und Mädchen können vaginale Blutungen auftreten. Es gibt kein spezifisches Gegenmittel. Die Behandlung erfolgt symptomatisch.
5.1
PHARMAKOLOGISCHE EIGENSCHAFTEN Pharmakodynamische Eigenschaften
Pharmakotherapeutische Gruppe: Gestagene und Estrogene, fixe
Kombinationen
ATC-Code: G03A A07
Leona HEXAL ist ein Kombinationspräparat zur oralen Kontrazeption (KOK) und enthält Ethinylestradiol (EE) und Levonorgestrel.
Ethinylestradiol
Wirkmechanismus
Ethinylestradiol ist ein potentes oral wirksames synthetisches Estrogen. Wie das natürlich vorkommende Estradiol wirkt Ethinylestradiol auf die Epithelien der weiblichen Genitalorgane proliferativ.
Pharmakodynamische Wirkungen
Es stimuliert die Produktion des Zervixschleims, vermindert seine Viskosität und steigert seine Spinnbarkeit. Ethinylestradiol fördert das Wachstum der Ductus lactiferi und hemmt die Laktation. Ethinylestradiol stimuliert die extrazelluläre Flüssigkeitsretention.
Ethinylestradiol beeinflusst Parameter des Fett- und Kohlenhydratstoffwechsels, der Hämostase, des Renin-Angiotensin-Aldosteron-Systems sowie Serumbindungsproteine.
Levonorgestrel
Wirkmechanismus
Levonorgestrel als die biologisch wirksame d-Konfiguration von Norgestrel hat eine sehr hohe Gestagen-Potenz.
Pharmakodynamische Wirkungen
Der spezifischste progestative Effekt ist die sekretorische Umwandlung des Endometriums. Levonorgestrel hemmt die Gonadotropinsekretion im Hypophysenvorderlappen. Die Ovulationshemmdosis liegt bei 0,06 mg täglich.
Neben seiner gestagenen Wirksamkeit hat Levonorgestrel noch relativ starke antiestrogene sowie geringe androgene Eigenschaften. Die antiestrogene Komponente äußert sich in einer deutlichen Abnahme der Spinnbarkeit des Zervixschleims und einem Verschwinden der Farnkrautkristallisation.
Ähnlich dem Progesteron besitzt Levonorgestrel einen thermogenetischen Effekt.
Klinische Prüfungen wurden an 2.498 Frauen zwischen 18 und 40 Jahren durchgeführt. Der aus diesen Prüfungen errechnete Pearl Index lag bei 0,69 (95 %-Konfidenzintervall 0,30-1,36) basierend auf 15.026 Zyklen.
5.2 Pharmakokinetische Eigenschaften
Levonorgestrel
Resorption
Levonorgestrel wird nach oraler Gabe rasch und nahezu vollständig resorbiert. Maximale Levonorgestrel-Serumkonzentrationen von etwa 2,3 ng/ml werden etwa 1,3 Stunden nach der Einnahme erreicht. Die Bioverfügbarkeit beträgt nahezu 100 %.
Verteilung
Levonorgestrel ist an Serumalbumin und sexualhormonbindendes Globulin (SHBG) gebunden. Nur 1,1 % der Gesamtkonzentration des Wirkstoffes im Serum liegen als freies Steroid vor, etwa 65 % sind an SHBG spezifisch und etwa 35 % an Albumin nicht-spezifisch gebunden. Der durch Ethinylestradiol induzierte Anstieg von SHBG beeinflusst die relative Verteilung von Levonorgestrel in verschiedenen Proteinfraktionen. Die Induktion des bindenden Proteins verursacht einen Anstieg der SHBG-gebundenen Fraktion und eine Abnahme der albumingebundenen Fraktion. Das scheinbare Verteilungsvolumen von Levonorgestrel beträgt nach einer einmaligen Dosis 129 l.
Biotransformation
Levonorgestrel wird vornehmlich durch Reduktion an der A4-3-oxo-Gruppe und Hydroxylierung an Position 2a, 1ß und 16ß und anschließender Konjugation verstoffwechselt. Die Mehrzahl der Metaboliten, die im Blut zirkulieren, sind Sulfate des 3a, 5ß-Tetrahydrolevonorgestrels, während die Ausscheidung vorwiegend in Form von Glukuroniden erfolgt. Ein Teil des unveränderten Levonorgestrels zirkuliert auch als 17ß-Sulfat. Die metabolische Clearance kann interindividuell um ein Mehrfaches variieren und dies kann teilweise die beobachteten großen Schwankungen der Levonorgestrel-Konzentrationen bei den Anwenderinnen erklären.
Elimination
Die Serumspiegel von Levonorgestrel sinken in 2 Phasen. Die terminale Phase ist durch eine Halbwertszeit von etwa 25 Stunden gekennzeichnet. Levonorgestrel und seine Metaboliten werden hauptsächlich mit dem Urin (4068 %) und zu ca. 16-48 % mit den Fäzes ausgeschieden.
Fließgleichgewicht (Steady State)
Während der kontinuierlichen Anwendung von Levonorgestrel/Ethinylestradiol steigen die Levonorgestrel-Spiegel im Serum um das 3-fache und erreichen während der 2. Hälfte des Behandlungszyklus ihr Fließgleichgewicht (Steady State). Die Pharmakokinetik von Levonorgestrel wird beeinflusst durch die SHBG-Spiegel im Serum, die während der Anwendung von Estradiol um das 1,5- bis 1,6-fache erhöht sind. Deshalb sind beim Fließgleichgewicht die Clearance-Rate aus dem Serum und das Verteilungsvolumen leicht vermindert (0,7 ml/min/kg bzw. etwa 100 l).
Ethinylestradiol
Resorption
Ethinylestradiol wird nach oraler Gabe rasch und vollständig resorbiert. Maximale Serumkonzentrationen von etwa 50 pg/ml werden ca. 1-2 Stunden nach Tabletteneinnahme erreicht. Während der Resorption und des First-PassLeberstoffwechsels wird Ethinylestradiol umfassend metabolisiert, was zu einer mittleren oralen Bioverfügbarkeit von 45 % führt (interindividuelle Schwankung etwa 20-65 %).
Verteilung
Ethinylestradiol wird ausgeprägt (etwa 98 %), aber nicht-spezifisch an Serumalbumin gebunden und induziert einen Anstieg der Serumkonzentrationen von SHBG. Das scheinbare Verteilungsvolumen von Ethinylestradiol beträgt 2,8-8,6 l/kg.
Biotransformation
Ethinylestradiol wird durch präsystemische Konjugation in der Schleimhaut des Dünndarms und in der Leber abgebaut. Ethinylestradiol wird primär durch aromatische Hydroxylierung metabolisiert, dabei werden verschiedene hydroxylierte und methylierte Metabolite gebildet, die als freie Metaboliten oder als Glucuronid- oder Sulfat-Konjugate im Serum nachweisbar sind. Ethinylestradiol unterliegt einem enterohepatischen Kreislauf.
Elimination
Die Serumspiegel von Ethinylestradiol sinken in 2 Phasen, die durch Halbwertszeiten von etwa 1 Stunde bzw. 10-20 Stunden gekennzeichnet sind.
Ethinylestradiol wird nicht in unveränderter Form ausgeschieden. Die Metaboliten werden über den Urin und die Galle in einem Verhältnis von 4:6 ausgeschieden.
Fließgleichgewicht (Steady State)
Nach der kontinuierlichen Anwendung von Levonorgestrel/Ethinylestradiol steigt die Ethinylestradiol-Konzentration im Serum etwa um das 2-fache. Aufgrund der täglichen Anwendung und der variablen Halbwertszeit in der terminalen Phase der Serumclearance wird das Fließgleichgewicht nach etwa 1 Woche erreicht.
5.3 Präklinische Daten zur Sicherheit
Die Toxizitätsprofile von Ethinylestradiol und Levonorgestrel sind gut bekannt. Wegen ausgeprägter Speziesunterschiede besitzen tierexperimentelle Untersuchungsergebnisse nur einen beschränkten prädiktiven Wert für die Anwendung beim Menschen.
Bei Versuchstieren zeigte Ethinylestradiol bereits in relativ geringer Dosierung einen embryoletalen Effekt. Missbildungen des Urogenitaltrakts und Feminisierung männlicher Feten wurden beobachtet. Levonorgestrel zeigte im Tierexperiment einen embryoletalen Effekt und, in hohen Dosen, eine virilisierende Wirkung auf weibliche Feten. Reproduktionstoxikologische Studien an Ratten, Mäusen und Kaninchen erbrachten keinen Hinweis auf eine über die beschriebenen Effekte auf die sexuelle Differenzierung hinausgehende teratogene Wirkung.
Präklinische Daten für Ethinylestradiol und Levonorgestrel aus konventionellen Studien zur chronischen Toxizität, Genotoxizität und zum karzinogenen Potential zeigten keine speziellen Risiken für den Menschen außer denen, die bereits in anderen Abschnitten der Fachinformation beschrieben sind.
6. PHARMAZEUTISCHE ANGABEN
6.1 Liste der sonstigen Bestandteile
Tablettenkern
• Lactose-Monohydrat
• Magnesiumstearat (Ph.Eur.) [pflanzlich]
• Maisstärke
• Povidon K 25
• Talkum
Tablettenüberzug
• Calciumcarbonat
• Carnaubawachs
• Macrogol 6000
• Povidon K 90
• Sucrose
• Talkum
6.2 Inkompatibilitäten
Nicht zutreffend
6.3 Dauer der Haltbarkeit
2 Jahre
6.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung
Nicht über 30 °C lagern.
6.5 Art und Inhalt des Behältnisses
PVC/PVDC-Aluminium-Blisterpackungen mit 21 überzogenen Tabletten Kalenderpackungen mit 1 x 21, 3 x 21 und 6 x 21 überzogenen Tabletten Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht.
6.6 Besondere Vorsichtsmaßnahmen für die Beseitigung
Keine besonderen Anforderungen
Nicht verwendetes Arzneimittel oder Abfallmaterial ist entsprechend den nationalen Anforderungen zu entsorgen.
7. INHABER DER ZULASSUNG
Hexal AG Industriestraße 25 83607 Holzkirchen Telefon: (08024) 908-0 Telefax: (08024) 908-1290 E-Mail: medwiss@hexal.com
67195.00.00
9.
10.
DATUM DER ERTEILUNG DER ZULASSUNG
10. März 2008
STAND DER INFORMATION
Februar 2016
VERKAUFSABGRENZUNG
Verschreibungspflichtig
11.