Magnesiocard 2,5Mmol
F a c h i n f o r m a t i o n
1. BEZEICHNUNG DER ARZNEIMITTEL
Magnesiocard® 2,5 mmol, Filmtabletten
Magnesiocard® 5 mmol, Pulver zur Herstellung einer Lösung zum Einnehmen Magnesiocard® 7,5 mmol, Brausetabletten
Magnesiocard® forte 10 mmol, Pulver zur Herstellung einer Lösung zum Einnehmen
Magnesiocard® forte 10 mmol Orange, Pulver zur Herstellung einer Lösung zum Einnehmen
2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Wirkstoff: Magnesiumaspartat-hydrochlorid
Magnesiocard® 2,5 mmol 1 Filmtablette enthält:
Magnesiumaspartat-hydrochlorid 3 H2O 614,8 mg, entsprechend 2,5 mmol = 60,8 mg Magnesium
Magnesiocard® 5 mmol
1 Beutel mit 5 g Pulver zur Herstellung einer Lösung zum Einnehmen enthält: Magnesiumaspartat-hydrochlorid 3 H2O 1229,6 mg, entsprechend 5 mmol = 121,5 mg Magnesium
Magnesiocard® 7,5 mmol 1 Brausetablette enthält:
Magnesiumaspartat-hydrochlorid 3 H2O 1844,4 mg, entsprechend 7,5 mmol = 182,3 mg Magnesium
Magnesiocard® forte 10 mmol / -forte 10 mmol Orange 1 Beutel mit 4 g Pulver zur Herstellung einer Lösung zum Einnehmen enthält: Magnesiumaspartat-hydrochlorid 3 H2O 2460 mg, entsprechend 10 mmol = 243 mg Magnesium
Sonstige Bestandteile mit bekannter Wirkung
Magnesiocard® 5 mmol:
1 Beutel enthält 3,2 g Sucrose (Zucker).
Magnesiocard® 7,5 mmol: 1 Brausetablette enthält 12,5 mg Aspartam als Quelle für Phenylalanin (entsprechend 7 mg/Dosis), 2,6 mmol (100 mg) Kalium und 6 mmol (138 mg) Natrium.
Magnesiocard® forte 10 mmol Orange enthält Sorbitol (Ph.Eur.)(siehe Abschnitt 4.4).
Vollständige Auflistung der sonstigen Bestandteile, siehe Abschnitt 6.1.
3. DARREICHUNGSFORM
Magnesiocard® 2,5 mmol:
Filmtablette
Weiße, längliche Filmtablette ohne Bruchrille. Magnesiocard® 5 mmol:
Pulver zur Herstellung einer Lösung zum Einnehmen In Beutel verpacktes, weißes Pulver.
Magnesiocard® 7,5 mmol: Brausetablette
Runde, weiße Brausetablette.
Magnesiocard® forte 10 mmol:
Pulver zur Herstellung einer Lösung zum Einnehmen In Beutel verpacktes, weißes Pulver.
Magnesiocard® forte 10 mmol Orange:
Pulver zur Herstellung einer Lösung zum Einnehmen In Beutel verpacktes, orangefarbenes Pulver.
4. KLINISCHE ANGABEN
4.1 Anwendungsgebiete
Behandlung von therapiebedürftigen Magnesiummangelzuständen, die keiner parenteralen Substitution bedürfen.
Nachgewiesener Magnesiummangel, wenn er Ursache für Störungen der Muskeltätigkeit (neuromuskuläre Störungen, Wadenkrämpfe) ist.
4.2 Dosierung, Art und Dauer der Anwendung
Dosierung
Als mittlere Tagesdosis empfiehlt sich 0,185 mmol Magnesium (4,5 mg) pro kg Körpergewicht. Bei chronischen und schweren akuten Magnesium-Mangelzuständen kann die Tagesdosis, falls keine Kontraindikationen vorliegen, bis zur Beseitigung des
Mangels unbedenklich auf 0,37 mmol Magnesium (9 mg) pro kg Körpergewicht erhöht werden. Es gelten folgende Dosierungsrichtlinien für die mittlere Tagesdosis:
Magnesiocard® 2,5 mmol:
Erwachsene:
3mal täglich 2 Filmtabletten (entsprechend 364,8 mg Magnesium).
Kinder und Jugendliche Jugendliche über 14 Jahre:
3mal täglich 2 Filmtabletten (entsprechend 364,8 mg Magnesium).
Kinder von 10 - 14 Jahren:
2mal täglich 2 Filmtabletten (entsprechend 243,2 mg Magnesium).
Kinder von 4 - 9 Jahren:
1 bis 2mal täglich 2 Filmtabletten (entsprechend 121,6 - 243,2 mg Magnesium).
Magnesiocard® 5 mmol:
Erwachsene:
3mal täglich den Inhalt je eines Beutels (entsprechend 364,5 mg Magnesium).
Kinder und Jugendliche Jugendliche über 14 Jahre:
3mal täglich den Inhalt je eines Beutels (entsprechend 364,5 mg Magnesium).
Kinder von 10 - 14 Jahren:
2mal täglich den Inhalt je eines Beutels (entsprechend 243,0 mg Magnesium).
Kinder von 4 - 9 Jahren:
1 - 2mal täglich den Inhalt je eines Beutels (entsprechend 121,5 - 243,0 mg Magnesium).
Magnesiocard® 7,5 mmol:
Erwachsene:
1-2mal täglich 1 Brausetablette (entsprechend 182,3 - 364,6 mg Magnesium).
Kinder und Jugendliche Jugendliche über 14 Jahre:
1-2mal täglich 1 Brausetablette (entsprechend 182,3 - 364,6 mg Magnesium).
Kinder von 10 - 14 Jahren:
1mal täglich 1 Brausetablette (entsprechend 182,3 mg Magnesium).
Kinder von 4 - 9 Jahren sollten niedriger dosierte Darreichungsformen von Magnesiocard® erhalten.
Magnesiocard® forte 10 mmol / -forte 10 mmol Orange:
Erwachsene:
1 - 2mal täglich den Inhalt je eines Beutels (entsprechend 243,0 - 486,0 mg Magnesium).
Kinder und Jugendliche Jugendliche über 14 Jahre:
1 - 2mal täglich den Inhalt je eines Beutels (entsprechend 243,0 - 486,0 mg Magnesium).
Kinder ab 4 Jahren sollten niedriger dosierte Darreichungsformen von Magnesiocard® erhalten.
Art der Anwendung
Magnesiocard® 2,5 mmol:
Filmtabletten mit etwas Flüssigkeit einnehmen.
Magnesiocard® 5 mmol:
Der Inhalt eines Beutels wird in einem halben Glas Wasser, Tee oder Fruchtsaft verrührt und getrunken.
Magnesiocard® 7,5 mmol:
Eine Brausetablette wird in einem halben Glas Wasser, Tee oder Fruchtsaft aufgelöst und getrunken.
Magnesiocard® forte 10 mmol / -forte 10 mmol Orange:
Der Inhalt eines Beutels wird in einem halben Glas Wasser, Tee oder Fruchtsaft verrührt und getrunken.
Magnesiocard® 2,5 mmol / -5 mmol / -7,5 mmol / -forte 10 mmol / -forte 10 mmol Orange sollten vor dem Essen eingenommen werden, da sich dadurch die Resorption verbessert.
Dauer der Anwendung
Magnesiocard® 2,5 mmol / -5 mmol / -7,5 mmol /-forte 10 mmol / -forte 10 mmol Orange sollten täglich über mindestens 4 Wochen eingenommen werden. Auch eine Dauertherapie mit Magnesiocard® 2,5 mmol / -5 mmol / -7,5 mmol /-forte 10 mmol / -forte 10 mmol Orange (über Jahre) ist bei normaler Nierenfunktion unbedenklich, da überschüssiges Magnesium über die Niere ausgeschieden wird.
4.3 Gegenanzeigen
Überempfindlichkeit gegen den Wirkstoff oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile.
Niereninsuffizienz mit Anurie, Exsikkose, Infektsteindiathese (Calcium-MagnesiumAmmoniumphosphatsteine).
Mit fortschreitender Niereninsuffizienz muss bei Kreatinin im Serum über 500 ^mol/l (6 mg pro 100 ml) mit einer Magnesiumretention gerechnet werden. Der Wert im Serum steigt dabei gewöhnlich nicht über 1,3 mmol/l Mg an. Da eine Hypermagnesiämie erst nach Abfall des Glomerulumfiltrats unter 30 ml/min auftritt, kann man annehmen, dass sich im Verlauf der chronischen Niereninsuffizienz auch eine adaptive Mehrausscheidung des Magnesiums pro Einzelnephron einstellen muss.
4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung
Kinder und Jugendliche
Über die Anwendung von Magnesiocard® 2,5 mmol / -5 mmol / -7,5 mmol / -forte 10 mmol / -forte 10 mmol Orange bei Kindern unter 4 Jahren liegen keine ausreichenden Erfahrungen vor. Magnesiocard® 2,5 mmol / -5 mmol / -7,5 mmol / -forte 10 mmol / -forte 10 mmol Orange sollten daher bei Kindern unter 4 Jahren nicht angewendet werden.
Magnesiocard® 5 mmol:
Patienten mit der seltenen hereditären Fructose-Intoleranz, Glucose-Galactose-Malabsorption oder Saccharase-Isomaltase-Mangel sollten Magnesiocard® 5 mmol nicht einnehmen.
1 Beutel enthält 3,2 g Sucrose (Zucker). Dies ist bei Patienten mit Diabetes mellitus zu berücksichtigen.
Der häufige und dauernde Gebrauch von Magnesiocard® 5 mmol kann schädlich für die Zähne sein (Karies).
Magnesiocard® 7,5 mmol:
1 Brausetablette enthält 12,5 mg Aspartam als Quelle für Phenylalanin (entsprechend 7 mg/Dosis) und kann schädlich sein für Patienten mit Phenylketonurie.
Eine Brausetablette enthält 2,6 mmol (100 mg) Kalium und 6 mmol (138 mg) Natrium. Dies ist zu berücksichtigen bei Patienten mit eingeschränkter Nierenfunktion sowie Personen unter kontrollierter Kaliumdiät und/oder Natrium kontrollierter (natriumarmer/-kochsalzarmer) Diät.
Magnesiocard® forte 10 mmol Orange:
Patienten mit der seltenen hereditären Fructose-Intoleranz sollten Magnesiocard® forte 10 mmol Orange nicht einnehmen.
4.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen
Magnesiocard® 2,5 mmol / -5 mmol / -7,5 mmol / -forte 10 mmol / -forte 10 mmol Orange sollten zeitlich 3 - 4 Stunden versetzt zu Tetrazyklinen oder Natriumfluorid-Präparaten eingenommen werden, um eine gegenseitige Beeinträchtigung der Resorption zu vermeiden.
4.6 Fertilität, Schwangerschaft und Stillzeit
Für Magnesium liegen keine Hinweise auf ein Fehlbildungsrisiko vor. Magnesiocard® 2,5 mmol / -5 mmol / -7,5 mmol /-forte 10 mmol / -forte 10 mmol Orange können in der Schwangerschaft und Stillzeit angewendet werden.
4.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen
Magnesiocard® 2,5 mmol / -5 mmol / -7,5 mmol /-forte 10 mmol / -forte 10 mmol Orange haben keinen Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen.
Gelegentlich (>1/1.000, <1/100) kann es bei der oralen Anwendung von Magnesiocard®
2,5 mmol / -5 mmol / -7,5 mmol / -forte 10 mmol / -forte 10 mmol Orange zu weichen Stühlen oder Durchfällen kommen, die sich aber durch Reduzierung der Dosis leicht beheben lassen.
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-RisikoVerhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung dem Bundesinstitut für Arzneimittel und Medizinprodukte, Abt. Pharmakovigilanz, Kurt-Georg-Kiesinger-Allee 3, D-53175 Bonn, Website: www.bfarm.de anzuzeigen.
4.9 Überdosierung
Symptome
Bei einer oralen Therapie mit Magnesiocard® 2,5 mmol / -5 mmol / -7,5 mmol / -forte 10 mmol / -forte 10 mmol Orange und intakter Nierenfunktion treten auch bei Überdosierung keine Intoxikationserscheinungen auf. Es können allerdings Durchfälle auftreten, die sich durch Reduzierung der Tagesdosis beheben lassen. Eventuelle Müdigkeitserscheinungen können ein Hinweis darauf sein, dass eine erhöhte Magnesiumkonzentration im Blut erreicht ist.
Nur bei schwerer Niereninsuffizienz mit Anurie kann es zur Kumulation von Magnesium und zu Intoxikationserscheinungen kommen.
Pharmakologische und toxische Effekte erhöhter Magnesium-Plasmaspiegel:
|
Mg-Plasma-Konzentration mmol/l |
Symptome und unerwünschte Wirkungen |
|
> 1,5 |
Blutdruckabfall, Brechreiz, Erbrechen |
|
> 2,5 |
ZNS-Depressionen |
|
> 3,5 |
Hyporeflexie, EKG-Veränderungen |
|
> 5,0 |
Beginnende Atemdepression |
|
> 5,5 |
Koma |
|
> 7,0 |
Herzstillstand, Atemlähmung |
Notfallmaßnahmen, Gegenmittel: Calcium-Injektion i.v.
5. PHARMAKOLOGISCHE EIGENSCHAFTEN
5.1 Pharmakodynamische Eigenschaften
Pharmakotherapeutische Gruppe: Mineralstoffpräparat.
ATC-Code: A12CC50
Magnesium wirkt als physiologischer Calcium-Antagonist.
Unter den intrazellulären Kationen steht Magnesium nach Kalium an zweiter Stelle. Magnesium ist ein Kofaktor zahlreicher Enzymsysteme, die u. a. am PhosphatStoffwechsel beteiligt sind. Von besonderer Bedeutung ist der Einfluss des Magnesiums auf die Muskelkontraktion.
5.2 Pharmakokinetische Eigenschaften
Resorption
Aus Magnesiocard® 2,5 mmol / -5 mmol / -7,5 mmol / -forte 10 mmol / -forte 10 mmol Orange wird Magnesium zu ca. 50 - 60 % in den distalen Dünndarmabschnitten resorbiert; bei Vorliegen eines Magnesiummangels steigt die Resorptionsquote bis auf 70 %.
Verteilung
Magnesium wird aktiv über die Zellmembran nach den Gesetzen der Michaelis-Menten-Kinetik in die Zelle aufgenommen. Influx und Efflux sind gekoppelt und werden bestimmt durch ein energieabhängiges Transportsystem.
Die Verteilung des Magnesiums im Organismus ist wie folgt:
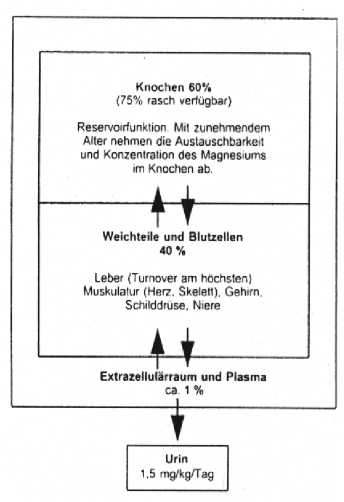
Blut-Liquor-Schranke
Magnesium wird entgegen einem elektrochemischen Gradienten durch ein Carriersystem über die Liquorschranke befördert. Die Liquor-Magnesium-Konzentration wird innerhalb sehr enger Grenzen aufrechterhalten und durch das aktive Magnesium-Transport-System reguliert.
Plazentaschranke
Für Magnesium besteht ein aktives Transportsystem, das die Passage über die Plazentaschranke reguliert. Die fetale Plasma-Magnesium-Konzentration ist höher als die maternale Magnesium-Konzentration. Der Transportprozess erfolgt gegen einen Konzentrationsgradienten.
Muttermilch
Die Magnesiumkonzentration der Muttermilch präeklamptischer Patientinnen nach MgSO4-Infusionen ist in den ersten 24 Stunden post partum signifikant erhöht. Es besteht eine direkte Korrelation zwischen Serum-Magnesium und MagnesiumKonzentration der Muttermilch.
Metabolismus
Magnesiumaspartat-hydrochlorid wird durch Enzyme in Mg2+, Asparaginsäure und Cl-gespalten. Die Asparaginsäure wird zu Oxalacetat abgebaut, das in den Zitronensäurezyklus eingeht.
Elimination
Resorbiertes Mg2+ wird innerhalb von 36 Stunden über die Nieren ausgeschieden.
Akute Toxizität
Vergiftungen nach oraler Einnahme von Magnesiumsalzen sind selten, kommen jedoch im Zusammenhang mit einer Niereninsuffizienz vor.
Beim Menschen können orale Dosen von 50 g Magnesium in Form von Magnesiumsulfat tödlich sein (siehe 4.9 Überdosierung).
Chronische Toxizität Siehe 4.8 Nebenwirkungen.
Reproduktionstoxizität
Es liegen keine Hinweise auf ein Fehlbildungsrisiko vor.
6. PHARMAZEUTISCHE ANGABEN
6.1 Liste der sonstigen Bestandteile
Magnesiocard® 2,5 mmol:
Kartoffelstärke, hochdisperses Siliciumdioxid, Magnesiumstearat (Ph.Eur.), Methacrylsäure-Ethylacrylat-Copolymer (1:1) (Ph.Eur.), Talkum, Dimeticon, Triethylcitrat.
Magnesiocard® 2,5 mmol enthält kein Gluten und keine Lactose.
Magnesiocard® 5 mmol:
Sucrose, Citronensäure, Saccharin-Natrium, Macrogol 6000, Zitronenaroma. Magnesiocard® 5 mmol enthält kein Gluten und keine Lactose.
Magnesiocard® 7,5 mmol:
Citronensäure, Natriumhydrogencarbonat, Natriumcarbonat, Kaliumhydrogencarbonat, Acesulfam-Kalium, Aspartam (enthält Phenylalanin), Macrogol 6000, hochdisperses Siliciumdioxid, Zitronen- und Limettenaroma.
Magnesiocard® 7,5 mmol enthält kein Gluten und keine Lactose.
Magnesiocard® forte 10 mmol:
Citronensäure, Macrogol 6000, Natriumcyclamat, Saccharin-Natrium, hochdisperses Siliciumdioxid, Grapefruitaroma.
Magnesiocard® forte 10 mmol enthält kein Gluten und keine Lactose.
Magnesiocard® forte 10 mmol Orange:
Citronensäure, Macrogol 6000, Natriumcyclamat, Saccharin-Natrium, hochdisperses Siliciumdioxid, Betacaroten, Maltodextrin, Arabisches Gummi, mittelkettige Triglyceride, Sorbitol (Ph.Eur.), Ascorbinsäure, all-rac-a-Tocopherol, Siliciumdioxid-Hydrat, Orangenaroma.
Magnesiocard® forte 10 mmol Orange enthält kein Gluten und keine Lactose.
Nicht zutreffend.
6.3 Dauer der Haltbarkeit
Magnesiocard® 2,5 mmol / -forte 10 mmol: 3 Jahre Magnesiocard® 5 mmol / -7,5 mmol / -forte 10 mmol Orange: 5 Jahre
6.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung
Magnesiocard® 5 mmol / -forte 10 mmol:
Nicht über 25°C aufbewahren.
Magnesiocard® 7,5 mmol:
In der Originalverpackung aufbewahren. Das Röhrchen fest verschlossen halten, um den Inhalt vor Feuchtigkeit zu schützen!
Magnesiocard® 2,5 mmol/ -forte 10 mmol Orange:
Nicht über 30°C aufbewahren.
6.5 Art und Inhalt des Behältnisses
Magnesiocard® 2,5 mmol, Filmtabletten (Blister im Umkarton):
50 Filmtabletten 100 Filmtabletten 200 Filmtabletten 1000 Filmtabletten
Magnesiocard® 5 mmol,
Pulver zur Herstellung einer Lösung zum Einnehmen (Beutel im Umkarton):
20 Beutel 50 Beutel 100 Beutel 500 Beutel
Magnesiocard® 7,5 mmol, Brausetabletten (Röhrchen im Umkarton):
20 Brausetabletten 50 Brausetabletten 100 Brausetabletten
Magnesiocard® forte 10 mmol / -forte 10 mmol Orange,
Pulver zur Herstellung einer Lösung zum Einnehmen (Beutel im Umkarton):
20 Beutel 50 Beutel 100 Beutel
500 Beutel
6.6 Besondere Vorsichtsmaßnahmen für die Beseitigung
Keine besonderen Anforderungen.
7. INHABER DER ZULASSUNG
Verla-Pharm Arzneimittel GmbH & Co. KG
Hauptstraße 98
D-82327 Tutzing
Postfach 1261
D-82324 Tutzing
Telefon: (08158)257-0
Telefax: (08158)257-254
33210.00. 01
44735.00. 02
44739.00. 02
33210.00. 00
44735.01.01
44739.01.01
33210.00. 02
44735.00. 00
44739.00. 00
Magnesiocard® forte 10 mmol: 33210.01.00
Magnesiocard® forte 10 mmol Orange: 44735.00.01
44739.00.01
9. DATUM DER ERTEILUNG DER ZULASSUNG/VERLÄNGERUNG DER ZULASSUNG
Magnesiocard® 2,5 mmol (33210.00.01):
Datum der Erteilung der Zulassung: 27. August 1997 Datum der letzten Verlängerung der Zulassung: 02. Juli 2003
Magnesiocard® 2,5 mmol (44735.00.02/44739.00.02):
Datum der Erteilung der Zulassung: 19. Juli 1999
Datum der letzten Verlängerung der Zulassung: 14. Februar 2005
Magnesiocard® 5 mmol (33210.00.00):
Datum der Erteilung der Zulassung: 27. August 1997 Datum der letzten Verlängerung der Zulassung: 02. Juli 2003
Magnesiocard® 5 mmol (44735.01.01/44739.01.01):
Datum der Erteilung der Zulassung: 19. Juli 1997
Datum der letzten Verlängerung der Zulassung: 14. Februar 2005
Magnesiocard® 7,5 mmol (33210.00.02):
Datum der Erteilung der Zulassung: 27. August 1997 Datum der letzten Verlängerung der Zulassung: 02. Juli 2003
Magnesiocard® 7,5 mmol (44735.00.00/44739.00.00):
Datum der Erteilung der Zulassung: 10. Mai 1999
Datum der letzten Verlängerung der Zulassung: 14. Februar 2005
Magnesiocard® forte 10 mmol (33210.01.00):
Datum der Erteilung der Zulassung: 27. August 1997 Datum der letzten Verlängerung der Zulassung: 02. Juli 2003
Magnesiocard® forte 10 mmol Orange (44735.00.01/44739.00.01):
Datum der Erteilung der Zulassung: 10. Mai 1999
Datum der letzten Verlängerung der Zulassung: 14. Februar 2005
10. STAND DER INFORMATION
11.2015
Verkaufsabgrenzung: Apothekenpflichtig
Seite 12 von 12