Metronidazol Hexal 400Mg Tabletten
F achinformation
1. BEZEICHNUNG DES ARZNEIMITTELS
Metronidazol HEXAL® 400 mg Tabletten Wirkstoff: Metronidazol
2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
1 Tablette enthält 400 mg Metronidazol.
Sonstiger Bestandteil: Lactose-Monohydrat
Vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt 6.1.
3. DARREICHUNGSFORM
Tablette
Weiße, längliche Tablette mit Bruchkerbe auf beiden Seiten.
Die Tablette kann in gleiche Dosen geteilt werden.
4. KLINISCHE ANGABEN
4.1 Anwendungsgebiete
Bei folgenden Indikationen ist Metronidazol bei Erwachsenen und Kindern angezeigt:
• Trichomoniasis,
• bakterielle Vaginose (Aminkolpitis, unspezifische Kolpitis),
• Amöbiasis,
• Lambliasis (Giardiasis),
• Infektionen mit Beteiligung von Anaerobiern, besonders Infektionen, die vom weiblichen Genitale, Magen-Darm-Trakt, Hals-Nasen-Ohren- und Zahn-Mund-Kiefer-Bereich ausgehen,
• Infektionsprophylaxe bei operativen Eingriffen im gynäkologischen Bereich oder im MagenDarm-Trakt.
Die offiziellen Richtlinien für den angemessenen Gebrauch von antimikrobiellen Wirkstoffen sind bei der Anwendung von Metronidazol zu berücksichtigen.
4.2 Dosierung und Art der Anwendung
Dosierung
Erwachsene
Die empfohlene Tagesdosis beträgt 0,2 bis maximal 2 g; die mittlere Dosis 0,8-1 g. Sie wird gewöhnlich auf 2 - 3 Einzeldosen verteilt.
Unkomplizierte Infektionen
Bei niedriger Dosierung (0,6 g/Tag oder weniger) ist eine mehrtägige Behandlung (5-7 Tage) erforderlich.
Bei höherer Dosierung (1-2 g/Tag) kann eine kurze Therapiedauer (1-3 Tage) ausreichend sein.
Bakterielle Vaginose und Trichomoniasis Therapie mit Einmalgabe von 2 g möglich.
Alternativ bei
• Bakterieller Vaginose
1 g Metronidazol/Tag (aufgeteilt in 2-3 Einzeldosen) für insgesamt 7 Tage.
• Trichomoniasis (insbesondere in hartnäckigen Fällen)
0,8-1(-1,6) g Metronidazol/Tag (aufgeteilt in 2-3 Einzeldosen) für insgesamt 7 Tage.
Bei Trichomoniasis ist eine Untersuchung und ggf. synchrone Behandlung der/des Sexualpartner/s angezeigt.
Bei
• Endometritis und Adnexitis,
• Entzündungen im Hals-Nasen-Ohren- und Zahn-Mund-Kiefer-Bereich,
• Peritonitis und Abszessen im Bauchraum
muss die Therapie systemisch (oral oder intravenös) erfolgen. Die Initialdosis sollte 1,6 - 2 g sein mit einer täglichen Erhaltungsdosis von 1 g für 5 - 7 Tage. Nur in Ausnahmefällen sollte die Dosis auf 1,4 g/Tag gesteigert werden.
Die Prophylaxe sollte auf eine einmalige Gabe von 0,6 g bis maximal 2 g beschränkt bleiben.
Kinder und Jugendliche
Kinder bis 12 Jahre erhalten zur Therapie von Infektionen, die durch anaerobe Bakterien verursacht sind, 20 mg bis 30 mg/kg KG (Körpergewicht) einmal pro Tag. Abhängig vom Schweregrad kann die Dosis auf 40 mg/kg KG pro Tag erhöht werden. Die Dauer der Behandlung beträgt üblicherweise 7 Tage.
Bei bakterieller Vaginose bei Heranwachsenden beträgt die Dosis zweimal täglich 400 mg über 5 bis 7 Tage oder 2 g als Einmalgabe.
Bei urogenitaler Trichomoniasis erhalten Heranwachsende 2 g als Einmalgabe oder zweimal täglich 400 mg über 5 bis 7 Tage.
Kinder unter 10 Jahren nehmen 40 mg/kg KG als Einmalgabe (max. 2 g) oder 7 Tage lang 15 mg bis 30 mg/kg KG pro Tag, aufgeteilt auf zwei bis drei Dosen täglich.
Bei Lambliasis (Giardiasis) werden Kinder über 10 Jahre mit 2 g einmal pro Tag über 3 Tage oder mit 400 mg dreimal täglich über 5 Tage behandelt.
Kinder von 7 bis 10 Jahren: 1000 mg einmal täglich über 3 Tage.
Kinder von 3 bis 7 Jahren: 600 mg bis 800 mg einmal täglich über 3 Tage.
Kinder von 1 bis 3 Jahren: 500 mg einmal täglich über 3 Tage.
Alternativ erhalten Kinder unter 10 Jahren 15 mg bis 40 mg/kg KG pro Tag über 3 Tage, aufgeteilt auf zwei bis drei Dosen täglich.
Bei Amöbiasis erhalten Kinder über 10 Jahre 400 mg bis 800 mg dreimal täglich über 5 bis 10 Tage. Kinder unter 10 Jahren erhalten 35 mg bis 50 mg/kg KG pro Tag, aufgeteilt auf drei Dosen täglich, über 5 bis 10 Tage (max. 2,4 g/Tag).
Zur perioperativen Prophylaxe bei Kindern bis 11 Jahre werden einmalig 20 mg bis 30 mg/kg KG ein bis zwei Stunden vor dem Eingriff gegeben.
Für Kinder unter 6 Jahren sind Darreichungsformen wie Tabletten, die unzerkaut einzunehmen sind, nicht geeignet.
Niereninsuffizienz und Dialyse
Metronidazol wird mit zunehmender Einschränkung der Nierenfunktion (Niereninsuffizienz) vermehrt fäkal ausgeschieden (biliär mit dem Stuhl).
Bei Nierenversagen (Anurie) sollte die Dosierung auf 400 bis 500 mg Metronidazol im 12-stündigen Intervall herabgesetzt werden. Da Metronidazol-Metaboliten durch Hämodialyse rasch entfernt werden, ist bei hämodialysierten Patienten keine Herabsetzung der Dosis erforderlich (siehe Abschnitt 4.4).
Leberfunktionsstörungen
Metronidazol sollte bei Patienten mit Leberfunktionsstörungen mit Vorsicht angewendet werden (siehe Abschnitt 4.4).
Art der Anwendung
Die Tabletten werden unzerkaut mit ausreichend Flüssigkeit während der Mahlzeiten oder danach geschluckt.
Die Dauer der Anwendung ist abhängig von der jeweiligen Erkrankung (siehe oben) und darf in der Regel 10 Tage nicht überschreiten (siehe auch Abschnitt 4.4).
4.3 Gegenanzeigen
Überempfindlichkeit gegen den Wirkstoff Metronidazol, andere 5-Nitroimidazole oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile.
Eine Ausnahme besteht, wenn eine lebensbedrohliche Infektion vorliegt und andere Arzneimittel wirkungslos sind.
4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung
Metronidazol sollte im 1. Trimenon der Schwangerschaft nur bei schweren, lebensbedrohlichen Infektionen eingesetzt werden (siehe Abschnitte 4.6 und 5.3).
Bei Patienten mit schweren Leberschäden, Störungen der Blutbildung sowie Erkrankungen des Zentral- oder peripheren Nervensystems ist vor der Therapie mit Metronidazol eine sorgfältige Nutzen-Risiko-Abwägung nötig.
Die Eliminations-Halbwertszeit von Metronidazol bleibt auch bei Niereninsuffizienz unverändert. Daher ist eine Dosisreduktion von Metronidazol nicht erforderlich. Bei diesen Patienten kann es jedoch zur Akkumulation von Metronidazol-Metaboliten kommen. Die klinische Bedeutung ist derzeit nicht bekannt.
Bei Patienten unter Hämodialyse werden Metronidazol und seine Metabolite während einer 8-stündigen Dialyse vollständig entfernt. Daher sollte Metronidazol sofort nach der Hämodialyse wieder verabreicht werden.
Bei Patienten mit Niereninsuffizienz, die sich einer intermittierenden Peritonealdialyse oder einer kontinuierlichen ambulanten Peritonealdialyse unterziehen müssen, ist keine Dosisanpassung von Metronidazol erforderlich.
Nicht gleichzeitig mit Alkohol einnehmen (siehe Abschnitt 4.5).
Die Behandlung mit Metronidazol oder einem anderen Nitroimidazol-haltigen Arzneimittel darf in der Regel 10 Tage nicht überschreiten. Diese Frist darf nur in Einzelfällen bei besonders strenger Indikationsstellung überschritten werden. Die Behandlung sollte möglichst selten wiederholt werden. Die Begrenzung der Therapiedauer ist erforderlich, weil sich eine Schädigung menschlicher Keimzellen nicht ausschließen lässt und weil in tierexperimentellen Studien eine Zunahme von bestimmten Tumoren gesehen wurde (siehe Abschnitt 5.3).
Sollte aus zwingenden Gründen Metronidazol länger als die empfohlene Zeitdauer gegeben werden müssen, wird empfohlen, dass regelmäßig Blutuntersuchungen, besonders die Bestimmung der Leukozytenzahl, durchgeführt werden (siehe Abschnitt 4.8). Außerdem sollte besonders auf periphere oder zentralnervöse Nebenwirkungen geachtet werden, wie z. B. Parästhesien, Ataxien, Schwindel und Krampfanfalle.
Bei schweren und anhaltenden Durchfällen ist an eine pseudomembranöse Kolitis zu denken, die lebensbedrohlich sein kann (siehe Abschnitt 4.8).
In diesen Fällen ist eine Beendigung der Therapie mit Metronidazol in Abhängigkeit von der Indikation zu erwägen und ggf. sofort eine angemessene Behandlung einzuleiten. Arzneimittel, die die Peristaltik hemmen, dürfen nicht eingenommen werden.
Beim Auftreten schwerer akuter Überempfindlichkeitsreaktionen (z. B. Anaphylaxis) (siehe Abschnitt 4.8) muss die Behandlung mit Metronidazol sofort abgebrochen werden und die üblichen entsprechenden Notfallmaßnahmen eingeleitet werden.
Bei Trichomoniasis ist eine Untersuchung und gegebenenfalls synchrone Behandlung der/des Sexualpartner/s angezeigt. Geschlechtsverkehr sollte während der Therapie unterbleiben. Es besteht die Möglichkeit, dass nach Eliminierung von Trichomonas vaginalis eine Infektion mit Gonokokken persistiert.
Metronidazol wird hauptsächlich über Oxidation in der Leber metabolisiert. Eine erhebliche Beeinträchtigung der Clearance von Metronidazol kann bei fortgeschrittener Leberinsuffizienz auftreten.
Bei Patienten mit hepatischer Enzephalopathie kann es zu einer signifikanten Kumulierung kommen, und die resultierenden hohen Plasmakonzentrationen von Metronidazol können die Symptome der Enzephalopathie verstärken. Metronidazol sollte daher bei Patienten mit hepatischer Enzephalopathie mit Vorsicht angewendet werden. Die tägliche Dosis sollte auf ein Drittel reduziert werden und nur einmal täglich verabreicht werden.
Patienten sollen gewarnt werden, dass durch Metronidazol der Ham dunkel sein kann.
Durch die inadequate Evidenz eines Mutagenitätsrisikos beim Menschen (siehe Abschnitt 5.3), sollte die Behandlung mit Metroniazol über einen längerdauernden Zeitraum als üblich sorgfältig abgewogen werden.
Dieses Arzneimittel enthält Lactose. Patienten mit der seltenen hereditären Galactose-Intoleranz, Lactase-Mangel oder Glucose-Galactose-Malabsorption sollten Metronidazol HEXAL nicht einnehmen.
4.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen Alkohol/Disulfiram
Patienten sollten angewiesen werden, während der Behandlung mit Metronidazol und für mindestens 48 Stunden danach keinen Alkohol zu trinken, da die Möglichkeit einer Disulfiram-ähnlichen Reaktion besteht. Über psychotische Reaktionen wurde bei Patienten berichtet, die Metronidazol und Disulfiram gleichzeitig einnahmen.
Antikoagulanzien
Über die Potenzierung einer gerinnungshemmenden Wirkung wurde berichtet, wenn Metronidazol zusammen mit oralen Antikoagulanzien vom Warfarintyp angewendet wurde. Die Dosis des Antikoagulans muss möglicherweise reduziert werden. Die Thromboplastinzeiten sollten überwacht werden. Es besteht keine Wechselwirkung mit Heparin.
Lithium
Bei Patienten, die gleichzeitig mit Lithium und Metronidazol behandelt wurden, wurde über eine Retention von Lithium und begleitende Hinweise auf eine mögliche Nierenschädigung berichtet. Eine Therapie mit Lithium sollte reduziert oder beendet werden, bevor Metronidazol gegeben wird. Bei Patienten, die mit Lithium behandelt werden, während sie Metronidazol erhalten, sollten die Plasmakonzentrationen von Lithium, Kreatinin und der Elektrolyte überwacht werden.
Barbiturate/Phenytoin
Patienten, die Phenobarbital oder Phenytoin erhalten, metabolisieren Metronidazol mit einer wesentlich höheren Rate als normal, wodurch die Halbwertszeit sich auf etwa 3 Stunden verringert.
Cimetidin
Cimetidin kann in Einzelfallen die Elimination von Metronidazol beeinträchtigen und dadurch zu erhöhten Metronidazol-Serumkonzentrationen führen.
Ciclosporin
Bei Patienten, die mit Ciclosporin behandelt werden, besteht das Risiko für einen Anstieg der Serumspiegel von Ciclosporin. Die Serumspiegel von Ciclosporin und Kreatinin sollten engmaschig überwacht werden, wenn eine gleichzeitige Anwendung erforderlich ist.
5-Fluorouracil
Metronidazol verringert die Clearance von 5-Fluorouracil, sodass es zu einer verstärkten Toxizität von 5-Fluorouracil kommen kann.
Busulfan
Die Plasmaspiegel von Busulfan können durch Metronidazol ansteigen, wodurch es zu schwerer Busulfan-Toxizität kommen kann.
Beeinflussung von Laboruntersuchungen
Metronidazol beeinflusst Messungen von Triglyceriden, Glucose, LDH, GOT und GPT.
4.6 Fertilität, Schwangerschaft und Stillzeit
Metronidazol passiert die Plazentaschranke. Obwohl es bis heute keinen gesicherten Hinweis dafür gibt, dass Metronidazol zu einer Schädigung des Embryos oder Feten führt, sollte Metronidazol im 1. Trimenon nur bei schweren, lebensbedrohlichen Infektionen eingesetzt werden. Im 2. und 3. Trimenon und während der Laktationsperiode kann Metronidazol nach Nutzen-Risiko-Abwägung auch bei anderen Indikationen eingesetzt werden. Sollte aus zwingenden Gründen Metronidazol während der Schwangerschaft gegeben werden müssen, sollte soweit möglich eine lokale Darreichungsform angewandt werden.
Bei der oralen Anwendung in der Stillperiode sollte während der Therapie das Stillen unterbrochen werden (siehe Abschnitt 5.3)
4.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen
Metronidazol kann Nebenwirkungen haben (z. B. Verwirrtheitszustände, Schwindel, Halluzinationen, Krampfanfälle oder Sehstörungen), die das Reaktionsvermögen so weit verändern, dass die Fähigkeit zur aktiven Teilnahme am Straßenverkehr oder zum Bedienen von Maschinen beeinträchtigt wird (die Patienten sollten dann diese Tätigkeiten nicht mehr ausführen). Dies gilt in verstärktem Maße bei Behandlungsbeginn und im Zusammenwirken mit Alkohol.
4.8 Nebenwirkungen
Bei den Häufigkeitsangaben zu Nebenwirkungen werden folgende Kategorien zugrunde gelegt:
Sehr häufig Häufig Gelegentlich Selten Sehr selten Nicht bekannt
(> 1/10)
(> 1/100 bis < 1/10)
(> 1/1.000 bis < 1/100)
(> 1/10.000 bis < 1/1.000)
(< 1/10.000)
(Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar)
Schwerwiegende unerwünschte Reaktionen treten unter den empfohlenen Standard-Dosierungen selten auf. Ärzte, die in der klinischen Praxis eine Dauertherapie zur Linderung chronischer Erkrankungen über längere - als die empfohlenen - Zeiträume in Erwägung ziehen, werden aufgefordert, den möglichen therapeutischen Nutzen sorgfältig gegen das Risiko einer peripheren Neuropathie abzuwägen.
|
Tabelle: Nebenwirkungen | |||
|
Häufig (> 1/100 bis < 1/10) |
Gelegentlich (> 1/1.000 bis < 1/100) |
Sehr selten (< 1/10.000) |
nicht bekannt (Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar) |
|
Infektionen und parasitäre Erkrankungen | |||
|
Sprosspilzinfektionen (z. B. Candida) im Genitalbereich | |||
|
Erkrankungen des Blutes und des Lymphsystems | |||
|
Leukopenie, Granulozytopenie |
Agranulozytose, Thrombozytopenie, Panzytopenie | ||
|
Erkrankungen des Immunsystems | |||
|
anaphylaktische Reaktionen, angioneurotisches Ödem (Quincke-Ödem), Urtikaria, Arzneimittelfieber |
Anaphylaktischer Schock (siehe Abschnitt „Notfallmaßnahmen bei Nebenwirkungen“) | ||
|
Psychiatrische Erkrankungen und Erkrankungen des Nervensystems | |||
|
Kopfschmerzen, Schwindel, Schläfrigkeit, Schlaflosigkeit, Halluzination, Verwirrtheitszustände, Erregbarkeit, Depression, Ataxie, periphere Neuropathien und Krampfanfälle1, 2 |
Enzephalopathie (z. B. Verwirrtheit, Fieber, Kopfschmerzen, Halluzinationen, Paralyse, Lichtempfindlichkeit , Störungen der Seh-und Bewegungsfähigkeit, Nackensteife) sowie subakutes Kleinhirnsyndrom (z. B. Ataxie, Dysarthrie, Gangstörungen, Nystagmus und Tremor), die sich bei Absetzen des Medikaments zurückbilden können |
aseptische Meningitis | |
|
Augenerkrankungen | |||
|
Sehstörungen wie Diplopie und Myopie (meist temporär) |
Neuropathie der Nervus opticus/Optikusneuritis | ||
|
Erkrankungen des Gastrointestinaltrakts | |||
|
Geschmacksstörung (z. B. metallischer Geschmack), bitteres Aufstoßen, Zungenbelag, Glossitis, Stomatitis, Magendrücken, Übelkeit, Erbrechen, |
Pankreatitis2, pseudomembranöse Enterokolitis (siehe Abschnitt „Notfallmaßnahmen bei Nebenwirkungen“) | ||
|
Appetitlosigkeit, Diarrhoe | |||
|
Leber- und Gallenerkrankungen | |||
|
Leberfunktionsstörunge n (z. B. Erhöhung von Transaminasen [AST, ALT], alkalische Phosphatase und Bilirubin im Serum) |
Ikterus2, cholestatische Hepatitis |
Leberversagen (mit Erfordernis einer Lebertransplantation) bei Patienten, die gleichzeitig mit anderen Antibiotika behandelt wurden | |
|
Erkrankungen der Haut und des Unterhautzellgewebes | |||
|
Hautreaktionen (z. B. urtikarielles Exanthem, Pustelausschläge, Pruritus, Flush) |
Erythema exsudativum multiforme, Stevens-J ohnson-Syndrom, toxische epidermale Nekrolyse | ||
|
Skelettmuskulatur-, Bindegewebs- und Knochenerkrankungen | |||
|
Myalgie, Arthralgie | |||
|
Erkrankungen der N |
ieren und Harnwege | ||
|
Dunkelfärbung des Urins ohne Krankheitswert (Ursache: Metabolit von Metronidazol) |
Dysurie, Zystitis, Harninkontinenz | ||
|
Allgemeine Erkrankungen und Beschwerden am Verabreichungsort | |||
|
Schwächegefühl | |||
|
1 nach sehr hoher Dosierung oder Langzeitbehandlung, 2 reversibel nach Dosisreduktion oder Absetzen | |||
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung dem
Bundesinstitut für Arzneimittel und Medizinprodukte Abt. Pharmakovigilanz Kurt-Georg-Kiesinger-Allee 3 D-53175 Bonn Website: www.bfarm.de
anzuzeigen.
Notfallmaßnahmen bei Nebenwirkungen
Therapie der pseudomembranösen Enterokolitis
Bei Auftreten einer pseudomembranösen Enterokolitis ist eine Beendigung der Therapie in Abhängigkeit von der Indikation zu erwägen und ggf. sofort eine angemessene Behandlung einzuleiten (z. B. Einnahme von speziellen Antibiotika/Chemotherapeutika, deren Wirksamkeit klinisch erwiesen ist). Arzneimittel, die die Peristaltik hemmen, sind kontraindiziert.
Schwere akute Überempfindlichkeitsreaktionen (z. B. anaphylaktischer Schock)
Bei schweren akuten Überempfindlichkeitsreaktionen (z. B. anaphylaktischem Schock) muss die Behandlung mit Metronidazol HEXAL sofort abgebrochen werden und die üblichen entsprechenden Notfallmaßnahmen (z. B. Antihistaminika, Kortikosteroide, Sympathomimetika und ggf. Beatmung) eingeleitet werden.
Art und Schweregrad von Nebenwirkungen sind bei Kindern und Erwachsenen gleich.
4.9 Überdosierung
Nach Einmaldosen von bis zu 15 g Metronidazol in suizidaler Absicht wurden Übelkeit, Erbrechen, Hyperreflexie, Ataxie, Tachykardie, Atemnot und Desorientierung beobachtet. Todesfälle sind nicht beschrieben.
Ein spezifisches Antidot ist nicht bekannt. Bei einer symptomatischen Therapie ist mit einer vollständigen Rückbildung der Beschwerden nach wenigen Tagen zu rechnen.
5. PHARMAKOLOGISCHE EIGENSCHAFTEN
5.1 Pharmakodynamische Eigenschaften
Pharmakotherapeutische Gruppe
Metronidazol ist ein Antibiotikum aus der Gruppe der Nitroimidazole.
ATC-Code: J01XD01 Wirkungsweise
Metronidazol selbst ist antimikrobiell unwirksam. Es stellt die stabile und penetrationsfähige Ausgangsverbindung dar, aus der unter anaeroben Bedingungen durch die mikrobielle Pyruvat-Ferredoxin-Oxidoreduktase unter Oxidation von Ferredoxin und Flavodoxin Nitroso-Radikale gebildet werden, die an der DNS angreifen. Nitroso-Radikale bilden Addukte mit Basenpaaren in der DNS, wodurch es zu DNS-Strangbrüchen und nachfolgend zum Zelltod kommt.
Beziehung zwischen Pharmakokinetik und Pharmakodynamik
Die Wirksamkeit hängt im Wesentlichen von dem Quotienten aus maximaler Serumkonzentration (Cmax) und minimaler Hemmkonzentration (MHK) des Erregers ab.
Resistenzmechanismen
Die Resistenzmechanismen gegen Metronidazol bei anaeroben Bakterien sind erst teilweise aufgeklärt:
- Metronidazol-resistente Bacteroides-Stämme besitzen Resistenzdeterminanten, die Nitroimidazol-Reduktasen kodieren, die Nitroimidazole in Aminoimidazole umwandeln, wodurch die Bildung der für die antibakterielle Wirkung verantwortlichen Nitroso-Radikale verhindert wird.
- Die Metronidazol-Resistenz bei Helicobacter pylori beruht auf Mutationen in einem Gen, das für die NADPH-Nitroreduktase kodiert. Diese Mutationen bewirken einen Austausch von Aminosäuren und damit einen Funktionsverlust des Enzyms. Somit unterbleibt der Aktivierungsschritt vom Metronidazol zum reaktiven Nitroso-Radikal.
Es besteht zwischen Metronidazol und den anderen Nitroimidazolderivaten (Tinidazol, Ornidazol, Nimorazol) vollständige Kreuzresistenz.
Grenzwerte
Die Testung von Metronidazol erfolgt unter Benutzung der üblichen Verdünnungsreihe. Folgende minimale Hemmkonzentrationen für sensible und resistente Keime wurden festgelegt:
|
EUCAST (European Committee on Antimicrobial Susceptibility Testing) Grenzwerte | ||
|
Erreger |
Sensibel |
Resistent |
|
P Clostridium difficile |
< 2 mg/l |
> 2 mg/l |
|
r Andere Gram-positive Anaerobier |
< 4 mg/l |
> 4 mg/l |
|
äHelicobacter pylori |
< 1 mg/l |
> 1 mg/l |
|
v “Gram-negative Anaerobier |
< 4 mg/l |
> 4 mg/l |
Prävalenz der erworbenen Resistenz in Deutschland
Die Prävalenz der erworbenen Resistenz einzelner Spezies kann örtlich und im Verlauf der Zeit variieren. Deshalb sind - insbesondere für die adäquate Behandlung schwerer Infektionen - lokale Informationen über die Resistenzsituation erforderlich. Falls auf Grund der lokalen Resistenzsituation die Wirksamkeit von Metronidazol in Frage gestellt ist, sollte eine Therapieberatung durch Experten angestrebt werden. Insbesondere bei schwerwiegenden Infektionen oder bei Therapieversagen ist eine mikrobiologische Diagnose mit dem Nachweis des Erregers und dessen Empfindlichkeit gegenüber Metronidazol anzustreben.
Prävalenz der erworbenen Resistenz in Deutschland auf der Basis von Daten der letzten 5 Jahre aus nationalen Resistenzüberwachungsprojekten und -studien (Stand: Januar 2015):_
Üblicherweise empfindliche Spezies
Anaerobe Mikroorganismen
Bacteroides ^ fragilis
Clostridium difficile
Clostridium perfringens
O A
Fusobacterium spp.
O
Peptoniphilus spp.
O
Peptostreptococcus spp.
o
Porphyromonas spp.
o
Prevotella spp.
o
Veillonella spp.
o
Andere Mikroorganismen
Entamoeba histolytica °
Gardnerella vaginalis °
Giardia lamblia °
Trichomonas vaginalis °
Spezies, bei denen erworbene Resistenzen ein Problem bei der Anwendung darstellen können
Aerobe Gram-negative Mikroorganismen
Helicobacter pylori
Alle obligat aeroben Bakterien
Gram-positive Mikroorganismen
Enterococcus spp._
Staphylococcus spp._
Streptococcus spp._
Gram-negative Mikroorganismen_
Enterobacteriaceae_
Haemophilus spp._
° Bei Veröffentlichung der Tabellen lagen keine aktuellen Daten vor. In der Primärliteratur, Standardwerken und Therapieempfehlungen wird von einer Empfindlichkeit ausgegangen.
A Nur bei Penicillin-Allergie
5.2 Pharmakokinetische Eigenschaften
Nach oraler Applikation wird Metronidazol rasch und nahezu vollständig resorbiert mit maximalen Serumspiegeln nach 1 bis 2 Stunden. Bei rektaler Applikation stehen ca. 80 % der Substanz systemisch zur Verfügung, wobei das Maximum im Serum nach ca. 4 Stunden erreicht wird. Nach vaginaler Applikation können nur ca. 20 % im Serum gefunden werden, wobei das Maximum hier noch später, nach 8 bis 24 Stunden, erreicht wird. Die Serumhalbwertszeit beträgt ca. 8 (6 bis 10) Stunden. Im menschlichen Organismus werden verschiedene Metaboliten gebildet. Hauptmetaboliten sind der Hydroxymetabolit (1-(2-Hydroxyethyl)-2-hydroxymethyl-5-nitroimidazol) und der „saure“ Metabolit (2-Methyl-5-nitroimidazol-1-yl-essigsäure).
Circa 80 % der Substanz werden über die Niere ausgeschieden, wobei der nicht metabolisierte Anteil weniger als 10 % ausmacht. Geringe Mengen (ca. 6 %) werden auch über die Leber ausgeschieden. Niereninsuffizienz verlängert die Ausscheidung nur unwesentlich. Bei schwerer Leberinsuffizienz ist mit einer verzögerten Elimination zu rechnen. Die Halbwertszeit kann bei Patienten mit stark eingeschränkter Leberfunktion bis auf 30 Stunden verlängert sein. Die Proteinbindung liegt unter 20 %. Das scheinbare Verteilungsvolumen beträgt etwa 36 Liter.
5.3 Präklinische Daten zur Sicherheit Akute Toxizität
Die akute Toxizität ist an Mäusen bei zwei Applikationsarten geprüft worden. Die LD50-Werte betragen bei oraler Zufuhr 3800 mg/kg KG (Körpergewicht), bei intraperitonealer Zufuhr 3950 mg/kg KG. Die akute Toxizität ist danach sehr gering.
Akute Vergiftungen beim Menschen sind nicht bekannt geworden. Der toxische Blutspiegel wird mit 200 Mikrogramm/ml angegeben, das ist zehnfach höher als bei bestimmungsgemäßer oraler Therapie.
Chronische/subchronische Toxizität
In chronischen Toxizitätsstudien konnten bei Gabe von Metronidazol über 26 bis 80 Wochen bei Ratten keine Nebenwirkungen festgestellt werden. Erst bei Dosen von 300 bis 600 mg/kg KG/Tag traten Testisdystrophien und Prostataatrophien auf. Toxische Effekte bei Hunden bei Gabe von 75 mg/kg KG/Tag äußerten sich in Form von Ataxien und Tremor. Bei Untersuchungen an Affen zeigte sich nach einer einjährigen Gabe von 45, 100 bzw. 225 mg/kg KG/Tag eine dosisabhängige Zunahme von Leberzelldegenerationen.
Als niedrigste toxische Dosis bei 8 Wochen langer, kontinuierlicher, oraler Zufuhr bei Menschen wurden 18 mg/kg KG/Tag angegeben. Insgesamt seltene Nebenwirkungen sind cholestatische Hepatose und periphere Neuropathien.
Mutagenes und tumorerzeugendes Potential
Tierexperimente an verschiedenen Nagern haben gezeigt, dass es sich bei Metronidazol um einen tumorerzeugenden Stoff handelt, dessen tumorerzeugendes Potential schwach ausgeprägt ist. Wenn auch Verlaufsbeobachtungen beim Menschen keinen Beweis dafür erbracht haben, dass die Verabreichung von Metronidazol zu einem erhöhten Tumorrisiko führt, bleibt doch das theoretische Risiko durch den Reduktionsmetaboliten, der durch die Bakterienflora gebildet wird und in sehr geringen Mengen im Urin nachweisbar ist.
Metronidazol zeigte in einer Reihe von Tests an Bakterien mit verschiedenen Aktivierungssystemen deutliche mutagene Wirkungen. Eine Anzahl weiterer In-vitro- und In-vivo-Tests verlief negativ. In Lymphozyten von Patienten wurden nach längerer Therapie mit Metronidazol erhöhte Quoten an Chromosomenmutationen gefunden.
Reproduktionstoxizität
Tierversuche haben bei Ratten bis zu Dosen von 200 mg/kg KG/Tag und bei Kaninchen bis zu 150 mg/kg KG/Tag keine teratogenen Effekte oder andere embryotoxische Wirkungen ergeben.
Metronidazol besitzt eine gute Gewebegängigkeit, so dass die Plazenta keine Schranke darstellt.
Auch der Gehalt in der Muttermilch ist hoch (mehr als 50 % des Serumwertes).
Die Sicherheit einer Anwendung von Metronidazol in der Schwangerschaft ist nicht ausreichend belegt. Insbesondere für die Frühschwangerschaft liegen widersprüchliche Berichte vor. Einige Studien haben Hinweise auf eine erhöhte Fehlbildungsrate ergeben. Das Risiko möglicher Spätfolgen, einschließlich des kanzerogenen Risikos, ist bisher nicht geklärt. Im Falle einer uneingeschränkten Anwendung von Nitroimidazolen durch die Mutter besteht für das Ungeborene bzw. Neugeborene das Risiko einer Krebsauslösung oder Erbgutschädigung. Gesicherte Hinweise für eine Schädigung des Embryos oder Feten gibt es bislang nicht.
6. PHARMAZEUTISCHE ANGABEN
6.1 Liste der sonstigen Bestandteile
Mikrokristalline Cellulose Cellulosepulver Crospovidon Lactose-Monohydrat Macrogol 6000 Magnesiumstearat (Ph.Eur.) Vorverkleisterte Stärke (Maisstärke) Povidon K30
Hochdisperses Siliciumdioxid
Hinweis für Diabetiker 1 Tablette enthält 0,025 BE.
6.2 Inkompatibilitäten
Nicht zutreffend
6.3 Dauer der Haltbarkeit
5 Jahre.
6.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung
Nicht über 30 °C lagern.
In der Originalverpackung aufbewahren, um den Inhalt vor Licht zu schützen.
6.5 Art und Inhalt des Behältnisses
PVC/Aluminium-Blisterpackungen Packungen mit 14 und 20 Tabletten.
Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht.
6.6 Besondere Vorsichtsmaßnahmen für die Beseitigung und sonstige Hinweise zur Handhabung
Keine besonderen Anforderungen.
Nicht verwendete Arzneimittel oder Abfallmaterial ist entsprechend den nationalen Anforderungen zu entsorgen.
7. INHABER DER ZULASSUNG
Hexal AG Industriestraße 25 83607 Holzkirchen Telefon: (08024) 908-0 Telefax: (08024) 908-1290 E-Mail: medwiss@hexal.com
8. ZULASSUNGSNUMMER
36917.00.00
9. DATUM DER ERTEILUNG DER ZULASSUNG/VERLÄNGERUNG DER ZULASSUNG
Datum der Erteilung der Zulassung: 17. März 1997 Datum der Verlängerung der Zulassung: 18. Oktober 2002
10. STAND DER INFORMATION
Januar 2016
11. VERKAUFSABGRENZUNG
V erschreibungspflichtig
Bioverfügbarkeit
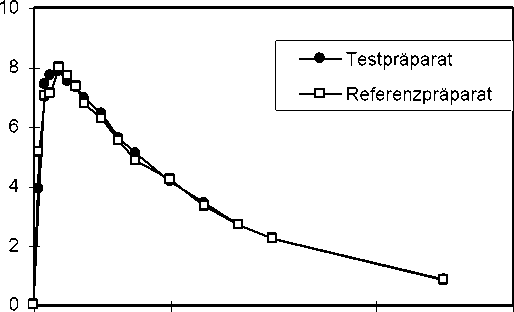
Eine im Jahr 1995/1996 durchgeführte Bioverfügbarkeitsuntersuchung an 20 gesunden Probanden (10 Frauen, 10 Männer; 18-43 Jahre) ergab im Vergleich zum Referenzpräparat:
Testpräparat Referenzpräparat
Cmax [hg/ml] 9,97 ± 2,36 10,28 ± 3,26
maximale Plasmakonzentration
tmax [h] 1,28 ± 1,05 1,19 ± 0,89
Zeitpunkt der maximalen Plasmakonzentration
AUC0-t [hg/ml* h] 81,35 ± 13,48 80,62 ± 14,21 Fläche unter der KonzentrationsZeit-Kurve
Angabe der Werte als Mittelwert und Streubreite (Standardabweichung)
Mittlere Plasmaspiegelverläufe im Vergleich zu einem Referenzpräparat in einem KonzentrationsZeit-Diagramm:
E
o)
o
'S
v
N
o
0 4 8 12 16 20 24 28