Nasacort Sanofi-Aventis 55 Mikrogramm/Sprühstoß Nasenspray, Suspension
FACHINFORMATION
1. BEZEICHNUNG DES ARZNEIMITTELS
NASACORT Sanofi-Aventis 55 Mikrogramm/Sprühstoß Nasenspray, Suspension
2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Eine Sprühflasche NASACORT Sanofi-Aventis* enthält 6,5 g Suspension mit 3,575 mg Triamcinolonacetonid oder 16,5 g Suspension mit 9,075 mg Triamcinolonacetonid. Ein Sprühstoß enthält 55 Mikrogramm Triamcinolonacetonid.
Sonstiger Bestandteil mit bekannter Wirkung: 15 Mikrogramm Benzalkoniumchlorid/Sprühstoß Vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt 6.1.
3. DARREICHUNGSFORM
Nasenspray, Suspension.
Unparfümierte, thixotrope wässrige Suspension mit mikrokristallinem Triamcinolonacetonid.
4. KLINISCHE ANGABEN
4.1 Anwendungsgebiete
Zur Behandlung der Symptome der saisonalen allergischen Rhinitis.
4.2 Dosierung und Art der Anwendung
Dosierung
Erwachsene ab 18 Jahren:
Empfohlene tägliche Anfangsdosierung: 220 Mikrogramm (entspricht 1 mal täglich 2 Sprühstößen in jedes Nasenloch). Sobald die Symptome unter Kontrolle sind, kann die Dosis auf 110 Mikrogramm (entspricht 1 mal täglich 1 Sprühstoß in jedes Nasenloch) reduziert werden.
Die Anwendung von Nasacort Sanofi-Aventis über einen Zeitraum von mehr als drei Monaten wird ohne ärztliche Aufsicht nicht empfohlen. Wenn sich die Symptome einer saisonalen allergischen Rhinitis innerhalb von 14 Tagen nicht bessern oder verschlechtern, muss ein Arzt konsultiert werden.
NASACORT Sanofi-Aventis steht für NASACORT Sanofi-Aventis 55 Mikrogramm/Sprühstoß.
Besondere Patientengruppen
Kinder und Jugendliche
NASACORT Sanofi-Aventis wird für Kinder und Jugendliche unter 18 Jahren nicht empfohlen.
Art der Anwendung
NASACORT Sanofi-Aventis ist nur zur nasalen Anwendung bestimmt.
Sprühflasche vor jedem Gebrauch leicht schütteln.
Nach Freisetzung von 5 Sprühstößen vor der ersten Anwendung (bis ein feiner Nebel entsteht) ist eine Dosierung von Mikrogramm ^g Triamcinolonacetonid pro Sprühstoß gewährleistet (In-vitro-Testergebnisse). Dies ist auch ausreichend, falls NASACORT Sanofi-Aventis 2 Wochen nicht angewendet wird.
Falls das Präparat länger als 2 Wochen nicht benutzt wurde, reicht die Freisetzung eines Sprühstoßes aus, um eine exakte Dosierung sicherzustellen. Der Sprühkopf sollte währenddessen von Ihnen wegzeigen.
Nach Gebrauch des Nasensprays: Wischen Sie den Sprühkopf vorsichtig mit einem sauberen Tuch oder Taschentuch ab und setzen Sie die Schutzkappe wieder auf.
Falls das Nasenspray nicht funktioniert, kann es verstopft sein und Sie müssen es wie folgt reinigen. Versuchen Sie niemals eine Verstopfung mit Hilfe einer Nadel oder ähnlichen spitzen Gegenständen zu beseitigen oder das sehr kleine Sprühloch zu vergrößern, da dadurch der Sprühmechanismus zerstört würde.
Das Nasenspray muss mindestens ein Mal pro Woche gereinigt werden, sollte es verstopfen ist eine häufigere Reinigung nötig.
Reinigung des Nasensprays
1. Ziehen Sie nur die Schutzkappe und den Sprühkopf ab.
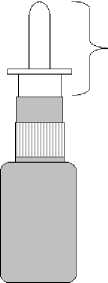
2. Weichen Sie die Schutzkappe und den Sprühkopf für ein paar Minuten in warmem Wasser ein und spülen Sie anschließend beide Teile unter kaltem, fließendem Wasser ab.
3. Schütteln oder klopfen Sie überschüssiges Wasser ab und lassen Sie Schutzkappe und Sprühkopf an der Luft trocknen.
4. Setzen Sie den Sprühkopf wieder auf.
5. Pumpen Sie bis ein feiner Nebel aufsteigt und verwenden Sie das Nasenspray wie gewöhnlich.
Die Sprühflasche mit 6,5 g Suspension sollte nach 30 Sprühstößen bzw. 1 Monat nach Öffnen nicht mehr verwendet werden, entsprechend sollte die Sprühflasche mit 16,5 g Suspension nach 120 Sprühstößen bzw. 2 Monate nach Öffnen nicht mehr verwendet werden. Flüssigkeitsreste sollten nicht in ein anderes Behältnis umgefüllt werden.
4.3 Gegenanzeigen
Überempfindlichkeit gegen den Wirkstoff oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile.
4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung
Besteht Grund zur Annahme einer Beeinträchtigung der Nebennierenrindenfunktion, sind bei der Umstellung von systemischer Steroidbehandlung auf NASACORT Sanofi-Aventis entsprechende Vorsichtsmaßnahmen zu beachten.
Bei Infektionen des Nasen-Rachenraumes mit Candida albicans, die in seltenen Fällen im Rahmen klinischer Studien mit NASACORT Sanofi-Aventis auftraten, kann eine geeignete lokale Behandlung und gegebenenfalls eine vorübergehende Unterbrechung der Therapie mit NASACORT Sanofi-Aventis erforderlich sein.
Aufgrund des inhibierenden Effektes von Kortikosteroiden auf die Wundheilung sollte NASACORT Sanofi-Aventis bei Geschwüren des Nasenseptums sowie nach Operationen und Verletzungen im Nasenraum bis zur vollständigen Abheilung mit Vorsicht angewendet werden.
Speziell unter hoher Dosierung und lang andauernder Anwendung sind auch bei nasal applizierten Kortikosteroiden systemische Wirkungen nicht auszuschließen. Im Vergleich zu oralen Kortikosteroiden ist die Wahrscheinlichkeit des Auftretens dieser systemischen Wirkungen viel geringer und sie können je nach Patient und Kortikoidpräparat variieren. Mögliche systemische Wirkungen umfassen das Cushing Syndrom, cushingoide Merkmale, Suppression der Nebennieren, Wachstumsretardierung bei Kindern und Jugendlichen, Katarakt, Glaukom sowie in noch selteneren Fällen eine Reihe verschiedener psychologischer Effekte oder Verhaltensauffälligkeiten, einschließlich psychomotorischer Hyperaktivität, Schlafstörungen, Ängstlichkeit, Depression oder Aggression (besonders bei Kindern),
Bei Überschreiten der empfohlenen Dosierung besteht die Möglichkeit einer klinisch relevanten Funktionsminderung der Nebennierenrinde. Bei Hinweisen auf eine deutliche Überschreitung der empfohlenen Dosierungen sollte unter Stress-Situationen (z.B. vor Operationen) eine systemische Kortikosteroidgabe erwogen werden.
Bei Patienten, die nasale Kortikosteroide erhielten, wurden Glaukome und Katarakte beschrieben. Deshalb ist bei Patienten mit Sehveränderungen oder mit erhöhtem Augeninnendruck, Glaukom und/oder Katarakten in der Vorgeschichte eine engmaschige Kontrolle erforderlich.
NASACORT Sanofi-Aventis enthält Benzalkoniumchlorid, das Hautreizungen hervorrufen kann.
Kinder und Jugendliche
NASACORT Sanofi-Aventis wird für Kinder und Jugendliche unter 18 Jahren nicht empfohlen.
4.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen
Es wurden keine Wechselwirkungsstudien durchgeführt.
4.6 Fetilität, Schwangerschaft und Stillzeit
Es liegen nur begrenzte klinische Erfahrungen bei Anwendung während der Schwangerschaft vor. Tierexperimentelle Untersuchungen zeigten, dass Kortikosteroide teratogene Wirkungen induzieren. Es kann nicht ausgeschlossen werden, dass Triamcinolonacetonid in die Muttermilch übertritt. Triamcinolonacetonid sollte daher während der Schwangerschaft und Stillzeit nur angewendet werden, wenn der potenzielle Nutzen für die Mutter gegenüber dem Risiko für das Kind überwiegt.
4.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen
NASACORT Sanofi-Aventis hat keinen oder einen vernachlässigbaren Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen.
4.8 Nebenwirkungen
Die in klinischen Studien mit NASACORT Sanofi-Aventis am häufigsten berichteten unerwünschten Reaktionen betrafen die Nasen-Rachen-Schleimhaut.
Bei den Häufigkeitsangaben zu Nebenwirkungen werden folgende Kategorien zugrunde gelegt:
Sehr häufig (> 1/10)
Häufig (> 1/100 bis < 1/10)
Gelegentlich (>1/1.000 bis < 1/100)
Selten (> 1/10.000 bis < 1/1.000)
Sehr selten (<1/10.000) und nicht bekannt (Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar)
Innerhalb jeder Häufigkeitsgruppe werden die Nebenwirkungen nach abnehmendem Schweregrad angegeben.
Die häufigsten Nebenwirkungen waren:
• Infektionen und parasitäre Erkrankungen Häufig: Influenza, Pharyngitis, Rhinitis
• Erkrankungen des Immunsystems
Nicht bekannt: Überempfindlichkeitsreaktionen (einschließlich Hautausschlag, Urtikaria, Juckreiz und Gesichtsödem)
• Psychiatrische Erkrankungen Nicht bekannt: Schlaflosigkeit
• Erkrankungen des Nervensystems Häufig: Kopfschmerzen
Nicht bekannt: Schwindel, Geruchs- und Geschmacksstörungen
• Augenerkrankungen
Nicht bekannt: Katarakt, Glaukom, erhöhter Augeninnendruck 1
Häufig: Bronchitis, Epistaxis, Husten Selten: Septumperforationen
Nicht bekannt: Irritation und Austrocknung der Nasenschleimhäute, nasale Kongestion, Niesen, Dyspnoe
• Erkrankungen des Gastrointestinaltrakts Häufig: Dyspepsie, Zahnprobleme
Nicht bekannt: Nausea
• Allgemeine Erkrankungen und Beschwerden am Verabreichungsort Nicht bekannt: Müdigkeit
• Untersuchungen
Nicht bekannt: erniedrigte Kortisol-Blutspiegel
Speziell unter hoher Dosierung und langandauernder Anwendung sind auch bei nasal applizierten Kortikosteroiden systemische Wirkungen nicht auszuschließen.
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung dem
Bundesinstitut für Arzneimittel und Medizinprodukte Abt. Pharmakovigilanz Kurt-Georg-Kiesinger-Allee 3 D-53175 Bonn Website: www.bfarm.de
anzuzeigen.
4.9 Überdosierung
Auf Grund der Gesamtmenge des in der Flasche enthaltenen Wirkstoffes sind akute Überdosierungen ebenso wie bei anderen nasal applizierten Kortikosteroiden unwahrscheinlich. Klinisch relevante systemische Nebenwirkungen sind auch nach einmaliger nasaler oder oraler Applikation des gesamten Flascheninhaltes nicht zu erwarten. Bei versehentlicher oraler Einnahme sind leichte gastrointestinale Beschwerden möglich.
5. PHARMAKOLOGISCHE EIGENSCHAFTEN
5.1 Pharmakodynamische Eigenschaften
Pharmakotherapeutische Gruppe: Dekongestiva und andere Rhinologika zur topischen Anwendung, Kortikosteroide, ATC Code: R 01 AD11
Wirkmechanismus
Triamcinolonacetonid ist ein stärker wirksames Derivat des Triamcinolons und besitzt eine gegenüber Prednison etwa achtmal stärkere Wirksamkeit. Obwohl der genaue Wirkmechanismus noch nicht vollständig bekannt ist, sind Kortikosteroide sehr wirksame Substanzen zur Behandlung von allergischen Erkrankungen.
Pharmakodynamische Wirkungen
NASACORT Sanofi-Aventis hat keinen Soforteffekt auf die allergischen Symptome. Eine Verbesserung der Symptomatik beginnt bei manchen Patienten bereits im Laufe des ersten Behandlungstages. Die volle Wirksamkeit ist nach 3 bis 4 Tagen zu erwarten. Bei vorzeitigem Absetzen von NASACORT Sanofi-Aventis dauert es einige Tage, bis wieder Symptome auftreten können.
In klinischen Studien wurde nach nasaler Applikation von Dosierungen bis zu 440 pg täglich weder bei Erwachsenen noch bei Kindern eine Suppression der Hypothalamus-Hypophysenvorderlappen-Nebennierenrinden-Funktion festgestellt.
5.2 Pharmakokinetische Eigenschaften
Untersuchungen mit einer nasal applizierten Einzeldosis von 220 Mikrogramm an erwachsenen Probanden und Patienten ergaben, dass die Absorption von NASACORT Sanofi-Aventis gering ist. Die maximale Plasmakonzentration 1,5 Stunden nach nasaler Applikation beträgt durchschnittlich 0,5 ng/ml (0,1-1 ng/ml). Nach 12 Stunden sinkt die Wirkstoffkonzentration im Plasma auf weniger als 0,06 ng/ml und liegt nach 24 Stunden unterhalb der Nachweisgrenze. Die durchschnittliche Plasmaeliminationshalbwertszeit beträgt 3,1 Stunden. Sowohl bei Probanden als auch bei Patienten konnte eine Dosisproportionalität zwischen 110 Mikrogramm und 220 Mikrogramm einer nasal applizierten Einzeldosis belegt werden. Nach Mehrfachapplikation ergaben Plasmaspiegel, AUC, Cmax und Tmax bei Kindern und Erwachsenen ähnliche Werte.
5.3 Präklinische Daten zur Sicherheit
In präklinischen Studien wurden lediglich glukokortikoidtypische Wirkungen beobachtet.
Wie bei anderen Kortikosteroiden wurden nach inhalativer oder anderer Applikation von Triamcinolonacetonid an Ratten und Kaninchen teratogene Effekte gezeigt, die Gaumenspalten und/ oder Hydrocephalus internus und axiale skelettale Anomalien zur Folge hatten. Teratogene Effekte (ZNS- und kraniale Missbildungen) wurden auch bei Primaten beobachtet.
In-vitro-Tests erbrachten keine Hinweise auf Mutagenität.
Karzinogenitätstests an Nagern ergaben keine erhöhte Inzidenz individueller Tumor-Typen.
6. PHARMAZEUTISCHE ANGABEN 6.1 Liste der sonstigen Bestandteile
- Mikrokristalline Cellulose und Carmellose-Natrium (Ph.Eur.),
- Polysorbat 80,
- gereinigtes Wasser,
- Levoglucose,
- Benzalkoniumchlorid-Lösung,
- Natriumedetat (Ph.Eur.),
- Salzsäure 10 % oder Natriumhydroxid zur pH-Einstellung.
6.2 Inkompatibilitäten Nicht zutreffend.
6.3 Dauer der Haltbarkeit
Ungeöffnet: 2 Jahre
Nach dem ersten Öffnen des Behältnisses:
Sprühflasche mit 6,5 g Suspension (30 Sprühstöße): 1 Monat Sprühflasche mit 16,5 g Suspension (120 Sprühstöße): 2 Monate
6.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung
Nicht über 25°C lagern.
Aufbewahrungsbedingungen nach Anbruch des Arzneimittels siehe Abschnitt 6.3.
6.5 Art und Inhalt des Behältnisses
NASACORT Sanofi-Aventis ist erhältlich in einer 20 ml Hochdruckpolyethylen (HDPE) -flasche mit einem Dosierpump-Spray-Aufsatz.
Eine Flasche NASACORT Sanofi-Aventis enthält entweder 6,5 g Suspension (entspricht 30 Sprühstößen) oder 16,5 g Suspension (entspricht 120 Sprühstößen).
Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht.
6.6 Besondere Vorsichtsmaßnahmen für die Beseitigung Keine besonderen Anforderungen
7. INHABER DER ZULASSUNG
Sanofi-Aventis Deutschland GmbH 65926 Frankfurt am Main
Postanschrift:
Postfach 80 08 60 65908 Frankfurt am Main
Telefon: (01 80) 2 22 20 102
Telefax: (01 80) 2 22 20 112
E-Mail: medinfo.de@sanofi.com
8. ZULASSUNGSNUMMER(N) 82818.00.00
9. DATUM DER ERTEILUNG DER ZULASSUNG/VERLÄNGERUNG DER ZULASSUNG
14.09.2012
10. STAND DER INFORMATION
September 2014
11. VERKAUFSABGRENZUNG
7
Erkrankungen der Atemwege, des Brustraums und Mediastinums
0,06 € / Anruf (dt.Festnetz); max 0,42 €/min (Mobilfunk).