Penicillin V Dura 1 Mega
Fachinformation
1. Bezeichnung des Arzneimittels
Penicillin V dura 1 Mega Penicillin V dura 1,5 Mega Filmtabletten
Zur Anwendung bei Erwachsenen und Kindern über 12 Jahren
2. Qualitative und quantitative Zusammensetzung
Penicillin V dura 1 Mega 1 Filmtablette enthält:
1 Million (1 Mega) Einheiten, entsprechend 653,6 mg PhenoxymethylpenicillinKalium bzw. 590 mg Phenoxymethylpenicillin.
Penicillin V dura 1,5 Mega 1 Filmtablette enthält:
1,5 Mega Einheiten, entsprechend 980,4 mg Phenoxymethylpenicillin-Kalium bzw. 885 mg Phenoxymethylpenicillin.
Die vollständige Auflistung der sonstigen Bestandteile siehe unter Abschnitt 6.1.
3. Darreichungsform
Filmtablette
Penicillin V dura 1 Mega
Weiße, gewölbte Onlongtablette mit beidseitiger Teilungsrille.
Penicillin V dura 1,5 Mega
Weiße bis cremefarbene längliche, bikonvexe Filmtablette mit beidseitiger Bruchkerbe.
4. Klinische Angaben
4.1 Anwendungsgebiete
Zur Behandlung von leichten bis mittelschweren Infektionen, die durch Phenoxymethylpenicillin-sensible Erreger bedingt und einer oralen Penicillin-Therapie zugänglich sind, wie z. B.
- Infektionen des Hals-Nasen-Ohren-Bereiches (Pharyngitis, Tonsillitis, Sinusitis, Otitis media),
- Infektionen der tiefen Atemwege (Bronchitis, Bronchopneumonie, Pneumonie),
- Infektionen im Zahn-, Mund- und Kieferbereich,
- Endokarditisprophylaxe bei Eingriffen im Zahn-, Mund- und Kieferbereich oder am oberen Respirationstrakt,
- Infektionen der Haut (Pyodermie, Furunkulose, Phlegmone),
- Lymphadenitis, Lymphangitis,
- Infektionen verursacht durch ß-hämolysierende Streptokokken der Gruppe A, z. B. Scharlach, Erysipel, Rezidivprophylaxe bei rheumatischem Fieber.
Gegebenenfalls ist eine Kombination mit einem weiteren geeigneten Antibiotikum möglich.
Die offiziellen Richtlinien für den angemessenen Gebrauch von antimikrobiellen Wirkstoffen sind bei der Anwendung von Penicillin V dura zu berücksichtigen.
4.2 Dosierung, Art und Dauer der Anwendung Dosierung mit Einzel- und Tagesgaben
Die antibakterielle Aktivität des Phenoxymethylpenicillin wird sowohl auf der Basis von Einheiten als auch auf Masse-(Gewichts-)Basis festgelegt. Dabei gilt folgende Beziehung:
1mg Phenoxymethylpenicillin (freie Säure) entspricht 1.695 Einheiten und 1 mg Phenoxymethylpenicillin-Kalium entspricht 1.530 Einheiten 500.000 Einheiten entsprechen ungefähr 295 mg Phenoxymethylpenicillin bzw. 326,8 mg Phenoxymethylpenicillin-Kalium
Dosierung (generelle Rahmenempfehlungen):
Üblicherweise wird die Tagesdosis in 3-4 Einzeldosen gleichmäßig über den Tag verteilt - möglichst im Abstand von 6-8 Stunden - verabreicht.
Bei Infektionen des Hals-, Nasen-, Ohrenbereichs ist die Verabreichung der Tagesdosis in nur zwei Einzeldosen - vorzugsweise im Abstand von 12 Stunden -möglich.
Zur Beachtung:
Alle Milligramm-Angaben in den folgenden Ausführungen beziehen sich auf Phenoxymethylpenicillin (freie Säure).
Erwachsene und Jugendliche ab 12 Jahren
Diese erhalten je nach Schwere und Lokalisation der Infektion üblicherweise 3-4x tgl. jeweils 295 - 885 mg Phenoxymethylpenicillin (entsprechend je 0,5-1,5 Millionen internationale Einheiten).
Kinder unter 12 Jahren
Reife Neugeborene, Säuglinge, Kleinkinder und Kinder bis zum Alter von 12 Jahren erhalten eine auf das jeweilige Körpergewicht und Lebensalter abgestimmte Tagesdosis.
Penicillin V dura ist für Säuglinge, Kleinkeinder und Kinder unter 12 Jahren aufgrund der Darreichungsform und mangelnder Dosierbarkeit nicht geeignet. Für Säuglinge, Kleinkinder und Kinder unter 12 Jahren stehen niedriger dosierbare, flüssige Darreichungsformen zur Verfügung.
Spezielle Dosierungsangaben für einzelne Altersgruppen:
Soweit nicht anders verordnet, gelten folgende Dosierungsempfehlungen: Erwachsene und Kinder über 12 Jahre nehmen 3-mal täglich 1 bis 1% Filmtabletten Penicillin V dura 1 Mega bzw. 1 Filmtablette Penicillin V dura 1,5 Mega, entsprechend je 590 bis 885 mg Phenoxymethylpenicillin (je 1 bis 1,5 Millionen
Einheiten), ein. Für niedrigere Dosierungen stehen andere Darreichungsformen zur Verfügung.
Bei schweren Fällen bzw. bei minderempfindlichen Erregern oder ungünstig gelegenem Infektionsort kann die Tagesdosis auf das Doppelte und mehr gesteigert werden.
Dosierung bei eingeschränkter Nierenfunktion:
Bis zu einer Kreatininclearance von 30 - 15 ml/min ist es bei einem Dosierungsintervall von 8 Stunden im allgemeinen nicht erforderlich, die Dosis von Phenoxymethylpenicillin zu verringern.
Art und Dauer der Anwendung
Penicillin V dura sollte jeweils etwa 1 Stunde vor den Mahlzeiten eingenommen werden, um eine möglichst hohe Resorptionsquote zu erreichen.
Die Filmtabletten sind unzerkaut (schlechter Geschmack des Wirkstoffes) mit reichlich Flüssigkeit (z.B. 1 Glas Wasser) einzunehmen.
Um Kindern die regelmäßige Einnahme zu erleichtern, können sie Penicillin V dura auch während der Mahlzeiten einnehmen.
Penicillin V dura soll in der Regel 7 - (10) Tage lang eingenommen werden, mindestens bis 2-3 Tage nach Abklingen der Krankheitserscheinungen.
Die Behandlungsdauer ist vom Ansprechen der Erreger bzw. dem klinischen Erscheinungsbild abhängig. Sollte nach 3-4 Tagen ein Therapieeffekt nicht erkennbar sein, so ist eine erneute Sensibilitätsbestimmung durchzuführen und gegebenenfalls das Antibiotikum zu wechseln.
Bei der Behandlung von Infektionen mit ß-hämolysierenden Streptokokken sollte die Therapiedauer mindestens 10 Tage betragen, um Spätkomplikationen (rheumatisches Fieber, Glomerulonephritis) vorzubeugen.
4.3 Gegenanzeigen
Überempfindlichkeit (Allergie) gegen Phenoxymethylpenicillin-Kalium, Pfefferminzöl oder einen der sonstigen Bestandteile.
Wegen der Gefahr eines anaphylaktischen Schocks darf Penicillin V dura bei Patienten mit Penicillin-Überempfindlichkeit nicht angewandt werden.
4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung
Allergische Diathese:
Eine mögliche Kreuzallergie mit anderen Betalaktam-Antibiotika (u. a. Cephalosporine) kann bestehen.
Bei Patienten mit allergischer Reaktionsbereitschaft (z. B. Heuschnupfen, Asthma bronchiale) ist das Risiko für schwerwiegendere Überempfindlichkeitsreaktionen erhöht, weshalb Penicillin V dura in solchen Fällen mit besonderer Vorsicht angewandt werden sollte.
Bei Patienten, die an Hautpilzerkrankungen leiden, ist das Risiko allergischer Reaktionen erhöht.
Bei Patienten mit schweren Magen-Darmstörungen mit Erbrechen und Durchfällen sollte von der Behandlung mit Phenoxymethylpenicillin abgesehen werden, da eine ausreichende Resorption nicht gewährleistet ist. (Hier empfiehlt sich eine parenterale Therapie, z. B. mit Benzylpenicillin oder einem anderen geeigneten Antibiotikum).
Mögliche Resistenzentwicklung:
Langfristige und wiederholte Anwendung von Penicillin V dura kann zu Superinfektion mit resistenten Keimen oder mit Sprosspilzen führen.
Hinweis für Patienten mit Herzerkrankungen oder schweren Elektrolytstörungen anderer Genese:
Bei Patienten mit Herzerkrankungen oder schweren Elektrolytstörungen anderer Genese sollte auf die Kaliumzufuhr durch das Präparat geachtet werden. Penicillin V dura 1 Mega:
Dieses Arzneimittel enthält 1,68 mmol (64 mg) Kalium pro Filmtablette.
Penicillin V dura 1,5 Mega:
Dieses Arzneimittel enthält 2,52 mmol (96 mg) Kalium pro Filmtablette.
Bei Patienten mit eingeschränkter Nierenfunktion oder Patienten mit kontrollierter Kaliumdiät ist der Kaliumgehalt zu berücksichtigen.
Gegenmaßnahmen bei Nebenwirkungen:
Anaphylaktische Reaktionen
Bei anaphylaktischen Reaktionen muss die Behandlung mit Penicillin V dura sofort abgebrochen werden und die üblichen Sofortmaßnahmen (z.B. die Gabe von Antihistaminika, Kortikosteroiden, Sympathomimetika und ggf. Durchführung einer Beatmung) müssen eingeleitet werden.
Eine urtikarielle Sofortreaktion deutet meist auf eine echte Penicillin-Allergie hin und zwingt zum Therapieabbruch
Pseudomembranöse Enterokolitis
Hier ist eine Beendigung der Therapie mit Penicillin V dura in Abhängigkeit von der Indikation zu erwägen und ggf. sofort eine angemessene Behandlung einzuleiten (z.B. Einnahme von speziellen Antibiotika/ Chemotherapeutika, deren Wirksamkeit klinisch erwiesen ist). Arzneimittel, die die Peristaltik hemmen, sind kontraindiziert.
4.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen
Penicillin V dura sollte nicht mit bakteriostatisch wirkenden Chemotherapeu-tika/Antibiotika (z. B. Tetracycline, Sulfonamide oder Chloramphenicol) kombiniert werden, da ein antagonistischer Effekt möglich ist.
Die gleichzeitige Gabe von Probenecid führt als Folge einer Hemmung der renalen Ausscheidung zu höheren und längeranhaltenden PhenoxymethylpenicillinKonzentrationen im Serum und in der Galle. Auch Indometacin, Phenylbutazon, Salicylate und Sulfinpyrazon führen zu erhöhten und verlängerten Serumspiegeln.
Die Resorption oral applizierter Penicilline kann bei unmittelbar vorausgegangener oder andauernder Darmsterilisation mit nicht resorbierbaren Aminoglykosi-den (z. B. Neomycin) reduziert sein.
Einfluss auf Laboruntersuchungen:
Unter einer Therapie mit Penicillin V dura können nichtenzymatische Methoden zur Harnzuckerbestimmung ein positives Resultat ergeben.
Ebenso kann der Urobilinogen-Nachweis gestört werden.
4.6 Schwangerschaft und Stillzeit
Beobachtungen am Menschen haben bisher keinen Hinweis auf Schädigung des im Mutterleib befindlichen Kindes ergeben. Experimentelle Studien haben keine fruchtschädigende Wirkung erkennen lassen.
Da bisher keinerlei schädigende Wirkungen von Phenoxymethylpenicillin bekannt geworden sind, ist eine Anwendung von Penicillin V dura während der gesamten Schwangerschaft und Stillzeit bei entsprechender Indikation möglich. Phenoxymethylpenicillin wird in die Muttermilch ausgeschieden.
Die maximalen Milchspiegel betragen etwa 50 % der maximalen Serumspiegel. Beim gestillten Säugling ist die Möglichkeit einer Sensibilisierung bzw. einer Beeinflussung der physiologischen Darmflora mit Auftreten von Durchfall oder Sprosspilzbesiedlung zu beachten.
4.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen
Nicht zutreffend.
4.8 Nebenwirkungen
Bei den Häufigkeitsangaben zu Nebenwirkungen werden folgende Kategorien zugrunde gelegt:
Sehr häufig (>1/10)
Häufig (>1/100 bis <1/10)
Gelegentlich (>1/1.000 bis <1/100)
Selten (>1/10.000 bis <1/1.000)
Sehr selten (<1/10.000)
Nicht bekannt (Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar) Wirkungen auf den Magen-Darm-Trakt:
Gastrointestinale Störungen kommen häufig unter der Therapie mit Penicillin V dura vor. Dazu zählen Übelkeit, Erbrechen, Appetitlosigkeit, Magendrücken, Bauchschmerzen, Flatulenz und Durchfälle. Diese Störungen sind meist leichter Natur und klingen häufig während, sonst nach Absetzen der Therapie ab.
Sehr selten kann sich unter Therapie mit Penicillin V dura eine pseudomembranöse Enterokolitis, meist verursacht durch Clostridium difficile, entwickeln. ( s.a. Abschnitt 4.4).
Haut- und Hautanhangsgebilde (siehe auch Überempfindlichkeitserscheinungen) Häufig können Hautausschläge (Exantheme) und Schleimhautentzündungen, besonders im Bereich des Mundes (Glossitis, Stomatitis) auftreten. Selten kann es zur Ausbildung einer schwarzen Haarzunge kommen. Nach Einnahme von
Penicillin V dura kann es vorübergehend zu trockenem Mund und zu Geschmacksveränderungen kommen.
Überempfindlichkeitserscheinungen
Häufig sind allergische Reaktionen zu erwarten, meist in Form von Hautreaktionen (z. B. Exantheme, Juckreiz, Urtikaria ). Eine urtikarielle Sofortreaktion deutet meist auf eine echte Penicillin-Allergie hin und zwingt zum Therapieabbruch. Sehr selten werden schwerwiegende allergische Reaktionen als Folge einer Sensibilisierung gegen die 6-Amino-Penicillansäure-Gruppe, z. B. in Form von Arzneimittelfieber, Gelenkschmerzen, angioneurotischem Ödem, Larynxödem, Bronchospasmen, Herzjagen, Luftnot, Serumkrankheit, allergischer Vaskulitis sowie Blutdruckabfall bis hin zu bedrohlichem Schock, beobachtet.
Über schwere Hautreaktionen wie z.B. Stevens-Johnson-Syndrom ist berichtet worden.
Überempfindlichkeitsreaktionen aller Schweregrade - bis zum anaphylaktischen Schock - sind auch nach oraler Gabe von Penicillinen beobachtet worden. Schwere anaphylaktoide Reaktionen, die nach oraler Gabe von Penicillinen wesentlich seltener auftreten als nach intravenöser oder intramuskulärer Gabe, erfordern unter Umständen entsprechende Notfallmaßnahmen.( Siehe auch Abschnitt : 4.4)
Blut und Blutkörperchen
Sehr selten sind Blutbildveränderungen in Form von Granulozytopenie, Agranulozytose, Thrombozytopenie, Panzytopenie, hämolytische Anämie, Eosinophilie beobachtet worden. Diese Erscheinungen sind reversibel.
Niere, Harnwege und Geschlechtsorgane
Sehr selten kann es zu einer interstitiellen Nephritis kommen.
4.9 Überdosierung
Die Toxizität von Phenoxymethylpenicillin ist äußerst gering, die therapeutische Breite ist außerordentlich groß.
Wie bei anderen Penicillinen ist die einmalige orale Aufnahme mehrfach therapeutischer Dosen von Phenoxymethylpenicillin nicht akut toxisch.
Bei oraler Verabreichung ist es praktisch unmöglich, Konzentrationen zu erreichen, die zur Auslösung neurotoxischer Symptome führen.
Notfallmaßnahmen:
Spezielle Maßnahmen bei Überdosierung, außer dem Absetzen des Medikamentes, sind nicht erforderlich.
Eine Elimination von Phenoxymethylpenicillin kann mittels Hämodialyse erzielt werden.
5. PHARMAKOLOGISCHE EIGENSCHAFTEN
5.1 Pharmakodynamische Eigenschaften
Pharmakotherapeutische Gruppe
Phenoxymethylpenicillin (Penicillin V) ist ein biosynthetisches, säurestabiles, nicht Be-talaktamase-festes Betalaktam-Antibiotikum.
ATC-Code
J01CE02
Wirkungsweise
Der Wirkungsmechanismus von Phenoxymethylpenicillin beruht auf einer Hemmung der bakteriellen Zellwandsynthese (in der Wachstumsphase) durch Blockade der Penicillinbindenden Proteine (PBPs) wie z. B. der Transpeptidasen. Hieraus resultiert eine bakterizide Wirkung.
Beziehung zwischen Pharmakokinetik und Pharmakodynamik
Die Wirksamkeit hängt im wesentlichen von der Zeitdauer ab, während der der Wirkstoffspiegel oberhalb der MHK des Erregers liegt.
Resistenzmechanismen
Eine Resistenz gegenüber Phenoxymethylpenicillin kann auf folgenden Mechanismen beruhen:
- Inaktivierung durch Betalaktamasen: Phenoxymethylpenicillin ist nicht Be-talaktamase-fest und wirkt daher nicht gegen Betalaktamase-bildende Bakterien (z. B. Staphylokokken oder Gonokokken).
- Reduzierte Affinität von PBPs gegenüber Phenoxymethylpenicillin: Die erworbene Resistenz bei Pneumokokken und einigen anderen Streptokokken gegenüber Phenoxymethylpenicillin beruht auf Modifikationen vorhandener PBPs als Folge einer Mutation. Für die Resistenz bei Methicillin (Oxacillin)-resistenten Staphylokokken hingegen ist die Bildung eines zusätzlichen PBPs mit verminderter Affinität gegenüber Phenoxymethylpenicillin verantwortlich.
- Unzureichende Penetration von Amoxcillin durch die äußere Zellwand kann bei Gram-negativen Bakterien dazu führen, dass die PBPs nicht ausreichend gehemmt werden.
- Durch Effluxpumpen kann Amoxicillin aktiv aus der Zelle transportiert werden.
Eine partielle oder vollständige Kreuzresistenz von Phenoxymethylpenicillin besteht mit anderen Penicillinen und Cephalosporinen.
Grenzwerte
Die Testung auf Empfindlichkeit gegenüber Phenoxymethylpenicillin erfolgt mit Hilfe von Benzylpenicillin unter Benutzung der üblichen Verdünnungsreihe. Folgende minimale Hemmkonzentrationen für sensible und resistente Keime wurden festgelegt:
EUCAST (European Committee on Antimicrobial Susceptibility Testing) Grenzwerte
|
Erreger |
Sensibel |
Resistent |
|
Streptococcus spp. (Gruppen A, B, C, G) |
< 0,25 mg/l |
> 0,25 mg/l |
|
Streptococcus pneumoniae |
< 0,06 mg/l |
> 2 mg/l |
|
Streptokokken der „Viridans“-Gruppe |
< 0,25 mg/l |
> 2 mg/l |
|
Neisseria aonorrhoeae |
< 0,06 mg/l |
> 1 mg/l |
|
Neisseria meninaitidis |
< 0,06 mg/l |
> 0,25 mg/l |
|
Gram-negative Anaerobier |
< 0,25 mg/l |
> 0,5 mg/l |
|
Gram-positive Anaerobier |
< 0,25 mg/l |
> 0,5 mg/l |
|
Nicht speziesspezifische Grenzwerte* |
< 0,25 mg/l |
> 2 mg/l |
* Basieren hauptsächlich auf der Serumpharmakokinetik
Prävalenz der erworbenen Resistenz in Deutschland
Die Prävalenz der erworbenen Resistenz einzelner Spezies kann örtlich und im Verlauf der Zeit variieren. Deshalb sind - insbesondere für die adäquate Behandlung schwerer Infektionen - lokale Informationen über die Resistenzsituation erforderlich. Falls auf Grund der lokalen Resistenzsituation die Wirksamkeit von Phenoxymethylpenicillin in Frage gestellt ist, sollte eine Therapieberatung durch Experten angestrebt werden. Insbesondere bei schwerwiegenden Infektionen oder bei Therapieversagen ist eine mikrobiologische Diagnose mit dem Nachweis des Erregers und dessen Empfindlichkeit gegenüber Phenoxymethylpenicillin anzustreben.
Prävalenz der erworbenen Resistenz in Deutschland auf der Basis von Daten der letzen 5 Jahre aus nationalen Resistenzüberwachungsprojekten und -studien (Stand: Dezember 2009):
Üblicherweise empfindliche Spezies_
Aerobe Gram-positive Mikroorganismen_
Actinomyces israeli°_
Corynebacterium diphtheriae°_
Erysipelothrix rusiopathiae°_
Gardnerella vaginalis°_
Streptococcus agalactiae_
Streptococcus pneumoniae_
Streptococcus pyogenes_
Streptococcus dysgalactiae subsp. equisimilis°
(Streptokokken der Gruppen C & G)_
Streptokokken der „Viridans“-Gruppe°A_
Aerobe Gram-negative Mikroorganismen_
Borrelia burgdorferi0_
Eikenella corrodens°$_
Haemophilus influenzae°$_
Anaerobe Mikroorganismen_
Clostridium perfringens°_
Clostridium tetani°_
Fusobacterium spp.°_
Peptoniphilus spp. °_
Peptostreptococcus spp.°_
Veillonella parvula°_
Andere Mikroorganismen_
Treponema pallidum0_
Spezies, bei denen erworbene Resistenzen ein Problem bei der
Anwendung darstellen können_
Aerobe Gram-positive Mikroorganismen_
Enterococcus faecalis$
Staphylococcus aureus+
Staphylococcus epidermidis+
Staphylococcus haemolyticus+
Staphylococcus hominis+
Von Natur aus resistente Spezies
Aerobe Gram-positive Mikroorganismen
Enterococcus faecium
Nocardia asteroides
Aerobe Gram-negative Mikroorganismen
Alle Enterobacteriaceae-Spezies
Moraxella catarrhalis
Pseudomonas aeruginosa
Anaerobe Mikroorganismen
Bacteroides spp.
Andere Mikroorganismen
Chlamydia spp.
Chlamydophila spp.
Legionella pneumophila
Mycoplasma spp.
° Bei Veröffentlichung der Tabelle lagen keine aktuellen Daten vor. In der Primärliteratur, Standardwerken und Therapieempfehlungen wird von einer Empfindlichkeit ausgegangen.
$ Die natürliche Empfindlichkeit der meisten Isolate liegt im intermediären Bereich.
+ In mindestens einer Region liegt die Resistenzrate bei über 50%.
A Sammelbezeichnung für eine heterogene Gruppe von Streptokokken-Spezies. Resistenzrate kann in Abhängigkeit von der vorliegenden Streptokokken-Spezies variieren.
5.2 Pharmakokinetische Eigenschaften
Soweit nicht ausdrücklich erwähnt, beziehen sich die folgenden Angaben ausschließlich auf Phenoxymethylpenicillin-Kalium. Phenoxymethylpenicillin wird aufgrund seiner Säurestabilität nach weitgehend verlustfreier Magenpassage in den oberen Dünndarmabschnitten resorbiert. Die Resorptionsquote beträgt etwa 60 %. Das Ausmaß der Resorption hängt auch von der galenischen Form ab. Feste Darreichungsformen sind unproblematischer als Granulate zur Zubereitung einer Lösung/Suspension. Gleichzeitige Nahrungsaufnahme führt zu einer Verminderung der Resorption. Maximale Serumkonzentrationen werden nach ca. 30 - 60 Minuten erreicht. Nach oraler Gabe von 0,4 g, 1 g, 2 g und 3 g Peni-cillin-V wurden mittlere Spitzenkonzentrationen von 6,1; 15; 26,3 und 35,5 mg/l gemessen. In dem Dosisbereich von 0,12 bis 3 g besteht eine annähernd lineare Beziehung zwischen der Höhe der Dosis und der Fläche unter der Konzentrati-ons-Zeit-Kurve (AUC). Nach Gabe von Phenoxymethylpenicillin-Calcium in Form von Tabletten waren die mittleren Serumkonzentrationen niedriger als nach Gabe einer gleich hohen Dosis des Kalium-Salzes.
Die Bioverfügbarkeit des Phenoxymethylpenicillins ist am geringsten nach Verabreichung des Benzathin-Salzes. Die Resorption scheint verzögert zu sein wie bei einer retardierten Formulierung und die Serumspitzenkonzentrationen sind 3
bis 4mal niedriger als beim Kalium-Salz. Der limitierende Faktor bei der Resorption des Benzathin-Salzes ist wahrscheinlich die geringe Lösungsgeschwindigkeit und nicht die Resorptionskapazität der Dünndarmmukosa.
Verteilung:
Phenoxymethylpenicillin ist gut gewebegängig, und in verschiedenen Organen und Körperflüssigkeiten werden therapeutisch wirksame Konzentrationen erreicht. Die Liquorgängigkeit von Phenoxymethylpenicillin ist auch bei entzündeten Meningen gering.
Die Serumproteinbindung von Phenoxymethylpenicillin liegt bei 75 ± 14 % und ist damit höher als die des Benzylpenicillin mit 48 %. Das scheinbare Verteilungsvolumen beträgt 15,3 ± 1,17 l.
Plazentagängigkeit/Übergang in die Muttermilch:
29 Schwangere erhielten Phenoxymethylpenicillin unter der Geburt. Die fetalen Blutspiegel betrugen 44 % der Konzentrationen im mütterlichen Blut. Im Fruchtwasser wurden 58 % der mütterlichen Serumkonzentrationen erreicht. Nach einmaliger Einnahme von Phenoxymethylpenicillin lag der Quotient aus Milchkonzentrationen und korrespondierenden Serumkonzentrationen zwischen 0,05 und
1,02 mit einem Mittelwert von 0,15. Etwa 0,2 % der Dosis, die eine stillende Mutter einnimmt, gelangen durch das Stillen in den kindlichen Organismus.
Elimination:
Etwa 34 ± 20 % einer Dosis werden in Form von inaktiven Umwandlungsprodukten (z. B. Penicilloinsäure) im Urin aufgefunden. Die Exkretion von unverändertem Phenoxymethylpenicillin und seinen Umwandlungsprodukten erfolgt fast ausschließlich über die Nieren. Phenoxymethylpenicillin wird durch glomeruläre Filtration und tubuläre Sekretion ausgeschieden. Innerhalb von 12 Stunden werden 29 bis 43 % der verabreichten Dosis in unveränderter mikrobiologisch aktiver Form im Urin wiedergefunden. Innerhalb von 24 Stunden wird praktisch die gesamte resorbierte Menge in Form der Muttersubstanz und der Umwandlungsprodukte mit dem Urin ausgeschieden.
Bei Nierengesunden liegt die Serum-Halbwertszeit bei 30 bis 45 Minuten. Die Halbwertszeit ist dosisabhängig. Bei Untersuchungen der Halbwertszeit fand sich nach Gabe einer 0.4 g-Dosis eine Halbwertszeit von 0.5 Stunden und nach einer 3 g-Do-sis eine Halbwertszeit von 1.1 Stunden. Bei Neugeborenen und Patienten mit eingeschränkter Nierenfunktion ist die Ausscheidung verzögert. Für die totale Clearance von Phenoxymethylpenicillin wurde nach i. v.-Gabe ein Wert von ca.
800 ml/min ermittelt und in einer anderen Untersuchung ein niedrigerer Wert von 476 ± 236 ml/min.
Bioverfügbarkeit
Eine im Jahr 1999 durchgeführte Bioverfügbarkeitsuntersuchung an 22 Probanden (10 weibliche, 12 männliche Probanden) ergab im Vergleich zum Referenzpräparat:
|
Testpräparat |
Referenzpräparat | |||
|
Mittelwer t |
Standard abweichung |
Mittelwert |
Standard- abweichun g | |
|
Maximale Plasmakonzentration ( Cmax ): |
10,037 |
± 3,713 |
9,841 |
± 3,874 |
|
Fläche unter der Konzentrations-ZeitKurve ( AUC ): |
14,182 |
± 4,424 |
14,988 |
± 4,352 |
|
Zeitpunkt der maximalen Plasmakonzentration ( t max ) |
0,69 |
± 0,20 |
0,77 |
± 0,43 |
Angabe der Werte als arithmetisches Mittel und Standardabweichung.
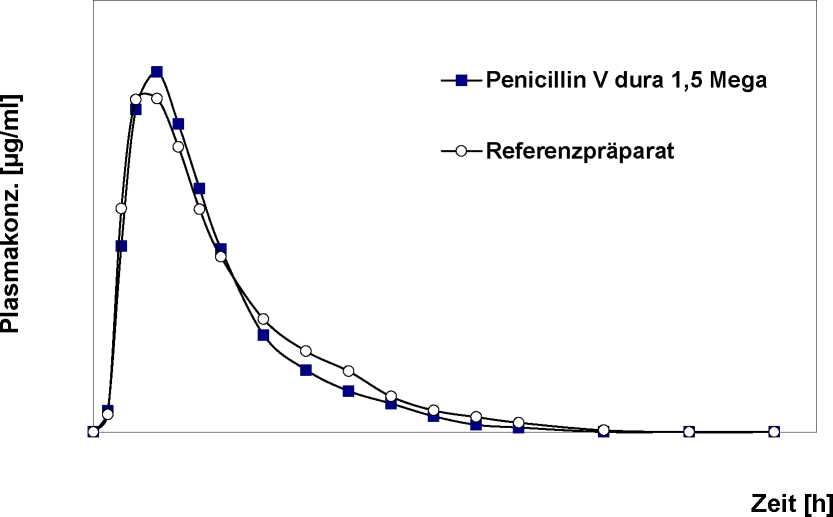
Mittlere Plasmaspiegelverläufe im Vergleich zu einem Referenzpräparat in einem Konzentrations-Zeit-Diagramm:
5.3 Präklinische Daten zur Sicherheit
Bisherige Genotoxizitätsuntersuchungen von Phenoxymethylpenicillin ergaben keine Hinweise auf klinisch relevante Effekte.
Langzeituntersuchungen an Ratten und Mäusen ergaben keine Anhaltspunkte für ein tumorgenes Potential von Phenoxymethylpenicillin.
Untersuchungen an verschiedenen Tierspezies haben keine Hinweise auf teratogene Wirkung von Phenoxymethylpenicillin ergeben.
6. PHARMAZEUTISCHE ANGABEN
6.1
Liste der sonstigen Bestandteile
Penicillin V dura 1 Mega/-1,5 Mega
Magnesiumstearat (Ph.Eur.); Macrogol 6000; Maltodextrin; Povidon K25; Talkum; Saccharin-Natrium; Hypromellose; Pfefferminzöl; Titandioxid (E171).
6.2 Inkompatibilitäten
Bisher keine bekannt.
6.3 Dauer der Haltbarkeit
Die Dauer der Haltbarkeit beträgt 4 Jahre.
Diese Arzneimittel sollen nach Ablauf des Verfallsdatums nicht mehr angewendet werden.
6.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung
Nicht über 25°C aufbewahren!
In der Originalverpackung aufbewahren, um den Inhalt vor Feuchtigkeit zu schützen.
6.5 Art und Inhalt des Behältnisses
Alu-PVC-PVDC-Blister
Originalpackungen mit:
10 Filmtabletten (N1)
20 Filmtabletten (N2)
30 Filmtabletten (N2)
6.6 Besondere Vorsichtsmaßnahmen für die Beseitigung und sonstige Hinweise zur Handhabung
Keine besonderen Anforderungen.
Nicht verwendetes Arzneimittel oder Abfallmaterial ist entsprechend den nationalen Anforderungen zu entsorgen.
7. Inhaber der Zulassung
Mylan dura GmbH Postfach 10 06 35 64206 Darmstadt
8. Zulassungsnummer
Penicillin V dura 1 Mega
38399.00. 00
Penicillin V dura 1,5 Mega
6041341.00. 00
9. Datum der Erteilung der Zulassung / Verlängerung der Zulassung
Penicillin V dura 1 Mega
04.11.1996 / 21.02.2005 Penicillin V dura 1,5 Mega
12.08.1996 / 06.11.2006
10. Stand der Information
März 2016
11. Verkaufsabgrenzung
Verschreibungspflichtig