Ropivacain-Kk 10 Mg/Ml Injektionslösung
Fachinformation
1. BEZEICHNUNG DES ARZNEIMITTELS
Ropivacain-KK 10 mg/ml Injektionslösung
2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Ropivacainhydrochlorid Monohydrat
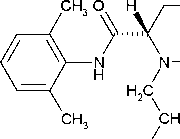
■ HCl ■ H2O
H3C
Molekülformel: C17H26N2O HCl H2O Molekulargewicht:328,9
1 ml enthält 10,58 mg Ropivacainhydrochlorid Monohydrat (entsprechend 10 mg Ropivacainhydrochlorid).
1 Ampulle mit 10 ml bzw. 20 ml Injektionslösung enthält 105,8 mg bzw. 211,6 mg Ropivacainhydrochlorid Monohydrat (entsprechend 100 mg bzw. 200 mg
Ropivacainhydrochlorid).
Vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt 6.1.
3. DARREICHUNGSFORM
Klare, farblose Lösung
4. KLINISCHE ANGABEN
4.1 Anwendungsgebiete
Ropivacain-KK ist bei Erwachsenen und Jugendlichen über 12 Jahren indiziert zur Anästhesie in der Chirurgie
- Epiduralanästhesie für chirurgische Eingriffe, einschließlich Kaiserschnitt
- Plexusblockaden
- Leitungs- und Infiltrationsanästhesie
4.2. Dosierung, Art und Dauer der Anwendung
Art der Anwendung: Zur perineuralen und epiduralen Anwendung
Ropivacain soll nur von oder unter der Aufsicht von Ärzten angewendet werden, die in der Regionalanästhesie erfahren sind.
Dosierung
Erwachsene und Jugendliche älter als 12 Jahre
Die folgende Tabelle dient als Leitfaden für gebräuchliche Blockaden. Es soll die kleinste Dosis angewendet werden, die eine wirksame Blockade hervorruft. Für die Festlegung der Dosis sind die Erfahrungen des Arztes sowie die Kenntnisse des Allgemeinzustandes des Patienten ausschlaggebend.
|
Konzentration von Ropivacain- hydrochlorid [mg/ml] |
Volumen [ml] |
Dosis von Ropivacain- hydrochlorid [mg] |
Beginn [Minuten] |
Dauer [Stunden] | |
|
Chirurgische Anästhesie | |||||
|
Lumbale Epiduralanästhesie | |||||
|
Chirurgie |
o y-1 o ^ |
15 -25 15-20 |
113-188 150-200 |
10-20 10-20 |
3- 5 4- 6 |
|
Kaiserschnitt |
7,5 |
15-20 |
113-1501) |
10-20 |
3-5 |
|
Thorakale Epiduralanästhesie | |||||
|
Blockade bei postoperativem Schmerz |
7,5 |
5-15 (abhängig vom Injektionsort) |
38-113 |
10-20 |
n/z2) |
|
Plexusblockaden (*) | |||||
|
(Plexus-brachialis-Blockaden) |
7,5 |
30-40 |
225-3 003) |
10-25 |
6-10 |
|
Leitungs- und Infiltrationsanästhesie |
7,5 |
1-30 |
7,5-225 |
1-15 |
2-6 |
|
(z.B. kleinere Nervenblockaden und Infiltration) |
Die in der Tabelle angegebenen Dosierungen sind so festgelegt, dass eine wirksame Blockade erreicht wird. Sie sollten als Richtlinien zur Anwendung bei Erwachsenen betrachtet werden. Individuelle Abweichungen hinsichtlich Einsetzen und Dauer der Blockade treten auf. Die Angaben in der Spalte „Dosis" geben die erwarteten durchschnittlichen Dosisbereiche an. Hinsichtlich der Faktoren, die spezifische Blocktechniken betreffen, und für individuelle Patientenbedürfnisse sollte Fachliteratur konsultiert werden.
* Hinsichtlich der Plexusblockaden kann nun für die Plexus-brachialis-Blockaden eine
Dosierungsempfehlung gegeben werden. Für andere Plexusblockaden können geringere Dosen erforderlich sein. Es liegen bisher keine Erfahrungen für spezifische Dosisempfehlungen für andere Blockaden vor.
1) Zunehmende Dosen sind anzuwenden, als Anfangsdosis ca. 100 mg (97,5 mg = 13ml; 105 mg = 14 ml) innerhalb von 3 bis 5 min. Zwei zusätzliche Dosen, insgesamt 50 mg, können bei Bedarf verabreicht werden.
2) n/z = nicht zutreffend.
3) Die Dosis für eine Plexusblockade ist je nach Verabreichungsort und Patientenzustand anzupassen.
Interskalenäre und supraklavikuläre Plexus-brachialis-Blockaden können - unabhängig vom verwendeten Lokalanästhetikum - zu einer größeren Häufigkeit von schwerwiegenden Nebenwirkungen führen (siehe Abschnitt 4.4 „Warnhinweise und Vorsichtsmaßnahmen für die Anwendung._
Im Allgemeinen erfordert die Anästhesie für Operationen (z. B. epidurale Applikation) die Anwendung höherer Konzentrationen und Dosen. Zur Epiduralanästhesie wird Ropivacain 10 mg/ml empfohlen, da hier eine ausgeprägte motorische Blockade für die Operation erforderlich ist. Zur Schmerztherapie (z B. epidurale Applikation zur Behandlung akuter Schmerzzustände) werden die niedrigeren Konzentrationen und Dosen empfohlen.
Anwendungshinweise
Zur Vermeidung einer intravasalen Injektion wird eine wiederholte Aspiration vor und während der Injektion empfohlen. Wenn eine hohe Dosis injiziert werden soll, wird die vorherige Verabreichung einer Testdosis von 3-5 ml Lidocain mit Adrenalin (Epinephrin) empfohlen. Eine versehentliche intravaskuläre Injektion lässt sich an einer vorübergehenden Erhöhung der Herzfrequenz und eine unbeabsichtigte intrathekale Injektion durch Anzeichen einer Spinalblockade erkennen.
Eine Aspiration sollte vor und während der Applikation der Hauptdosis durchgeführt werden. Die Hauptdosis sollte langsam oder in steigenden Dosen mit einer Geschwindigkeit von 25-50 mg/min injiziert werden, wobei die vitalen Funktionen des Patienten unter dauerndem verbalen Kontakt streng zu überwachen sind. Beim Auftreten toxischer Symptome muss die Injektion sofort gestoppt werden.
Zur Epiduralanästhesie bei chirurgischen Eingriffen wurden Einzeldosen bis zu 250 mg Ropivacain angewendet und gut vertragen.
Eine begrenzte Anzahl von Patienten erhielt zur Plexus-brachialis-Blockade eine Einzeldosis von 300 mg, die gut vertragen wurde.
Bei länger dauernden Blockaden, entweder durch kontinuierliche epidurale Infusion oder durch wiederholte Bolusinjektion, müssen die Risiken toxischer Plasmakonzentrationen oder lokaler Nervenläsionen bedacht werden. Die bei Operationen und postoperativer Analgesie über einen Zeitraum von 24 Stunden kumulativ verabreichten Dosen von bis zu 675 mg Ropivacain wurden vom Erwachsenen gut vertragen, ebenso wie die über einen Zeitraum von 72 Stunden kontinuierlich über eine epidurale Infusion verabreichten Dosen von bis zu 28 mg/Stunde. Eine begrenzte Anzahl von Patienten erhielt höhere Dosen bis zu 800 mg pro Tag, die mit relativ wenigen unerwünschten Wirkungen verbunden waren.
Zur Behandlung postoperativer Schmerzen wird folgende Technik empfohlen:
Falls dies nicht schon präoperativ geschehen ist, wird via Epiduralkatheter mit Ropivacain 7,5 mg/ml Injektionslösung eine Epiduralanästhesie eingeleitet. Die Analgesie wird mit einer Infusion von Ropivacain 2 mg/ml Infusionslösung aufrechterhalten. Infusionsgeschwindigkeiten von 6-14 ml/ Stunde (12-28 mg) sichern bei mäßigen bis schweren postoperativen Schmerzen in den meisten Fällen eine ausreichende Analgesie mit nur geringer und nicht progressiver motorischer Blockade. Die maximale Anwendungsdauer der Epiduralblockade beträgt 3 Tage. Der analgetische Effekt sollte engmaschig überwacht werden, damit bei geringem Restschmerz der Katheter baldmöglichst entfernt werden kann. Mit dieser Technik wird eine signifikante Reduktion des Bedarfes an Opioiden erreicht.
In klinischen Prüfungen wurde Ropivacain 2 mg/ml Infusionslösung als Epiduralinfusion alleine oder gemischt mit 1-4 gg/ml Fentanyl über bis zu 72 Stunden zur Behandlung von postoperativen Schmerzen gegeben. Die Kombination von Ropivacain und Fentanyl verbesserte die Schmerzlinderung, verursachte aber opioidtypische Nebenwirkungen. Die Kombination von Ropivacain und Fentanyl wurde nur für Ropivacain 2 mg/ml Infusionslösung untersucht.
Bei länger andauernden kontinuierlichen peripheren Nervenblockaden, entweder durch kontinuierliche Infusion oder wiederholte Injektionen, muss das Risiko von toxischen Plasmakonzentrationen des Lokalanästhetikums bzw. von lokalen Nervenläsionen bedacht werden. In klinischen Prüfungen wurde vor dem Eingriff eine femorale Nervenblockade mit 300 mg Ropivacain 7,5 mg/ml und einer Interskalenusblock mit 225 mg Ropivacain 7,5 mg/ml gesetzt. Die Schmerzfreiheit wurde anschließend mit Ropivacain 2 mg/ml aufrechterhalten. Infusionsraten oder intermittierende Injektionen von 10-20 mg pro Stunde über 48 Stunden führten zu ausreichender Analgesie und wurden gut vertragen.
Konzentrationen über 7,5 mg/ml Ropivacain sind für die Indikation Kaiserschnitt nicht dokumentiert.
Die Anwendung von Ropivacain 7,5 mg/ml und 10 mg/ml bei Kindern kann mit toxischen systemischen und zentralen Nebenwirkungen verbunden sein. Die Anwendung geringerer Konzentrationen (Ropivacain 2 mg/ml und 5 mg/ml) sind für diese Patientengruppen geeigneter.
Die Anwendung von Ropivacain bei Frühgeborenen ist nicht belegt.
Anwendungshinweise
Zur Vermeidung einer intravasalen Injektion wird eine wiederholte Aspiration vor und während der Injektion empfohlen. Die Vitalfunktionen des Patienten sollten während der Injektion eng überwacht werden. Falls toxische Symptome auftreten, muss die Injektion sofort gestoppt werden.
Eine einzelne kaudale Epiduralinjektion von Ropivacain 2 mg/ml bewirkt bei der Mehrzahl der Patienten eine adäquate postoperative Analgesie unterhalb T12, wenn eine Dosis von 2 mg/kg in einem Volumen von 1 ml/kg verwendet wird. Um eine andersartige Ausbreitung der Nervenblockade zu erreichen, kann das Volumen der kaudalen Epiduralinjektion so angepasst werden, wie es in der Fachliteratur empfohlen wird. Bei Kindern ab 4 Jahre wurden Dosierungen bis zu 3 mg/kg bei einer Ropivacain-Konzentration von 3 mg/ml untersucht. Allerdings ist diese Konzentration vermehrt mit dem Auftreten motorischer Blockaden verbunden.
Die Fraktionierung der berechneten Dosis des Lokalanästhetikums wird bei jeder Anwendungsart empfohlen.
4.3 Gegenanzeigen
- Überempfindlichkeit gegenüber Ropivacain oder anderen Lokalanästhetika vom Amidtyp oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile.
- Allgemeine Gegenanzeigen in Verbindung mit einer Epiduralanästhesie sollten unabhängig vom verwendeten Lokalanästhetikum berücksichtigt werden.
- Intravenöse Regionalanästhesie.
- Parazervikalanästhesie in der Geburtshilfe.
- Hypovolämie.
4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen für der Anwendung
Regionalanästhesien sollten ausschließlich in entsprechend eingerichteten Räumlichkeiten und durch entsprechend ausgebildetes Personal erfolgen. Ausrüstung und Arzneimittel für das Monitoring und eine notfallmäßige Wiederbelebung sind bereitzustellen. Patienten, bei denen eine große Blockade vorgenommen wird, sollten in einem bestmöglichen klinischen Zustand sein und vor Beginn der Blockade einen intravenösen Zugang erhalten. Der verantwortliche Arzt sollte die erforderlichen Vorsichtsmaßnahmen ergreifen, um eine intravasale Injektion zu vermeiden (siehe Abschnitt 4.2). Er sollte entsprechend ausgebildet sein und über ausreichende Kenntnisse bezüglich der Anzeichen und Behandlung von Nebenwirkungen, systemischer Toxizität und anderen Komplikationen wie z.B. einer unbeabsichtigten subarachnoidalen Injektion, die eine hohe Spinalanästhesie mit Apnoe und Hypotension verursachen kann, verfügen (siehe Abschnitt 4.8 und 4.9). Nach der Plexus-brachialis-Blockade und der Epiduralanästhesie traten Krämpfe vergleichsweise am häufigsten auf. Dies resultiert wahrscheinlich aus einer akzidentellen intravasalen Injektion oder einer zu schnellen Resorption vom Injektionsort.
Vorsicht ist erforderlich, um Injektionen in entzündete Gebiete zu vermeiden.
Herz-Kreislauf
Patienten, die mit Antiarrhythmika der Klasse III (z.B. Amiodaron) behandelt werden, sind streng zu überwachen. Ein EKG-Monitoring sollte in Betracht gezogen werden, da sich kardiale Effekte addieren können.
In sehr seltenen Fällen wurde über das Auftreten eines Herzstillstandes während der Anwendung von Ropivacain zur Epiduralanästhesie oder zur peripheren Nervenblockade vor allem nach einer unbeabsichtigten, versehentlichen intravasalen Injektion bei älteren Patienten und bei Patienten mit begleitender Herzerkrankung berichtet. In einigen Fällen war die Wiederbelebung schwierig. Bei einem Herzstillstand können längere Wiederbelebungsversuche erforderlich sein, um die Möglichkeit eines erfolgreichen Ausgangs zu verbessern.
Blockade von Kopf und Hals
Bestimmte lokalanästhetische Verfahren wie z.B. Injektionen in der Kopf- und Halsregion, können unabhängig vom verwendeten Lokalanästhetikum mit einer erhöhten Häufigkeit schwerwiegender unerwünschter Wirkungen verbunden sein. Es ist dafür zu sorgen, dass Injektionen in entzündete Bereiche vermieden werden.
Plexusblockaden
Plexusblockaden können implizieren, dass ein großes Volumen eines Lokalanästhetikums in stark vaskularisierten Regionen, oft in der Nähe großer Gefäße, angewendet wird. Dort besteht ein erhöhtes Risiko einer intravasalen Injektion und/oder einer schnellen systemischen Absorption, was zu hohen Plasmakonzentrationen führen kann.
Die Anwendung bei Kindern unter 1 Jahr kann so lange nicht empfohlen werden, bis weitere Erfahrungen vorliegen.
Überempfindlichkeit
Eine mögliche Kreuzallergie mit anderen Lokalanästhetika vom Amidtyp sollte in Betracht gezogen werden. (siehe Abschnitt 4.3).
Hypovolämie
Patienten mit Hypovolämie können während einer Epiduralanästhesie unabhängig vom verwendeten Lokalanästhetikum eine plötzliche und schwere Hypotonie entwickeln.
Patienten im schlechten Allgemeinzustand
Patienten in altersbedingt schlechtem Allgemeinzustand oder mit anderen beeinträchtigenden Faktoren, wie teilweisem oder vollständigem AV-Block, fortgeschrittener Leber- oder Nierenfunktionsstörung, benötigen besondere Aufmerksamkeit, auch wenn bei diesen Patienten eine Regionalanästhesie besonders häufig angezeigt ist.
Patienten mit Funktionsstörungen von Leber und NiereRopivacain wird in der Leber metabolisiert und sollte daher bei Patienten mit schwerer Lebererkrankungen mit besonderer Vorsicht angewendet werden. Bei wiederholter Verabreichung kann eine Verminderung der Dosierung zur Anpassung an die verzögerte Ausscheidung erforderlich werden. Bei Anwendung von Einzeldosen oder bei Kurzzeitanwendung ist bei Patienten mit eingeschränkter Nierenfunktion eine Anpassung der Dosis im Allgemeinen nicht erforderlich. Azidose und verminderte Plasmaproteinkonzentrationen, wie sie häufig bei Patienten mit chronischem Nierenversagen beobachtet werden, erhöhen möglicherweise die systemische Toxizität.
Akute Porphyrie
Ropivacain kann möglicherweise eine Porphyrie auslösen und sollte bei Patienten mit akuter Porphyrie nur angewendet werden, wenn keine sicherere Alternative zur Verfügung steht. Entsprechende Vorsichtsmaßnahmen bei gefährdeten Patienten sollte gemäß Fachliteratur und /oder in Absprache mit einem Spezialisten erfolgen.
Chondrolyse
Nach Markteinführung wurde bei Patienten, die postoperativ intraartikuläre Dauerinfusionen von Lokalanästhetika (einschließlich Ropivacain) erhalten haben, über Chondrolyse berichtet. Bei der Mehrheit der berichteten Fälle war das Schultergelenk betroffen. Intraartikuläre Dauerinfusionen mit Ropivacain sollten vermieden werden, da die Wirksamkeit und Unbedenklichkeit nicht erwiesen wurden.
Langzeitanwendung
Eine längere Anwendung von Ropivacain sollte bei Patienten vermieden werden, die gleichzeitig mit starken CYP1A2-Hemmem wie Fluvoxamin und Enoxacin behandelt werden (siehe Abschnitt 4.5).
Kinder
Bei Neugeborenen kann besondere Vorsicht geboten sein, da die Stoffwechselfunktionen noch nicht vollständig ausgereift sind. In klinischen Untersuchungen variierten die Plasmakonzentrationen von Ropivacain bei Neugeborenen stark. Möglicherweise ist daher das Risiko für eine systemische Toxizität in dieser Altersgruppe erhöht, besonders bei kontinuierlicher epiduraler Infusion.
Die empfohlenen Dosierungsangaben bei Neugeborenen basieren auf begrenzten klinischen Daten.
Ropivacain sollte bei diesen Patienten nur unter ständiger Beobachtung bezüglich Anzeichen systemischer Toxizität (z.B. Anzeichen von ZNS-Toxizität, EKG, Blutsauerstoffsättigungswert) und lokalen neurotoxischen Ereignissen (z.B. verlängerte Erholungsphase) angewendet werden. Aufgrund einer langsamen Ausscheidung von Ropivacain bei Neugeborenen sollten diese Kontrollen auch nach der Infusion fortgeführt werden.
Die Sicherheit und Wirksamkeit von Ropivacain 7,5 mg/ml und 10 mg/ml ist für Kinder bis einschließlich 12 Jahre nicht belegt.
Sonstige Bestandteile mit bekannter Wirkung
1 ml Ropivacain-KK 10 mg/ml Injektionslösung enthält 0,13 mmol (2,9 mg) Natrium. Dies ist zu berücksichtigen bei Personen unter Natrium kontrollierter (natriumarmer/-kochsalzarmer) Diät.
4.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen
Ropivacain sollte mit Vorsicht angewendet werden bei Patienten, die andere Lokalanästhetika oder Arzneimittel erhalten, die strukturell mit Anästhetika vom Amidtyp verwandt sind, da sich die systemischen toxischen Wirkungen addieren. Dies trifft auf z.B. für bestimmte Antiarrhythmika wie Lidocain und Mexiletin zu. Die gleichzeitige Anwendung von Ropivacain und Allgemeinanästhetika oder Opioiden kann die jeweiligen (Neben-)Wirkungen verstärken. Es sind keine spezifischen Interaktionsstudien mit Ropivacain und Antiarrhythmika der Klasse III (z.B. Amiodaron) durchgeführt worden, dennoch ist Vorsicht geboten (siehe auch Abschnitt 4.4).
Das Cytochrom-P-450(CYP)1A2 ist beteiligt an der Bildung von 3-Hydroxy-Ropivacain, dem Hauptmetaboliten. Bei gleichzeitiger Anwendung von Fluvoxamin, einem selektiven und wirksamen CYP1A2-Hemmer, war die Plasmaclearance von Ropivacain in vivo um bis zu 77 % vermindert. Somit können starke CYP1A2-Hemmer wie Fluvoxamin und Enoxacin, wenn sie während einer längeren Anwendung von Ropivacain gleichzeitig gegeben werden, Wechselwirkungen mit Ropivacain haben. Eine längere Anwendung von Ropivacainsollte bei Patienten vermieden werden, die begleitend mit starken CYP1A2-Hemmern behandelt werden (siehe Abschnitt 4.4).
Bei gleichzeitiger Verabreichung von Ketoconazol, einem selektiven und wirksamen CYP3A4-Hemmer, wurde die Plasmaclearance von Ropivacain in vivo um 15 % vermindert. Die Hemmung dieses Isoenzyms ist jedoch wahrscheinlich nicht klinisch relevant.
In vitro ist Ropivacain ein kompetitiver Hemmer von CYP2D6, jedoch hemmt es dieses Isoenzym offensichtlich nicht bei klinisch erreichten Plasmakonzentrationen.
4.6 Fertilität, Schwangerschaft und Stillzeit
Schwangerschaft
Mit Ausnahme der epiduralen Anwendung in der Geburtshilfe gibt es keine ausreichenden Daten zur Anwendung von Ropivacain in der Schwangerschaft beim Menschen. In tierexperimentellen Studien zeigten sich keine direkten oder indirekten schädlichen Auswirkungen auf
Schwangerschaft, embryonale/fötale Entwicklung, Entbindung oder postnatale Entwicklung (siehe Abschnitt 5.3).
Stillzeit
Es gibt keine Untersuchungen bei Frauen zur Frage des Übertritts von Ropivacain in die Muttermilch.
4.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen
Es wurden keine Studien zu den Auswirkungen auf die Verkehrstüchtigkeit und das Bedienen von Maschinen durchgeführt. Abhängig von der Dosis kann jedoch ein geringer Einfluss auf psychische Funktionen und die Koordination erwartet werden. Auch wenn sonst keine deutlichen Zeichen einer ZNS-Toxizität vorhanden sind, können die motorische Beweglichkeit und die Reaktionsfähigkeit vorübergehend vermindert sein.
4.8 Nebenwirkungen
Allgemein
Das Nebenwirkungsprofil von Ropivacain entspricht dem anderer lang wirksamer Lokalanästhetika vom Amidtyp.
Die Nebenwirkungen müssen von den physiologischen Wirkungen der Nervenblockade selbst, z. B. einer Abnahme des Blutdrucks und einer Bradykardie während der Spinal-/Epiduralanästhesie, unterschieden werden.
Tabelle der Nebenwirkungen
Die verwendeten Häufigkeitsangaben in der Tabelle sind wie folgt: Sehr häufig (>1/10)
Häufig (>1/100 bis <1/10)
Gelegentlich (>1/1000 bis <1/100)
Selten (>1/10 000 bis <1/1000)
Sehr selten (<1/10 000)
|
Systemorganklasse |
Häufigkeit |
Nebenwirkung |
|
Psychiatrische Erkrankungen |
Gelegentlich |
Angst |
|
Erkrankungen des Nervensystems |
Häufig |
Parästhesien Schwindel Kopfschmerzen |
|
Gelegentlich |
ZNS-Toxizitätssymptome (Krämpfe, tonisch-klonische Krämpfe, Anfälle, Benommenheit, zirkumorale Parästhesie, Taubheit der Zunge, Hyperakusis, Tinnitus, Sehstörungen, Dysarthrie, Muskelzucken, Tremor)*, Hypästhesie | |
|
Herzerkrankungen |
Häufig |
Bradykardie Tachykardie |
|
Selten |
Herzstillstand Herzrhythmusstörungen | |
|
Gefäßerkrankungen |
Sehr häufig |
Hypotonie a |
|
Häufig |
Hypertonie | |
|
Gelegentlich |
Synkope | |
|
Erkrankung der Atemwege und |
Gelegentlich |
Dyspnoe |
|
des Brustraums und Mediastinums | ||
|
Erkrankungen des Gastrointestinaltrakts |
Sehr häufig |
Übelkeit |
|
Gelegentlich |
Erbrechen b | |
|
Erkrankungen der Nieren und Harnwege |
Häufig |
Harnretention |
|
Allgemeine Erkrankungen und Beschwerden am Verabreichungsort |
Häufig |
Temperaturerhöhung Rigor Rückenschmerzen |
|
Gelegentlich |
Absinken der Körpertemperatur | |
|
Selten |
allergische Reaktion (anaphylaktische Reaktioinen, angioneurotisches Ödem und Urtiakaria) |
a Eine Hypotonie kommt bei Kindern seltener vor (< 1/100) b Erbrechen tritt bei Kindern häufiger auf (> 1/10)
* Diese Symptome treten normalerweise aufgrund versehentlicher intravasaler Injektion, Überdosierung oder schneller Absorption auf (siehe Abschnitt 4.9)
Klassenbezogene Nebenwirkungen:
Neurologische Komplikationen
Neuropathie und Verletzung des Rückenmarks (z. B. Arteria-spinalis-anterior-Syndrom, Arachnoiditis, Cauda equina Syndrom) wurden mit der Regionalanästhesie in Zusammenhang gebracht und können in seltenen Fällen zu bleibenden Schäden führen. Diese Komplikationen sind unabhängig vom verwendeten Lokalanästhetikum.
Totale spinale Blockade
Eine totale spinale Blockade kann auftreten, wenn eine epidurale Dosis versehentlich intrathekal angewendet wird.
Akute systemische Toxizität
Systemische toxische Reaktionen betreffen in erster Linie das zentrale Nervensystem (ZNS) und das kardiovaskuläre System. Solche Reaktionen werden durch hohe Blutkonzentrationen eines Lokalanästhetikums verursacht, die bei einer (versehentlichen) intravasalen Injektion, Überdosierung oder außergewöhnlich schneller Absorption aus stark vaskularisierten Regionen auftreten können (siehe Abschnitt 4.4). ZNS-Reaktionen sind bei allen Lokalanästhetika vom Amidtyp ähnlich, während kardiale Reaktionen stärker, sowohl quantitativ als auch qualitativ, von dem Wirkstoff abhängen.
ZNS Toxizität
Bei toxischen Wirkungen auf das ZNS können Stufen mit Symptomen ansteigenden Schweregrades unterschieden werden. Anfänglich werden Symptome wie Seh- oder Hörstörungen, periorales Taubheitsgefühl. Schwindelgefühl, Benommenheit, Kribbeln und Parästhesien beobachtet. Dysarthrie, Rigor und Tremor sind schwerwiegender und können den Beginn von generalisierten Krämpfen andeuten. Solche Anzeichen dürfen nicht als Symptome einer neurologischen Erkrankung fehlgedeutet werden. Bewusstlosigkeit und tonisch-klonische Krämpfe können folgen, die einige Sekunden bis mehrere Minuten dauern können. Hypoxie und Hyperkapnie treten zusammen mit Respirationsstörungen während der Konvulsionen durch die erhöhte Muskelaktivität rasch auf. In schweren Fällen kann sogar eine Apnoe auftreten. Die respiratorische und metabolische Azidose verstärkt und verlängert die toxischen Wirkungen der Lokalanästhetika.
Nach Rückverteilung des Lokalanästhetikums aus dem ZNS und anschließender Metabolisierung und Exkretion tritt die Regeneration ein. Der Zustand des Patienten kann sich rasch normalisieren, wenn keine großen Mengen des Arzneimittels injiziert wurden.
Kardiovaskuläre Toxizität
Die Symptome der kardiovaskulären Toxizität zeigen eine schwerwiegendere Situation an. Hypotonie, Bradykardie, Arrhythmie und sogar Herzstillstand können infolge hoher systemischer Konzentrationen des Lokalanästhetikums auftreten. Die intravenöse Infusion von Ropivacain bewirkte bei freiwilligen Probanden eine Verringerung der Reizleitung und Kontraktilität.
Toxischen Wirkungen auf das kardiovaskuläre System gehen im Allgemeinen Toxizitätssymptome vom Zentralnervensystem voraus, es sei denn, der Patient erhält eine Allgemeinanästhesie oder ist durch Substanzen wie Benzodiazepine oder Barbiturate stark sediert.
Kinder
Häufigkeit, Art und Schwere der Nebenwirkungen bei Kindern sind erwartungsgemäß mit denen bei Erwachsenen vergleichbar mit Ausnahme von Hypotension, die bei Kindern weniger häufig (< 1 von 10) und Erbrechen, das bei Kindern häufiger (> 1 von 10) auftritt.
Bei Kindern können frühe Anzeichen einer lokalen Toxizität des Anästhetikums schwer erkennbar sein, da sie ggf. nicht in der Lage sind, diese verbal adäquat auszudrücken (siehe Abschnitt 4.4). Die häufigsten bei Kindern beobachteten klinisch relevanten Nebenwirkungen sind Erbrechen, Übelkeit, Juckreiz und Harnstau
Behandlung von akuter systemischer Toxizität
Siehe Abschnitt 4.9.
Meldung des Verdachts auf Nebenwirkungen
Diese Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung dem Bundesinstitut für Arzneimittel und Medizinprodukte, Abt. Pharmakovigilanz, Kurt-Georg-Kiesinger-Allee 3, D-53175 Bonn, Website: http://www.bfarm.de anzuzeigen.
4.9 Überdosierung Symptome
Eine unbeabsichtigte intravasale Injektion kann unmittelbare (innerhalb von Sekunden bis zu wenigen Minuten) systemische toxische Reaktionen verursachen. Bei einer Überdosierung werden abhängig von der Injektionsstelle Spitzenplasmakonzentrationen erst nach ein bis zwei Stunden nach der Injektion erreicht. Zeichen von Toxizität können daher verzögert auftreten (siehe Abschnitt 4.8).
Akuttherapie
Ausrüstung und Arzneimittel für das Monitoring sowie eine notfallmäßige Wiederbelebung müssen sofort zur Verfügung stehen. Wenn Anzeichen einer akuten systemische Intoxikation auftreten, muss die Injektion des Lokalanästhetikums sofort gestoppt werden . Symptome, die das ZNS betreffen (Krämpfe, Depression des ZNS), müssen umgehend durch entsprechende Unterstützung der Atemwege/des Atmens und durch Verabreichung eines Antikonvulsivums behandelt werden. Wenn die Krämpfe nicht spontan innerhalb von 15-20 Sekunden abklingen, muss ein Antikonvulsivum intravenös verabreicht werden. Thiopental Natrium, 1-3 mg/kg, intravenös löst die Krämpfe rasch. Alternativ kann Diazepam, 0,1 mg/kg, intravenös gegeben werden, auch wenn die Wirkung langsamer eintritt. Suxamethonium (Succinylcholin) stoppt die Muskelkrämpfe rasch, aber der Patient benötigt eine kontrollierte Beatmung und tracheale Intubation.
Sollte ein Kreislaufstillstand eintreten, müssen umgehend kardiopulmonale Wiederbelebungsmaßnahmen ergriffen werden. Eine optimale Sauerstoffzufuhr, künstliche Beatmung, Kreislaufunterstützung und die Behandlung der Azidose sind lebenswichtig.
Bei kardiovaskulärer Depression (Hypotonie. Bradykardie) sollte eine angemessene Behandlung mit intravenösen Flüssigkeiten, vasopressorischen, chronotropen und/oder inotropen Arzneimitteln in Betracht gezogen werden. Kindern sollten Dosen entsprechend ihrem Alter und Gewicht verabreicht werden.
Bei einem Herzstillstand kann ein erfolgreicher Ausgang längere Wiederbelebungsversuche voraussetzen.
5. PHARMAKOLOGISCHE EIGENSCHAFTEN
5.1. Pharmakodynamische Eigenschaften
Pharmakotherapeutische Gruppe: Lokalanästhetika, Amide ATC-Code: N01 B B09
Ropivacain ist ein langwirksames Lokalanästhetikum vom Amidtyp mit sowohl anästhetischen als auch analgetischen Wirkungen. In hohen Dosen ruft es eine für chirurgische Eingriffe geeignete Anästhesie hervor, während es in niedrigeren Dosen sensorische Blockaden (Analgesie) mit begrenzter und nichtprogressiver motorischer Blockade bewirkt.
Der Wirkmechanismus beruht auf einer reversiblen Verminderung der Membranpermeabilität der Nervenfaser für Natriumionen. Als Folge davon vermindert sich die Depolarisationsgeschwindigkeit und die Reizschwelle wird erhöht. Dies führt schließlich zu einer lokalen Blockade der Nervenimpulse.
Besonders charakteristisch für Ropivacain ist die lange Wirkdauer. Wirkungseintritt und Wirkdauer der Lokalanästhesie hängen vom Applikationsort ab. Durch Zugabe eines Vasokonstriktors (z. B. Adrenalin [Epinephrin]) kann die Wirkdauer nicht verlängert werden. Weitere Informationen siehe Dosierungstabelle unter 4.2.
Gesunde Probanden vertrugen eine intravenöse Infusion mit Ropivacain bei geringen Dosen sehr gut und bei den maximal tolerierten Dosen mit den erwarteten ZNS-Symptomen. Die klinischen Erfahrungen mit diesem Arzneimittel deuten auf eine große therapeutische Breite hin, wenn es entsprechend den empfohlenen Dosierungen verwendet wird.
5.2. Pharmakokinetische Eigenschaften
Ropivacain hat ein chirales Zentrum und ist als reines S-(-)-Enantiomer verfügbar. Es ist stark fettlöslich. Alle Metaboliten haben lokalanästhetische Wirkung, jedoch mit beträchtlich geringerer Stärke und kürzerer Dauer als Ropivacain.
Die Plasmakonzentration von Ropivacain hängt von der Dosis, der Art der Applikation und der Vaskularisierung des Gewebes der Injektionsstelle ab. Ropivacain hat eine lineare Pharmakokinetik und die maximale Plasmakonzentration ist proportional zur Dosis.
Ropivacain wird vollständig in zwei Phasen aus dem Epiduralraum resorbiert. Die Halbwertszeiten für die schnelle und die langsame Phase des biphasischen Prozesses liegen bei Erwachsenen im Bereich von 14 Minuten bzw. 4 Stunden. Die langsame Resorption ist der limitierende Faktor der Eliminierung von Ropivacain, was erklärt, warum die gemessene terminale Halbwertszeit nach epiduraler Verabreichung länger ist als nach intravenöser Verabreichung.
Bei Kindern verläuft die Resorption von Ropivacain aus dem Epiduralraum ebenfalls zweiphasig.
Ropivacain hat eine mittlere Gesamtplasmaclearance von 440 ml/min, eine renale Clearance von 1 ml/min, ein Verteilungsvolumen im Steady state von 47 l und eine terminale Halbwertszeit von 1,8 h nach intravenöser Verabreichung. Ropivacain hat ein mittleres hepatisches Extraktionsverhältnis von ca. 0,4. Es ist im Plasma hauptsächlich an alpha-1-saures Glykoprotein (AAG) gebunden, der ungebundene Anteil beträgt ca. 6 %.
Bei kontinuierlicher epiduraler und interskalenärer Infusion wurde im Zusammenhang mit einem postoperativen Anstieg des alpha-1-sauren Glykoproteins (AAG) ein Anstieg der Gesamtkonzentration im Plasma beobachtet.
Schwankungen der ungebundenen, d.h. pharmakologisch aktiven Fraktion waren sehr viel geringer als die der Gesamtplasmakonzentration.
Ropivacain besitzt eine mittlere bis geringe hepatische Eliminationsrate. Daher sollte seine Eliminationsgeschwindigkeit von der ungebundenen Plasmakonzentration abhängen. Ein postoperativer Anstieg des AAG verringert die ungebundene Fraktion aufgrund der zunehmenden Proteinbindung. Wie man in Studien bei Kindern und Erwachsenen gesehen hat, wird hierdurch wiederum die Gesamtclearance herabgesetzt, was zu einem Anstieg der Gesamtplasmakonzentration führt. Die Clearance der ungebundenen Anteile von Ropivacain bleibt unverändert, wie sich während postoperativer Infusionen anhand der stabilen Konzentrationen der ungebundenen Fraktion zeigen ließ. Pharmakodynamische Effekte und Toxizität hängen demnach mit dem ungebundenen Anteil im Plasma zusammen.
Ropivacain überwindet die Plazentaschranke leicht und es stellt sich schnell ein Gleichgewicht der ungebundenen Konzentration im Plasma ein. Das Ausmaß der Plasmaproteinbindung im Fetus ist geringer als bei der Mutter, was beim Fetus zu geringeren Gesamtplasmakonzentrationen führt als bei der Mutter.
Ropivacain wird extensiv metabolisiert, vorwiegend durch aromatische Hydroxylierung. Insgesamt werden nach intravenöser Verabreichung 86 % der Dosis über den Urin ausgeschieden, jedoch nur ca. 1 % als unveränderte Substanz. Der Hauptmetabolit ist das 3-Hydroxy-Ropivacain (ca. 37 %), das hauptsächlich in konjugierter Form über den Urin ausgeschieden wird. Die Ausscheidung von 4-Hydroxy-Ropivacain, dem N-dealkylierten (PPX) und dem 4-Hydroxy-dealkylierten Metaboliten beträgt ca. 1 bis 3 % der Dosis. Konjugiertes und unkonjugiertes 3-Hydroxy-Ropivacain treten nur in gerade nachweisbaren Konzentrationen im Plasma auf.
Ein ähnliches Metabolitenmuster wurde bei Kindern älter als 1 Jahr festgestellt.
Eine eingeschränkte Nierenfunktion hat weniger bis gar keinen Einfluss auf die Pharmakokinetik von Ropivacain. Die renale PPX-Clearance korreliert signifikant mit der Kreatinin-Clearance. Das Fehlen der Korrelation zwischen der Gesamt-Exposition, die als AUC dargestellt wird, und der Kreatinin-Clearance deutet darauf hin, dass für die vollständige Elimination von PPX zusätzlich zur renalen Ausscheidung ein nicht renaler Eliminationsweg von Bedeutung ist. Einige Patienten mit eingeschränkter Nierenfunktion können eine erhöhte PPX-Exposition aufweisen, die auf eine reduzierte nicht renale Elimination zurückzuführen ist. Aufgrund der reduzierten ZNS-Toxizität von PPX im Vergleich zu Ropivacain werden die klinischen Auswirkungen bei einer Kurzbehandlung als geringfügig angesehen. Patienten mit terminaler Niereninsuffizienz, die eine regelmäßige Dialysebehandlung bekommen, wurden nicht untersucht.
Es gibt keinen Hinweis auf eine In-vivo-Razemisierung von Ropivacain.
Kinder
Die Pharmakokinetik von Ropivacain wurde ein einer gepoolten PK Patientenanalyse mit Daten von 192 Kindern zwischen 0 und 12 Jahren untersucht. Die Clearance des ungebundenen Ropivacains und des PPX sowie das Verteilungsvolumen der ungebundenen Fraktion hängen bis zur vollständigen Ausreifung der Leberfunktion von Körpergewicht und Alter ab. Danach hängt die Clearance vorwiegend vom Körpergewicht ab. Der Reifungsprozess ist für die Clearance des ungebundenen Ropivacain offenbar mit 3 Jahren abgeschlossen, für die Clearance von PPX bereits mit 1 Jahr und für das Verteilungsvolumen der ungebundenen Fraktion von Ropivacain mit 2 Jahren. Das Verteilungsvolumen des ungebundenen PPX ist nur vom Körpergewicht abhängig. PPX kann während der Epiduralinfusion kumulieren, da es eine längere Halbwertszeit und eine geringere Clearance besitzt.
Die Clearance (CIu) des ungebundenen Ropivacains erreichte bei Kindern über 6 Monaten Werte die im für Erwachsenen typischen Bereich lagen. Die in der Tabelle aufgeführten Werte der totalen Clearance (CL) wurden nicht durch den postoperativen Anstieg des AAG beeinflusst.
|
Berechnung der p |
harmakokinetischen Parameter aus der gepool |
ten pädiatrischen PK Analyse: | ||||
|
Altersgruppe |
Körpergewicht3 |
Club |
Vuc |
CLd |
t y2e |
t V ppxf |
|
kg |
(l/h/kg) |
(l/kg) |
(l/h/kg) |
(h) |
(h) | |
|
Neugeborenen |
3,27 |
2,40 |
21,86 |
0,096 |
6,3 |
43,3 |
|
1 Monat |
4,29 |
3,60 |
25,94 |
0,143 |
5,0 |
25,7 |
|
6 Monate |
7,85 |
8,03 |
41,71 |
0,320 |
3,6 |
14,5 |
|
1 Jahr |
10,15 |
11,32 |
52,60 |
0,451 |
3,2 |
13,6 |
|
4 Jahre |
16,69 |
15,91 |
65,24 |
0,633 |
2,8 |
15,1 |
|
10 Jahre |
32,19 |
13,94 |
65,57 |
0,555 |
3,3 |
17,8 |
a Mittleres Körpergewicht der jeweiligen Altersgruppe gemäß WHO Datenbank b Clearance des ungebundenen Ropivacains c Verteilungsvolumen des ungebundenen Ropivacains d Totale Ropivacainclearance e Terminale Halbwertszeit von Ropivacain f Terminale Halbwertszeit von PPX
Die nach einer einzeitigen Kaudal-Blockade kalkulierten mittleren maximalen Plasmakonzentration (Cumax) waren bei Neugeborenen höher und die Zeit bis Cumax (tmax) erreicht war nahm mit zunehmenden Alter ab (Tabelle unten). Die kalkulierten mittleren ungebundenen Plasmakonzentrationen lagen nach 72-stündiger epiduraler Infusion in den empfohlenen Dosierungen bei Neugeborenen ebenfalls höher als bei Kleinkindern und Kindern (siehe Abschnitt 4.4).
Kalkulierte mittlere und beobachtete Bereiche von ungebundenem Cumax nach einzeitiger KaudalBlockade:
|
Altersgruppe |
Dose (mg/kg) |
Cu max (mg/l)3 |
rp b T max |
Cu max (mg/l)c |
|
0-1 Monate |
2,00 |
0,0582 |
2,00 |
0,05-0,08 (n=5) |
|
1-6 Monate |
2,00 |
0,0375 |
1,50 |
0,02-0,09 (n= 18) |
|
6-12 Monate |
2,00 |
0,0283 |
1,00 |
0,01-0,05 (n=9) |
|
1-10 Jahre |
2,00 |
0,0221 |
0,50 |
0,01-0,05 (n=60) |
a Ungebundene maximale Plasmakonzentrationen b Zeit, bis die ungebundene maximale Plasmakonzentration erreicht ist. c Beobachtete und dosisangepasste ungebundene maximale Plasmakonzentrationen.
Im Alter von 6 Monaten, dem Zeitpunkt für eine Änderung der empfohlenen Dosierung zur kontinuierlichen epiduralen Infusion, erreicht die Clearance des ungebundenen Ropivacains 34% und die Clearance des ungebundenen PXX 71% des Wertes beim Erwachsenen. Im Vergleich zu älteren Kindern ist die systemische Verfügbarkeit bei Neugeborenen und Kindern zwischen 1 und 6 Monate höher, was mit der Unreife ihrer Leberfunktion zusammenhängt. Dies wird jedoch zum Teil dadurch kompensiert, dass bei Kleinkindern unter 6 Monaten für die kontinuierliche Infusion einen um 50 % reduzierte Dosierung empfohlen wird.
Eine auf den in der Patientenanalyse ermittelten PK-Parametern und ihrer Varianz basierte Kalkulation für die Summe der Plasmakonzentrationen von ungebundenem Ropivacain und PPX zeigt, dass für eine einzeitige Kaudal-Blockade die empfohlene Dosis in der jüngsten Altersgruppe um den Faktor 2,7 gesteigert werden muss und bei den 1- bis 10-Jährigen um den Faktor 7,4. Dies ist notwendig, damit der obere Grenzwert des 90%-Konfidenzintervalls den Grenzwert für eine systemische Toxizität erreicht. Die entsprechenden Faktoren für die kontinuierliche epidurale Infusion sind 1,8 bzw. 3,8.
Eine auf den in der Patientenanalyse ermittelten PK-Parametern und ihrer Varianz basierte Kalkulation für die Summe der Plasmakonzentrationen von ungebundenem Ropivacain und PPX zeigt, dass bei den 1- bis 12-Jährigen, die 3 mg/kg für eine einzeitige periphere Blockade des Ilioinguinalnervs erhalten, die mittlere ungebundene Spitzenkonzentration nach 0,8 Std. 0,0347
mg/l beträgt. Dies entspricht einem Zehntel der Toxizitätsgrenze (0,34 mg/l). Das obere 90%-Konfidenzintervall für die maximale ungebundene Plasmakonzentration beträgt 0,074 mg/l. Dies entspricht einem Fünftel der Toxizitätsgrenze. Ähnliche Werte ergeben sich für die kontinuierliche periphere Nervenblockade (0,6 mg/kg Ropivacain für 72 Stunden), der eine einzeitige periphere Nervenblockade mit 3 mg/kg vorausging. Hier beträgt die mittlere ungebundene Spitzenkonzentration 0,053 mg/l. Das obere 90%-Konfidenzintervall für die maximale ungebundene Spitzenkonzentration beträgt 0,088 mg/l. Dies entspricht einem Viertel der Toxizitätsgrenze.
5.3 Präklinische Daten zur Sicherheit
Aus den üblichen Studien zur Sicherheitspharmakologie, akuten und chronischen Toxizität bei einmaliger und wiederholter Gabe, Reproduktionstoxizität, Mutagenität und lokalen Verträglichkeit ließen sich keine Risiken für die Anwendung beim Menschen erkennen, abgesehen von den Risiken, die auf Grund des Wirkmechanismus bei hohen Dosen von Ropivacain erwartet werden können (z. B. ZNS-Symptome einschließlich Konvulsionen, Kardiotoxizität)
6. PHARMAZEUTISCHE ANGABEN
6.1 Liste der sonstigen Bestandteile
Natriumchlorid, Natriumhydroxidlösung 4% / Salzsäure 3,6% zur pH-Wert-Einstellung, Wasser für Injektionszwecke
6.2 Inkompatibilitäten
Die Verträglichkeit mit anderen Lösungen als den unter Punkt 6.6 erwähnten wurde nicht untersucht. In alkalischen Lösungen können Niederschläge auftreten, da Ropivacain bei einem pH > 6 schwer löslich ist.
6.3 Dauer der Haltbarkeit
Kunststoffampullen:
3 Jahre
Dauer der Haltbarkeit nach dem ersten Öffnen:
Aus mikrobiologischer Sicht sollte das Produkt unmittelbar verwendet werden. Wird es nicht unmittelbar verwendet, liegen die Verwendungsdauer und Aufbewahrungsbedingungen, vor der Anwendung in der Verantwortlichkeit des Anwenders; die Verwendungsdauer des Produktes ist normalerweise nicht länger als 24 Stunden bei 2 bis 8 °C.
Zur Mischung siehe Abschnitt 6.6.
6.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung
Nicht über 30 °C lagern.
Nicht einfrieren.
Zur Lagerung nach dem Öffnen siehe Abschnitt 6.3.
Für Kinder unzugänglich aufbewahren.
6.5 Art und Inhalt des Behältnisses und Packungsgrößen
5 Polypropylen Ampullen mit je 10 ml Injektionslösung steril verpackt
50 (5 x 2 x 5) Polypropylen Ampullen mit je 10 ml Injektionslösung steril verpackt
[Klinikpackung]
5 Polypropylen Ampullen mit je 20 ml Injektionslösung steril verpackt
50 (5 x 2 x 5) Polypropylen Ampullen mit je 20 ml Injektionslösung steril verpackt
[Klinikpackung]
6.6 Besondere Vorsichtsmaßnahmen für die Beseitigung und sonstige Hinweise zur Handhabung
Die Ropivacain-KK Produkte enthalten keine Konservierungsstoffe und sind deshalb nur zum einmaligen Gebrauch geeignet. Nicht verbrauchte Lösungen sind zu verwerfen.
Das noch nicht geöffnete Behältnis darf nicht autoklaviert werden.
Die Kompatibilität einer Ropivacain 2 mg/ml Infusionslösung in Kunststoffinfusionsbeuteln wurde chemisch und physikalisch mit den folgenden Produkten untersucht und veröffentlicht im Journal of Clinical Pharmacy and Therapeutics (2002) 27, 39-45:
|
Konzentration von Ropivacain: 1 bis 2 mg/ml | |
|
Zusatz |
Konzentration * |
|
Fentanylcitrat |
1,0 - 10,0 gg/ml |
|
Sufentanylcitrat |
0,4 - 4,0 gg/ml |
|
Morphinsulfat |
20,0 - 100,0 gg/ml |
|
Clonidinhydrochlorid |
5,0 - 50,0 gg/ml |
* Die in der Tabelle wiedergegebenen, Konzentrationsbereiche sind größer als die in der klinischen Praxis. Die epidurale Infusion von Ropivacain/Sufentanilcitrat, Ropivacain/Morphinsulfat bzw. Ropivacain/Chlonidinhydrochlorid wurde in klinischen Studien nicht untersucht.
Aus mikrobiologischer Sicht sollten die Mischungen unmittelbar verwendet werden. Werden diese nicht unmittelbar verwendet, liegen die Verwendungsdauer und Aufbewahrungsbedingungen vor der Anwendung in der Verantwortlichkeit des Anwenders; die Verwendungsdauer der Mischungen ist normalerweise nicht länger als 24 Stunden bei 2 bis 8 °C.
7. INHABER DER ZULASSUNG
Pharma Resources GmbH Domeierstraße 29/31 31785 Hameln Germany
Telefon : +49 5151 609 96-0 Telefax: +49 5151 609 96-30 E-Mail: info@pha-res.com
8. ZULASSUNGSNUMMER(N)
Ropivacain-KK 10 mg/ml Injektionslösung: 70369.00.00
9. DATUM DER ERTEILUNG DER ZULASSUNG/VERLÄNGERUNG DER ZULASSUNG
27.10.2008
10. STAND DER INFORMATION
06/2015
11. VERKAUFSABGRENZUNG
Verschreibungspflichtig