Salbulair N 100 Μg Autohaler Druckgasinhalation, Suspension
FACHINFORMATION
1. BEZEICHNUNG DES ARZNEIMITTELS
Salbulair® N100 fig Autohaler Druckgasinhalation, Suspension Wirkstoff: Salbutamolsulfat
2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Wirkstoff: Salbutamolsulfat
Jeder Sprühstoß zu je 30 mg enthält 0,1 mg Salbutamol.
Sonstiger Bestandteil mit bekannter Wirkung: Ethanol 99,4 % V/V.
Vollständige Auflistung der sonstigen Bestandteile, siehe Abschnitt 6.1.
3. DARREICHUNGSFORM
Druckgasinhalation, Suspension
4. KLINISCHE ANGABEN
4.1 Anwendungsgebiete
Symptomatische Behandlung von Erkrankungen mit reversibler Obstruktion der Atemwege wie z. B. Asthma bronchiale oder chronisch obstruktive bronchiale Erkrankung (COPD) mit reversibler Komponente.
Verhütung von durch Anstrengung oder Allergenkontakt verursachte Asthmaanfälle.
Salbulair® N 100 pg Autohaler wird angewendet bei Erwachsenen, Jugendlichen und Kindern im Alter von 4 bis 11 Jahren (für die Anwendung bei Kleinkindern und Kindern unter 4 Jahren siehe Abschnitte
4.2 und 5.1).
Hinweis:
Eine längerfristige Behandlung soll symptomorientiert und nur in Verbindung mit einer entzündungshemmenden Dauertherapie erfolgen.
4.2 Dosierung und Art der Anwendung
Dosierung
Die Dosierung richtet sich nach Art und Schwere der Erkrankung.
Soweit vom Arzt nicht anders verordnet, gelten für Erwachsene und Kinder von 4 bis 11 Jahren folgende Dosierungsempfehlungen:
Erwachsene (einschließlich ältere Personen und Jugendliche ab 12 Jahren)
1 Einzeldosis = 1-2 Sprühstöße entspr. 0,1-0,2 mg Salbutamol.
Kinder 4-11 Jahre
1 Einzeldosis = 1 Sprühstoß entspr. 0,1 mg Salbutamol.
Zur Akutbehandlung plötzlich auftretender Bronchialkrämpfe und anfallsweise auftretender Atemnot wird eine Einzeldosis inhaliert. Sollte sich die Atemnot 5-10 Minuten nach Inhalation der ersten Einzeldosis nicht spürbar gebessert haben, kann eine weitere Einzeldosis genommen werden. Kann ein schwerer Anfall von Luftnot auch durch eine zweite Einzeldosis nicht behoben werden, können weitere Einzeldosen erforderlich werden. In diesen Fällen muss unverzüglich ärztliche Hilfe in Anspruch genommen werden.
Zur gezielten Vorbeugung bei Anstrengungsasthma oder vorhersehbarem Allergenkontakt wird eine Einzeldosis, wenn möglich etwa 10-15 Minuten vorher, inhaliert.
Die Sicherheit, nicht jedoch die Wirksamkeit, von Salbulair® N 100 pg Dosieraerosol bei Kindern unter 4 Jahren ist als vergleichbar mit derjenigen bei Kindern über 4 Jahren erwiesen. Zurzeit vorliegende Daten werden in Abschnitt 5.1 beschrieben; eine Dosierungsempfehlung kann jedoch nicht gegeben werden.
Die Tagesgesamtdosis für Erwachsene soll 0,8 mg Salbutamol nicht überschreiten. Für Kinder (im Alter von 4 bis 11 Jahren) soll die Tagesgesamtdosis 0,4 mg Salbutamol nicht überschreiten. Eine höhere Dosierung lässt im Allgemeinen keinen zusätzlichen therapeutischen Nutzen erwarten, die Wahrscheinlichkeit des Auftretens auch schwerwiegender Nebenwirkungen kann aber erhöht werden.
Dieses Arzneimittel ist ausschließlich zum Inhalieren bestimmt.
Ältere Personen
siehe Erwachsene und Schulkinder.
Art und Dauer der Anwendung Zur Inhalation.
Beim Salbulair N Autohaler handelt es sich um ein atemzugausgelöstes Inhalationsgerät, das automatisch während der Inhalation die festgesetzte Dosis des Arzneimittels über das Mundstück freisetzt, wobei die Notwendigkeit einer guten manuellen Koordination entfällt. Vor dem ersten Gebrauch und wenn der Autohaler zwei Wochen oder länger nicht benutzt wurde, werden zunächst 4 Sprühstöße in die Luft abgegeben wie nachfolgend beschrieben:
Gemäß Bedienungsanleitung inhalieren:
1. Die Schutzkappe über dem Mundstück wird von hinten nach vorne abgenommen, indem man den kleinen Vorsprung der Schutzkappe an der Rückseite des Autohalers nach unten drückt (vgl. Abb.
A).
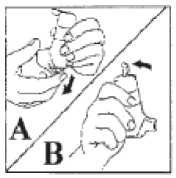
2. Der Autohaler wird gut geschüttelt. Der Autohaler wird senkrecht mit dem Mundstück nach unten gehalten und der graue Hebel am oberen Ende des Autohalers nach oben gedrückt, bis er einrastet (vgl. Abb. B). Das Mundstück wird dabei vom Anwender weggerichtet, damit die Sprühstöße in die Luft abgegeben werden können.
3. Damit ein Sprühstoß freigegeben werden kann, wird der Dosisfreigabeschieber an der Unterseite des Autohalers in Richtung des Pfeils, zur Öffnung des Mundstückes hin, gedrückt (vgl. Abb. C).
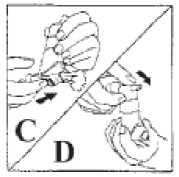
4. Damit der nächste Sprühstoß freigegeben werden kann, wird der graue Hebel nach unten gedrückt (vgl. Abb. D). Die Schritte B bis D werden wiederholt, bis insgesamt 4 Sprühstöße in die Luft abgegeben wurden.
Wichtiger Hinweis:
Der Autohaler setzt automatisch - durch den Atemzug ausgelöst - eine Medikamentendosis frei.
Für die Freisetzung des Wirkstoffs wird durchschnittlich eine Atemflussrate von 30 l/min benötigt.
Die Auslösung wird akustisch als „Klicken“ wahrgenommen. Sollte eine atemzugsausgelöste
Wirkstofffreisetzung nicht möglich sein, kann die Auslösung auch mittels Dosisfreigabeschieber
erfolgen (vgl. Abb. C).
Anleitung zur Benutzung des Autohalers:
1. Die Schutzkappe über dem Mundstück wird von hinten nach vorne abgenommen, indem man den kleinen Vorsprung der Schutzkappe an der Rückseite des Autohalers nach unten drückt (vgl. Abb.
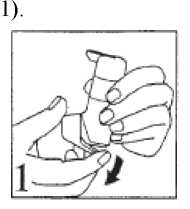
2. Der Autohaler wird gut geschüttelt. Der Autohaler wird senkrecht mit dem Mundstück nach unten gehalten und der graue Hebel am oberen Ende des Autohalers nach oben gedrückt, bis er einrastet
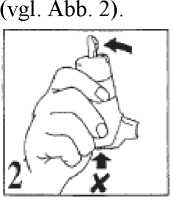
Es muss dabei beachtet werden, dass die Lufteinlassöffnung (in Abb. 2 mit X gekennzeichnet) am unteren Teil des Autohalers nicht durch die Hand blockiert wird.
3. Tief ausatmen (vgl. Abb. 3).
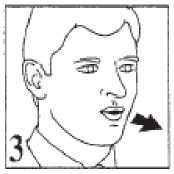
4. Das Mundstück in den Mund nehmen und mit den Lippen umschließen. Dann kräftig durch das Mundstück einatmen (vgl. Abb. 4).
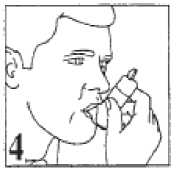
Beim Einatmen wird automatisch ein Sprühstoß mit dem Medikament freigesetzt. Die Einatmung sollte nicht gestoppt werden, damit der Sprühnebel möglichst tief eingeatmet wird.
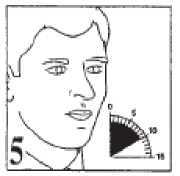
5. Den Atem so lange wie möglich (etwa 10 Sekunden) anhalten, bevor langsam ausgeatmet wird (vgl. Abb. 5). Dann sollte normal weitergeatmet werden.
6. Nach Entnahme eines Sprühstoßes wird der graue Hebel wieder in die Ausgangsposition (waagerecht) zurückgedrückt (vgl. Abb. 6).
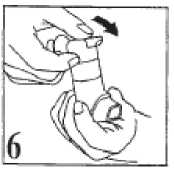
Werden mehrere Sprühstöße benötigt, wird die Anwendung gemäß Schritt 2-6 wiederholt. Nach abschließender Benutzung wird die Schutzkappe wieder aufgesetzt.
Reinigung des Mundstücks:
Die wöchentliche Reinigung des Mundstücks mit einem trockenen Tuch ist ausreichend. Das zum Reinigen verwendete Tuch oder andere Gegenstände dürfen nicht in den Autohaler gesteckt werden, da funktionelle Teile beschädigt werden können. Den Autohaler nicht auseinandernehmen.
Die Dauer der Behandlung richtet sich nach Art, Schwere und Verlauf der Erkrankung und ist vom Arzt individuell zu entscheiden.
Hinweise:
Um eine falsche Anwendung zu vermeiden, ist eine gründliche Einweisung des Patienten in den korrekten Gebrauch vorzunehmen. Kinder sollten dieses Arzneimittel nur unter Aufsicht eines Erwachsenen und nach Vorschrift des Arztes anwenden.
Übermäßiger Gebrauch von ß2-Sympathomimetika-Inhalaten wie Salbutamol kann gesundheitsschädigend sein (siehe 4.4 - Warnhinweise).
4.3 Gegenanzeigen
Überempfindlichkeit gegen den Wirkstoff oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile.
4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung
Salbulair N Autohaler sollte nur bei strenger Indikationsstellung und mit Vorsicht angewendet werden bei:
- schweren Herzerkrankungen, insbesondere frischem Herzinfarkt, koronarer Herzkrankheit, hypertropher obstruktiver Kardiomyopathie und tachykarden Arrhythmien
- Einnahme von Herzglykosiden
- schwerer und unbehandelter Hypertonie
- Aneurysmen
- Hyperthyreose
- schwer kontrollierbarem Diabetes mellitus
- Phäochromozytom.
Salbutamol sollte nicht als einzige Therapie bei Patienten mit persistierendem Asthma eingesetzt werden.
Ein ansteigender Bedarf von ß2-Sympathomimetika wie Salbulair N Autohaler ist ein Anzeichen für eine Verschlechterung der Erkrankung.
Kommt es trotz Therapie zu keiner befriedigenden Besserung oder gar zu einer Verschlechterung des Leidens, muss der Therapieplan durch den Arzt überdacht und ggf. durch eine Kombination mit entzündungshemmenden Arzneimitteln, eine Dosisanpassung einer bereits bestehenden entzündungshemmenden Therapie oder die zusätzliche Gabe weiterer Arzneimittel neu festgesetzt werden. Bei akuter oder sich rasch verschlimmernder Atemnot muss unverzüglich ärztliche Hilfe in Anspruch genommen werden.
Eine erhebliche Überschreitung, insbesondere der vorgegebenen Einzeldosen beim akuten Anfall, aber auch der Tagesdosis kann gefährlich sein wegen der kardialen Nebenwirkungen, insbesondere in Verbindung mit Elektrolyt-Verschiebungen (Hypokaliämie) und muss deshalb vermieden werden.
Es ist wiederholt über ein erhöhtes Risiko für schwere Komplikationen und Todesfälle bei der Behandlung des Asthma bronchiale mit ß-Sympathomimetika zur Inhalation berichtet worden, ohne dass die ursächlichen Zusammenhänge bisher hinreichend geklärt werden konnten.
Bei der Inhalation von Salbulair N Autohaler in hohen Dosen kann der Blutzuckerspiegel ansteigen. Bei Diabetikern sollten engmaschige Blutzuckerkontrollen durchgeführt werden.
Zur Beurteilung von Krankheitsverlauf und Therapieerfolg ist eine tägliche Selbstkontrolle nach ärztlicher Anleitung wichtig. Dies erfolgt z. B. durch regelmäßige Messung der max. Atemstoßstärke mittels Peak-flow-Meter.
Die Anwendung von Salbulair N Autohaler kann bei Dopingkontrollen zu positiven Ergebnissen führen.
Die Anwendung von Salbulair N Autohaler als Dopingmittel kann zu einer Gefährdung der Gesundheit führen.
Enthält Alkohol (weniger als 100 mg pro Einzelgabe).
4.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen
Die gleichzeitige Anwendung von Salbulair N Autohaler und ß-Rezeptorenblockern führt zu einer gegenseitigen Wirkungsabschwächung, wobei die Gabe von ß-Rezeptoren-Blockern bei Patienten mit Asthma bronchiale das Risiko der Auslösung schwerer Bronchospasmen birgt.
Weiterhin kann die Blutzucker senkende Wirkung von Antidiabetika bei Behandlung mit Salbulair N Autohaler vermindert werden. Hiermit ist jedoch im Allgemeinen erst bei höheren Dosen zu rechnen wie sie bei systemischer Gabe (als Tabletten oder Injektion/Infusion) üblich sind.
Eine wechselseitige Wirkungsverstärkung und ein erhöhtes Risiko für unerwünschte Wirkungen sind möglich bei gleichzeitiger Gabe von Salbulair N Autohaler und Methylxanthinen (wie z. B. Theophyllin) oder anderen Sympathomimetika.
Ein erhöhtes Risiko für unerwünschte Wirkungen ist möglich bei gleichzeitiger Gabe von Salbulair N Autohaler und Digitalisglykosiden.
Bei der Anwendung halogenierter Anästhetika wie z. B. Halothan, Methoxyfluran oder Enfluran muss bei Patienten, die mit Salbulair N Autohaler behandelt werden, mit einem erhöhten Risiko für schwere Herzrhythmusstörungen und Blutdrucksenkung gerechnet werden (siehe Hinweise).
Hinweise:
Wenn eine Narkose unter Verwendung von halogenierten Anästhetika geplant ist, sollte darauf geachtet werden, dass Salbutamol innerhalb von mindestens 6 Stunden vor Narkosebeginn möglichst nicht mehr angewendet wird.
Bei hoch dosierter Therapie mit Salbulair N Autohaler kann eine Hypokaliämie auftreten.
Diese kann bei gleichzeitiger Anwendung anderer Arzneimittel, insbesondere Methylxanthinen (z. B. Theophyllin), Kortikoiden, Diuretika oder Digitalisglykosiden, oder bei gleichzeitig bestehender Hypoxämie noch verstärkt werden. Eine Kontrolle der Blutsalze ist angezeigt, damit ggf. Kalium zugeführt werden kann.
4.6 Fertilität, Schwangerschaft und Stillzeit
Wirkstoff Salbutamol Schwangerschaft
Salbutamol passiert die Plazentaschranke.
Für den Menschen liegen über eine Anwendung während der Schwangerschaft unzureichende Erfahrungen vor.
Tachykardie und Hypoglykämie des Neugeborenen sind bei der Anwendung von Salbutamol als Tokolytikum beschrieben worden. Tierexperimentelle Studien haben bei der Ratte in sehr hoher Dosierung Reproduktionstoxizität gezeigt (siehe 5.3 - Präklinische Daten zur Sicherheit). Das potentielle Risiko für den Menschen ist nicht bekannt.
Obwohl bisher keine teratogenen Wirkungen beim Menschen bekannt sind, sollte Salbutamol in der Schwangerschaft, insbesondere während des ersten Schwangerschaftsdrittels nur nach besonders kritischer Indikationsstellung angewandt werden.
Das Gleiche gilt wegen der Wehen hemmenden Wirkung für die Anwendung am Ende der Schwangerschaft.
Stillzeit
Es ist unbekannt, ob Salbutamol unerwünschte Wirkungen auf das Neugeborene hat. Da Salbutamol wahrscheinlich in die Muttermilch übergeht, wird die Anwendung in der Stillzeit nur nach sorgfältiger Nutzen-Risiko-Abwägung empfohlen.
Treibmittel Norfluran
Studien mit dem Treibmittel Norfluran an trächtigen und säugenden Ratten und Kaninchen zeigten kein spezielles Risiko.
4.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen
Durch individuell auftretende unterschiedliche Reaktionen, insbesondere bei höherer Dosierung, kann die Fähigkeit zur aktiven Teilnahme am Straßenverkehr oder zum Bedienen von Maschinen beeinträchtigt werden. Dies gilt in verstärktem Maße bei Behandlungsbeginn sowie bei Zusammenwirken mit Alkohol oder Beruhigungs- und Schlafmitteln.
4.8 Nebenwirkungen
|
sehr häufig |
> 1/10 |
|
häufig |
> 1/100 bis < 1/10 |
|
gelegentlich |
> 1/1.000 bis < 1/100 |
|
selten |
> 1/10.000 bis < 1/1.000 |
|
sehr selten |
< 1/10.000 |
|
nicht bekannt |
Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar |
Abhängig von der Dosierung und der individuellen Empfindlichkeit können gelegentlich auftreten:
- feinschlägiger Tremor, Übelkeit, Missempfindungen im Mund- und Rachenbereich, Schwitzen, Unruhe, Kopfschmerzen, Schwindel sowie selten Muskelkrämpfe (diese Nebenwirkungen können sich bei Fortführung der Behandlung im Verlaufe von 1-2 Wochen zurückbilden).
- weiterhin wurden beobachtet:
Tachykardie, Tachyarrhythmie, Palpitationen sowie in seltenen Fällen ventrikuläre Extrasystolen, Angina pectoris und Beeinflussung des Blutdrucks (Senkung oder Steigerung) metabolische Veränderungen, wie Hypokaliämie, Hyperglykämie, Anstieg des Blutspiegels von Insulin, freien Fettsäuren, Glycerol und Ketonkörpern.
- vereinzelt ist über zentralnervös stimulierende Wirkungen nach Inhalation von Salbutamol berichtet worden, die sich in Übererregbarkeit, hyperaktiven Verhaltensauffälligkeiten, Schlafstörungen sowie Halluzinationen äußerten. Diese Beobachtungen wurden überwiegend bei Kindern im Alter bis zu 12 Jahren gemacht.
- es liegen Berichte über das Auftreten paradoxer Bronchospasmen nach Gabe von inhalativen Arzneimitteln vor (siehe unter „Hinweise“).
- sehr selten sind Überempfindlichkeitsreaktionen wie z. B. Juckreiz, Exanthem, Blutdruckabfall, Thrombopenie, Gesichtsödem und Nephritis beschrieben worden.
- nach Inhalation kann es zu einer Reizung im Rachenbereich und Husten kommen.
- mit nicht bekannter Häufigkeit kann es zum Auftreten einer Myokardischämie kommen.
Hinweis:
Verschlimmert sich die Atemnot nach der Inhalation akut (paradoxe Bronchospastik), so sollte die Behandlung sofort abgebrochen und der Behandlungsplan überprüft werden.
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung dem Bundesinstitut für Arzneimittel und Medizinprodukte, Abt. Pharmakovigilanz, Kurt-Georg-Kiesinger-Allee 3, D-53175 Bonn, Website: www.bfarm.de anzuzeigen.
4.9 Überdosierung
Symptome einer Überdosierung
Im Falle einer Überdosierung treten die bereits benannten Nebenwirkungen sehr schnell und ggf. in verstärktem Umfang in Erscheinung.
Typische Symptome sind:
Tachykardie, Palpitationen, Arrhythmien, Ruhelosigkeit, Schlafstörungen, Brustschmerzen und heftiger Tremor insbesondere an den Händen, aber auch am ganzen Körper. Gelegentlich sind nach exzessiven Salbutamol-Dosen psychotische Reaktionen beobachtet worden.
Bei Überdosierung von Salbutamol kann es verstärkt zu Verschiebungen von Kalium in den Intrazellularraum mit der Folge einer Hypokaliämie sowie zu Hyperglykämie, Hyperlipidämie, Hyperketonämie und Laktatazidose kommen.
Therapiemaßnahmen bei Überdosieruns
Die Behandlung nach ß-sympathomimetischer Überdosierung erfolgt hauptsächlich symptomatisch. Nachfolgend sind eine Reihe zu empfehlender Maßnahmen angeführt:
- für den Fall, dass große Mengen des Arzneimittels geschluckt wurden, sollte eine Magenspülung erwogen werden. Aktivkohle und Abführmittel können die unerwünschte Resorption des ß-Sympathomimetikums günstig beeinflussen.
- die kardialen Symptome können mit einem kardioselektiven ß-Rezeptorenblocker behandelt werden, hierbei ist jedoch ein erhöhtes Risiko für die Auslösung einer Bronchospastik bei Patienten mit Asthma bronchiale zu beachten.
- zur kardialen Überwachung ist EKG-Monitoring angezeigt.
- im Falle von ausgeprägteren Blutdrucksenkungen ist eine Volumensubstitution (z. B. Plasmaersatzmittel) zu empfehlen.
Es muss mit der Entwicklung einer Hypokaliämie gerechnet werden, sodass entsprechende Kontrollen des Elektrolythaushaltes und ggf. Substitutionen zu empfehlen sind. Zu beachten ist dabei auch eine eventuell vorausgehende Behandlung mit anderen Pharmaka, die eine Hypokaliämie verursachen können.
5. PHARMAKOLOGISCHE EIGENSCHAFTEN
5.1 Pharmakodynamische Eigenschaften
Pharmakotherapeutische Gruppe: Broncholytikum/Antiasthmatikum/ß2-Sympathomimetikum ATC-Code: R03AC02
Salbutamol ist ein direkt wirkendes Sympathomimetikum. Es ist ein überwiegend selektiver ß2-Adrenozeptor-Agonist, der sowohl die glatte als auch die quergestreifte Muskulatur beeinflusst. Die muskulären Wirkungen bestehen u. a. in Relaxation der Bronchial- und Gefäßmuskulatur, des Uterus sowie Tremor der Skelettmuskulatur. Die Relaxation der glatten Muskulatur ist dosisabhängig und soll über Effekte auf das Adenylatcyclase-cAMP-System in der Weise ausgelöst werden, dass sich das Pharmakon über den ß-adrenergen Rezeptor an die Zellmembran bindet und hierdurch eine Umwandlung von ATP in cAMP und, vermittelt über Guanosin-bindendes Nukleotid-Protein, eine Aktivierung der Proteinkinase-A bewirkt. Dies wiederum hat eine Vermehrung des Anteils an gebundenem intrazellulärem Calcium durch erhöhte Proteinphosphorylierung zur Folge, sodass das intrazellulär ionisierte Calcium nur vermindert verfügbar ist. Dies inhibiert die Aktin-Myosin-Bindung, sodass ein verminderter Spannungszustand der kontraktilen Elemente zu einer muskulären Relaxation führt.
ß2-Agonisten wie Salbutamol haben außerdem einen antiallergischen Effekt über eine Hemmung der Freisetzung bronchokonstriktorischer Mediatoren aus Mastzellen wie Histamin, neutrophile chemotactive factor (NCF) und Prostaglandin D2 (PGD-2). Diese Effekte sind sowohl durch In-vitro-Studien mit humanen Mastzellen als auch durch In-vivo-Untersuchungen mit Mediatorbestimmungen in Antigen-Provokations-Tests nachgewiesen worden. Ebenso wie bei der ß-Adrenozeptor-Wirkung auf die Bronchialmuskulatur wird es bei der Regulierung der Mastzell-Funktion als wahrscheinlich angesehen, dass das cAMP-System als second messenger in Erscheinung tritt.
Als weitere Wirkung auf das Bronchialsystem konnte eine Steigerung der mukoziliären Clearance nachgewiesen werden, wobei Wirkungsmechanismus und klinische Relevanz noch nicht eindeutig geklärt sind.
Eine Stimulation von ß2-Rezeptoren der Gefäßwände durch Salbutamol führt zu einer Vasodilatation vor allem in der Peripherie und infolgedessen zur reflektorischen Steigerung der Herzfrequenz, das Herzschlagvolumen wird hingegen nur wenig beeinflusst. Die Chronotropie von Salbutamol ist erheblich geringer im Vergleich zu ß1-Rezeptor stimulierenden Substanzen wie etwa Isoprenalin. Verschiedene Untersuchungen haben nach Vernebler-Inhalations- sowie parenteraler Anwendung von Salbutamol eine Senkung des diastolischen Blutdrucks gezeigt, während hinsichtlich des systolischen Blutdrucks uneinheitlich Anstiege bzw. Senkungen beobachtet wurden.
Darüber hinaus sind weitgefächerte metabolische Wirkungen von Salbutamol durch eine Erregung von ß2-Rezeptoren nachgewiesen worden. Hierzu zählen Anstiege der Blutkonzentrationen von freien Fettsäuren, Glycerol, Insulin, Laktat und Glukose sowie ein Absinken der Kaliumionenkonzentration. Der hypokaliämische Effekt ist nicht direkt mit dem Anstieg des Insulinspiegels korreliert und soll Folge einer direkten ß2-Rezeptorstimulation sein, deren Wirkung über eine Membran gebundene Na+-K+-ATPase vermittelt werden soll.
Nach Inhalation von Salbutamol tritt die bronchodilatatorische Wirkung nach 5-15 Minuten ein, was auf eine lokale Wirkung hindeutet, während zum Zeitpunkt der maximalen Plasmakonzentration ein vergleichsweise geringer therapeutischer Effekt festzustellen ist. Eine maximale Verbesserung der Lungenfunktion wurde in verschiedenen Untersuchungen 1-2 Stunden nach der Inhalation gemessen, die Wirkungsdauer wurde mit 3-4 Stunden festgestellt.
Therapeutische Äquivalenzprü fung
Eine im Jahr 1993 durchgeführte Untersuchung zur therapeutischen Äquivalenz im cross-over an 24 Patienten mit reversiblem Asthma bronchiale ergab nach Inhalation von 16 kumulativen Dosen, die je 0,1 mg Salbutamol entsprechen, im Vergleich zum Referenzpräparat:
|
Lungenfunktionsparameter (Einheit) |
Testpräparat |
Referenzpräparat |
|
FEV1 [I ]* |
2,60 |
2,64 |
|
45 Minuten vor Dosierungsbeginn |
(± 0,65) |
(± 0,71) |
|
FEVi-Anstieg [I ]* |
1, 90 |
0,99 |
|
nach Inhalation von 16 kumulativen Dosen (entsprechend 1,6 mg Salbutamol) |
(± 0,51) |
(± 0,51) |
* Angabe der Werte als Mittelwert und Streubreite
Minierer FüV, - Anstieg gegenüber Ausgangswert
1.2
0,7
OS’
S = Testpröparai
V - Vergleichspräparat
5.3
0,0
Kumulative Inhalationen in Abstand von 5» Minuten
Klinische Prüfungen bei Kindern unter 4 Jahren
Klinische Studien bei Kindern (SB020001, SB030001, SB030002) zeigen, dass die Anwendung des Dosier-Aerosols in der empfohlenen Dosierung bei Patienten unter 4 Jahren mit Bronchospasmus verbunden mit reversibler obstruktiver Atemwegserkrankung ein Verträglichkeitsprofil aufweist, das mit der Anwendung bei Kindern über 4 Jahre, bei Jugendlichen und bei Erwachsenen vergleichbar ist.
Bei Neugeborenen und Kleinkindern bis zu einem Alter von 20 Monaten kann die Wirkung von Salbutamol verringert sein oder fehlen.
Untersuchungen hinsichtlich der Möglichkeit eines Wirksamkeitsverlustes (Tachyphylaxie) bei Langzeitanwendung von Salbutamol kamen zu keinem übereinstimmenden Ergebnis.
Im Falle eines Wirksamkeitsverlustes bei längerfristiger Anwendung kann die kombinierte Anwendung mit Glukokortikoiden die verminderte Ansprechbarkeit der ß2-Rezeptoren wieder erhöhen.
5.2 Pharmakokinetische Eigenschaften
Resorption und Metabolisierung von Salbutamol verlaufen in Lunge und Gastrointestinaltrakt unterschiedlich.
Nach der Inhalation gelangen etwa 10-20 % des Wirkstoffes in die tieferen Bronchialwege, während sich der Rest im Mund und oberen Abschnitt des Atemtraktes absetzt und sukzessive verschluckt wird. In verschiedenen Untersuchungen wurde nach inhalativer Anwendung von Salbutamol ein im Vergleich zur peroralen Applikation ähnlicher, jedoch zeitlich verzögerter Plasmaspiegelverlauf sowie ein ähnliches Konzentrationsverhältnis von Salbutamol zu seinen Metaboliten gefunden. Der maximale Plasmaspiegel wird demzufolge nach 3-5 Stunden erreicht und das Verhältnis von freiem
Wirkstoff zu Metaboliten beträgt etwa 1 : 4, womit es als sehr wahrscheinlich anzusehen ist, dass die gemessenen Plasmakonzentrationen dem nach Verschlucken resorbierten Wirkstoffanteil entsprechen. Nach Inhalation von Salbutamol mit Hilfe eines Verneblers in drei Dosisstufen von 1,5 mg, 3 mg und 7,5 mg wurden mittlere maximale Plasmaspiegel von jeweils 0,2 ng/ml, 1,1 ng/ml und 2,5 ng/ml gemessen.
Der Wirkungseintritt sowie der maximale therapeutische Effekt erscheinen nach inhalativer Anwendung im Vergleich zur peroralen Gabe erheblich rascher (Wirkungseintritt 5-15 Minuten nach der Inhalation), dabei zeigt der Plasmaspiegel keine Korrelation mit der pharmakodynamischen Zeitwirkungskurve.
Salbutamol wird nach oraler Verabreichung gut (zu ca. 85 %) resorbiert, zwischen 58 und 78 % der Substanz werden innerhalb von 24 Stunden und 65-84 % innerhalb von 72 Stunden mit dem Urin ausgeschieden. Die Substanz wird zu einem erheblichen Teil präsystemisch in der Darmwand sowie der Leber metabolisiert. Im Gegensatz z. B. zu Isoprenalin ist Salbutamol kein Substrat für die Catechol-O-Methyltransferase und Monoamin-Oxidase. Die Metabolisierung erfolgt hingegen im Wesentlichen über eine Sulfat-Konjugation, als Hauptmetabolit wurde ein 4'-O-Sulfatester identifiziert, der wahrscheinlich in der Darmmukosa gebildet wird und pharmakologisch inaktiv ist.
Nach Verabreichung von Salbutamol-Tabletten bei Erwachsenen konnte Salbutamol bereits nach 30 Minuten im Serum nachgewiesen werden, die maximale Plasmakonzentration wurde nach 2-3 Stunden festgestellt. Dabei betrug die Ratio von freiem Salbutamol zu Metabolit 1 : 5. Es wurde über maximale Plasmakonzentrationen nach einer oralen Einzeldosis von 4 mg Salbutamol von 10-16,9 ng/ml berichtet, die Plasmahalbwertszeit wurde zwischen 2,7 und 5 Stunden bestimmt.
Die Proteinbindung beträgt etwa 10 %, das spezifische scheinbare Verteilungsvolumen 3,4 + 0,6 l/kg. In einer späteren Studie wurde ein mittleres scheinbares Verteilungsvolumen von 156 l ermittelt. Dieses hohe Verteilungsvolumen ist durch eine extensive Verteilung in die Gewebe zu erklären, die durch tierexperimentelle Untersuchungen erhärtet wurde.
Die totale Plasmaclearance nach i.v. Infusion wurde mit 6,6-7,7 ml/min/kg bestimmt. Die Ausscheidung erfolgt zum größten Teil über die Nieren, wobei das Verhältnis von freiem Salbutamol zu Metaboliten von der Art der Anwendung abhängig ist. Nach oraler Gabe finden sich dabei vorwiegend die metabolisierte (55 % als Sulfatester), nach i.v. Gabe die nicht-metabolisierte Form. Nach einer Pulver-Inhalation im empfohlenen Dosisbereich folgt das Exkretionsmuster dem nach oraler Gabe, während nach Inhalation höherer Dosen die Ausscheidung eines relativ höheren Anteils der unveränderten Substanz eine größere pulmonale Resorption widerspiegelt.
Die Plazentagängigkeit von Salbutamol wurde in vitro ebenso wie in vivo nachgewiesen.
5.3 Präklinische Daten zur Sicherheit
Untersuchungen zur Mutagenität ergaben keine Hinweise auf ein genotoxisches Potential von Salbutamol. Unter Langzeitgabe von sehr hohen Dosen von Salbutamol an Ratten kommt es wie auch bei anderen Beta-Sympathomimetika zur Ausbildung von gutartigen Leiomyomen des Mesovariums. Nach vorherrschender Meinung ist eine Übertragbarkeit auf den Menschen jedoch nicht gegeben.
Reproduktionstoxikologische Studien an drei Tierspezies (Ratte, Maus, Kaninchen) haben keine Hinweise auf ein teratogenes Potential von Salbutamol ergeben. Embryo- bzw. fetotoxische Effekte (verringertes Geburtsgewicht, gesteigerte Mortalitätsrate) wurden bei der Ratte nach oraler Gabe von 50 mg/kg/Tag beobachtet. Fertilitätsstörungen bei männlichen und weiblichen Ratten traten bis zu einer Dosis von 50 mg/kg/Tag nicht auf.
Treibmittel Norfluran
In tierexperimentellen Studien zeigte Norfluran nur bei sehr hohen Konzentrationen signifikante pharmakologische Wirkungen, wobei Bewusstlosigkeit und eine relativ schwache Herzsensibilisierung gefunden wurden. Die Stärke der Herzsensibilisierung war geringer als durch Treibmittel 11 (Trichlorfluormethan).
In toxikologischen Studien wurde gezeigt, dass bei wiederholten hohen Dosen von Norfluran der Sicherheitsabstand für den Menschen basierend auf der systemischen Gabe in der Größenordnung von 2200, 1314 und 381 für Maus, Ratte und Hund liegen würde.
In-vitro- und In-vivo-Studien einschließlich Langzeitinhalationsstudien an Nagern haben keine Hinweise auf eine mutagene, klastogene und kanzerogene Wirkung des Norflurans ergeben.
6. PHARMAZEUTISCHE ANGABEN
6.1 Liste der sonstigen Bestandteile
Ethanol 99,4 % V/V (Alkohol), Ölsäure, Norfluran (Treibmittel)
6.2 Inkompatibilitäten
Nicht zutreffend.
6.3 Dauer der Haltbarkeit
2 Jahre.
Dieses Arzneimittel soll nach Ablauf des Verfallsdatums nicht mehr angewendet werden.
6.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung
Nicht über 25 °C lagern.
Behälter steht unter Druck!
Vor Hitze, direkter Sonnenbestrahlung und Frost schützen!
Nicht gegen Flammen oder auf glühende Gegenstände sprühen!
Nicht gewaltsam öffnen oder verbrennen!
6.5 Art und Inhalt des Behältnisses
Packung mit 1 Aluminium-Druckbehältnis mit 6,7 g Druckgasinhalation, Suspension, im Autohaler (entsprechend mindestens 200 Einzeldosen)
Packung mit 2 Aluminium-Druckbehältnissen mit je 6,7 g Druckgasinhalation, Suspension im Autohaler (entsprechend mindestens 2 x 200 Einzeldosen)
6.6 Besondere Vorsichtsmaßnahmen für die Beseitigung und sonstige Hinweise zur Handhabung
Zur Handhabung siehe Abschnitt 4.2.
Nicht verwendetes Arzneimittel oder Abfallmaterial ist entsprechend den örtlichen Anforderungen zu beseitigen.
7. INHABER DER ZULASSUNG
TEVA GmbH Graf-Arco-Str. 3 89079 Ulm
8. ZULASSUNGSNUMMER
41205.00.00
9. DATUM DER ERTEILUNG DER ZULASSUNG / VERLÄNGERUNG DER ZULASSUNG
Datum der Erteilung der Zulassung: 11. Juni 1998
Datum der letzten Verlängerung der Zulassung: 26. November 2004
10. STAND DER INFORMATION
November 2013
11. VERKAUFSABGRENZUNG
Verschreibungspflichtig