Togal Classic Duo
Togal® Classic Duo
Fachinformation
TOGAL-WERK AG ♦ MÜNCHEN
4.1 Dosierung und Art der Anwendung
|
Alter (bzw. Körpergewicht) |
Einzeldosis |
Tages gesamtdosis |
|
Erwachsene und Jugendliche ab 12 Jahren |
1 Tablette (entsprechend 250 mg Acetylsalicylsäure und 200 mg Paracetamol) |
bis 4 Tabletten (entsprechend 1000 mg Acetylsalicylsäure und 800 mg Paracetamol) |
1. Bezeichnung des Arzneimittels
Togal Classic Duo
Wirkstoffe (pro Tablette): Acetylsalicylsäure 250 mg, Paracetamol 200 mg
2. Qualitative und quantitative Zusammen
setzung
Wirkstoffe: Acetylsalicylsäure, Paracetamol 1 Tablette enthält:
250 mg Acetylsalicylsäure (ASS),
200 mg Paracetamol
Vollständige Auflistung der sonstigen Bestandteile siehe unter Abschnitt 6.1.
3. Darreichungsform
Tabletten
4. Klinische Angaben 4.1. Anwendungsgebiete
Akute leichte bis mäßig starke Schmerzen wie Kopfschmerzen, Zahnschmerzen, Regelschmerzen. Hinweis:
Schmerzmittel sollen längere Zeit oder in höheren Dosen nicht ohne Befragen des Arztes angewendet werden.
Bitte beachten Sie die Angaben für Kinder (siehe Pkt. 4.4).
Die Einzeldosis kann, falls erforderlich, in Abständen von 4 - 8 Stunden bis zu 4-mal täglich eingenommen werden.
Die Tabletten mit reichlich Flüssigkeit (z. B. einem Glas Wasser) einnehmen.
Nicht auf nüchternen Magen einnehmen.
Togal Classic Duo soll längere Zeit oder in höheren Dosen nicht ohne Befragen des Arztes angewendet werden.
4.3. Gegenanzeigen Togal Classic Duo ist kontraindiziert:
■ bei Überempfindlichkeit gegenüber Acetylsalicylsäure, Paracetamol oder einen der sonstigen Bestandteile von Togal Classic Duo
■ wenn in der Vergangenheit gegen Salicylate oder andere nicht-steroidale Entzündungshemmer mit Asthmaanfällen oder in anderer Weise allergisch reagiert wurde.
■ bei gastrointestinalen Blutungen oder Perforation (Magen- oder Darmdurchbruch) in der Vorgeschichte, die durch eine vorherige Therapie mit NSAR bedingt waren
■ bei aktiven oder in der Vorgeschichte bekannten Magen- und Zwölffingerdarmgeschwüren / Hämorrhagie mit mindestens zwei unverkennbaren Episoden von erwiesener Ulzeration oder Blutungen.
■ bei krankhaft erhöhter Blutungsneigung
■ bei Leber- und Nierenversagen
■ bei schwerer Herzinsuffizienz
■ in Kombination mit Methotrexat 15 mg oder mehr pro Woche
■ bei schwerer hepatozellulärer Insuffizienz
■ bei Kindern unter 12 Jahren
■ während des dritten Trimesters der Schwangerschaft.
4.4 Warnhinweise und Vorsichtsmaßnahmen für die Anwendung
Eine besonders sorgfältige ärztliche Überwachung ist erforderlich bei Patienten mit
■ Überempfindlichkeit gegen andere Entzündungshemmer / Antirheumatika oder andere allergene Stoffe
■ Allergien (z. B. mit Hautreaktionen, Juckreiz, Nesselfieber) oder Asthma, Heuschnupfen, Nasenschleimhautschwellungen (Nasenpolypen), chronischen Atemwegserkrankungen
■ eingeschränkter Leber- und Nierenfunktion
■ Magen-Darm-Störungen oder
chronisch-entzündlichen Darmerkrankungen (Colitis ulcerosa, Morbus Crohn); diese Erkrankungen können sich verschlimmern
■ Gilbert-Syndrom (Meulengracht-Krankheit) und
■ bei chronischem Alkoholmissbrauch.
Bluthochdruck und/oder Herzinsuffizienz in der Anamnese: vor Behandlungsbeginn ist der Arzt bzw. der Apotheker zu befragen. Im Zusammenhang mit einer NSAR-Behandlung wurde über Flüssigkeitseinlagerung / Ödeme berichtet.
Vor Operationen (auch bei kleineren Eingriffen, wie z. B. Zahnextraktionen)
Es kann zu verstärkter Blutungsneigung kommen.
Gastrointestinale Wirkungen
Die gleichzeitige Gabe von Acetylsalicylsäure und anderen NSAR einschließlich COX-2-selektiven Inhibitoren sollte vermieden werden.
Während der Behandlung mit allen NSAR sind schwerwiegende gastrointestinale Blutungen, Geschwüre oder Perforationen, auch mit letalem Ausgang, zu jedem Zeitpunkt der Therapie mit oder ohne Warnsignale oder früheren schwerwiegenden gastrointestinalen Nebenwirkungen, berichtet worden.
Bei älteren Menschen treten Nebenwirkungen vermehrt auf, insbesondere Blutungen und Perforationen im Gastrointestinaltrakt, die lebensbedrohlich sein können. Patienten mit einer früheren gastrointestinalen Erkrankung, speziell ältere Menschen, sollen jedes unübliche Symptom im Magen-Darm-Bereich (besonders gastrointestinale Blutungen) berichten, vor allem zu Beginn einer Therapie.
Vorsicht ist bei Patienten geboten, die gleichzeitig mit Arzneimitteln behandelt werden, die das Risiko einer Gastrotoxizität oder Blutung erhöhen können, wie z. B. orale Corticoide, Antikoagulantien, wie z. B. Warfarin, selektive Serotonin-Aufnahme-Inhibitoren oder Thrombozytenaggregationshemmer, wie z. B. Acetylsalicylsäure in geringen Dosen zur Behandlung kardiovaskulärer Erkrankungen.
Beim Auftreten von gastrointestinalen Blutungen und Geschwüren soll die Behandlung mit Acetylsalicylsäure abgebrochen werden.
Das Risiko einer gastrointestinalen Blutung, Ulzeration und Perforation erhöht sich mit ansteigender Dosis der NSAR, für Patienten mit Magen- und/oder Zwölffingerdarmgeschwüren in der Vorgeschichte, insbesondere wenn diese in Verbindung mit Haemorrhagie und Perforation auftreten (siehe Kapitel 4.3 Gegenanzeigen) und für ältere Patienten. Diese Patientengruppen sollten einleitend mit der niedrigsten möglichen Dosis behandelt werden.
Eine Behandlung mit NSAR in Kombination mit Arzneimitteln, die den Gastrointestinaltrakt schützen (z. B. Protonen-Pumpen-Hemmer) sollte in diesen Fällen in Erwägung gezogen werden. Ebenso gilt dies für Patienten, die darauf angewiesen sind, gleichzeitig Acetylsalicylsäure (in niedrigen Dosen, z. B. zur Herzinfarkt-Prophylaxe) oder andere Arzneimittel einzunehmen, die das Risiko gastrointestinaler Nebenwirkungen erhöhen (siehe Kapitel 4.5 Wechselwirkungen).
Hautreaktionen
Sehr selten wurde im Zusammenhang mit einer Behandlung mit NSAR von starken Hautreaktionen, z. T. mit tödlichem Ausgang, einschließlich exfoliativer Dermatitis, Stevens-Johnson-Syndrom und toxischer epidermaler Nekrolyse (Lyell-Syndrom) berichtet (siehe Kapitel 4.8 Nebenwirkungen)
Es scheint zu Beginn der Behandlung ein höheres Risiko für das Auftreten dieser Reaktionen zu bestehen. Das Auftreten der Hautreaktion fällt in der Mehrzahl der Fälle in den ersten Monat der Behandlung. Acetylsalicylsäure sollte bei den ersten Anzeichen einer Überempfindlichkeit (z. B. Hautausschläge, Schleimhautläsionen) abgesetzt werden.
Sonstige Hinweise
Bei dauerhafter Einnahme von Schmerzmitteln können Kopfschmerzen auftreten, die zu erneuter Einnahme führen und damit wiederum eine Fortdauer der Kopfschmerzen bewirken können. Bei abruptem Absetzen nach längerem hochdosiertem, nicht bestimmungsgemäßem Gebrauch von Analgetika können Kopfschmerzen sowie Müdigkeit, Muskelschmerzen, Nervosität und vegetative Symptome auftreten. Die Absetzsymptomatik klingt innerhalb weniger Tage ab. Bis dahin soll die Wiedereinnahme von Schmerzmitteln unterbleiben und die erneute Einnahme nicht ohne ärztlichen Rat erfolgen.
Die Langzeitanwendung der fixen Kombination kann bei gleichzeitiger Exposition mit nephrotoxischen Substanzen, vorbestehender Nierenschädigung, genetischer Disposition oder Syndromen, die zu einer Nierenschädigung disponieren, zu einem erhöhten Erkrankungsrisiko für eine Analgetika-Nephropathie führen.
Acetylsalicylsäure vermindert in niedriger Dosierung die Harnsäureausscheidung. Bei Patienten, die bereits zu geringer Harnausscheidung neigen, kann dies unter Umständen einen Gichtanfall auslösen.
Nebenwirkungen können durch die Anwendung der geringsten effektiven Dosis über die kürzest mögliche Zeit reduziert werden.
Bei Anwendung von NSAR können durch gleichzeitigen Genuss von Alkohol wirkstoffbedingt Nebenwirkungen, insbesondere solche,
TOGAL-WERK AG ♦ MÜNCHEN_Togal» Classic Duo
Bei den Häufigkeitsangaben zu Nebenwirkungen werden folgende Kategorien zugrunde gelegt:
|
Sehr häufig |
> 1/10 |
|
Häufig |
> 1/100 bis < 1/10 |
|
Gelegentlich |
> 1/1.000 bis < 1/100 |
|
Selten |
> 1/10.000 bis < 1/1.000 |
|
Sehr selten |
< 1/10.000 |
|
Nicht bekannt |
Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar. |
die den Gastrointestinaltrakt oder das zentrale Nervensystem betreffen, verstärkt werden.
Eine Überschreitung der empfohlenen Paracetamol-Dosis kann zu sehr schweren Leberschäden führen. Die Gabe eines Antidots sollte so rasch wie möglich erfolgen (siehe Abschnitt 4.9).
Um das Risiko einer Überdosierung zu vermeiden, sollte sichergestellt werden, dass gleichzeitig eingenommene Medikamente kein Paracetamol enthalten.
Bei hohem Fieber, Anzeichen einer Sekundärinfektion oder Anhalten der Symptome über mehr als drei Tage, muss der Arzt konsultiert werden.
Kinder und Jugendliche
Über die Anwendung der fixen Kombination bei Kindern und Jugendlichen liegen keine ausreichenden Erkenntnisse vor. Darüber hinaus soll Acetylsalicylsäure bei Kindern und Jugendlichen ab 12 Jahren mit fieberhaften Erkrankungen nur auf ärztliche Anweisung und nur dann angewendet werden, wenn andere Maßnahmen nicht wirken. Sollte es bei diesen Erkrankungen zu lang anhaltendem Erbrechen kommen, so kann dies ein Zeichen des sehr seltenen, aber lebensbedrohlichen Reye-Syndroms sein.
4.5 Wechselwirkungen mit anderen Mitteln und sonstige Wechselwirkungen
Acetylsalicylsäure:
Verstärkung der Wirkung bis hin zu erhöhtem Nebenwirkungsrisiko:
■ Antikoagulantien:
Es gibt begrenzte Hinweise auf eine Verstärkung der blutgerinnungshemmenden Wirkung oraler Antikoagulantien (wie z. B. Warfarin) und damit ein erhöhtes Blutungsrisiko (Kontrolle der Blutgerinnung).
■ Thrombozytenaggregationshemmer oder nicht-steroidale Antiphlogistika / Analgetika, selektive Serotonin-Wiederaufnahme-Hemmer und orale Glucocorticoide: Erhöhung des Risikos für gastrointestinale Ulcera und Blutungen.
■ Digoxin
■ Antidiabetika: Der Blutzuckerspiegel kann sinken.
■ Methotrexat
■ Valproinsäure.
Abschwächung der Wirkung:
■ Diuretika (in Dosierungen ab 3 g Acetylsalicylsäure und mehr)
■ ACE-Hemmer (in Dosierungen ab 3 g Acetylsalicylsäure und mehr)
■ Urikosurika (z. B. Probenecid, Benzbromaron) Paracetamol:
■ Die Einnahme von Probenecid hemmt die Bindung von Paracetamol an Glucuronsäure und führt dadurch zu einer Reduzierung der Paracetamol-Clearance um ungefähr Faktor 2. Bei gleichzeitiger Einnahme von Probenecid sollte die Paracetamoldosis verringert werden.
■ Besondere Vorsicht ist bei der gleichzeitigen Einnahme von Arzneimitteln, die zu einer Enzyminduktion führen, sowie bei potentiell hepatotoxischen Substanzen geboten (siehe Abschnitt 4.9)
■ Bei gleichzeitiger Anwendung von Paracetamol und AZT (Zidovudin) wird die Neigung zur Ausbildung einer Neutropenie verstärkt. Dieses Arzneimittel soll daher nur nach ärztlichem Anraten gleichzeitig mit AZT angewendet werden.
■ Die gleichzeitige Einnahme von Mitteln, die zu einer Beschleunigung der Magenentleerung führen, wie z. B. Metoclopramid, bewirkt eine Beschleunigung der Aufnahme und des Wirkungseintritts von Paracetamol.
■ Die gleichzeitige Einnahme von Mitteln, die zu einer Verlangsamung der Magenentleerung führen.
■ Colestyramin verringert die Aufnahme von Paracetamol.
Auswirkungen auf die Laborwerte
Die Einnahme von Paracetamol kann die Harnsäurebestimmung mittels Phosphorwolframsäure sowie die Blutzuckerbestimmung mittels Glucose-Oxydase-Peroxydase beeinflussen.
4.6 Fertilität, Schwangerschaft und Stillzeit Schwangerschaft
Es liegen keine Erfahrungen zur Sicherheit des Kombinationspräparates in der Schwangerschaft vor, sondern nur Daten über die Anwendung der einzelnen Wirkstoffe.
Acetylsalicylsäure:
Eine Hemmung der Prostaglandinsynthese kann die Schwangerschaft und / oder embryonale / fetale Entwicklung negativ beeinflussen.
Daten aus epidemiologischen Studien weisen auf ein erhöhtes Risiko für Fehlgeburten sowie kardiale Missbildungen und Gastroschisis nach der Anwendung eines Prostaglandinsynthesehemmers in der Frühschwangerschaft hin. Es wird angenommen, dass das Risiko mit der Dosis und der Dauer der Therapie steigt.
Bei Tieren wurde nachgewiesen, dass die Gabe eines Prostaglandinsynthesehemmers zu erhöhtem prä- und post-implantärem Verlust und zu embryo-fetaler Letalität führt. Ferner wurden erhöhte Inzidenzen verschiedener Missbildungen, einschließlich kardiovaskulärer Missbildungen, bei Tieren berichtet, die während der Phase der Organogenese einen Prostaglandinsynthesehemmer erhielten.
Während des ersten und zweiten Schwangerschaftstrimesters sollte Acetylsalicylsäure nur gegeben werden, wenn dies unbedingt notwendig ist. Falls Acetylsalicylsäure von einer Frau angewendet wird, die versucht schwanger zu werden, oder wenn Acetylsalicylsäure während des ersten und zweiten Trimesters der Schwangerschaft angewendet wird, sollte die Dosis so niedrig und die Dauer der Anwendung so kurz wie möglich gehalten werden.
Während des dritten Schwangerschaftstrimesters können alle Prostaglandinsynthesehemmer:
■ den Fetus folgenden Risiken aussetzen:
- kardiopulmonale Toxizität (mit vorzeitigem Verschluss des Ductus arteriosus und pulmonaler Hypertonie)
- Nierenfunktionsstörung, die zu Nierenversagen mit Oligohydramniose fortschreiten kann;
■ die Mutter und das Kind, am Ende der Schwangerschaft, folgenden Risiken aussetzen:
- mögliche Verlängerung der Blutungszeit, ein thrombozytenaggregationshemmender
Effekt, der selbst bei sehr geringen Dosen auftreten kann;
- Hemmung von Uteruskontraktionen, mit der Folge eines verspäteten oder verlängerten Geburtsvorganges.
Daher ist Acetylsalicylsäure während des dritten Schwangerschaftstrimesters kontraindiziert (siehe Abschnitt 4.3)
Paracetamol:
Epidemiologische Daten zur oralen Anwendung therapeutischer Dosen von Paracetamol haben bisher keinen Hinweis auf mögliche unerwünschte Wirkungen auf die Schwangerschaft oder die Gesundheit des Fetus / Neugeborenen ergeben. Prospektive Daten zur Überdosierung während der Schwangerschaft zeigten keinen Anstieg des Risikos von Fehlbildungen. Reproduktionsstudien zur oralen Anwendung ergaben keinen Hinweis auf das Auftreten von Fehlbildungen oder Fetotoxizität.
Stillzeit
Acetylsalicylsäure und Paracetamol, die Wirkstoffe von Togal Classic Duo, gehen in die Muttermilch über. Nachteilige Folgen für den Säugling durch Paracetamol und Acetylsalicylsäure sind bisher nicht bekannt geworden. Bei kurzfristiger Anwendung der empfohlenen Dosis wird eine Unterbrechung des Stillens in der Regel nicht erforderlich sein. Bei längerer Anwendung bzw. Einnahme höherer Dosen sollte dennoch abgestillt werden.
Fertilität
Es existiert eine gewisse Evidenz dafür, dass Arzneistoffe, die die Cyclooxygenase / Prostaglandinsynthese hemmen, die weibliche Fertilität über eine Wirkung auf die Ovulation beeinträchtigen können. Dies ist nach Absetzen der Behandlung reversibel.
4.7 Auswirkungen auf die Verkehrstüchtigkeit und das Bedienen von Maschinen
Es sind keine besonderen Vorsichtsmaßnahmen erforderlich.
4.8. Nebenwirkungen
Die Aufzählung der folgenden unerwünschten Wirkungen umfasst alle bekannt gewordenen Nebenwirkungen unter der Behandlung mit Acetylsalicylsäure sowie Paracetamol auch solche unter hochdosierter Langzeittherapie.
Erkrankungen des Blutes und des Lymphsystems
Blutungen, wie z. B. Nasenbluten, Zahnfleischbluten oder Hautblutungen, mit einer möglichen Verlängerung der Blutungszeit. Diese Wirkung kann über 4 - 8 Tage nach der Einnahme anhalten.
TOGAL-WERK AG ♦ MÜNCHEN
Selten bis sehr selten
sind auch schwerwiegende Blutungen, wie z. B. intracerebrale Blutungen, besonders bei Patienten mit nicht-eingestelltem Bluthochdruck und / oder gleichzeitiger Behandlung mit Antikoagulantien berichtet worden, die in Einzelfällen lebensbedrohlich sein können.
Sehr selten:
Veränderungen im Blutbild, wie Thrombozytopenie, Agranulozytose.
Erkrankungen des Immunsystems
Gelegentlich:
Überempfindlichkeitsreaktionen, wie Hautreaktionen.
Selten:
Überempfindlichkeitsreaktionen eventuell mit Blutdruckabfall, Anfällen von Atemnot, anaphylaktischem Schock, Quincke-Ödeme vor allem bei Asthmatikern.
Erkrankungen des Nervensystems
Kopfschmerzen, Schwindel, gestörtes Hörvermögen, Tinnitus und mentale Verwirrung können Anzeichen einer Überdosierung sein.
Erkrankungen des Gastrointestinaltrakts
Häufig:
Magen-Darm-Beschwerden, wie Sodbrennen, Übelkeit, Erbrechen, Bauchschmerzen. Gelegentlich:
Durchfall, Blähungen, Verstopfung.
Selten:
Magen-Darm-Blutungen, die sehr selten zu einer Eisenmangelanämie führen können. Magen-Darm-Geschwüre, unter Umständen mit Blutung und Durchbruch, insbesondere bei älteren Patienten. Sollten stärkere Schmerzen im Oberbauch, Bluterbrechen, Blut im Stuhl oder eine Schwarzfärbung des Stuhls auftreten, so wird der Patient aufgefordert, das Arzneimittel abzusetzen und sofort den Arzt zu informieren.
Über eine Verschlimmerung einer Colitis oder eines Morbus Crohn wurde berichtet. Weniger häufig wurde das Auftreten einer Gastritis beobachtet.
Leber- und Gallenerkrankungen
Selten:
Erhöhungen der Leberwerte wurden beobachtet.
Erkrankungen der Haut und des Unterhautzellgewebes
Sehr selten:
Schwere Hautreaktionen, wie Hautausschlag mit Rötung und Blasenbildung (z. B. Erythema exsudativum multiforme,
Stevens-Johnson-Syndrom, toxische epidermale Nekrolyse).
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer
Nebenwirkung über das
Bundesinstitut für Arzneimittel und
Medizinprodukte
Abt. Pharmakovigilanz
Kurt-Georg-Kiesinger-Allee 3 D-53175 Bonn
anzuzeigen.
4.9 Überdosierung
Ein Intoxikationsrisiko besteht insbesondere bei älteren Personen, kleinen Kindern, Personen mit Lebererkrankungen, chronischem Alkoholmissbrauch, chronischer Fehlernährung und gleichzeitiger Einnahme von Arzneimitteln, die zu einer Enzyminduktion führen (therapeutische Überdosierung) oder versehentliche Intoxikationen. Überdosierungen können zum Tode führen.
Symptomatologie:
Die Symptome einer Überdosierung von Togal Classic Duo setzen sich aus den Symptomen der Intoxikationen mit den Einzelstoffen zusammen.
Acetylsalicylsäure:
Mäßige Intoxikation:
Tinnitus, Hörstörungen, Kopfschmerzen und Vertigo werden in allen Fällen von Überdosierung festgestellt und können durch Reduzierung der Dosierung abgestellt werden.
Schwere Intoxikation:
Fieber, Hyperventilation, Ketose, respiratorische Alkalose, metabolische Azidose, Koma, kardiovaskulärer Schock, Atemversagen, schwere Hypoglykämie.
Paracetamol;
In der Regel treten Symptome innerhalb von 24 Stunden auf: Übelkeit, Erbrechen, Anorexie, Blässe und Unterleibsschmerzen. Danach kann es zu einer Besserung des subjektiven Befindens kommen, es bleiben jedoch leichte Leibschmerzen als Hinweis auf eine Leberschädigung.
Eine Überdosierung mit ca. 6 g oder mehr Paracetamol als Einzeldosis bei Erwachsenen oder mit 140 mg / kg Körpergewicht als Einzeldosis bei Kindern führt zu Leberzellnekrosen, die zu einer totalen irreversiblen Nekrose und später zu hepatozellulärer Insuffizienz, metabolischer Azidose und Enzephalopathie führen können. Diese wiederum können zu Koma, auch mit tödlichem Ausgang, führen. Gleichzeitig wurden erhöhte Konzentrationen der Lebertransaminasen (AST, ALT), Lactatdehydro-genase und des Bilirubins in Kombination mit einer erhöhten Prothrombinzeit beobachtet, die 12 - 48 Stunden nach der Anwendung auftreten können. Klinische Symptome der Leberschäden werden in der Regel nach 2 Tagen sichtbar und erreichen nach 4 - 6 Tagen ein Maximum.
Auch wenn keine schweren Leberschäden vorliegen, kann es zu akutem Nierenversagen mit akuter Tubulusnekrose kommen. Zu anderen, leberunabhängigen Symptomen, die nach einer Überdosierung mit Paracetamol beobachtet wurden, zählen Myokardanomalien und Pankreatitis.
Therapiemaßnahmen bei Überdosierung:
Die Notfallbehandlung hat entsprechend der derzeitigen wissenschaftlichen Empfehlungen zu erfolgen.
Bereits bei Verdacht auf Intoxikation mit Paracetamol ist in den ersten 10 Stunden die intravenöse Gabe von SH-Gruppen-Donatoren, wie z. B. N-Acetylcystein, sinnvoll.
N-Acetylcystein kann aber auch nach 10 bis zu 48 Stunden noch einen gewissen Schutz bieten. In diesem Fall erfolgt eine längerfristige Einnahme. Durch Dialyse kann die Plasmakonzentration von Paracetamol abgesenkt werden. Bestimmungen der Plasmakonzentration von Paracetamol sind empfehlenswert.
5. Pharmakologische Eigenschaften
5.1 Pharmakodynamische Eigenschaften Pharmakotherapeutische Gruppe:
Nervensystem, andere Analgetika und Anti-pyretika
ATC-Code: N02BA51
Acetylsalicylsäure gehört zur Gruppe der säurebildenden nicht-steroidalen Antiphlogistika mit analgetischen, antipyretischen und antiphlogistischen Eigenschaften. Ihr Wirkungsmechanismus beruht auf der irreversiblen Hemmung von Cyclo-Oxygenase-Enzymen, die an der Prostaglandinsynthese beteiligt sind. Acetylsalicylsäure hemmt außerdem die Thrombozytenaggregation, da sie die Synthese von Thromboxan A2 in den Thrombozyten blockiert.
Der analgetische und antipyretische Wirkungsmechanismus von Paracetamol ist nicht eindeutig geklärt. Eine zentrale und periphere Wirkung ist wahrscheinlich. Nachgewiesen ist eine ausgeprägte Hemmung der cerebralen Prostaglandinsynthese, während die periphere Prostaglandinsynthese nur schwach gehemmt wird. Ferner hemmt Paracetamol den Effekt endogener Pyrogene auf das hypothalamische Temperaturregulationszentrum. Acetylsalicylsäure und Paracetamol besitzen verschiedene sich ergänzende Wirkungsmechanismen und eine in etwa gleiche Wirkdauer. In verschiedenen Tierversuchen ist eine additive Wirkung für Analgesie und bei Hyperthermie belegt. In einer humanpharmakologischen Untersuchung konnte experimentell eine additive analgetische Wirkung bestimmt werden.
5.2 Pharmakokinetische Eigenschaften
Nach oraler Verabreichung wird Acetylsalicylsäure schnell und vollständig aus dem Gastrointestinaltrakt resorbiert. Während und nach der Resorption wird Acetylsalicylsäure in ihren aktiven Hauptmetaboliten Salicylsäure umgewandelt. Die maximalen Plasmaspiegel von Acetylsalicylsäure und Salicylsäure werden nach 10 - 20 Minuten bzw. 0,3 - 2 Stunden erreicht. Sowohl Acetylsalicylsäure als auch Salicylsäure werden weitgehend an Plasmaproteine gebunden und schnell in alle Teile des Körpers verteilt. Salicylsäure tritt in die Muttermilch über und ist plazentagängig.
Salicylsäure wird vor allem durch Metabolisierung in der Leber eliminiert; die Metaboliten sind Salicylursäure, Salicylphenolglucuronid, Salicyl-acylglucuronid, Gentisinsäure und Gentisursäure. Die Eliminationskinetik von Salicylsäure ist dosisabhängig, da der Metabolismus durch die Kapazität der Leberenzyme begrenzt wird. Die Eliminationshalbwertzeit variiert daher und liegt nach niedrigen Dosen zwischen 2 - 3 Stunden, während sie nach hohen Dosen bis zu 15 Stunden beträgt. Salicylsäure und ihre Metaboliten werden vor allem über die Nieren ausgeschieden.
Nach oraler Gabe wird Paracetamol rasch und vollständig resorbiert. Maximale Plasmakonzen-
TOGAL-WERK AG ♦ MÜNCHEN
|
Testpräparat |
Referenz präparat | |
|
maximale Plasmakonzentration (cmax): |
6,37 ± 1,21 (ASS) 31,9 ± 5,3 (SA) pg/ml |
5,84 ± 2,16 30,1 ± 5,7 pg/ml |
|
Zeitpunkt der maximalen Plasmakonzen tration (W): |
0,57 ± 0,22 (ASS) 1,58 ± 0,32 (SA) h |
0,69 ± 0,35 1,71 ± 0,36 h |
|
Fläche unter der KonzentrationsZeit-Kurve (AUC): |
6,8 ± 0,97 (ASS) 176 ± 45 (SA) pg/ml • h |
6,62 ± 1,39 170 ± 44 pg/ml • h |
Angabe der Werte als Mittelwerte und Streubreite.
trationen werden 30 - 60 Minuten nach der Einnahme erreicht. Paracetamol verteilt sich rasch in allen Geweben. Blut-, Plasma- und Speichelkonzentrationen sind vergleichbar. Die Plasmaproteinbindung ist gering.
Paracetamol wird vorwiegend in der Leber auf hauptsächlich zwei Wegen metabolisiert: Konjugation mit Glucuronsäure und Schwefelsäure. Bei Dosen, die die therapeutische Dosis übersteigen, ist der zuletzt genannte Weg rasch gesättigt. Ein geringer Teil der Metabolisierung erfolgt über den Katalysator Cytochrom P 450 (hauptsächlich CYP2E1) und führt zur Bildung des Metaboliten N-Acetyl-p-benzochinonimin, der normalerweise rasch durch Glutathion entgiftet und durch Cystein und Mercaptursäure gebunden wird. Im Falle einer massiven Intoxikation ist die Menge dieses toxischen Metaboliten erhöht.
Die Ausscheidung erfolgt vorwiegend im Urin. 90 % der aufgenommenen Menge werden innerhalb von 24 Stunden vorwiegend als Glucuronide (60 - 80 %) und Sulfatkonjugate (20 - 30 %) über die Nieren ausgeschieden. Weniger als 5 % werden in unveränderter Form ausgeschieden.
Die Eliminationshalbwertzeit beträgt in etwa zwei Stunden. Bei Leber- und Nierenfunktionsstörungen, nach Überdosierungen sowie bei Neugeborenen ist die Halbwertzeit verlängert. Das Maximum der Wirkung und die durchschnittliche Wirkdauer (4 - 6 Stunden) korrelieren in etwa mit der Plasmakonzentration. Bei schwerer Niereninsuffizienz (Creatinin-Clearance < 10 ml/min) ist die Ausscheidung von Paracetamol und seinen Metaboliten verzögert.
Eine relevante gegenseitige Beeinflussung der Kombinationspartner in Bezug auf die pharmakokinetischen Kenndaten ist nach bisheriger Beobachtung nicht gegeben.
5.3 Präklinische Daten zur Sicherheit Acetylsalicylsäure
In tierexperimentellen Untersuchungen traten neben den bereits unter "Nebenwirkungen” beschriebenen Effekten Nierenschäden nach Verabreichung hoher Acetylsalicylsäuredosen auf. Acetylsalicylsäure wurde ausführlich in vitro und in vivo bezüglich mutagener Wirkungen untersucht. Die Gesamtheit der Befunde ergibt keine relevanten Verdachtsmomente für eine mutagene Wirkung. Gleiches gilt für Untersuchungen zur Kanzerogenität.
Salicylate haben in Tierversuchen an mehreren Tierspezies teratogene Wirkungen gezeigt (z. B. kardiale Missbildungen, skelettale Missbildungen und Bauchwanddefekte). Implantationsstörungen, embryo- und fetotoxische Wirkungen sowie Störungen der Lernfähigkeit sind bei Nachkommen nach pränataler Exposition beschrieben worden.
Paracetamol
Im Tierversuch zur akuten, subchronischen und chronischen Toxizität von Paracetamol an Ratte und Maus traten Läsionen im Magen-Darm-Trakt, Blutbildveränderungen, Degenerationen des Leber- und Nierenparenchyms bis hin zu Nekrosen auf. Die Ursachen dieser Veränderungen sind einerseits auf den Wirkungsmechanismus (s. o.) und andererseits auf den Metabolismus von Paracetamol zurückzuführen. Die Metabolite, denen die toxischen Wirkungen zugeschrieben werden und die entsprechenden Organveränderungen sind auch beim Menschen nachgewiesen. Daher sollte Paracetamol nicht über längere Zeit und in höheren Dosen eingenommen werden. Fälle von reversibler chronischer aggressiver Hepatitis sind bereits bei oralen Tagesdosen von 3,9 und 2,9 g und einer Anwendungsdauer von 1 Jahr beschrieben. Orale Tagesdosen mit deutlich leberschädigender Wirkung liegen bei Nichtalkoholikern im Bereich von 5,8 g, wobei Intoxikationssymptome bereits 3 Wochen nach Einnahme auftreten können.
Umfangreiche Untersuchungen ergaben keine Evidenz für ein relevantes genotoxisches Risiko von Paracetamol im therapeutischen, d. h. nicht-toxischen Dosisbereich. Aus Langzeituntersuchungen an Ratten und Mäusen liegen keine Hinweise auf relevante tumorigene Effekte in nicht hepatotoxischen Dosierungen von Paracetamol vor.
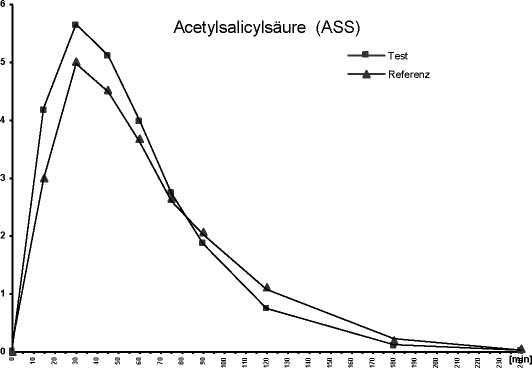
5.4 Bioverfügbarkeit
Eine im Jahr 1998 durchgeführte Bioverfügbarkeitsuntersuchung an 18 Probanden ergab im Vergleich zum Referenzpräparat hinsichtlich Acetylsalicylsäure (ASS) und Salicylsäure (SA):
Mittlere Plasmaspiegelverläufe im Vergleich zu
einem Referenzpräparat,
siehe Konzentrations-Zeit-Diagramm
zu 5.4 Bioverfügbarkeit
Mittlere Plasmaspiegelverläufe im Vergleich zu einem Referenzpräparat in einem Konzentrations-Zeit-Diagramm:
6. Pharmazeutische Angaben
6.1 Liste der sonstigen Bestandteile
Mikrokristalline Cellulose, Povidon K 30, Croscarmellose-Natrium, Stearinsäure,
hochdisperses Siliciumdioxid
6.2 Inkompatibilitäten
Bisher keine bekannt.
6.3 Dauer der Haltbarkeit
Die Dauer der Haltbarkeit beträgt 2 Jahre.
6.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung
Nicht über + 25°C aufbewahren.
In der Originalverpackung aufbewahren, um den Inhalt vor Feuchtigkeit zu schützen.
6.5 Art und Inhalt des Behältnisses
Originalpackung mit 10 Tabletten Originalpackung mit 14 Tabletten Originalpackung mit 20 Tabletten Originalpackung mit 28 Tabletten Originalpackung mit 30 Tabletten
Es werden möglicherweise nicht alle Packungsgrößen in Verkehr gebracht.
7. Inhaber der Zulassung
TOGAL-WERK AG Telefon: 089 / 92 59-0 Kardinal-Faulhaber-Str. 5 Telefax: 089 / 92 59-95 80333 München E-Mail: info@togal.de
8. Zulassungsnummer
44267.00.00
9. Datum der Erteilung der Zulassung / Verlängerung der Zulassung
Erteilung der Zulassung: 25.11.1999
Verlängerung der Zulassung: 10.04.2008
10. Stand der Information
02/2014
11. Verkaufsabgrenzung
Apothekenpflichtig
[mg/l]
Seite 4 / 4