Xeomin 100 Einheiten Pulver Zur Herstellung Eine Injektionslösung
Gebrauchsinformation: Information für Patienten/Anwender
XEOMIN® 100 Einheiten Pulver zur Herstellung einer Injektionslösung
Clostridium Botulinum Neurotoxin Typ A (150 kD), frei von Komplexproteinen
Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen, denn sie enthält wichtige Informationen.
• Heben Sie die Packungsbeilage auf. Vielleicht möchten Sie diese später nochmals lesen.
• Wenn Sie weitere Fragen haben, wenden Sie sich an Ihren Arzt, Apotheker oder das medizinische Fachpersonal.
• Dieses Arzneimittel wurde Ihnen persönlich verschrieben. Geben Sie es nicht an Dritte weiter. Es kann anderen Menschen schaden, auch wenn diese die gleichen Beschwerden haben wie Sie.
• Wenn Sie Nebenwirkungen bemerken, wenden Sie sich an Ihren Arzt, Apotheker oder das medizinische Fachpersonal. Dies gilt auch für Nebenwirkungen, die nicht in dieser Packungsbeilage angegeben sind.
Was in dieser Packungsbeilage steht:
1. Was ist XEOMIN und wofür wird es angewendet?
2. Was sollten Sie vor der Anwendung von XEOMIN beachten?
3. Wie ist XEOMIN anzuwenden?
4. Welche Nebenwirkungen sind möglich?
5. Wie ist XEOMIN aufzubewahren?
6. Inhalt der Packung und weitere Informationen
1. Was ist XEOMIN und wofür wird es angewendet?
XEOMIN ist ein Arzneimittel zur Erschlaffung der Muskulatur.
XEOMIN wird angewendet zur Behandlung der folgenden Erkrankungen bei Erwachsenen:
• Lidkrampf (Blepharospasmus)
• Schiefhals (Torticollis spasmodicus)
• erhöhte Muskelspannung/unkontrollierbare Muskelsteifigkeit in Armen oder Händen nach Schlaganfall (Spastik der oberen Extremitäten nach Schlaganfall mit klinischem Bild einer Handgelenkbeugung und gefausteter Hand)
2. Was sollten Sie vor der ANWENDUNG von XEOMIN beachten?
XEOMIN darf nicht angewendet werden,
• wenn Sie allergisch gegen Botulinum Neurotoxin Typ A oder einen der in Abschnitt 6 genannten sonstigen Bestandteile dieses Arzneimittels sind
• wenn Sie an einer allgemeinen Erkrankung der Muskeltätigkeit leiden (z.B. Myasthenia gravis, Lambert-Eaton-Syndrom)
• wenn bei Ihnen eine Infektion an der Injektionsstelle vorliegt.
Warnhinweise und Vorsichtsmaßnahmen
Nebenwirkungen können durch falsch platzierte Injektionen von Botulinum Neurotoxin Typ A hervorgerufen werden, welche zeitweise nahe gelegene Muskeln lähmen. Nebenwirkungen, die
möglicherweise mit der Verteilung des Toxins an vom Anwendungsort entfernten Stellen in Zusammenhang stehen, wurden mit Botulinumtoxin sehr selten berichtet (z.B. übermäßige Muskelschwäche, Schwierigkeiten beim Schlucken oder versehentliches Verschlucken von Essen oder Flüssigkeit in die Atemwege). Bei Patienten, die die empfohlenen Dosen erhalten, kann eine übersteigerte Muskelschwäche auftreten.
Zu hohe Dosen oder zu häufige Injektionen können das Risiko einer Antikörperbildung erhöhen. Antikörperbildung kann auch bei anderen Anwendungen zu einem Therapieversagen mit Botulinumtoxin Typ A führen.
Sprechen Sie mit Ihrem Arzt bevor XEOMIN angewendet wird:
• wenn Sie an einer Form von Blutgerinnungsstörung leiden
• wenn Sie mit Substanzen, die die Blutgerinnung hemmen (z.B. Cumarine, Heparin, Acetylsalicysäure), behandelt werden
• wenn Sie an einer ausgeprägten Schwäche oder an Gewebsschwund des Muskels, in den das Arzneimittel injiziert werden soll, leiden
• wenn Sie an Amyotrophe Lateralsklerose (ALS) leiden, die zu allgemeinem Muskelschwund führen kann.
• wenn Sie an Erkrankungen leiden, die das Zusammenspiel von Nerven und Skelettmuskeln stören (periphere neuromuskuläre Fehlfunktionen)
• wenn Sie unter Schluckstörungen leiden oder gelitten haben.
• wenn Sie in der Vergangenheit bei Injektionen mit Botulinumtoxin Typ A Probleme hatten;
• wenn Sie demnächst operiert werden.
Folgeinjektionen mit XEOMIN
Bei Folgeinjektionen mit XEOMIN, kann die Wirkung möglicherweise verstärkt oder vermindert sein. Mögliche Ursachen hierfür können sein:
• unterschiedliches Vorgehen bei der Herstellung der Injektionslösung durch Ihren Arzt
• unterschiedlich gewählte Behandlungsintervalle
• Injektionen in einen anderen Muskel
• geringfügig schwankende Aktivität des in XEOMIN enthaltenen Wirkstoffs
• Nicht-Ansprechen / Therapieversagen im Verlauf der Behandlung
Wenn Sie für einen längeren Zeitraum nur wenig körperlich aktiv waren, sollte nach der Injektion von XEOMIN jegliche körperliche Aktivität nur schrittweise wieder begonnen werden.
Verständigen Sie Ihren Arzt und suchen Sie sofort ärztliche Hilfe auf, wenn Sie eines der folgenden Symptome bei sich beobachten:
• Atem-, Schluck- oder Sprechstörungen
• Nesselsucht (Urtikaria), Schwellung einschließlich Schwellung von Gesicht oder Rachen, Atemgeräusche, Ohnmachtsgefühl und Kurzatmigkeit (mögliche Symptome einer schweren allergischen Reaktion)
Wenn Sie zu häufig mit Botulinumtoxin behandelt werden, kann es in Ihrem Körper zu Antikörperbildung kommen. Dadurch kann die Wirksamkeit von Botulinumtoxin herabgesetzt werden.
Lidkrampf (Blepharospasmus)
Bitte sprechen Sie mit Ihren Arzt bevor Sie mit XEOMIN behandelt werden, wenn:
• Sie eine Augenoperation hinter sich haben. Ihr Arzt wird dann die entsprechenden Vorsichtsmaßnahmen treffen.
• bei Ihnen das Risiko einer Erkrankung mit dem Namen Engwinkelglaukom besteht. Diese Erkrankung kann zu einem erhöhten Augeninnendruck und in Folge dessen zu einer Schädigung des Sehnervs führen. Ihr Arzt kann Ihnen sagen, ob Sie gefährdet sind.
Während der Behandlung können in den weichen Augenlidgeweben punktförmige Blutungen auftreten. Durch sanfte Druckbehandlung an der Injektionsstelle unmittelbar nach der Injektion kann Ihr Arzt dies vermeiden.
Wenn Sie eine XEOMIN-Injektion in Ihren Augenmuskel erhalten haben, kann es zu verringertem Blinzeln kommen. Dies kann den Schutz der Hornhaut herabsetzen. Durch den geringeren Schutz der Hornhaut kann es zu oberflächlichen Schäden und Hornhautgeschwüren kommen.
Schiefhals (Torticollis spasmodicus)
Nach der Injektion können milde bis schwere Schluckstörungen auftreten. Dies kann zu Problemen bei der Atmung führen und Sie könnten einem höheren Risiko ausgesetzt sein, feste oder flüssige Stoffe einzuatmen. Fremdstoffe, die in Ihre Lungen gelangen, können zu einer Lungenentzündung führen. Wenn nötig, wird Ihr Arzt entsprechend medizinisch eingreifen (z.B. in Form von künstlicher Ernährung).
Die Schluckstörungen können bis zu zwei bis drei Wochen nach der Injektion andauern, jedoch ist für einen Patienten ein Andauern bis zu fünf Monaten bekannt.
Erhöhte Muskelspannung/unkontrollierbare Muskelsteifigkeit in Armen oder Händen nach Schlaganfall (Spastik der oberen Extremitäten nach Schlaganfall)
XEOMIN eignet sich für die Behandlung erhöhter Muskelspannung/unkontrollierbarer Muskelsteifigkeit von z.B. Ellbogen, Unterarm oder Hand (Teile der oberen Extremitäten). XEOMIN ist wirksam in Kombination mit den üblichen Standard-Behandlungsmethoden. XEOMIN sollte zusammen mit diesen anderen Methoden angewendet werden. Es ist unwahrscheinlich, dass die Behandlung den Bewegungsumfang der Gelenke verbessern kann, wenn die umgebende Muskulatur bereits ihre Dehnungsfähigkeit verloren hat.
Kinder und Jugendliche
Die Anwendung von XEOMIN bei Kindern und Jugendlichen im Alter von 0-17 Jahren wurde bisher nicht geprüft und wird daher nicht empfohlen.
Anwendung von XEOMIN zusammen mit anderen Arzneimitteln
Informieren Sie Ihren Arzt oder Apotheker, wenn Sie andere Arzneimittel einnehmen/anwenden, kürzlich andere Arzneimittel eingenommen/angewendet haben oder beabsichtigen, andere Arzneimittel einzunehmen/anzuwenden.
Die Wirkung von XEOMIN kann verstärkt werden durch:
• Mittel zur Behandlung bestimmter Infektionskrankheiten (Spectinomycin oder Antibiotika vom Aminoglykosid-Typ [z.B. Neomycin, Kanamycin, Tobramycin])
• Andere muskelentspannende Mittel( z.B. Muskelrelaxantien vom Tubocurarin-Typ). Solche Arzneimittel werden z.B. bei Vollnarkosen angewendet. Informieren Sie vor einer Operation Ihren Narkosearzt darüber, falls XEOMIN bei Ihnen angewendet wurde.
In diesen Fällen muss XEOMIN mit Vorsicht angewendet werden.
Die Wirkung von XEOMIN kann möglicherweise durch bestimmte Arzneimittel gegen Malaria und Rheuma (sogenannte Aminochinoline) abgeschwächt werden.
Schwangerschaft, Stillzeit und Zeugungs-/Gebärfähigkeit
Wenn Sie schwanger sind oder stillen, oder wenn Sie vermuten, schwanger zu sein oder beabsichtigen, schwanger zu werden, fragen Sie vor der Einnahme/Anwendung dieses Arzneimittels Ihren Arzt oder Apotheker um Rat.
Wenn Sie schwanger sind, sollte XEOMIN nicht angewendet werden, es sei denn, Ihr Arzt entscheidet, dass dies zwingend erforderlich ist und der potentielle Nutzen das mögliche Risiko rechtfertigt.
Die Anwendung von XEOMIN in der Stillzeit wird nicht empfohlen.
Verkehrstüchtigkeit und das Bedienen von Maschinen
Sie sollten kein Fahrzeug führen oder an anderen potenziell gefährliche Tätigkeiten beteiligt sein, wenn ein Herabhängen des Augenlides, Schwäche (Kraftlosigkeit), Muskelschwäche, Schwindel oder Sehstörungen auftreten. Fragen Sie in Zweifelsfällen Ihren behandelnden Arzt um Rat.
3. Wie ist XEOMIN anzuwenden?
XEOMIN darf nur von Ärzten mit entsprechender Fachkenntnis in der Behandlung mit Botulinumtoxin Neurotoxin angewendet werden.
Die optimale Dosis und die Anzahl an Injektionsstellen im jeweiligen Muskel wird von Ihrem behandelnden Arzt individuell für Sie festgelegt. Die Ergebnisse der Anfangsbehandlung mit XEOMIN sollten ausgewertet werden und gegebenenfalls zu einer Dosisanpassung führen, bis der gewünschte therapeutische Effekt erreicht wird.
Bitte sprechen Sie mit Ihrem Arzt, wenn Sie den Eindruck haben, dass die Wirkung von XEOMIN zu stark oder zu schwach ist. Bei Therapieversagen sind alternative Behandlungsmethoden in Betracht zu ziehen.
Lidkrampf (Blepharospasmus)
Die erste Wirkung der Injektion stellt sich üblicherweise innerhalb von vier Tagen ein. Die Wirkung einer Behandlung hält im Allgemeinen etwa 3-4 Monate an, sie kann jedoch erheblich länger oder kürzer andauern. Bei Bedarf kann die Behandlung anschließend wiederholt werden. Die empfohlene erstmalige Dosis beträgt 25 Einheiten pro Auge. Die empfohlene Gesamtdosis bei Wiederholungsbehandlung beträgt bis zu 100 Einheiten je Behandlungssitzung.
Eine Behandlung häufiger als alle drei Monate erbringt normalerweise keinen zusätzlichen therapeutischen Effekt.
Schiefhals (Torticollis spasmodicus)
Der erste Effekt der Injektion stellt sich üblicherweise innerhalb von sieben Tagen ein. Die Wirkung einer Behandlung hält im Allgemeinen etwa 3-4 Monate an, sie kann jedoch erheblich länger oder kürzer andauern. Behandlungsintervalle von weniger als 10 Wochen werden nicht empfohlen. Die empfohlene Dosierung an einer Injektionsstelle beträgt bis zu 50 Einheiten und die maximale Gesamtdosis für die erste Behandlungssitzung 200 Einheiten. Dosierungen bis zu 300 Einheiten können von Ihrem Arzt bei Folgebehandlungen verabreicht werden, je nachdem, wie Sie auf die Behandlung ansprechen.
Erhöhte Muskelspannung/unkontrollierbare Muskelsteifigkeit in Armen oder Händen nach Schlaganfall (Spastik der oberen Extremitäten nach Schlaganfall)
Nach Angaben der Patienten setzte die Wirkung 4 Tage nach Behandlungsbeginn ein. Die maximale Wirkung hinsichtlich der Verbesserung der Muskelspannung wurde innerhalb von 4 Wochen beobachtet. Im Allgemeinen hält die Wirkung der Behandlung 12 Wochen an. Die empfohlene Dosis beträgt bis zu 400 Einheiten pro Therapiesitzung. Der Zeitraum zwischen den Therapiesitzungen sollte mindestens 12 Wochen betragen. Gelöstes XEOMIN ist für Injektionen in den Muskel bestimmt.
Wenn eine größere Menge XEOMIN angewendet wurde als erforderlich
Symptome einer Überdosierung
Symptome einer Überdosierung treten nicht unmittelbar nach einer Injektion auf und können allgemeine Schwäche, Herabhängen des Lids, Doppeltsehen, Atem-und Sprechstörungen und eine Lähmung der
Atemmuskulatur oder Schluckstörungen, welche möglicherweise eine Lungenentzündung hervorrufen, beinhalten.
Maßnahmen bei Überdosierung
Wenn Sie Symptome einer Überdosierung an sich feststellen, informieren Sie bzw. Ihre Angehörigen umgehend einen Arzt und lassen Sie sich ins Krankenhaus einweisen. Eventuell ist eine Überwachung über mehrere Tage und eine künstliche Beatmung erforderlich.
Wenn Sie weitere Fragen zur Anwendung dieses Arzneimittels haben, wenden Sie sich an Ihren Arzt, Apotheker oder das medizinische Fachpersonal.
4. Welche Nebenwirkungen sind möglich?
Wie alle Arzneimittel kann auch dieses Arzneimittel Nebenwirkungen haben, die aber nicht bei jedem auftreten müssen.
Nebenwirkungen, wie beispielsweise starke Muskelschwäche oder Schluckbeschwerden, können durch Injektionen von XEOMIN hervorgerufen werden, die von der Injektionsstelle entfernte Muskelgruppen lähmen.
Schluckstörungen können das Einatmen von Fremdkörpern verursachen, mit der Folge einer Lungenentzündung, in manchen Fällen auch mit tödlichem Verlauf.
Bei Anwendung von XEOMIN kann es zu allergischen Reaktionen kommen. Selten wurden schwerwiegende Überempfindlichkeitsreaktionen (Anaphylaxie) oder allergische Reaktionen gegen das Serum in dem Produkt (Serumkrankheit) berichtet, welche z.B. Schwierigkeiten beim Atmen (Dyspnoe), Nesselsucht (Urtikaria), Schwellungen des Weichgewebes (Weichteilödem) verursachen können. Einige dieser Reaktionen wurden nach Anwendung eines herkömmlichen Botulinumtoxin Typ A-Komplexes berichtet. Sie traten nach alleiniger Gabe des Toxins auf oder in Kombination mit anderen Produkten, die dafür bekannt sind, ähnliche Reaktionen auszulösen.
Eine allergische Reaktion kann folgende Symptome verursachen:
• Schwierigkeiten beim Atmen, Schlucken oder Sprechen aufgrund einer Schwellung des Gesichts, der Lippen, des Mund- oder Rachenraumes
• Schwellung der Hände, der Füße oder der Fußgelenke.
Wenn Sie eine dieser Nebenwirkungen bemerken, informieren Sie bitte sofort Ihren Arzt oder bitten Sie Ihre Angehörigen dies zu tun und begeben Sie sich in die Notaufnahme Ihres nächstgelegenen Krankenhauses.
Gewöhnlich treten Nebenwirkungen innerhalb der ersten Woche nach der Injektion auf und sind vorübergehend. Nebenwirkungen können mit dem Arzneimittel, dem Injektionsverfahren oder mit beidem zusammenhängen. Nebenwirkungen können auf das Gebiet um die Injektionsstelle beschränkt sein (z.B. lokale Muskelschwäche, lokale Schmerzen, Entzündung, Kribbeln, verringertes Berührungsempfinden der Haut, Druckempfindlichkeit, Schwellung (allgemein), Schwellungen des Weichgewebes (Ödem), Hautrötung (Erythem), Juckreiz, lokale Infektion, Bluterguss, Blutungen und/oder blaue Flecken).
Die Injektion mit der Nadel kann Schmerzen verursachen. Diese Schmerzen oder die Angst vor dem Nadeleinstich können zu Ohnmachtsanfällen oder Blutdruckabfall führen.
Lidkrampf (Blepharospasmus)
Folgende Nebenwirkungen wurden bei der Anwendung von XEOMIN beobachtet:
Sehr Häufig (kann mehr als 1 von 10 Behandelten betreffen):
Herabhängen des Oberlids (Ptosis), trockene Augen
Häufig (kann bis zu 1 von 10 Behandelten betreffen):
Verschwommenes Sehen, Sehstörungen, Doppeltsehen, vermehrter Tränenfluss, Mundtrockenheit, Schluckstörungen (Dysphagien), Kopfschmerzen, Schmerzen an der Injektionsstelle, Müdigkeit, Muskelschwäche, Schwäche der Gesichtsmuskeln, Hautausschlag
Schiefhals (Torticollis spasmodicus)
Folgende Nebenwirkungen wurden bei der Anwendung von XEOMIN beobachtet:
Sehr häufig (kann mehr als 1 von 10 Behandelten betreffen):
Schluckstörungen (Dysphagie)
Häufig (kann bis zu 1 von 10 Behandelten betreffen):
Nackenschmerzen, Muskelschwäche, Muskelschmerzen (Myalgie), Muskelsteifigkeit, Muskelkrämpfe, Kopfschmerzen, Schwindel, Schmerzen an der Injektionsstelle, allgemeine Schwäche (Asthenie), Mundtrockenheit, Übelkeit, vermehrtes Schwitzen, Infektion der oberen Atemwege, Ohnmachtsgefühl
Gelegentlich (kann bis zu 1 von 100 Behandelten betreffen):
Sprachstörungen (Dysphonie), Kurzatmigkeit (Dyspnoe), Hautausschlag
Die Behandlung des Schiefhalses kann Schluckstörungen unterschiedlichen Schweregrades hervorrufen. Dies kann zum Einatmen von Fremdkörpern führen, so dass medizinisches Eingreifen notwendig werden kann. Die Schluckstörungen können für zwei bis drei Wochen nach der Injektion anhalten, es wurde jedoch in einem Fall auch ein Andauern bis zu fünf Monaten berichtet. Die Schluckstörungen scheinen dosisabhängig zu sein.
Erhöhte Muskelspannung/unkontrollierbare Muskelsteifigkeit in Armen oder Händen nach Schlaganfall (Spastik der oberen Extremitäten nach Schlaganfall)
Folgende Nebenwirkungen wurden bei der Anwendung von XEOMIN beobachtet:
Häufig (kann bis zu 1 von 10 Behandelten betreffen):
Kopfschmerzen, verminderte Empfindlichkeit oder Empfindlichkeitsstörungen der Haut wie teilweises Taubheits- oder Hitzegefühl (Dysästhesie, Hypoästhesie), Muskelschwäche, Hitzegefühl, Schmerz an der Injektionsstelle, Schmerzen in Gliedmaßen, Schluckstörungen (Dysphagie).
Gelegentlich (kann bis zu 1 von 100 Behandelten betreffen):
allgemeine Schwäche (Asthenie), Muskelschmerzen (Myalgie).
Einige dieser unerwünschten Wirkungen können krankheitsbedingt sein.
Erfahrungen nach Markteinführung
Grippeähnliche Symptome und Überempfindlichkeitsreaktionen wie Schwellungen, Schwellungen des Weichgewebes (Ödem), Rötung, Juckreiz, Hautausschlag (lokal oder am ganzen Körper) und Atemnot wurden berichtet.
Meldung von Nebenwirkungen
Wenn Sie Nebenwirkungen bemerken, wenden Sie sich an Ihren Arzt, Apotheker oder das medizinische Fachpersonal. Dies gilt auch für Nebenwirkungen, die nicht in dieser Packungsbeilage angegeben sind. Sie können Nebenwirkungen auch direkt dem Bundesinstitut für Arzneimittel und Medizinprodukte, Abt. Pharmakovigilanz, Kurt-Georg-Kiesinger Allee 3, D-53175 Bonn, Website: http://www.bfarm.de anzeigen. Indem Sie Nebenwirkungen melden, können Sie dazu beitragen, dass mehr Informationen über die Sicherheit dieses Arzneimittels zur Verfügung gestellt werden.
5. Wie ist XEOMIN aufzubewahren?
Bewahren Sie dieses Arzneimittel für Kinder unzugänglich auf.
Sie dürfen dieses Arzneimittel nach dem auf dem Umkarton und dem Etikett der Durchstechflasche nach „Verwendbar bis“ angegebenen Verfalldatum nicht mehr verwenden. Das Verfalldatum bezieht sich auf den letzten Tag des angegebenen Monats.
Ungeöffnete Durchstechflasche: Nicht über 25°C lagern
Gebrauchsfertige Injektionslösung: Die chemische und physikalische Stabilität der gebrauchsfertigen Zubereitung wurde für 24 Stunden bei 2 bis 8°C nachgewiesen.
Aus mikrobiologischer Sicht sollte die gebrauchsfertige Zubereitung sofort verwendet werden. Wenn die gebrauchsfertige Zubereitung nicht sofort eingesetzt wird, ist der Anwender für die Dauer und die Bedingungen der Aufbewahrung verantwortlich. Sofern die Herstellung der gebrauchsfertigen Zubereitung nicht unter kontrollierten und validierten aseptischen Bedingungen erfolgt, ist diese nicht länger als 24 Stunden bei 2°C bis 8°C aufzubewahren.
Ihr Arzt wird XEOMIN nicht verwenden, wenn die Lösung eine Trübung aufweist oder sichtbare Partikel enthält.
Anweisungen zur Entsorgung finden Sie unter Informationen für medizinisches Fachpersonal am Ende der Packungsbeilage.
6. Inhalt der Packung und weitere Informationen Was XEOMIN enthält
Der Wirkstoff ist Clostridium Botulinum Neurotoxin Typ A (150 kD), frei von Komplexproteinen. Eine Durchstechflasche enthält 100 Einheiten Clostridium Botulinum Neurotoxin Typ A (150 kD), frei von Komplexproteinen.
Aufgrund der unterschiedlichen laborabhängigen Testmethoden zur Bestimmung der biologischen Wirkstärke sind diese Einheiten spezifisch für XEOMIN und daher nicht auf andere Botulinumtoxin-Präparate übertragbar.
Die sonstigen Bestandteile sind: Albumin vom Menschen, Sucrose
Wie XEOMIN aussieht und Inhalt der Packung
XEOMIN liegt als ein Pulver zur Herstellung einer Injektionslösung vor. Das Pulver ist weiß.
Nach Auflösen des Pulvers erhält man eine klare, farblose und partikelfreie Lösung.
Packungsgrößen mit 1, 2, 3,4 oder 6 Durchstechflaschen.
Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht.
Pharmazeutischer Unternehmer, Import und Vertrieb:
Max Pharma GmbH Am Gewerbegebiet 5 95185 Gattendorf
Umgepackt und gekennzeichnet von:
Galmed A.s.
Tesmska 1349/296
716 00 Ostrava Tschechische Republik
Hersteller
Merz Pharma GmbH & Co. KGaA Eckenheimer Landstraße 100 60318 Frankfurt/Main Postfach 11 13 53 60048 Frankfurt/Main Tel.: 069/15 03-1 Fax: 069/15 03-200
Dieses Arzneimittel ist in den Mitgliedsstaaten des Europäischen Wirtschaftsruames (EWR) unter den folgenden Bezeichnungen zugelassen:
Xeomin: Bulgarien, Dänemark, Deutschland, Estland, Finnland, Frankreich, Griechenland, Island, Irland, Italien, Kroatien, Lettland, Liechtenstein, Litauen, Luxemburg, Malta, Niederlande, Norwegen, Österreich, Polen, Portugal, Rumänien, Schweden, Tschechische Republik, Ungarn, Vereinigtes Königreich, Zypern XEOMEEN: Belgien
Diese Gebrauchsinformation wurde zuletzt überarbeitet im April 2016.
Die folgenden Informationen sind für medizinisches Fachpersonal bestimmt:
Hinweise zur Herstellung der gebrauchsfertigen Injektionslösung:
XEOMIN wird vor dem Gebrauch mit Natriumchlorid 9 mg/ml (0,9%) Injektionslösung rekonstituiert.
XEOMIN darf bei bestimmungsgemäßem Gebrauch nur zur Behandlung eines einzelnen Patienten bei einer Sitzung verwendet werden.
Die Rekonstitution des Flascheninhalts und das Aufziehen der Spritze sollten über plastikbeschichteten Papiertüchern erfolgen, um eventuelle Spritzer aufzufangen. Eine entsprechende Menge Natriumchlorid-Lösung wird mit einer Spritze aufgezogen. Nach dem vertikalen Einstechen der Nadel durch den Stopfen wird das Lösungsmittel vorsichtig in die Durchstechflasche injiziert, um Schaumbildung zu vermeiden. Es wird empfohlen eine 20-27G Kurzschliffkanüle für die Rekonstitution zu verwenden.
Die Durchstechflasche ist zu verwerfen, wenn in der Flasche kein Unterdruck vorhanden ist, der das Lösungsmittel aus der Spritze ansaugt. Entfernen Sie die Spritze von der Durchstechflasche und mischen Sie XEOMIN vorsichtig mit dem Lösungsmittel durch Schwenken und Drehen der Flasche -nicht zu stark schütteln. Falls erforderlich, sollte die zur Rekonstitution verwendete Kanüle in der Durchstechflasche verbleiben und die erforderliche Menge an Lösung sollte mit einer neuen sterilen, für die Injektion geeigneten Spritze aufgezogen werden.
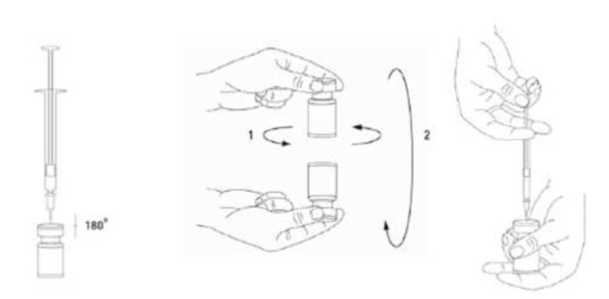
Die rekonstituierte XEOMIN-Lösung ist klar, farblos und frei von Partikeln.
XEOMIN darf nicht verwendet werden, wenn die rekonstituierte Lösung (hergestellt wie oben beschrieben) eine Trübung zeigt oder Ausflockungen oder Partikel enthält.
Die folgende Tabelle gibt mögliche Verdünnungen an:
|
Zueeeebene Menge Lösungsmittel |
Erhaltene Dosis in Einheiten pro 0,1 ml |
|
Natriumchlorid 9 mg/ml (0,9%) Iniektionslösuna) | |
|
0,5 ml |
20,0 Einheiten |
|
1,0 ml |
10,0 Einheiten |
|
2,0 ml |
5,0 Einheiten |
|
4,0 ml |
2,5 Einheiten |
|
8,0 ml |
1,25 Einheiten |
Hinweise zur Entsorgung
Injektionslösung, die länger als 24 Stunden aufbewahrt wurde, sowie nicht verwendete Reste der Injektionslösung müssen verworfen werden.
VORGEHENSWEISE ZUR SICHEREN ENTSORGUNG DER DURCHSTECHFLASCHEN, SPRITZEN UND VERWENDETEN MATERIALIEN
Unbenutzte Durchstechflaschen, Restlösung in Durchstechflaschen und/oder Spritzen sollten autoklaviert werden. Alternativ kann restliches XEOMIN durch Zusatz einer der folgenden Lösungen inaktiviert werden: 70% Ethanol, 50% Isopropanol, 0,1% Natriumdodecylsulfat (anionisches Detergens), verdünnte Natriumhydroxid-Lösung (0,1 N NaOH) oder verdünnte NatriumhypochloritLösung (mindestens 1,0% NaOCl).
Nach der Inaktivierung dürfen gebrauchte Durchstechflaschen, Spritzen und Materialien nicht entleert werden, sondern müssen in entsprechende Behälter geworfen und entsprechend den nationalen Vorschriften entsorgt werden.
EMPFEHLUNGEN BEI UNFÄLLEN WÄHREND DES UMGANGS MIT BOTULINUMTOXIN
Jegliches verschüttetes Arzneimittel muss aufgewischt werden: entweder - im Fall des Pulvers -mit einem saugfähigen Material, das mit einer der oben genannten Lösungen getränkt wurde -im Fall der rekonstituierten Lösung - mit einem trockenen saugfähigen Material.
Kontaminierte Oberflächen müssen mit einem saugfähigen Material gereinigt werden, das mit einer der oben genannten Lösungen getränkt wurde. Anschließend trocknen lassen.
Wenn eine Durchstechflasche zerbricht, wie oben beschrieben vorgehen: Glassplitter vorsichtig aufsammeln und das Arzneimittel aufwischen, dabei Schnittverletzungen der Haut vermeiden.
Wenn das Arzneimittel in Kontakt mit der Haut gelangt, den betroffenen Bezirk mit mit reichlich Wasser abspülen.
Wenn das Arzneimittel in Kontakt mit den Augen gelangt, die Augen gründlich mit reichlich Wasser oder einer Augenspüllösung ausspülen.
• Wenn das Arzneimittel in Kontakt mit einer Wunde, Schnittverletzung oder nicht-intakter Haut gelangt, gründlich mit reichlich Wasser spülen und die entsprechenden medizinischen Maßnahmen entsprechend der injizierten Dosis ergreifen.
Diese Anweisungen zur Anwendung, Handhabung und Entsorgung müssen strikt eingehalten werden.
10