Zofran I.v. 4Mg
Zofran®
Novartis Pharma
1. BEZEICHNUNG DER ARZNEIMITTEL
Zofran® 4 mg Filmtabletten
Filmtablette
Zofran® 8 mg Filmtabletten
Filmtablette
Zofran® 4 mg Zydis® Lingual
Schmelztablette
Zofran® 8 mg Zydis® Lingual
Schmelztablette
Zofran® Lösung 4 mg/5 ml
Zofran® i.v. 4 mg
4 mg/2 ml Injektionslösung Zofran® i.v. 8 mg
8 mg/4 ml Injektionslösung
2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Zofran 4 mg Filmtabletten
1 Filmtablette enthält 5 mg Ondansetronhydrochlorid-Dihydrat, entsprechend 4 mg Ondansetron.
Sonstiger Bestandteil mit bekannter Wirkung: Lactose (siehe Abschnitt 4.4).
Zofran 8 mg Filmtabletten
1 Filmtablette enthält 10 mg Ondansetronhydrochlorid-Dihydrat, entsprechend 8 mg Ondansetron.
Sonstiger Bestandteil mit bekannter Wirkung: Lactose (siehe Abschnitt 4.4).
Zofran 4 mg Zydis Lingual 1 Schmelztablette enthält 4 mg Ondansetron.
Sonstige Bestandteile mit bekannter Wirkung: Aspartam, Alkohol, Methyl(4-hydroxybenzoat), Propyl(4-hydroxybenzoat) (siehe Abschnitt 4.4).
Zofran 8 mg Zydis Lingual 1 Schmelztablette enthält 8 mg Ondansetron.
Sonstige Bestandteile mit bekannter Wirkung: Aspartam, Alkohol, Methyl(4-hydroxybenzoat), Propyl(4-hydroxybenzoat) (siehe Abschnitt 4.4).
Zofran Lösung
Jede Flasche enthält 50 ml Lösung zum Einnehmen. 5 ml Lösung enthalten 5 mg Ondansetronhydrochlorid-Dihydrat, entsprechend 4 mg Ondansetron.
Sonstige Bestandteile mit bekannter Wirkung: Sorbitol; enthält Alkohol (siehe Abschnitt 4.4).
Zofran i. v. 4 mg
1 Ampulle zu 2 ml Injektionslösung enthält 5 mg Ondansetronhydrochlorid-Dihydrat, entsprechend 4 mg Ondansetron.
Zofran i. v. 8 mg
1 Ampulle zu 4 ml Injektionslösung enthält 10 mg Ondansetronhydrochlorid-Dihydrat, entsprechend 8 mg Ondansetron.
Vollständige Auflistung der sonstigen Bestandteile, siehe Abschnitt 6.1.
3. DARREICHUNGSFORMEN
Zofran 4 mg Filmtabletten
Gelbe, ovale, bikonvexe Filmtabletten. Auf einer Tablettenseite tragen sie die Prägung „GX ET3“.
Zofran 8 mg Filmtabletten
Gelbe, ovale, bikonvexe Filmtabletten. Auf einer Tablettenseite tragen sie die Prägung „GX ET5“.
Zofran 4 mg Zydis Lingual/Zofran 8 mg Zydis Lingual Schmelztabletten
Weiße, runde, plano-konvexe, sich schnell auflösende Tabletten.
Zofran Lösung
Klare, farblose Lösung mit charakteristischem Erdbeer-Geruch.
Zofran i. v. 4 mg/Zofran i. v. 8 mg Injektionslösung
Klare, farblose sterile Lösung zur Injektion und Infusion.
4. KLINISCHE ANGABEN
4.1 Anwendungsgebiete Erwachsene
Zofran 4 mg Filmtabletten/Zofran 4 mg Zydis Lingual/Zofran Lösung
- Übelkeit, Brechreiz und Erbrechen bei Therapie mit Zytostatika und Strahlentherapie.
Zofran 8 mg Filmtabletten/Zofran 8 mg Zydis Lingual
- Übelkeit, Brechreiz und Erbrechen bei Therapie mit Zytostatika und Strahlentherapie.
- Prophylaxe von Übelkeit, Brechreiz und Erbrechen nach Operationen.
Zofran i. v. 4 mg
- Übelkeit, Brechreiz und Erbrechen bei Therapie mit Zytostatika.
- Prophylaxe und Therapie von Übelkeit, Brechreiz und Erbrechen nach Operationen.
Zofran i. v. 8 mg
- Übelkeit, Brechreiz und Erbrechen bei Therapie mit Zytostatika.
Kinder und Jugendliche
- Ondansetron ist angezeigt für die Behandlung von Übelkeit, Brechreiz und Erbrechen unter einer Therapie mit Zytostatika;
- Zur Prophylaxe und Therapie von Übelkeit, Brechreiz und Erbrechen nach Operationen wurden keine Studien zur Anwendung von oral gegebenem Ondansetron durchgeführt; für diese Anwendung wird die intravenöse Gabe empfohlen.
4.2 Dosierung und Art der Anwendung
Dosierung
Durch Zytostatika und Bestrahlung hervorgerufene Übelkeit, Brechreiz und Erbrechen
Das emetogene Potenzial einer Krebsbehandlung kann je nach Dosen und Kombinationen der verwendeten Chemotherapie- und Strahlentherapie-Schemata variieren. Die Wahl der Dosis und des Dosis-Schemas muss sich daher nach dem emetogenen Potenzial richten.
Erwachsene
Orale Darreichungsformen:
Die empfohlene orale Dosis beträgt 8 mg, 1 bis 2 Stunden vor der Chemotherapie oder Bestrahlung eingenommen, gefolgt von 8 mg oral alle 12 Stunden über maximal 5 Tage.
Bei hochemetogener Chemotherapie kann eine orale Einzeldosis bis maximal 24 mg Ondansetron zusammen mit 12 mg Dexamethason-21-dihydrogenphosphat, Dinatriumsalz, oder Äquivalent oral 1 bis 2 Stunden vor der Chemotherapie gegeben werden. Nach den ersten 24 Stunden kann die Ondansetron-Behandlung oral über bis zu 5 Tage nach einem Behandlungszyklus fortgesetzt werden. Die empfohlene Dosis beträgt 8 mg, zweimal täglich eingenommen.
Intravenöse Darreichungsformen:
Die empfohlene intravenöse Ondansetron-Dosis beträgt 8 mg als langsame intravenöse Injektion über nicht weniger als 30 Sekunden, unmittelbar vor der Behandlung verabreicht.
Bei hochemetogener Chemotherapie kann eine maximale anfängliche Einzeldosis von 16 mg Ondansetron i.v. als Infusion (verdünnt in 50 bis 100 ml Kochsalzlösung oder einer anderen kompatiblen Lösung, siehe Abschnitt 6.6) über mindestens 15 Minuten gegeben werden. Einzeldosen über 16 mg dürfen aufgrund des dosisabhängig steigenden Risikos einer QT-Verlängerung nicht verwendet werden.
Die Wirksamkeit von Ondansetron bei hochemetogener Chemotherapie kann durch die einmalige intravenöse Gabe von 20 mg Dexamethason-21-dihydrogenphosphat, Dinatriumsalz, vor Beginn der Chemotherapie gegeben, gesteigert werden.
Intravenöse Dosen über 8 mg bis zu einem Maximum von 16 mg müssen in 50 ml bis
100 ml 0,9 %iger Natriumchlorid-Lösung zur Injektion oder 5 %iger Dextrose-Lösung zur Injektion vor der Anwendung verdünnt und über mindestens 15 Minuten infundiert werden (siehe Abschnitt 6.6). Intravenöse Ondansetron-Dosen von 8 mg und niedriger müssen nicht verdünnt, sondern können als langsame intravenöse Injektion in nicht weniger als 30 Sekunden verabreicht werden.
Nach der initialen Ondansetron-Dosis von 8 mg können 2 zusätzliche intravenöse Dosen von je 8 mg (über mindestens 30 Sekunden) im Abstand von je 4 Stunden verabreicht werden, oder eine kontinuierliche Infusion von 1 mg/h über bis zu 24 Stunden.
Zur Vorbeugung von verzögertem oder verlängertem Erbrechen wird die orale Behandlung empfohlen.
Kinder und Jugendliche (im Alter von 6 Monaten bis 17 Jahre)
Orale und intravenöse Darreichungsformen:
Die Dosis zur Behandlung der durch Chemotherapie hervorgerufenen Übelkeit, Brechreiz und Erbrechen kann auf Grundlage der Körperoberfläche (KOF) oder auf Grundlage des Körpergewichts berechnet werden. In klinischen Studien an Kindern und Jugendlichen wurde Ondansetron als intravenöse Infusion, verdünnt in 25 bis 50 ml Kochsalzlösung oder einer anderen kompatiblen Infusionslösung, über nicht weniger als 15 Minuten gegeben (siehe Abschnitt 6.6). Eine Dosierung nach Körpergewicht führt im Vergleich zu einer Dosierung nach Körperoberfläche zu höheren Tagesgesamtdosen (siehe Abschnitt 5.2).
Es sind keine Daten aus kontrollierten klinischen Studien zur Anwendung von Zofran zur Prävention von verzögerter oder prolongierter (verlängerter) Chemotherapie-induzierter Übelkeit, Brechreiz und Erbrechen vorhanden. Ebenso sind keine Daten aus kontrollierten klinischen Studien zur Anwendung von Zofran bei Strahlentherapie-induzierter Übelkeit, Brechreiz und Erbrechen bei Kindern vorhanden.
Dosierung nach Körperoberfläche:
Ondansetron sollte unmittelbar vor der Chemotherapie intravenös mit einer Initialdosis von 5 mg/m2 verabreicht werden. Die i.v.-Einzeldosis darf 8 mg nicht überschreiten. Die Gabe von oralen Dosen kann 12 Stunden später erfolgen und kann über einen Zeitraum von bis zu 5 Tagen fortgesetzt werden (siehe Tabelle 1). Die Gesamtdosis innerhalb von 24 Stunden (als abgeteilte Dosen) darf die Erwachsenen-Dosis von 32 mg nicht überschreiten.
Tabelle 1: Dosierung nach Körperoberfläche bei Chemotherapie-induzierter Übelkeit, Brechreiz und Erbrechen (Alter ab 6 Monate bis 17 Jahre)
|
Körper oberfläch e |
Tag 1 |
Tage 2-6 |
|
< 0,6 m2 |
Initial 5 mg/m2 i.v. plus 2 mg Ondansetron (entspricht 2,5 ml Zofran Lösung) nach 12 Stunden |
Alle 12 Stunden: 2 mg Ondansetron (entspricht 2,5 ml Zofran Lösung) |
|
> 0,6 m2 bis < 1,2 m2 |
Initial 5 mg/m2 i.v. plus 4 mg Ondansetron (entspricht 5 ml Zofran Lösung oder 1 Zofran 4 mg Filmtablette oder 1 Schmelztablette Zofran 4 mg Zydis Lingual) nach 12 Stunden |
Alle 12 Stunden 4 mg Ondansetron (entspricht 5 ml Zofran Lösung oder 1 Zofran 4 mg Filmtablette oder 1 Schmelztablette Zofran 4 mg Zydis Lingual) |
|
> 1,2 m2 |
Initial 5 mg/m2 i.v. oder 8 mg i.v. plus 8 mg Ondansetron (entspricht 10 ml Zofran Lösung oder 1 Zofran 8 mg Filmtablette oder 1 Schmelztablette Zofran 8 mg Zydis Lingual) nach 12 Stunden |
Alle 12 Stunden 8 mg Ondansetron (entspricht 10 ml Zofran Lösung oder 1 Zofran 8 mg Filmtablette oder 1 Schmelztablette Zofran 8 mg Zydis Lingual) |
Dosierung nach Körpergewicht:
Eine Dosierung nach Körpergewicht führt im Vergleich zu einer Dosierung nach Körperoberfläche zu höheren Tagesgesamtdosen (siehe Abschnitt 5.2).
Ondansetron sollte unmittelbar vor der Chemotherapie als intravenöse Einzeldosis von 0,15 mg/kg Körpergewicht verabreicht werden. Die i.v.-Einzeldosis darf 8 mg nicht überschreiten. Bei Bedarf können 2 weitere i.v.-Dosen mit einem Abstand von 4 Stunden verabreicht werden.
Die Gabe oraler Dosen kann 12 Stunden später erfolgen und kann über einen Zeitraum von bis zu 5 Tagen fortgesetzt werden (siehe Tabelle 2).
Die Gesamtdosis innerhalb von 24 Stunden (als abgeteilte Dosen) darf die ErwachsenenDosis von 32 mg nicht überschreiten.
Tabelle 2: Dosierung nach Körpergewicht bei Chemotherapie-induzierter Übelkeit, Brechreiz und Erbrechen (Alter ab 6 Monate bis 17 Jahre)
|
Körper gewicht |
Tag 1 |
Tage 2-6 |
|
< 10 kg |
Bis zu 3 Dosen a 0,15 mg/kg i.v. alle 4 Stunden |
2 mg Ondansetron (entspricht 2,5 ml Zofran Lösung) alle 12 Stunden |
|
> 10 kg |
Bis zu 3 Dosen a 0,15 mg/kg i.v. alle 4 Stunden |
4 mg Ondansetron (entspricht 5 ml Zofran Lösung oder 1 Zofran 4 mg Filmtablette oder 1 Schmelztablette Zofran 4 mg Zydis Lingual) alle 12 Stunden |
Ältere Patienten
Orale Darreichungsformen:
Eine Dosisanpassung oder Änderung der Einnahmefrequenz ist nicht erforderlich. Intravenöse Darreichungsformen:
Bei Patienten im Alter von 65 bis 74 Jahren kann das normale Dosisschema für Erwachsene angewendet werden. Alle intravenösen Dosen sollten in 50 bis 100 ml Kochsalzlösung oder einer anderen kompatiblen Infusionslösung verdünnt (siehe Abschnitt 6.6) und über mindestens 15 Minuten infundiert werden. Nach der initialen Dosis können 2 weitere Dosen a 8 mg, über 15 Minuten infundiert und im Abstand von mindestens 4 Stunden, gegeben werden.
Bei Patienten im Alter von 75 Jahren und älter sollte die initiale intravenöse Dosis 8 mg nicht überschreiten. Alle intravenösen Dosen sollten in 50 bis 100 ml Kochsalzlösung oder einer anderen kompatiblen Infusionslösung verdünnt (siehe Abschnitt 6.6) und über mindestens 15 Minuten infundiert werden. Nach der initialen Dosis können 2 weitere Dosen a 8 mg, über 15 Minuten infundiert und im Abstand von mindestens 4 Stunden, gegeben werden.
Patienten mit eingeschränkter Nieren funktion
Es ist keine Anpassung der Dosis, der Dosierungshäufigkeit oder Änderung des Verabreichungsweges erforderlich.
Patienten mit eingeschränkter Leberfunktion
Bei Patienten mit mittlerer bis schwerer Einschränkung der Leberfunktion sind die Clearance signifikant verringert und die Serumhalbwertszeit signifikant erhöht. Bei solchen Patienten sollte eine tägliche Gesamtdosis von 8 mg Ondansetron (oral oder intravenös) nicht überschritten werden.
Patienten, die schlechte Spartein-/Debrisoquin-Metabolisierer sind
Die Eliminationshalbwertszeit von Ondansetron ist bei Patienten, die als schlechte Spartein-/Debrisoquin-Metabolisierer eingestuft sind, nicht verändert. Folglich ist bei solchen Patienten kein Unterschied in der Exposition nach wiederholter Gabe im Vergleich zur allgemeinen Bevölkerung zu erwarten. Eine Änderung der Dosis oder der Dosisfrequenz ist nicht erforderlich.
Übelkeit, Brechreiz und Erbrechen nach Operationen Erwachsene:
Zur Prophylaxe postoperativer Übelkeit, Brechreiz und Erbrechen kann Ondansetron oral oder intravenös als langsame intravenöse Injektion gegeben werden.
Orale Darreichungsformen:
Zur Prophylaxe von postoperativer Übelkeit, Brechreiz und Erbrechen beträgt die empfohlene Dosis 16 mg Ondansetron oral 1 Stunde vor der Narkose.
Zur Behandlung bekannter Übelkeit, Brechreiz und Erbrechen nach Operationen wird die Behandlung mit Ondansetron als langsame intravenöse Injektion empfohlen.
Intravenöse Darreichungsformen:
Zur Prophylaxe postoperativer Übelkeit, Brechreiz und Erbrechen wird eine Einzeldosis von 4 mg als langsame intravenöse Injektion über mindestens 30 Sekunden bei Einleitung der Anästhesie empfohlen.
Zur Behandlung bekannter postoperativer Übelkeit, Brechreiz und Erbrechen wird eine Einzeldosis von 4 mg als langsame intravenöse Injektion über mindestens 30 Sekunden empfohlen.
Kinder und Jugendliche (im Alter von 1 Monat bis 17 Jahre)
Orale Darreichungsformen:
Es liegen keine Studien zur oralen Gabe von Ondansetron zur Prophylaxe oder Therapie postoperativer Übelkeit, Brechreiz und Erbrechen vor; in diesem Fall wird eine langsam zu verabreichende intravenöse Injektion (über nicht weniger als 30 Sekunden) empfohlen.
Intravenöse Darreichungsformen:
Zur Prophylaxe und Behandlung von postoperativer Übelkeit, Brechreiz und Erbrechen bei Kindern und Jugendlichen, die sich einer Operation unter Allgemeinanästhesie unterziehen, kann Ondansetron als eine langsame intravenöse Injektion (über nicht weniger als 30 Sekunden) in einer Dosis von 0,1 mg/kg KG bis zu einer maximalen Dosis von 4 mg Ondansetron entweder vor, während oder nach der Einleitung der Anästhesie oder nach der Operation verabreicht werden.
Für Kinder unter 2 Jahren sind nur begrenzte Daten über die Anwendung von Zofran zur Therapie von postoperativer Übelkeit, Brechreiz und Erbrechen verfügbar.
Ältere Patienten
Die Erfahrungen mit Ondansetron in der Prophylaxe/Therapie postoperativer Übelkeit, Brechreiz und Erbrechen bei älteren Patienten sind begrenzt. Von über 65-jährigen Patienten, die eine Chemotherapie erhielten, wurde Ondansetron gut vertragen.
Patienten mit eingeschränkter Nierenfunktion
Es ist keine Anpassung der Dosis, der Dosierungshäufigkeit oder Änderung des Verabreichungsweges erforderlich.
Patienten mit eingeschränkter Leberfunktion
Bei Patienten mit mittlerer bis schwerer Einschränkung der Leberfunktion sind die Clearance signifikant verringert und die Serumhalbwertszeit signifikant erhöht. Bei solchen Patienten sollte eine tägliche Gesamtdosis von 8 mg Ondansetron (oral oder intravenös) nicht überschritten werden.
Patienten, die schlechte Spartein-/Debrisoquin-Metabolisierer sind
Die Eliminationshalbwertszeit von Ondansetron ist bei Patienten, die als schlechte Spartein-/Debrisoquin-Metabolisierer eingestuft sind, nicht verändert. Folglich ist bei solchen Patienten kein Unterschied in der Exposition nach wiederholter Gabe im Vergleich zur allgemeinen Bevölkerung zu erwarten. Eine Änderung der Dosis oder der Dosisfrequenz ist nicht erforderlich.
Art der Anwendung Orale Darreichungsformen:
Zofran 4 mg Fiimtabietten/Zofran 8 mg Filmtabletten: zum Einnehmen
Zofran 4 mg Zydis Linguai/Zofran 8 mg Zydis Lingual: zum Einnehmen (auf der Zunge zergehen lassen und hinunterschlucken)
Entnahmehinweise:
Die Schmelztablette nicht durch die Blisterpackung drücken!


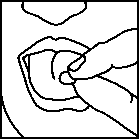
Lösen Sie an der Perforierung ein Segment vom Blister.
Trennen Sie die Schutzfolie ab. Nicht den Aufkleber abziehen. Die Darreichungsform vorsichtig mit leichtem Druck von unten entnehmen.
Legen Sie dann die
Schmelztablette auf die Zunge.
Zofran Lösung: zum Einnehmen
Die Abmessung erfolgt mit dem beigefügten Doppel-Dosierlöffel. Mit dem einen Dosierlöffelteil können 5 ml (entspricht 4 mg Ondansetron) Zofran Lösung abgemessen werden, mit dem anderen 2,5 ml (entspricht 2 mg Ondansetron).
Zur Beachtung
Die Flasche ist mit einem kindergesicherten Verschluss versehen. Zum Öffnen bitte gleichzeitig drücken und drehen.
Intravenöse Darreichungsformen:
Zofran i.v. 4 mg/Zofran i.v. 8 mg: zur intravenösen Injektion oder, nach vorgeschriebener Verdünnung, zur intravenösen Infusion.
Die Injektionslösung sollte entweder als langsame intravenöse Injektion über mindestens 30 Sekunden oder als Infusion, verdünnt mit Kochsalzlösung oder einer anderen kompatiblen Infusionslösung (siehe Abschnitt 6.6) und über mindestens 15 Minuten infundiert werden.
Weitere Angaben zur Mischbarkeit von Zofran i.v. 4 mg und Zofran i.v. 8 mg und Verabreichung mit anderen Arzneimittellösungen siehe Abschnitt 6.6.
4.3 Gegenanzeigen
Gleichzeitige Anwendung mit Apomorphin (siehe Abschnitt 4.5).
Zofran 4 mg Fiimtabietten/Zofran 8 mg Filmtabletten/Zofran i. v. 4 mg/Zofran i.v. 8 mg Überempfindlichkeit gegen den Wirkstoff oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile.
Zofran 4 mg Zydis Linguai/Zofran 8 mg Zydis Lingual
Überempfindlichkeit gegen den Wirkstoff, Methyl(4-hydroxybenzoat), Natriumsalz/Propyl(4-hydroxybenzoat), Natriumsalz oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile.
Zofran Lösung
Überempfindlichkeit gegen den Wirkstoff, Sorbitol oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile.
Zofran 4 mg Fiimtabietten/Zofran 4 mg Zydis Linguai/Zofran i. v. 8 mg Darf nicht angewendet werden bei Kindern mit einer Körperfläche von weniger als 0,6 m2 bzw. mit einem Körpergewicht bis zu 10 kg. Für diese Patientengruppe stehen geeignetere Darreichungsformen mit einem niedrigeren Wirkstoffgehalt zur Verfügung.
Zofran 8 mg Fiimtabietten/Zofran 8 mg Zydis Linguai
Darf nicht bei Kindern angewendet werden. Für diese Patientengruppe stehen geeignetere Darreichungsformen mit einem niedrigeren Wirkstoffgehalt zur Verfügung.
4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung
Überempfindlichkeitsreaktionen wurden bei Patienten beobachtet, die diese Erscheinungen auch nach Gabe anderer selektiver 5-HT3-Antagonisten gezeigt haben. Bei Auftreten von Atembeschwerden sollten diese symptomatisch behandelt und aufmerksam durch den Arzt überwacht werden, da Atembeschwerden Symptome einer beginnenden Überempfindlichkeitsreaktion sein können.
Ondansetron verlängert dosisabhängig das QT-Intervall (siehe Abschnitt 5.1). Außerdem wurden bei Patienten, die Ondansetron erhielten, in der Post-MarketingSpontanberichtserfassung Fälle von Torsade de Pointes berichtet. Bei Patienten mit angeborenem Long-QT-Syndrom sollte die Anwendung von Ondansetron vermieden werden. Bei Patienten, die eine verlängerte QTc-Zeit aufweisen oder bei denen sich eine verlängerte QTc-Zeit entwickeln kann, sollte Ondansetron mit Vorsicht angewendet werden. Zu dieser Gruppe gehören Patienten mit Elektrolytstörungen, kongestiver Herzinsuffizienz, Bradyarrhythmien oder Patienten, die andere Arzneimittel einnehmen, die eine Verlängerung des QT-Intervalls oder Elektrolytstörungen hervorrufen.
Eine Hypokaliämie oder Hypomagnesiämie sollte vor der Anwendung von Ondansetron korrigiert werden.
Über Fälle eines serotonergen Syndroms wurde bei gleichzeitiger Anwendung von Ondansetron mit anderen serotonergen Arzneimitteln (einschließlich selektiven Serotoninwiederaufnahme-Hemmern (SSRI) und Noradrenalinwiederaufnahme-Hemmern (SNRI)) berichtet. Wenn eine gemeinsame Behandlung mit Ondansetron und anderen serotonergen Arzneimitteln klinisch erforderlich sein sollte, wird eine engmaschige Überwachung des Patienten empfohlen.
Da Ondansetron die Dickdarmpassage verlangsamt, sollten Patienten mit Anzeichen einer subakuten Darmobstruktion nach Gabe von Ondansetron überwacht werden.
Die Prophylaxe von Übelkeit und Erbrechen mit Ondansetron kann nach Operationen an den Rachenmandeln okkulte Blutungen maskieren. Daher sollten betroffene Patienten nach Gabe von Ondansetron sorgfältig überwacht werden.
Kinder und Jugendliche
Kinder und Jugendliche, die Ondansetron zusammen mit hepatotoxischen Chemotherapeutika erhalten, sollten eng auf Leberfunktionsstörungen hin überwacht werden.
Sonstige Bestandteile
Zofran 4 mg Fiimtabietten/Zofran 8 mg Filmtabletten
Patienten mit der seltenen hereditären Galactose-Intoleranz, Lactase-Mangel oder Glucose-Galactose-Malabsorption sollten Zofran Filmtabletten nicht einnehmen.
Zofran 4 mg Zydis Linguai/Zofran 8 mg Zydis Lingual
Enthält Aspartam als Quelle für Phenylalanin und kann schädlich sein für Patienten mit Phenylketonurie. Für Patienten mit Phenylketonurie stehen nichtaspartamhaltige Darreichungsformen von Zofran (Zofran 4 mg Filmtabletten/Zofran 8 mg Filmtabletten) zur Verfügung.
Zofran 4 mg Zydis Lingual enthält bis zu 0,0015 mg Alkohol.
Zofran 8 mg Zydis Lingual enthält bis zu 0,003 mg Alkohol.
Zofran Lösung
Zofran Lösung enthält 3 mg Alkohol pro 5 ml Lösung.
5 ml Lösung enthalten ca. 2,1 g Sorbitol, entsprechend 0,175 BE. Patienten mit der seltenen hereditären Fructose-Intoleranz sollten Zofran Lösung nicht einnehmen.
Zofran i. v. 4 mg/Zofran i. v. 8 mg
Zofran i.v. 4 mg und Zofran i.v. 8 mg enthalten Natrium, aber weniger als 1 mmol (23 mg) Natrium pro ml. 1 ml Injektionslösung enthält 0,155 mmol bzw. 3,56 mg Natrium.
4.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen
Es deutet nichts darauf hin, dass Ondansetron den Metabolismus anderer, gewöhnlich gleichzeitig verabreichter Arzneimittel induziert oder hemmt. Spezielle Untersuchungen haben gezeigt, dass mit Ondansetron keine Wechselwirkungen mit Alkohol, Temazepam, Furosemid, Alfentanil, Tramadol, Morphin, Lidocain, Thiopental oder Propofol auftreten.
Ondansetron wird über mehrere hepatische Cytochrom-P450-Isoenzyme - CYP3A4, CYP2D6 und CYP1A2 - metabolisiert. Durch die Vielfalt der Cytochrom-P450-Isoenzyme, die Ondansetron verstoffwechseln können, kann eine Hemmung oder reduzierte Aktivität eines der Isoenzyme (z. B. bei einem genetisch bedingten CYP2D6-Mangel) normalerweise von anderen Isoenzymen ausgeglichen werden. Daher sollte es zu keiner signifikanten Veränderung der Clearance von Ondansetron oder des Dosisbedarfs kommen.
Die Anwendung von Ondansetron mit die QT-Zeit verlängernden Arzneimitteln kann die QT-Zeit zusätzlich verlängern. Die gleichzeitige Anwendung von Ondansetron mit kardiotoxischen Arzneimitteln (z. B. Anthracycline) kann das Risiko für das Auftreten von Arrhythmien erhöhen. Die gleichzeitige Anwendung von Ondansetron mit Arzneimitteln, die eine Verlängerung des QT-Intervalls und/oder Elektrolytstörungen hervorrufen, sollte mit Vorsicht erfolgen (siehe Abschnitt 4.4).
Apomorphin
Aufgrund von Berichten über starken Blutdruckabfall und Bewusstseinsverlust bei Anwendung von Ondansetron zusammen mit Apomorphinhydrochlorid ist die gleichzeitige Anwendung mit Apomorphin kontraindiziert.
Phenytoin, Carbamazepin und Rifampicin
Bei Patienten, die mit starken CYP3A4-Induktoren behandelt wurden (z. B. Phenytoin, Carbamazepin und Rifampicin), waren die orale Ondansetron-Clearance erhöht und die Ondansetron-Konzentration im Blut vermindert.
Serotonerge Arzneimittel (z. B. SSRI und SNRI)
Bei gleichzeitiger Anwendung von Ondansetron mit anderen serotonergen Arzneimitteln einschließlich selektiven Serotoninwiederaufnahme-Hemmern (SSRI) und Noradrenalinwiederaufnahme-Hemmern (SNRI) wurde ein Serotonin-Syndrom (einschließlich verändertem mentalen Status, autonomer Instabilität und neuromuskulären Veränderungen) beschrieben (siehe Abschnitt 4.4).
Tramadol
Daten aus kleineren Studien weisen darauf hin, dass Ondansetron den analgetischen Effekt von Tramadol herabsetzen kann.
4.6 Fertilität, Schwangerschaft und Stillzeit Schwangerschaft
Über die Anwendung in der Schwangerschaft liegen keine hinreichenden Daten vor. Daher wird eine Anwendung in der Schwangerschaft nicht empfohlen. Relevante epidemiologische Studien sind nicht vorhanden.
Tierexperimentelle Studien ergaben keine Hinweise auf direkte oder indirekte schädigende Wirkungen im Hinblick auf die Schwangerschaft, die embryo-fetale Entwicklung, den Geburtsvorgang oder die postnatale Entwicklung. Ondansetron darf während der Schwangerschaft, vor allem in den ersten drei Monaten, nur nach sorgfältiger Nutzen/Risiko-Abwägung angewendet werden.
Stillzeit
Untersuchungen haben gezeigt, dass Ondansetron in die Muttermilch von säugenden Tieren übergeht (siehe Abschnitt 5.3). Daher wird empfohlen, dass Mütter, die Ondansetron erhalten, ihre Säuglinge nicht stillen.
4.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen
Ondansetron zeigte in psychomotorischen Untersuchungen keine leistungsbeeinträchtigende oder sedierende Wirkung. Von den pharmakologischen Eigenschaften des Wirkstoffs Ondansetron kann eine nachteilige Wirkung auf diese Fähigkeiten nicht abgeleitet werden.
4.8 Nebenwirkungen
Nachfolgend sind die Nebenwirkungen nach Systemorganklassen und absoluter Häufigkeit (alle berichteten Ereignisse) aufgelistet. Die Häufigkeiten sind wie folgt definiert: sehr häufig (> 1/10), häufig (> 1/100 bis < 1/10), gelegentlich (> 1/1.000 bis < 1/100), selten (> 1/10.000 bis < 1/1.000), sehr selten (< 1/10.000).
Sehr häufige, häufige und gelegentliche Nebenwirkungen wurden allgemein aus Daten klinischer Prüfungen bestimmt; das Auftreten von Nebenwirkungen unter Placebo wurde berücksichtigt. Seltene und sehr seltene Nebenwirkungen wurden allgemein aufgrund der Daten aus der Spontanerfassung bestimmt.
Die nachfolgenden Häufigkeiten wurden unter Standarddosierung mit Ondansetron ermittelt. Erkrankungen des Immunsystems
Selten: Überempfindlichkeitsreaktionen vom Soforttyp (manchmal schwerwiegend)
einschließlich Anaphylaxie
Die Anaphylaxie kann lebensbedrohlich sein. Überempfindlichkeitsreaktionen wurden auch bei Patienten beobachtet, die diese Erscheinungen mit anderen selektiven 5-HT3-Antagonisten gezeigt haben.
Erkrankungen des Nervensystems Sehr häufig: Kopfschmerzen
Gelegentlich: Krampfanfälle, Bewegungsstörungen (einschließlich Extrapyramidalreaktionen wie dystonische Reaktionen, akute, krisenhafte Störungen der Okulomotorik mit Blickabweichung [Crisis oculogyris] und Dyskinesien), die aber ohne nachweisliche dauerhafte klinische Folgen blieben Selten: Benommenheit, vorwiegend bei schneller i.v.-Verabreichung
Augenerkrankungen
Selten: Vorübergehende Sehstörungen (z. B. Schleiersehen), vorwiegend bei i.v.-
Verabreichung
Sehr selten: Vorübergehende Blindheit, vorwiegend bei i.v.-Verabreichung
In der Mehrzahl der berichteten Fälle bildete sich die Blindheit innerhalb von 20 Minuten zurück. Die meisten Patienten wurden mit Chemotherapeutika behandelt, einschließlich Cisplatin. Die Ursache von einigen der berichteten Fälle von vorübergehender Blindheit war kortikalen Ursprungs.
Herzerkrankungen
Gelegentlich: Arrhythmie, Brustschmerzen mit oder ohne ST-Streckensenkung im EKG, Bradykardie
Selten: QTc-Verlängerung (einschließlich Torsade de Pointes)
Gefäßerkrankungen
Häufig: Wärmegefühl, Hitzewallungen mit Rötung der Haut
Gelegentlich: Hypotonie (Blutdruckabfall)
Erkrankungen der Atemwege, des Brustraums und Mediastinums Gelegentlich: Schluckauf
Erkrankungen des Gastrointestinaltrakts Häufig: Obstipation
Leber- und Gallenerkrankungen
Gelegentlich: Asymptomatische Erhöhung von Leberwerten*
* Diese Nebenwirkungen traten üblicherweise bei Patienten auf, die eine Chemotherapie mit Cisplatin erhalten hatten.
Erkrankungen der Haut und des Unterhautzellgewebes
Sehr selten: Toxische Hauteruptionen, einschließlich toxischer epidermaler Nekrolyse
Allgemeine Erkrankungen und Beschwerden am Verabreichungsort Häufig: Lokale Irritationen an der Einstichstelle bei i.v.-Verabreichung - insbesondere
bei wiederholter Anwendung
Zofran Zydis Lingual:
Methyl(4-hydroxybenzoat), Natriumsalz und Propyl(4-hydroxybenzoat), Natriumsalz (Parabene) können Überempfindlichkeitsreaktionen, auch Spätreaktionen, hervorrufen.
Kinder und Jugendliche
Das Nebenwirkungsprofil bei Kindern und Jugendlichen war mit dem bei Erwachsenen beobachteten Nebenwirkungsprofil vergleichbar.
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-RisikoVerhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung dem Bundesinstitut für Arzneimittel und Medizinprodukte, Abt. Pharmakovigilanz, Kurt-Georg-Kiesinger-Allee 3, D-53175 Bonn, Website: www.bfarm.de anzuzeigen.
4.9 Überdosierung
Symptome und Zeichen
Es liegen keine ausreichenden Erfahrungen mit einer Ondansetron-Überdosierung vor. Die Symptome waren ähnlich denen, die bei Patienten nach empfohlener Dosierung berichtet wurden (siehe Abschnitt 4.8). Manifestationen einer Überdosierung beinhalteten Sehstörungen, schwere Verstopfung, niedriger Blutdruck und eine vasovagale Episode mit vorübergehendem AV-Block II. Grades.
Ondansetron verlängert dosisabhängig das QT-Intervall. Im Falle einer Überdosierung wird eine EKG-Überwachung empfohlen.
Kinder und Jugendliche
Es wurden Fälle gemeldet, in denen Säuglinge und Kinder im Alter von 12 Monaten bis 2 Jahren versehentlich Überdosen von Ondansetron geschluckt haben und bei denen die aufgetretenen Symptome zu einem Serotonin-Syndrom passen (die geschätzte aufgenommene Menge überschritt 4 mg/kg).
Therapie
Es gibt kein spezifisches Gegenmittel gegen Ondansetron, daher sollten bei Verdacht auf Überdosierung erforderlichenfalls eine angemessene symptomatische Therapie und unterstützende Maßnahmen ergriffen werden.
Das weitere Vorgehen sollte wie klinisch indiziert oder entsprechend den Empfehlungen der nationalen Giftzentralen erfolgen.
Die Anwendung von Brechwurzel (Ipecacuanha) zur Behandlung einer Überdosierung mit Ondansetron wird nicht empfohlen, da ein Ansprechen der Patienten durch die eigene antiemetische Wirkung von Ondansetron unwahrscheinlich ist.
5. PHARMAKOLOGISCHE EIGENSCHAFTEN
5.1 Pharmakodynamische Eigenschaften
Pharmakotherapeutische Gruppe: Serotonin-5-HT3-Antagonisten, ATC-Code: A04AA01 Wirkmechanismus
Ondansetron ist ein hochselektiver, kompetitiver 5-HT3-Rezeptor-Antagonist. Der exakte pharmakologische Wirkungsmechanismus bei der Kontrolle von Übelkeit, Brechreiz und Erbrechen ist beim Menschen noch nicht aufgeklärt.
Tierexperimentelle Untersuchungen zeigen, dass sowohl eine zytotoxische Chemo- als auch eine Strahlentherapie eine Freisetzung von 5-Hydroxytryptamin (5-HT, Serotonin) im Dünndarm bewirken. 5-HT stimuliert 5-HT3-Rezeptoren an Neuronen in der Peripherie (viszeraler afferenter Vagus) und im Zentralnervensystem (Area postrema), wodurch ein Brechreiz hervorgerufen wird. Ondansetron antagonisiert direkt an 5-HT3-Rezeptoren die Wirkung von 5-HT und hemmt so den biochemisch/pharmakologischen Vorgang des Erbrechens.
Klinische Wirksamkeit und Sicherheit
In einer pharmakopsychologischen Probanden-Studie zeigte Ondansetron keine sedierende Wirkung.
Verlängerung des QT-Intervalls
Die Wirkung von Ondansetron auf das QT-Intervall wurde in einer doppelblinden, randomisierten Placebo- und positiv (Mofloxacin) kontrollierten Crossover-Studie mit 58 gesunden erwachsenen Männern und Frauen untersucht. Es wurden Dosen von 8 mg und 32 mg Ondansetron über 15 Minuten intravenös infundiert. Bei der höchsten getesteten Dosis von 32 mg betrug die maximale mittlere Änderung (Obergrenze des 90%-KI) des QTcF-Intervalls (Fridericia-Korrektur) gegenüber Placebo nach Basiskorrektur 19,6 msec (21,5 msec). Bei der niedrigeren getesteten Dosis von 8 mg betrug die maximale mittlere Änderung (Obergrenze des 90%-KI) des QTcF-Intervalls (Fridericia-Korrektur) gegenüber Placebo nach Basiskorrektur 5,8 msec (7,8 msec). In dieser Studie wurden keine QTcF-Intervalle von über 480 msec und keine Verlängerung des QTcF-Intervalls von über 60 msec gemessen. Bei den mittels Elektrokardiogramm gemessenen PR- bzw. QRS-Intervallen traten keine signifikanten Änderungen auf.
Kinder und Jugendliche
Durch Chemotherapie hervorgerufene Übelkeit, Brechreiz und Erbrechen:
Die Wirksamkeit von Ondansetron in der Kontrolle von Chemotherapie-induziertem Erbrechen und Übelkeit wurde in einer doppelblinden, randomisierten klinischen Studie mit 415 Patienten im Alter von 1 bis 18 Jahren untersucht (S3AB3006). Die Patienten erhielten an den Behandlungstagen entweder 5 mg/m2 Ondansetron intravenös und 4 mg Ondansetron oral nach 8 bis 12 Stunden oder 0,45 mg/kg Körpergewicht (KG) Ondansetron intravenös und eine orale Placebo-Gabe nach 8 bis 12 Stunden. Die komplette Kontrolle über das Erbrechen betrug am Therapietag mit den heftigsten Symptomen 49 % (5 mg/m2 i.v. und 4 mg Ondansetron p.o.) bzw. 41 % (0,45 mg/kg i.v. und Placebo p.o.). Nach der Chemotherapie erhielten beide Gruppen drei Tage lang 4 mg Ondansetron als Lösung zweimal täglich. Es wurde kein Unterschied in der Gesamtinzidenz oder hinsichtlich der Art der Nebenwirkungen zwischen beiden Behandlungsgruppen beobachtet.
Eine doppelblinde, randomisierte und Placebo-kontrollierte klinische Studie (S3AB4003) mit 438 Patienten im Alter von 1 bis 17 Jahren zeigte am Therapietag mit den heftigsten Symptomen eine komplette Kontrolle über das Erbrechen bei
- 73 % der Patienten, die eine intravenöse Gabe von 5 mg/m2 Ondansetron mit 2 bis 4 mg Dexamethason oral erhielten und bei
- 71 % der Patienten, die 8 mg Ondansetron als Lösung mit 2 bis 4 mg Dexamethason oral an den Therapietagen erhielten.
Nach der Chemotherapie erhielten beide Gruppen zwei Tage lang 4 mg Ondansetron als Lösung zweimal täglich. Es wurde kein Unterschied in der Gesamtinzidenz oder hinsichtlich der Art der Nebenwirkungen zwischen beiden Behandlungsgruppen beobachtet.
Die Wirksamkeit von Ondansetron bei 75 Kindern im Alter von 6 bis 48 Monaten wurde in einer offenen, unkontrollierten, einarmigen Studie untersucht (S3A40320). Alle Kinder erhielten drei Dosen Ondansetron i.v. (je 0,15 mg/kg KG), die 30 Minuten vor Beginn der Chemotherapie und dann 4 und 8 Stunden nach der ersten Dosis verabreicht wurden. Eine komplette Kontrolle über das Erbrechen wurde bei 56 % der Patienten erreicht.
In einer anderen offenen, unkontrollierten, einarmigen Studie (S3A239) mit 28 Kindern wurde die Wirksamkeit einer intravenösen Dosis von 0,15 mg/kg KG Ondansetron, gefolgt von zwei oralen Dosen mit 4 mg Ondansetron für Kinder unter 12 Jahren bzw. mit 8 mg Ondansetron für Kinder ab 12 Jahren, untersucht. Eine komplette Kontrolle über das Erbrechen wurde bei 42 % der Patienten erreicht.
Prophylaxe von postoperativer Übelkeit, Brechreiz und Erbrechen:
Die Wirksamkeit einer Einzeldosis Ondansetron in der Prophylaxe von postoperativer Übelkeit, Brechreiz und Erbrechen wurde in einer randomisierten, doppelblinden und Placebo-kontrollierten Studie mit 670 Kindern im Alter von 1 bis 24 Monaten untersucht (postkonzeptionell: Alter > 44 Wochen, Gewicht > 3 kg). Für die eingeschlossenen Patienten mit einem ASA-Status < III waren elektive chirurgische Eingriffe unter Allgemeinanästhesie vorgesehen. Nach Einleitung der Narkose wurde eine Einzeldosis von 0,1 mg/kg KG Ondansetron innerhalb von 5 Minuten verabreicht. Der Anteil der Patienten, die während der 24-stündigen Beobachtungsphase mindestens eine emetogene Episode erlitten (ITT), war in der Placebo-Gruppe größer als für die Patienten, die Ondansetron erhielten (28 % vs. 11 %,
p <0,0001).
Es wurden vier randomisierte, doppelblinde und Placebo-kontrollierte Studien mit 1469 männlichen und weiblichen Patienten im Alter von 2 bis 12 Jahren durchgeführt, die einer Allgemeinanästhesie unterzogen wurden. Die Patienten wurden entweder zur Behandlung mit einer Einzeldosis Ondansetron i.v. (0,1 mg/kg für Kinder mit einem Körpergewicht von 40 kg oder weniger, 4 mg für Kinder mit einem Körpergewicht über 40 kg; Patientenanzahl = 735) oder zur Behandlung mit Placebo (Patientenanzahl = 734) randomisiert. Die Studienmedikation wurde über mindestens 30 Sekunden, kurz vor oder nach Einleitung der Anästhesie, verabreicht. Die Wirksamkeit von Ondansetron in der Prophylaxe von postoperativer Übelkeit, Brechreiz und Erbrechen war im Vergleich zu Placebo signifikant erhöht. Die Ergebnisse dieser Studien sind in Tabelle 3 zusammengefasst.
Tabelle 3: Prophylaxe und Behandlung von postoperativer Übelkeit, Brechreiz und Erbrechen bei pädiatrischen Patienten - Ansprechen auf die Behandlung über 24 Stunden
|
Studie |
Endpunkt |
Ondansetron % |
Placebo % |
p-Wert |
|
S3A38 0 |
CR |
68 |
39 |
< 0,001 |
|
S3GT0 9 |
CR |
61 |
35 |
< 0,001 |
|
S3A38 1 |
CR |
53 |
17 |
< 0,001 |
|
S3GT1 1 |
Keine Übelkeit |
64 |
51 |
0,004 |
|
S3GT1 1 |
Kein Erbrechen |
60 |
47 |
0,004 |
CR = keine emetogenen Episoden, Notversorgung oder Studienabbruch
5.2 Pharmakokinetische Eigenschaften
Durchschnittswerte pharmakokinetischer Parameter:
|
8 mg oral |
8 mg i.v. | |
|
Zeitpunkt der maximalen Plasmakonzentration (tmax): |
1,6 h |
0,12 h |
|
Eliminationshalbwertszeit (t/): |
ca. 3 h |
ca. 3 h |
|
(bei älteren Patienten bis zu 5 h) | ||
Resorption
Die durchschnittliche Bioverfügbarkeit bei gesunden Freiwilligen beträgt nach Verabreichung einer einzelnen 8 mg Tablette ungefähr 55 bis 60 %. Zwischen Plasmaspiegeln und antiemetischer Wirkung besteht keine direkte Korrelation.
Verteilung
Die Plasmaproteinbindung (in vitro) beträgt 70 bis 76 %.
Biotransformation
Ondansetron wird über mehrere hepatische Cytochrom-P450-Isoenzyme - CYP3A4, CYP2D6 und CYP1A2 - metabolisiert. Ein Mangel an dem Enzym CYP2D6 (Debrisoquinpolymorphismus) beeinflusst nicht das pharmakokinetische Verhalten von Ondansetron. Die pharmakokinetischen Eigenschaften von Ondansetron sind bei wiederholter Gabe unverändert.
Elimination
Die Clearance von Ondansetron erfolgt vorwiegend über die hepatische Metabolisierung. Die Metabolite werden im Urin und in den Faeces ausgeschieden.
Besondere Patientenpopulationen
Kinder und Jugendliche (im Alter von 1 Monat bis 17 Jahre)
Bei pädiatrischen Patienten im Alter von 1 bis 4 Monaten (n=19), die sich einer Operation unterzogen, war die körpergewichtsnormierte Clearance um ca. 30 % verlangsamt gegenüber der Clearance bei den Patienten zwischen 5 und 24 Monaten (n=22), jedoch vergleichbar derjenigen bei Patienten im Alter von 3 bis 12 Jahren. Die Halbwertszeit bei der Patientenpopulation im Alter von 1 bis 4 Monaten betrug im Mittel 6,7 Stunden gegenüber
2,9 Stunden bei Patienten im Alter von 5 bis 24 Monaten bzw. 3 bis 12 Jahren. Die Unterschiede bei den pharmakokinetischen Parametern in der 1 bis 4 Monate alten Patientenpopulation lassen sich zum Teil durch den höheren Körperflüssigkeitsanteil bei Neugeborenen und Kleinkindern und durch das höhere Verteilungsvolumen für wasserlösliche Wirkstoffe wie z. B. Ondansetron erklären.
Bei pädiatrischen Patienten im Alter von 3 bis 12 Jahren, die sich elektiven chirurgischen Eingriffen unter Allgemeinanästhesie unterzogen, waren die absoluten Werte sowohl für die Clearance als auch für das Verteilungsvolumen von Ondansetron im Vergleich zu den Werten erwachsener Patienten verringert. Beide Parameter stiegen linear in Abhängigkeit vom Körpergewicht an und näherten sich im Alter von 12 Jahren denjenigen von jungen Erwachsenen. Nach Bereinigung von Clearance und Verteilungsvolumen um das Körpergewicht waren die Werte für diese Parameter zwischen den verschiedenen Altersgruppen ähnlich. Die Anwendung einer körpergewichtsbezogenen Dosierung berücksichtigt altersabhängige Veränderungen und bewirkt eine Normalisierung der systemischen Exposition bei pädiatrischen Patienten.
Die pharmakokinetische Analyse wurde bei einer Population von 428 Patienten (Krebspatienten, chirurgische Patienten und gesunde Freiwillige) im Alter von 1 Monat bis 44 Jahren nach intravenöser Verabreichung von Ondansetron durchgeführt. Auf Grundlage dieser Analyse war die systemische Exposition (AUC) von Ondansetron nach oraler oder intravenöser Verabreichung bei Kindern und Jugendlichen vergleichbar mit derjenigen bei Erwachsenen, mit Ausnahme von Kindern im Alter von 1 bis 4 Monaten. Das Volumen war altersabhängig und bei Erwachsenen niedriger als bei Kleinkindern und Kindern. Die Clearance war abhängig vom Gewicht, jedoch nicht vom Alter, mit der Ausnahme von 1- bis 4-monatigen Kindern. Es ist schwierig daraus zu folgern, ob eine zusätzliche Reduktion der Clearance in Abhängigkeit vom Alter der 1- bis 4-monatigen Kinder stattgefunden hat oder ob die Ursache einfach in der angeborenen Variabilität aufgrund der geringen Patientenzahl, die in dieser Altersgruppe untersucht wurde, zu sehen ist.
Da Patienten unter 6 Monaten bei postoperativer Übelkeit, Brechreiz und Erbrechen nur eine Einzeldosis Ondansetron erhalten, wird bei der Prophylaxe postoperativer Übelkeit eine verringerte Clearance als nicht klinisch relevant erachtet.
Ältere Patienten
Frühe Phase-I-Studien bei gesunden älteren Freiwilligen zeigten einen altersbedingten Abfall der Clearance und einen Anstieg der Halbwertszeit von Ondansetron. Jedoch führte eine breite interindividuelle Variabilität zu einer beträchtlichen Überlappung in den pharmakokinetischen Parametern zwischen jüngeren (<65 Jahre) und älteren Probanden (>65 Jahre), und es wurden auch insgesamt keine Unterschiede in der Sicherheit und Wirksamkeit zwischen jüngeren und älteren Krebspatienten in den klinischen Studien zur Chemotherapie-induzierten Übelkeit, Brechreiz und Erbrechen zur Unterstützung anderer Dosierungsempfehlungen für ältere Patienten beobachtet.
Basierend auf neueren Modellen bezüglich Ondansetron-Konzentrationen im Plasma und Expositions-Reaktions-Beziehungen wird eine größere Wirkung auf den QTcF-Wert bei Patienten ab einem Alter von 75 Jahren im Vergleich zu jüngeren Erwachsenen vorhergesagt. Für die intravenöse Gabe werden spezielle Dosis-Informationen für Patienten über 65 Jahre und für Patienten über 75 Jahre gegeben (siehe Abschnitt 4.2).
Patienten mit Nierenfunktionsstörungen
Bei Patienten mit mäßigen Nierenfunktionsstörungen (Kreatinin-Clearance 15 bis 60 ml/min) sind sowohl die systemische Clearance als auch das Verteilungsvolumen nach intravenöser Gabe von Ondansetron reduziert; dies führt zu einer leichten, aber klinisch nicht signifikanten Erhöhung der Eliminations-Halbwertszeit (auf 5,4 Stunden).
Eine Studie bei Patienten mit schweren Nierenfunktionsstörungen, die regelmäßige Hämodialysen benötigten, zeigte, dass die Pharmakokinetik von Ondansetron nach intravenöser Gabe praktisch unverändert bleibt (die Untersuchung erfolgte zwischen den Dialysen).
Patienten mit Leberfunktionsstörungen
Bei Patienten mit schweren Leberfunktionsstörungen ist die systemische Clearance von Ondansetron deutlich reduziert, die Eliminationshalbwertszeit (15 bis 32 Stunden) verlängert, und die orale Bioverfügbarkeit nähert sich infolge der verringerten prä-systemischen Verstoffwechselung 100 %.
5.3 Präklinische Daten zur Sicherheit
Basierend auf den konventionellen Studien zur Toxizität bei wiederholter Gabe, Genotoxizität und zum kanzerogenen Potenzial lassen die präklinischen Daten keine besonderen Gefahren für den Menschen erkennen.
Ondansetron und seine Metaboliten reichern sich in der Milch von Ratten mit einem Milch:Plasma-Verhältnis von 5,2:1 an.
Eine Studie an klonierten humanen kardialen Ionenkanälen hat gezeigt, dass Ondansetron das Potenzial besitzt, die kardiale Repolarisierung über eine Blockade der hERG-Kaliumkanäle zu beeinflussen. In einer Thorough-QT-Studie mit gesunden Probanden wurde eine dosisabhängige Verlängerung des QT-Intervalls beobachtet.
6. PHARMAZEUTISCHE ANGABEN
6.1 Liste der sonstigen Bestandteile
Zofran 4 mg Filmtabletten/Zofran 8 mg Filmtabletten Lactose
Mikrokristalline Cellulose Vorverkleisterte Stärke (Mais)
Magnesiumstearat (Ph. Eur.)
Hypromellose Titandioxid (E 171)
Eisen(III)-hydroxid-oxid (E 172).
Zofran 4 mg Zydis Linguai/Zofran 8 mg Zydis Lingual Gelatine
Mannitol (Ph. Eur.)
Aspartam
Methyl(4-hydroxybenzoat), Natriumsalz (E 219)
Propyl(4-hydroxybenzoat), Natriumsalz (E 217)
Erdbeer-Aroma (enthält Alkohol).
Zofran Lösung Citronensäure Natriumcitrat Natriumbenzoat (E 211)
Gereinigtes Wasser
Sorbitol-Lösung 70 % (kristallisierend) (Ph. Eur.) (E 420)
Erdbeer-Aroma (enthält Alkohol).
Zofran i. v. 4 mg/Zofran i. v. 8 mg Natriumchlorid Natriumcitrat 2 H2O Citronensäure-Monohydrat Wasser für Injektionszwecke.
6.2 Inkompatibilitäten
Orale Darreichungsformen Nicht zutreffend.
Intravenöse Darreichungsformen
Zofran Injektionslösungen sollen generell nicht in derselben Spritze oder Infusionsflasche mit anderen arzneimittelhaltigen Lösungen oder nicht überprüften Infusionslösungen gemischt werden (siehe Abschnitt 6.6).
Zofran Injektionslösungen sollen nur mit den empfohlenen Infusionslösungen gemischt werden (siehe Abschnitt 6.6).
6.3 Dauer der Haltbarkeit
36 Monate.
Zofran Lösung zusätzlich
Nach Anbruch 4 Wochen verwendbar.
6.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung
Zofran 4 mg Fiimtabietten/Zofran 8 mg Filmtabletten/Zofran i. v. 4 mg/Zofran i.v. 8 mg Nicht über 30 °C lagern.
Zofran 4 mg Zydis Linguai/Zofran 8 mg Zydis Lingual Keine.
Zofran Lösung
Aufrecht lagern. Nicht im Kühlschrank aufbewahren.
Zofran i. v. 4 mg/Zofran i. v. 8 mg
In der Originalverpackung aufbewahren, um den Inhalt vor Licht zu schützen.
6.5 Art und Inhalt der Behältnisse
Zofran 4 mg Fiimtabietten 6 Filmtabletten 10 Filmtabletten
Klinikpackungen mit 10 x 6 Filmtabletten Klinikpackungen mit 10 x 10 Filmtabletten Klinikpackungen mit 50 x 10 Filmtabletten Schüttpackung mit 500 Filmtabletten
Zofran 8 mg Fiimtabietten 6 Filmtabletten 10 Filmtabletten
Klinikpackungen mit 10 x 6 Filmtabletten Klinikpackungen mit 10 x 10 Filmtabletten Klinikpackungen mit 50 x 10 Filmtabletten Schüttpackung mit 500 Filmtabletten
Zofran 4 mg Zydis Linguai 6 Schmelztabletten 10 Schmelztabletten
Klinikpackungen mit 10 x 6 Schmelztabletten Klinikpackungen mit 10 x 10 Schmelztabletten
Zofran 8 mg Zydis Linguai 6 Schmelztabletten 10 Schmelztabletten
Klinikpackungen mit 10 x 6 Schmelztabletten Klinikpackungen mit 10 x 10 Schmelztabletten
Zofran Lösung
1 Flasche mit 50 ml Lösung
Klinikpackung mit 10 Flaschen mit 50 ml Lösung
Klinikpackung mit 50 Flaschen mit 50 ml Lösung
Zofran i. v. 4 mg
Packung mit 5 Ampullen zu je 2 ml Injektionslösung Klinikpackungen mit 10 x 5 Ampullen zu je 2 ml Injektionslösung Klinikpackung mit 5 x (10 x 5) Ampullen zu je 2 ml Injektionslösung
Zofran i. v. 8 mg
Packung mit 5 Ampullen zu je 4 ml Injektionslösung Klinikpackungen mit 10 x 5 Ampullen zu je 4 ml Injektionslösung Klinikpackung mit 5 x (10 x 5) Ampullen zu je 4 ml Injektionslösung Klinikpackung mit 10 x (10 x 5) Ampullen zu je 4 ml Injektionslösung
Es werden möglicherweise nicht alle Packungsgrößen in Verkehr gebracht.
6.6 Besondere Vorsichtsmaßnahmen für die Beseitigung und sonstige Hinweise zur Handhabung
Orale Darreichungsformen:
Keine besonderen Anforderungen.
Intravenöse Darreichungsformen:
Zofran i.v. 4 mg und Zofran i.v. 8 mg dürfen nicht im Autoklaven sterilisiert werden.
Zofran i.v. 4 mg/Zofran i.v. 8 mg ist mit folgenden gebräuchlichen Infusionslösungen mischbar:
Kochsalzlösung 0,9 %, Glucoselösung 5 %,
Mannitollösung 10 %, Ringerlösung,
Kaliumchlorid-/Natriumchloridlösung (0,3 %/0,9 %),
Kaliumchlorid-/Glucoselösung (0,3 %/5 %).
Die Lösungen sollen vor Gebrauch frisch zubereitet werden.
Die Kompatibilitätsuntersuchungen mit den oben genannten Lösungen zeigten, dass die Mischungen bis zu 7 Tage stabil sind (bei Raumtemperatur oder im Kühlschrank).
Verabreichung mit anderen Arzneimittellösungen
Die folgenden Infusionslösungen dürfen nur über ein Y-Stück dem Zofran enthaltenden Infusionssystem zugegeben werden, wobei die Ondansetron-Konzentration im Bereich von 16 bis 160 pg/ml (z. B. 8 mg/500 ml bzw. 8 mg/50 ml) und die Ondansetron-Infusionsrate bei 1 mg/Stunde liegen sollte.
|
Cisplatin-haltige Lösungen |
Die Konzentration Cisplatin-haltiger Lösungen, die über einen Zeitraum von einer bis acht Stunden gegeben werden kann, darf 0,48 mg/ml (z. B. 240 mg/500 ml) nicht überschreiten. |
|
Fluorouracil-haltige Lösungen |
Die Konzentration Fluorouracil-haltiger Lösungen, die mit einer Infusionsrate von mindestens 20 ml/Stunde (500 ml/24 Stunden) gegeben werden kann, darf 0,8 mg/ml (z. B. 2,4 g/3 l oder 400 mg/500 ml) nicht überschreiten. Höhere FluorouracilKonzentrationen führen zu einer Fällung des Ondansetrons. Die Fluorouracil-haltigen Lösungen können Magnesiumchlorid bis zu einer Konzentration von 0,045 % (m/v) enthalten. |
|
Carboplatin-haltige Lösungen |
Die Konzentration Carboplatin-haltiger Lösungen, die über einen Zeitraum von 10 Minuten bis zu einer Stunde gegeben werden kann, darf den Bereich 0,18 mg/ml bis 9,9 mg/ml (z. B. 90 mg/500 ml bzw. 990 mg/100 ml) nicht überschreiten. |
|
Etoposid-haltige Lösungen |
Die Konzentration Etoposid-haltiger Lösungen, die über einen Zeitraum von 30 Minuten bis zu einer Stunde gegeben werden kann, darf den Bereich 0,14 mg/ml bis 0,25 mg/ml (z. B. 70 mg/500 ml bzw. 250 mg/1 l) nicht überschreiten. |
|
Ceftazidim-haltige Lösungen |
Ceftazidim-Dosen von 250 bis 2000 mg, die nach den Angaben des Herstellers zubereitet werden (2,5 ml Wasser für Injektionszwecke für 250 mg und 10 ml für 2 g Ceftazidim), können als i.v.-Bolusinjektion über ca. 5 Minuten gegeben werden. |
|
Cyclophosphamid-haltige Lösungen |
Dosen von 100 mg bis 1 g Cyclophosphamid, die nach den Angaben des Herstellers zubereitet werden (5 ml Wasser für Injektionszwecke für 100 mg Cyclophosphamid), werden als i.v.-Bolusinjektion über ca. 5 Minuten gegeben. |
|
Doxorubicin-haltige Lösungen |
Dosen von 10 bis 100 mg Doxorubicin, die nach den Angaben des Herstellers zubereitet werden (5 ml Wasser für Injektionszwecke für 10 mg Doxorubicin), werden als i.v.-Bolusinjektion über ca. 5 Minuten gegeben. |
|
Dexamethason-21- dihydrogenphosphat, Dinatriumsalz |
20 mg Dexamethason-21-dihydrogenphosphat, Dinatriumsalz können als langsame intravenöse Injektion über 2 bis 5 Minuten mittels eines Y-Stückes dem Zofran enthaltenden Infusionssystem zugesetzt werden, mit dem 8 oder 16 mg Ondansetron in 50 bis 100 ml einer kompatiblen Infusionslösung (siehe Mischbarkeit von Zofran i.v. 4 mg und Zofran i.v. 8 mg) als Kurzzeit-Infusion über ca. 15 Minuten verabreicht werden. Die Kompatibilität von Dexamethason-21-dihydrogenphosphat mit Ondansetron wurde mittels Gabe dieser Arzneimittel über dasselbe Infusionsbesteck in Konzentrationen von 32 pg/ml bis 2,5 mg/ml Dexamethason-21-dihydrogenphosphat und 8 pg/ml bis 1 mg/ml Ondansetron gezeigt. |
Nach Anbruch der Ampullen ist der Rest zu verwerfen.
|
22.07.2016 |
Seite 23 |
MS 07/16 | |
|
V 004 |
7. INHABER DER ZULASSUNG
Novartis Pharma GmbH 90327 Nürnberg
Hausadresse:
Roonstraße 25 90429 Nürnberg Telefon: (09 11) 273-0 Telefax: (09 11) 273-12 653 Internet/E-Mail: www.novartis.de
Info-Service:
Telefon: (0 18 02) 23 23 00 (0,06 € pro Anruf aus dem deutschen Festnetz; max. 0,42 € pro Minute aus dem deutschen Mobilfunknetz)
Telefax: (09 11) 273-12 160
Mitvertrieb:
Hexal AG Industriestraße 25 83607 Holzkirchen Telefon: (08024) 908-0 Telefax: (08024) 908-1290 Internet/E-Mail: service@hexal.com
8. ZULASSUNGSNUMMERN
Zofran 4 mg Filmtabletten Zul.-Nr.: 22008.00.01
Zofran 8 mg Filmtabletten Zul.-Nr.: 22008.01.01
Zofran 4 mg Zydis Lingual Zul.-Nr.: 41349.00.00
Zofran 8 mg Zydis Lingual Zul.-Nr.: 41349.01.00
Zofran Lösung Zul.-Nr.: 37196.00.00
Zofran i.v. 4 mg Zul.-Nr.: 22008.00.00
Zofran i.v. 8 mg Zul.-Nr.: 22008.01.00
9. DATUM DER ERTEILUNG DER ZULASSUNGEN/VERLÄNGERUNG DER ZULASSUNGEN
Zofran 4 mg Fiimtabietten/Zofran 8 mg Filmtabletten
Datum der Erteilung der Zulassung: 31.10.1990
Datum der letzten Verlängerung der Zulassung: 25.06.2001
Zofran 4 mg Zydis Linguai/Zofran 8 mg Zydis Lingual
Datum der Erteilung der Zulassung: 23.11.1998
Datum der letzten Verlängerung der Zulassung: 19.07.2010
Zofran Lösung
Datum der Erteilung der Zulassung: 30.12.1998
Datum der letzten Verlängerung der Zulassung: 19.07.2010
Zofran i. v. 4 mg/Zofran i. v. 8 mg
Datum der Erteilung der Zulassung: 31.10.1990
Datum der letzten Verlängerung der Zulassung: 25.06.2001
10. STAND DER INFORMATION
August 2016
11. VERKAUFSABGRENZUNG
Verschreibungspflichtig.
((Novartis Logo))
Freigabeversion 1 - IB-F