Aarane N
Gebrauchsinformation: Information für Anwender
AARANE® N 1 mg/0,5 mg pro Sprühstoß Druckgasinhalation, Suspension
Wirkstoffe: Natriumcromoglicat (Ph. Eur.)/Reproterolhydrochlorid
Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen, denn sie enthält wichtige Informationen.
- Heben Sie die Packungsbeilage auf. Vielleicht möchten Sie diese später nochmals lesen.
- Wenn Sie weitere Fragen haben, wenden Sie sich an Ihren Arzt oder Apotheker.
- Dieses Arzneimittel wurde Ihnen persönlich verschrieben. Geben Sie es nicht an Dritte weiter. Es kann anderen Menschen schaden, auch wenn diese die gleichen Beschwerden haben wie Sie.
- Wenn Sie Nebenwirkungen bemerken, wenden Sie sich an Ihren Arzt oder Apotheker. Dies gilt auch für Nebenwirkungen, die nicht in dieser Packungsbeilage angegeben sind. Siehe Abschnitt 4.
Was in dieser Packungsbeilage steht
1. Was ist AARANE N und wofür wird es angewendet?
2. Was sollten Sie vor der Anwendung von AARANE N beachten?
3. Wie ist AARANE N anzuwenden?
4. Welche Nebenwirkungen sind möglich?
5. Wie ist AARANE N aufzubewahren?
6. Inhalt der Packung und weitere Informationen
1. Was ist AARANE N und wofür wird es angewendet?
AARANE N ist ein entzündungshemmendes und atemwegserweiterndes Mittel.
AARANE N wird angewendet zur Verhütung und Behandlung von Atemnot bei Asthma, das heißt allergischem Asthma und nicht allergischem Asthma sowie endogenen Asthmaformen, ausgelöst durch Belastung, Stress oder Infekt bei Patienten, die neben einer antientzündlichen Basistherapie zusätzlich eine bronchialerweiternde Therapie benötigen.
2. Was sollten Sie vor der Anwendung von AARANE N beachten?
AARANE N darf nicht angewendet werden,
- wenn Sie allergisch gegen Natriumcromoglicat, Reproterolhydrochlorid, Levomenthol/Pfefferminzöl oder einen der in Abschnitt 6. genannten sonstigen Bestandteile dieses Arzneimittels sind,
- bei Säuglingen und Kleinkindern unter 2 Jahren (Gefahr eines Kehlkopfkrampfes).
AARANE N sollte bei frischem Herzinfarkt, Herzrhythmusstörungen, hypertropher obstruktiver Kardiomyopathie (krankhafte Vergrößerung des Herzens), schwerer KHK (krankhafte Veränderung der Herzkranzgefäße), Phäochromozytom (Nebennierengeschwulst) und schwerer Schilddrüsenüberfunktion nicht oder nur nach sorgfältiger Nutzen-Risiko-Abwägung durch Ihren behandelnden Arzt angewendet werden. Dies gilt auch, wenn diese Angaben bei Ihnen früher einmal zutrafen.
Warnhinweise und Vorsichtsmaßnahmen
Bei Patienten mit tachykarden Herzrhythmusstörungen (Herzrasen) darf die Anwendung von AARANE N nur unter besonderen Vorsichtsmaßnahmen, z. B. Überwachung (EKG-Kontrolle), erfolgen.
Beim Auftreten eosinophiler Pneumonien (Spezialform einer Lungenentzündung) während einer Behandlung mit AARANE N sollte diese unverzüglich abgebrochen werden.
Da nach Anwendung hoher Dosen der Blutzuckerspiegel sowie die freien Fettsäuren ansteigen können, ist bei Diabetikern eine regelmäßige Blutzuckerkontrolle erforderlich. Bei einer höherdosierten Anwendung ist ebenfalls eine Kontrolle des Kaliumspiegels im Blutserum notwendig, besonders bei gleichzeitiger Behandlung mit wasserausschwemmenden Arzneimitteln (Diuretika) und solchen zur Behandlung von Herzleistungsstörungen (z. B. Herzglykosiden).
Ein ansteigender Bedarf von AARANE N ist ein Anzeichen für eine Verschlechterung der Erkrankung. In dieser Situation muss der Behandlungsplan durch den Arzt überdacht und gegebenenfalls durch die Gabe zusätzlicher entzündungshemmender oder weiterer Arzneimittel neu festgelegt werden.
Kommt es trotz der verordneten Behandlung zu keiner befriedigenden Besserung oder gar zu einer Verschlechterung des Leidens, ist ärztliche Beratung erforderlich, um die Behandlung gegebenenfalls durch eine Kombination mit anderen Arzneimitteln (zusätzlichen entzündungshemmenden wie Kortikoiden, die Bronchien erweiternden Stoffen wie Theophyllin) zu ergänzen oder eine Änderung der Dosierung festzulegen.
Eine plötzliche und zunehmende Verschlechterung der Asthmabeschwerden kann lebensbedrohlich sein. In diesen Fällen muss unverzüglich ärztliche Hilfe in Anspruch genommen werden. Eine erhebliche Überschreitung der vorgegebenen Dosis kann gefährlich sein.
Es ist wiederholt über ein erhebliches Risiko für das Auftreten schwerer Komplikationen der Grunderkrankung bis hin zu Todesfällen berichtet worden, wenn das Asthma mit ß-sympathomimetikahaltigen Monopräparaten zur Inhalation über längere Zeit mit hohen oder überhöhten Dosen behandelt wurde und die entzündungshemmende Behandlung unzureichend war.
Die ursächlichen Zusammenhänge konnten bisher nicht hinreichend geklärt werden. Eine entscheidende Rolle scheint aber die unzureichend entzündungshemmende Behandlung zu spielen.
Kinder
Kinder sollten ihrem Alter entsprechend vom Arzt über die einzuhaltende Dosierung sowie mögliche Nebenwirkungen unterrichtet werden.
Auswirkungen bei Fehlgebrauch zu Dopingzwecken
Die Anwendung von AARANE N kann bei Dopingkontrollen zu positiven Ergebnissen führen. Zudem kann es bei Missbrauch von AARANE N als Dopingmittel zu einer Gefährdung der Gesundheit kommen.
Anwendung von AARANE N zusammen mit anderen Arzneimitteln
Informieren Sie Ihren Arzt oder Apotheker, wenn Sie andere Arzneimittel einnehmen/anwenden, kürzlich andere Arzneimittel eingenommen/angewendet haben oder beabsichtigen, andere Arzneimittel einzunehmen/anzuwenden.
AARANE N wird wie folgt beeinflusst.
Verstärkung der Wirkung und möglicherweise Verstärkung von Nebenwirkungen:
- Bei gleichzeitiger Anwendung mit anderen atemwegserweiternden Mitteln wie Adrenergika oder Methylxanthinen (z. B. Theophyllin) ist auf eine mögliche Verstärkung der für Reproterolhydrochlorid beschriebenen Wirkungen und Nebenwirkungen zu achten.
- Die gleichzeitige Anwendung mit Monoaminoxidasehemmern (MAO-A-Hemmern) und trizyklischen Antidepressiva kann eine verstärkte Wirkung von Reproterolhydrochlorid auf das Herz-Kreislauf-System auslösen.
Abschwächung der Wirkung:
- Die gleichzeitige Anwendung mit blutdrucksenkenden Mitteln (in erster Linie ß-Rezeptorenblocker) hebt die Wirkung von Reproterolhydrochlorid auf und kann daher zu einem Asthmaanfall führen.
Anwendung von AARANE N zusammen mit Nahrungsmitteln, Getränken und Alkohol
Generell sollte bei einer medikamentösen Behandlung auf die Einnahme alkoholischer Getränke verzichtet werden. Ansonsten sind keine besonderen Vorsichtsmaßnahmen erforderlich.
Schwangerschaft und Stillzeit
Wenn Sie schwanger sind oder stillen oder wenn Sie vermuten, schwanger zu sein, oder beabsichtigen, schwanger zu werden, fragen Sie vor der Anwendung dieses Arzneimittels Ihren Arzt oder Apotheker um Rat.
In der Schwangerschaft darf AARANE N nur in schweren Krankheitsfällen unter strenger Abwägung des Nutzen-Risiko-Verhältnisses angewendet werden, da keine ausreichenden Erfahrungen mit AARANE N in der Schwangerschaft bestehen. Bei Neugeborenen sind beschleunigter Herzschlag und Absinken des Blutzuckerwertes beschrieben worden, wenn bei der Mutter ß-Sympathomimetika (bestimmte Arzneimittel, dazu gehört auch Reproterolhydrochlorid) angewendet worden waren.
Es ist nicht bekannt, ob Natriumcromoglicat in die Muttermilch übergehen kann. Nach inhalativer Anwendung von Reproterolhydrochlorid ist die in den Blutkreislauf der Mutter gelangte Dosis nicht messbar. Trotzdem sollten Sie Aarane während der Stillzeit nur anwenden, wenn der Arzt es für erforderlich hält.
Verkehrstüchtigkeit und Fähigkeit zum Bedienen von Maschinen
Durch individuell auftretende unterschiedliche Reaktionen kann in Einzelfällen, insbesondere zu Behandlungsbeginn sowie bei höherer oder überhöhter Dosierung, die Fähigkeit zur aktiven Teilnahme am Straßenverkehr oder zum Bedienen von Maschinen beeinträchtigt sein. Dies gilt besonders bei gleichzeitiger Einnahme von Alkohol, Beruhigungs- und Schlafmitteln.
3. Wie ist AARANE N anzuwenden?
Wenden Sie dieses Arzneimittel immer genau nach Absprache mit Ihrem Arzt an. Fragen Sie bei Ihrem Arzt oder Apotheker nach, wenn Sie sich nicht sicher sind.
Falls vom Arzt nicht anders verordnet, ist die übliche Dosis:
Die Dosierung richtet sich nach Art und Schwere der Erkrankung und muss dem Einzelfall angepasst werden.
Soweit nicht anders verordnet, gelten für Erwachsene und Kinder, sofern diese vom Alter her in der Lage sind, ein Dosieraerosol korrekt zu handhaben, folgende Empfehlungen:
Die Dosierung richtet sich nach dem Ausmaß der Atemwegsbeschwerden. Die Anfangsdosierung beträgt 4 x täglich 2 Sprühstöße AARANE N, das heißt je 2 Inhalationen nach dem Aufstehen, zur Mittagszeit, am frühen Abend und vor dem Schlafengehen, wobei ein Abstand von mindestens 3 Stunden einzuhalten ist. Nach Erreichen der therapeutischen Wirkung kann die Tagesdosis unter ärztlicher Anleitung schrittweise verringert werden, solange die Symptome unter Kontrolle sind.
Zur gezielten Vorbeugung bei Anstrengungsasthma oder vorhersehbarem Allergenkontakt können etwa 10-15 Minuten vorher 2 Sprühstöße AARANE N inhaliert werden. Dies ist in der Regel jedoch nur erforderlich, wenn die vorhergehende Inhalation mehr als 3 Stunden zurückliegt.
Zur Akutbehandlung plötzlich auftretender Bronchialkrämpfe und anfallsweise auftretender Atemnot kann zusätzlich ein weiterer Sprühstoß AARANE N inhaliert werden. Dies führt in den meisten Fällen bereits zu einer raschen Erleichterung der Atmung. Sollte sich die Atemnot 5 Minuten nach Inhalation des ersten Sprühstoßes nicht spürbar gebessert haben, kann ein weiterer Sprühstoß inhaliert werden. Kann ein schwerer Anfall von Luftnot auch durch einen zweiten Sprühstoß nicht behoben werden, können weitere Sprühstöße erforderlich werden. In diesen Fällen muss unverzüglich ärztliche Hilfe in Anspruch genommen werden.
Die gesamte Tagesdosis soll 16 Sprühstöße nicht überschreiten, da eine höhere Dosierung im Allgemeinen keinen zusätzlichen Nutzen für die Behandlung erwarten lässt, aber die Wahrscheinlichkeit des Auftretens auch schwerwiegender Nebenwirkungen erhöht.
Art und Dauer der Anwendung
AARANE N ist für die Anwendung zur Inhalation vorgesehen und sollte gemäß den Anweisungen des verschreibenden Arztes oder gemäß der Dosierungsanleitung angewendet werden.
Beachten Sie bitte die folgende Gebrauchsanleitung zur Handhabung des Dosieraerosols.
Gebrauchsanleitung zur Handhabung des Dosieraerosols
Bitte genau beachten!
Zur Anwendung ist das Dosieraerosol senkrecht, mit dem Boden nach oben zu halten, unabhängig von der Körperposition, in der inhaliert wird. Nach Möglichkeit sollte die Anwendung im Sitzen oder Stehen erfolgen.
Vor der Erstanwendung bitte 4 Sprühstöße in die Luft abgeben, um das Dosieraerosol gebrauchsfertig zu machen! Wurde AARANE N länger als 2 Tage nicht angewendet, müssen mindestens 2 Sprühstöße vor Gebrauch abgegeben werden.
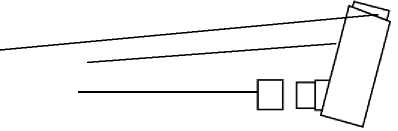
2. Dosieraerosol mit dem Mundstück nach unten kräftig schütteln.
Das AARANE N-Dosieraerosol
- Metallbehälter mit Wirkstoffen
- weißes Kunststoffgehäuse mit Mundstück
- grüne Schutzkappe
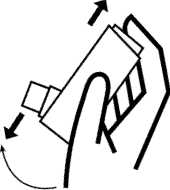
1. Grüne Schutzkappe entfernen.
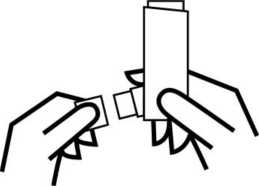
4. Das Mundstück mit den Lippen fest umschließen. Langsam und tief einatmen und gleichzeitig den Metallbehälter nach unten drücken, damit ein Sprühstoß freigesetzt wird.
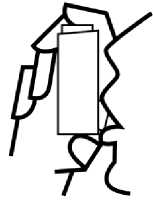
Tief ausatmen. Dabei nicht in das Mundstück hineinatmen.

5. Das Mundstück aus dem Mund nehmen. Atem einige Sekunden anhalten. Anschließend langsam durch die Nase ausatmen.
6. Im Regelfall nach etwa einer Minute die Inhalation unter Beachtung der Punkte 3 bis 5 wiederholen. Danach Schutzkappe aufsetzen.
Wichtige Hinweise zur Pflege und Reinigung
Bei AARANE N handelt es sich um eine Arzneimittelzubereitung, bei der zwei Wirkstoffe in fein verteilter, fester Form vorliegen. Selbst bei korrekter Anwendung sind Ablagerungen im Kunststoffgehäuse unvermeidlich.
Damit das Dosieraerosol immer funktioniert, muss das Kunststoffgehäuse sauber gehalten werden, indem es gepflegt, das heißt täglich gereinigt wird. So wird verhindert, dass die Dosierung ungenau wird oder die Sprühöffnung verstopft und deshalb kein Sprühstoß mehr freigesetzt werden kann.
Zum Reinigen des Dosieraerosols gehen Sie wie folgt vor:
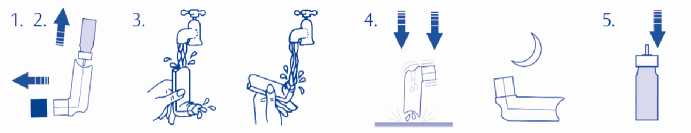
1. Entfernen Sie die grüne Schutzkappe.
2. Nehmen Sie den Metallbehälter aus dem weißen Kunststoffgehäuse heraus. (Abb. 6)
3. Spülen Sie das Kunststoffgehäuse zuerst von oben (Seite mit der Öffnung, in die der Metallbehälter eingesetzt wird), dann von unten (Seite, auf die die grüne Schutzkappe aufgesetzt wird) jeweils für eine Minute mit handwarmen Wasser (ca. 45 °C) durch, um Ablagerungen in der Sprühöffnung zu lösen. (Abb. 7, 8)
4. Entfernen Sie überschüssiges Wasser von der Innenseite des Kunststoffgehäuses, indem Sie es mit der Öffnung, in die der Metallbehälter eingesetzt wird, auf eine harte Oberfläche klopfen und lassen Sie es gut trocknen (z. B. über Nacht). (Abb. 9, 10)
5. Vergewissern Sie sich, dass das Kunststoffgehäuse gänzlich trocken ist und dass die Gummimanschette fest auf dem Metallbehälter sitzt. Setzen Sie dann alle Teile wieder zusammen,
d. h., stecken Sie den Metallbehälter wieder in das Kunststoffgehäuse, und setzen Sie die Schutzkappe wieder auf das Kunststoffgehäuse. (Abb. 11)
Zusätzliche Hinweise
• Die Gummimanschette auf dem Metallbehälter darf nicht entfernt werden, da sie für das einwandfreie Funktionieren des Dosieraerosols wichtig ist.
• Da einer der beiden in AARANE N enthaltenen Wirkstoffe wasseranziehend ist, vermeiden Sie ein Aufbewahren des Dosieraerosols in feuchter Umgebung, um ein Verkleben bzw. Verstopfen zu verhindern.
• Sollte das Dosieraerosol verstopfen, entfernen Sie die grüne Schutzkappe und nehmen den Metallbehälter aus dem weißen Kunststoffgehäuse heraus (vgl. Schritt 1 und 2). Weichen Sie das Kunststoffgehäuse 20 Minuten in heißem Leitungswasser ein und wiederholen Sie die Schritte 3 bis 5.
• Versuchen Sie niemals eine Verstopfung des Dosieraerosols mit einer Nadel oder ähnlichen Gegenständen zu beseitigen. Sie würden es beschädigen.
Dauer der Anwendung
Über die Dauer der Anwendung entscheidet Ihr behandelnder Arzt.
Spezielle Therapiehinweise
Die Behandlung des Asthmas ist im Regelfall eine Dauerbehandlung und sollte dem Schweregrad entsprechend stufenweise erfolgen. Der Erfolg der Behandlung sollte durch regelmäßige ärztliche Untersuchungen überprüft werden.
Es ist möglicherweise gefährlich, ohne ärztliche Anweisung den Gebrauch von AARANE N von sich aus zu erhöhen.
Ein ansteigender Bedarf von AARANE N ist ein Anzeichen für eine Verschlechterung der Erkrankung. In dieser Situation muss der Behandlungsplan durch den Arzt überdacht und gegebenenfalls durch die Gabe zusätzlicher entzündungshemmender oder weiterer Arzneimittel neu festgelegt werden.
Zur ärztlichen Beurteilung des Krankheitsverlaufes sowie des Erfolges der atemwegserweiternden und entzündungshemmenden Behandlung ist eine tägliche Selbstkontrolle nach ärztlicher Anleitung wichtig. Diese erfolgt z. B. durch die Aufzeichnung des mit dem Peak-flow-Meter gemessenen Atemstoßes.
Bitte sprechen Sie mit Ihrem Arzt oder Apotheker, wenn Sie den Eindruck haben, dass die Wirkung von AARANE N zu stark oder zu schwach ist.
Wenn Sie eine größere Menge von AARANE N angewendet haben, als Sie sollten
Überdosierungserscheinungen sind überwiegend auf den in AARANE N enthaltenen Wirkstoff Reproterolhydrochlorid zurückzuführen.
Bei starker Überdosierung von Reproterolhydrochlorid kann es zu Herzrasen, Herzklopfen, Herzrhythmusstörungen, niedrigem Blutdruck bis hin zum Schock, Übersäuerung des Körpers durch erhöhte Milchsäurekonzentration im Blut (Laktatazidose), Ruhelosigkeit, Brustschmerzen, Kopfschmerzen und heftigem Zittern an den Händen, aber auch am ganzen Körper kommen. Des Weiteren kann die Kaliumkonzentration im Serum absinken sowie der Blutzuckerwert ansteigen.
Bei Verdacht auf eine Überdosierung mit AARANE N dürfen keine weiteren Inhalationen erfolgen, und es ist sofort ein Arzt zu benachrichtigen, der eine symptomatische Behandlung einleiten kann.
Falls große Mengen des Dosieraerosols versehentlich verschluckt wurden, sollte eine Magenspülung erwogen werden; Aktivkohle und Abführmittel können die unerwünschte Wirkung des ß2-Sympathomimetikums vermindern. Als Gegenmittel eignen sich ßj-Rezeptorenblocker (z. B. Atenolol, Metoprolol), jedoch sind auch diese nur behutsam einzusetzen, um bei Patienten mit Asthma eine Verstärkung der Atemnot möglichst zu vermeiden. Bei Patienten mit Herzschwäche ist es besser, Beruhigungsmittel (z. B. Benzodiazepine) zu verabreichen. Gleichzeitig sollte die Herzfunktion mittels EKG überwacht werden.
Wenn Sie die Anwendung von AARANE N vergessen haben
Arzneimittel sollten grundsätzlich entsprechend den Empfehlungen des Arztes oder gemäß der Dosierungsanleitung angewendet werden.
Sollten Sie dennoch einmal die vorgeschriebene Anwendung von AARANE N vergessen haben, setzen Sie die Behandlung ganz normal fort. Auf keinen Fall sollten Sie beim nächsten Mal die doppelte Menge inhalieren.
Wenn Sie die Behandlung mit AARANE N abbrechen
Falls Sie die Behandlung unterbrechen oder vorzeitig beenden wollen, informieren Sie bitte Ihren Arzt, damit er mit Ihnen weitere Behandlungsmaßnahmen besprechen kann.
Wenn Sie weitere Fragen zur Anwendung dieses Arzneimittels haben, wenden Sie sich an Ihren Arzt oder Apotheker.
4. Welche Nebenwirkungen sind möglich?
Wie alle Arzneimittel kann auch dieses Arzneimittel Nebenwirkungen haben, die aber nicht bei jedem auftreten müssen.
Bei den Häufigkeitsangaben zu Nebenwirkungen werden folgende Kategorien zugrunde gelegt:
|
Sehr häufig: |
mehr als 1 Behandelter von 10 |
|
Häufig: |
1 bis 10 Behandelte von 100 |
|
Gelegentlich: |
1 bis 10 Behandelte von 1.000 |
|
Selten: |
1 bis 10 Behandelte von 10.000 |
|
Sehr selten: |
weniger als 1 Behandelter von 10.000 |
|
Nicht bekannt: |
Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar |
Einige Nebenwirkungen sind im Folgenden ohne Häufigkeitsangaben aufgeführt, das heißt: Die Häufigkeit konnte anhand der verfügbaren Daten nicht berechnet werden.
Reproterolhydrochlorid
Gelegentlich kann Reproterolhydrochlorid, insbesondere bei besonders empfindlichen Patienten und/oder höherer Dosierung feines Fingerzittern, Herzklopfen, Unruhegefühl oder mit nicht bekannter Häufigkeit Kopfschmerzen hervorrufen, was jedoch bei Fortführung der Behandlung nach 1-2 Wochen meistens wieder abklingt.
Ein im Zusammenhang mit der Behandlung mit AARANE N verstärktes Auftreten solcher Symptome sowie Herzrasen sind jedoch Zeichen einer Überdosierung. Das Arzneimittel sollte in solchen Fällen niedriger dosiert werden; der behandelnde Arzt ist umgehend zu informieren.
Bei der Behandlung mit Reproterolhydrochlorid kann die Kaliumkonzentration im Serum absinken sowie der Blutzuckerwert ansteigen (beachten Sie hierzu bitte auch den Warnhinweis unter „Warnhinweise und Vorsichtsmaßnahmen“). Die beschriebenen Effekte kommen jedoch im Allgemeinen erst unter höherer Dosierung zur Geltung.
Weitere unerwünschte Wirkungen sind beschrieben worden: Nervosität, Hyperaktivität, Schlafstörungen, Halluzinationen (insbesondere bei Kindern bis 12 Jahren), Schwindel, Herzrhythmusstörungen, verminderte Blutversorgung des Herzens (myokardiale Ischämie), Beeinflussung des Blutdrucks (Erniedrigung oder Erhöhung).
Natriumcromoglicat
Nach einer Inhalation von Natriumcromoglicat kann es zu einer mit Husten einhergehenden Reizung des Rachens und der Luftröhre kommen, die sehr selten zu einer Verkrampfung der Bronchien führen kann. In sehr seltenen Fällen kann der Bronchialkrampf so ausgeprägt sein, dass die Behandlung unterbrochen werden muss. Einer Verkrampfung der Bronchien wird in der vorliegenden Kombination durch das gleichzeitig inhalierte Reproterolhydrochlorid entgegengewirkt.
In sehr seltenen Fällen wurde das Auftreten eosinophiler Pneumonien (spezielle Form einer Lungenentzündung) beobachtet.
Sehr selten wurde über schwere allergische Sofortreaktionen (anaphylaktische Reaktionen) mit Krämpfen der Bronchialmuskulatur, niedrigem Blutdruck, Kreislaufversagen und Schwellung der Kehlkopfschleimhaut im Zusammenhang mit einer Natriumcromoglicat-Behandlung berichtet.
Weitere Überempfindlichkeitsreaktionen (Hautausschlag, Juckreiz, Nesselsucht, Haut- und Schleimhautschwellungen) und folgende unerwünschte Wirkungen sind beschrieben worden: Heiserkeit, Schwindel, Übelkeit, unangenehmer Geschmack, Gelenkschmerzen, Muskelschmerzen.
Andere mögliche Nebenwirkungen
AARANE N enthält als Aromastoff Dentomint mit Levomenthol/Pfefferminzöl. Bei entsprechend sensibilisierten Patienten können durch Levomenthol/Pfefferminzöl Überempfindlichkeitsreaktionen (einschließlich Atemnot) ausgelöst werden. Levomenthol/Pfefferminzöl kann bei Säuglingen und Kindern bis zu 2 Jahren einen Kehlkopfkrampf hervorrufen mit der Folge schwerer Atemstörungen.
Besondere Hinweise:
Bei Auftreten leichter Nebenwirkungen sollte AARANE N niedriger dosiert werden. Bei Auftreten schwerer Nebenwirkungen sollte AARANE N nicht mehr inhaliert und der Arzt umgehend über die bei Ihnen aufgetretenen Symptome informiert werden!
Meldung von Nebenwirkungen
Wenn Sie Nebenwirkungen bemerken, wenden Sie sich an Ihren Arzt oder Apotheker. Dies gilt auch für Nebenwirkungen, die nicht in dieser Packungsbeilage angegeben sind. Sie können Nebenwirkungen auch direkt dem
Bundesinstitut für Arzneimittel und Medizinprodukte Abt. Pharmakovigilanz Kurt-Georg-Kiesinger-Allee 3 D-53175 Bonn Website: www.bfarm.de
anzeigen. Indem Sie Nebenwirkungen melden, können Sie dazu beitragen, dass mehr Informationen über die Sicherheit dieses Arzneimittels zur Verfügung gestellt werden.
5. Wie ist AARANE N aufzubewahren?
Bewahren Sie dieses Arzneimittel für Kinder unzugänglich auf.
Sie dürfen dieses Arzneimittel nach dem auf dem Umkarton und dem Behältnis nach „Verwendbar bis“ angegebenen Verfalldatum nicht mehr verwenden. Das Verfalldatum bezieht sich auf den letzten Tag des angegebenen Monats.
Behälter steht unter Druck!
Vor Hitze, direkter Sonnenbestrahlung und Frost schützen!
Nicht gegen Flammen oder auf glühende Gegenstände sprühen!
Nicht gewaltsam öffnen oder verbrennen!
6. Inhalt der Packung und weitere Informationen Was AARANE N enthält
Die Wirkstoffe sind Natriumcromoglicat (Ph. Eur.) und Reproterolhydrochlorid.
Ein Sprühstoß zu 70 mg enthält 1 mg Natriumcromoglicat (Ph. Eur.) und 0,5 mg Reproterolhydrochlorid.
Pro Sprühstoß werden aus dem Ventil 1 mg Natriumcromoglicat sowie 0,5 mg Reproterolhydrochlorid freigesetzt (abgemessene Dosis). Dies entspricht einer aus dem Mundstück freigesetzten Dosis von 0,82 mg Natriumcromoglicat sowie 0,42 mg Reproterolhydrochlorid.
Die sonstigen Bestandteile sind:
Apafluran, Poly(oxyethylen)-25-glyceroltrioleat, Ethanol 96 %, Saccharin-Natrium 2 H2O, Dentomint PH/799959 Symrise (Aroma, enthält Levomenthol/Pfefferminzöl).
Wie AARANE N aussieht und Inhalt der Packung
1 Druckbehältnis enthält 10 ml Druckgasinhalation, Suspension zur Inhalation und reicht für mindestens 200 Sprühstöße.
AARANE N ist in Packungen mit 10 ml, 2 x 10 ml und 3 x 10 ml Druckgasinhalation, Suspension zur Inhalation sowie in Klinikpackungen mit 6 x 10 ml und 12 x 10 ml Druckgasinhalation, Suspension zur Inhalation erhältlich.
Pharmazeutischer Unternehmer
Sanofi-Aventis Deutschland GmbH 65926 Frankfurt am Main
Postanschrift:
Postfach 80 08 60 65908 Frankfurt am Main
Telefon: (01 80) 2 22 20 101
Telefax: (01 80) 2 22 20 111
Hersteller
Aventis Pharma, Holmes Chapel 72 London Road Holmes Chapel, Crewe Cheshire, CW4 8BE England
Diese Packungsbeilage wurde zuletzt überarbeitet im Dezember 2013.
Sehr geehrte Patientin, sehr geehrter Patient,
AARANE N enthält einen atemwegserweiternden (Reproterolhydrochlorid) und einen entzündungshemmenden (Natriumcromoglicat) Wirkstoff. Voraussetzung für den Erfolg der Behandlung mit AARANE N ist, dass Sie das Medikament entsprechend den Dosierungsempfehlungen Ihres Arztes anwenden.
Denken Sie bitte daran: Nur wenn Sie AARANE N gemäß den Anweisungen Ihres Arztes regelmäßig anwenden, kann das Arzneimittel seine volle Wirksamkeit entfalten.
Nutzen Sie die Möglichkeit zur Selbstkontrolle durch tägliche Bestimmung Ihres Atemstoßes mit einem Peak-flow-Meter. Das regelmäßige Aufschreiben der Ergebnisse ermöglicht Ihrem behandelnden Arzt eine bessere Beurteilung Ihrer Krankheit - eine wichtige Voraussetzung für Ihre Behandlung.
10
0,06 €/Anruf (dt. Festnetz); max. 0,42 €/min (Mobilfunk).