Mykotin Creme
Fachinformation
1. Bezeichnung des Arzneimittels
Mykotin® Creme
Wirkstoff: Miconazolnitrat
20,0 mg
2. Qualitative und quantitative Zusammensetzung
Wirkstoff:
1 g Creme enthält: Miconazolnitrat 20,0 mg
Vollständige Auflistung der sonstigen Bestandteile: siehe Abschnitt 6.1
3. Darreichungsform
Creme
4. Klinische Angaben
4.1 Anwendungsgebiete
- Interdigitalmykosen
- Mykosen der Haut und Hautfalten
- Oberflächliche Kandidosen
4.2 Dosierung, Art und Dauer der Anwendung
Dosierung:
Die Creme wird 1 - 3-mal täglich auf die erkrankten Hautregionen aufgetragen und leicht mit den Fingern einmassiert.
Art der Anwendung:
Die Creme ist zur Anwendung auf der Haut bestimmt.
Dauer der Anwendung:
Die Dauer der Behandlung richtet sich nach dem klinischen Bild. Die Behandlung sollte bis zur Verschwinden der positiven Pilzkulturen durchgeführt werden, mindestens jedoch noch 14 Tage nach Abklingen der Beschwerden. Zwischen dem letzten Auftragen und dem Anlegen einer Pilzkultur sollte ein therapiefreies Intervall von 3-4 Tagen liegen, damit evtl. Wirkstoffreste die Kultur nicht stören.
4.3 Gegenanzeigen
Mykotin® Creme darf nicht angewendet werden bei Patienten mit Überempfindlichkeit gegen den Wirkstoff Miconazol, Benzoesäure und andere Bestandteile der Creme.
Mykotin® Creme soll nicht an der laktierenden Mamma angewendet werden.
4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung
Benzoesäure kann leichte Reizungen an Haut, Augen und Schleimhäuten hervorrufen.
4.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen
Bei topischer Anwendung sind keine Wechselwirkungen bekannt und aufgrund der geringen Resorption auch nicht zu erwarten.
Bei einer Behandlung im Genital- oder Analbereich kann es wegen der enthaltenden Hilfsstoffe (Stearate und Paraffin) bei gleichzeitiger Anwendung von Kondomen aus Latex zu einer Verminderung der Reißfestigkeit und damit zur Beeinträchtigung der Sicherheit von Kondomen kommen.
4.6 Schwangerschaft und Stillzeit
Mykotin® Creme soll nicht an der laktierenden Mamma angewendet werden.
4.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen
Nicht zutreffend.
4.8 Nebenwirkungen
Bei der Bewertung von Nebenwirkungen werden folgende Häufigkeiten zugrunde gelegt:
|
Sehr häufig |
(> 1/10) |
|
Häufig |
(> 1/100 - < 1/10) |
|
Gelegentlich |
(> 1/1000 - < 1/100) |
|
Selten |
(> 1/10.000 - < 1/1000) |
|
Sehr selten |
(< 1/10.000) |
|
Nicht bekannt |
(Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar) |
Selten kann es unter der Anwendung von Mykotin® Creme zu Hautirritationen mit Rötung, Stechen, Brennen kommen. Systemische Nebenwirkungen bei lokaler Anwendung sind nicht bekannt.
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nut-zen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung dem Bundesinstitut für Arzneimittel und Medizinprodukte, Abt. Pharmakovigilanz, Kurt-Georg-Kiesinger-Allee 3, D-53175 Bonn, Website: www.bfarm.de, anzuzeigen.
4.9 Überdosierung
Entfällt.
5. Pharmakologische Eigenschaften
5.1 Pharmakodynamische Eigenschaften
Pharmakotherapeutische Gruppe:
Imidazol-Derivat / Azol-Antimykotikum Breitspektrum-Antimykotikum Miconazol
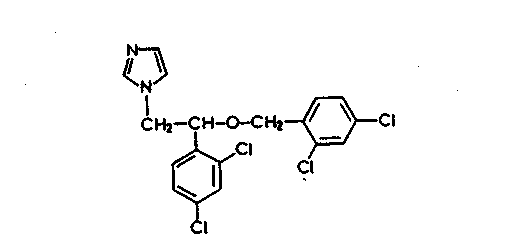
Miconazol wirkt in therapeutischen Dosen fungistatisch aufgrund der Hemmung der für den Zellaufbau essentiellen Ergosterinbiosynthese. Seine Wirkung erstreckt sich in vitro auf nahezu alle proliferierenden human- und tierpathogenen Pilze (MHK 0,001-1000 ^g/ml) sowie auf einige grampositive Bakterien wie Staphylokokken, Streptokokken und Strahlenpilze (Nocardia- und Streptomy-ces-Arten, MHK 0,1-10 ^g/ml), in deutlich geringerem Maße auch auf Cory-nebakterien und Trichomonas vaginalis. Unter klinischen Bedingungen wird jedoch bei topischen Pilzinfektionen, z.B. durch Hefen wie Candida- und Torulop-sis-Arten oder Dermatophyten eine deutliche Wirksamkeit beobachtet. Die Resistenzsituation ist bei proliferierenden Pilzen als günstig einzuschätzen. Echte Resistenzen sind nicht bekannt, jedoch können verschiedene morphologische Formen eines Organismus unterschiedlich empfindlich reagieren.
5.2 Pharmakokinetische Eigenschaften
Miconazol wird nach topischer Anwendung praktisch nicht, nach intravaginaler Anwendung nur zu einem sehr geringen Prozentsatz (< 1,4 %) resorbiert.
6. Pharmazeutische Angaben
6.1 Liste der sonstigen Bestandteile
Benzoesäure, Macrogolstearat 1500, Macrogolglycerololeate (Ph.Eur.), Dickflüssiges Paraffin, Gereinigtes Wasser.
6.2 Inkompatibilitäten
Keine bekannt.
6.3 Dauer der Haltbarkeit
Die Dauer der Haltbarkeit beträgt 3 Jahre.
Nach Anbruch der Tube beträgt die Haltbarkeit 12 Wochen.
6.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung
Keine.
6.5 Art und Inhalt des Behältnisses
Art des Behältnisses:
Tube
Packungsgrößen:
Originalpackung mit
20 g Creme 50 g Creme
7. Inhaber der Zulassung
Ardeypharm GmbH Loerfeldstraße 20 58313 Herdecke Telefon: 0 23 30 / 977 677 Telefax: 0 23 30 / 977 697 E-Mail: office@ardeypharm.de
8. Zulassungsnummer
35634.00.00
9. Datum der Erteilung der Zulassung / Verlängerung der Zulassung
23. Juni 1998 / 2. Juli 2003
10. Stand der Information
Juli 2015
11. Verkaufsabgrenzung
Apothekenpflichtig
Seite 5 von 5