Saroten Tabs 50 Mg
FACHINFORMATION
1. BEZEICHNUNG DES ARZNEIMITTELS
Saroten® Tabs 50 mg, Filmtabletten
2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Amitriptylinhydrochlorid
1 Filmtablette enthält:
50 mg Amitriptylin (als Hydrochlorid).
Sonstiger Bestandteil mit bekannter Wirkung: 53,8 mg Lactose (siehe Abschnitt 4.4.). Vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt 6.1.
3. DARREICHUNGSFORM
Filmtabletten
Bei Saroten Tabs 50 mg handelt es sich um teilbare Filmtabletten mit 3 Teilkerben. Die Teilkerben ermöglichen ein leichtes Brechen der Filmtablette in 4 Bruchstücke. Die Tablette kann in gleiche Dosen geteilt werden.
4. KLINISCHE ANGABEN
4.1 Anwendungsgebiete
- Depressive Erkrankungen
- Langfristige Schmerzbehandlung im Rahmen eines therapeutischen Gesamtkonzeptes
4.2 Dosierung und Art der Anwendung Dosierung
Dosierung und Dauer der Anwendung müssen der individuellen Reaktionslage, dem Anwendungsgebiet und der Schwere der Erkrankung angepasst werden. Aufgrund der viertelbaren Filmtabletten kann die zu verabreichende Dosis in Schritten von 12,5 mg Amitriptylin individuell angepasst werden.
Es gilt hier, dass zwar bei einem Ansprechen des Patienten die Dosis so klein wie möglich gehalten werden sollte, dass auf der anderen Seite aber bei einem Nichtansprechen der zur Verfügung stehende Dosierungsbereich ausgenutzt werden sollte.
Ältere Patienten benötigen oft eine deutlich geringere Dosis und zeigen schon häufig bei der Hälfte der üblichen Tagesdosis einen zufriedenstellenden Behandlungseffekt.
Auch bei geschwächten Patienten und Patienten mit zerebralen oder kardialen Schädigungen sowie bei Kreislauf- und Atmungsschwäche oder bei eingeschränkter Nieren- oder Leberfunktion ist eine Dosisreduktion von Amitriptylinhydrochlorid angezeigt.
Zur ambulanten Behandlung depressiver Erkrankungen wird eine Anfangsdosis von 2- bis 3-mal täglich Filmtablette Saroten Tabs 50 mg (entsprechend 50 bis 75 mg Amitriptylin/Tag) empfohlen. Die Dosis sollte dann täglich bis zum Wirkungseintritt gesteigert werden. Die maximale Tagesdosis darf ambulant 150 mg, stationär 300 mg Amitriptylin nicht übersteigen.
Ist eine schlafanstoßende Wirkung besonders gewünscht, kann ein größerer Teil der Tagesdosis zur Nacht gegeben werden.
Kinder und Jugendliche
Bei der Behandlung depressiver Erkrankungen bei Kindern und Jugendlichen unter 18 Jahren wird Amitriptylin in einer oralen Tagesdosierung zwischen 25 und 150 mg oder bis zu einer Maximaldosis von 4 - 5 mg/kg Körpergewicht eingesetzt. Entsprechend können 2-mal % bis 3-mal 1 Filmtablette Saroten Tabs 50 mg pro Tag gegeben werden. Hierbei ist jedoch das Nutzen-Risiko-Verhältnis sorgfältig abzuwägen (siehe Abschnitt 4.4).
Die Behandlung chronischer Schmerzen sollte mit einer abendlichen Dosierung von A Filmtablette Saroten Tabs 50 mg (entsprechend 25 mg Amitriptylin) begonnen werden, die schrittweise auf eine abendliche Gabe von 75 bis 100 mg (in Einzelfällen bis 150 mg) Amitriptylin gesteigert werden kann.
Art der Anwendung
Bei Saroten Tabs 50 mg handelt es sich um teilbare Filmtabletten mit 3 Teilkerben. Die Teilkerben ermöglichen ein leichtes Brechen der Filmtablette in 4 Bruchstücke. Die aktuell nicht benötigten Bruchstücke können in dem Reservoir der Tablettendose (unter dem Schieber des Deckels) bis zum nächsten Einnahmezeitpunkt aufbewahrt werden.
Die Einnahme der Filmtabletten erfolgt zu oder unabhängig von den Mahlzeiten unzerkaut mit ausreichend Flüssigkeit.
Die einleitende Behandlung ist durch schrittweise Dosissteigerung und die Beendigung der Behandlung durch langsame Verringerung der Dosis vorzunehmen.
Dauer der Anwendung
Über die Dauer der Behandlung muss der Arzt individuell entscheiden. Die mittlere Dauer einer Behandlungsperiode bis zum Nachlassen der Krankheitserscheinungen beträgt im Allgemeinen mindestens 4 - 6 Wochen.
Nach Rückbildung der depressiven Symptomatik sollte die Behandlung noch wenigstens 6 Monate weitergeführt werden. Über eine Reduktion der Erhaltungsdosis hat der behandelnde Arzt im Einzelfall zu entscheiden.
4.3 Gegenanzeigen
Saroten Tabs 50 mg darf nicht angewendet werden bei:
- Überempfindlichkeit gegen den Wirkstoff oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile
- akuten Alkohol-, Schlafmittel-, Schmerzmittel- und Psychopharmakavergiftungen
- Harnretention
- Delirien
- unbehandeltem Engwinkelglaukom
- Prostatahyperplasie mit Restharnbildung
- Pylorusstenose
- paralytischem Ileus
- Hypokaliämie
- Bradykardie
- angeborenem langen QT-Syndrom oder anderen klinisch signifikanten kardialen Störungen (insbesondere koronare Herzkrankheit, kürzlich zurückliegender Herzinfarkt, Erregungsleitungsstörungen, Arrhythmien)
- gleichzeitiger Behandlung mit Arzneimitteln, die ebenfalls das QT-Intervall im EKG verlängern oder eine Hypokaliämie hervorrufen können (siehe Abschnitt 4.5)
- gleichzeitiger Behandlung mit MAO-Hemmern (siehe Abschnitt 4.5)
4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung
Ein plötzliches Absetzen einer längerfristigen hochdosierten Behandlung mit Amitriptylin sollte vermieden werden, da hier mit Absetzsymptomen wie Unruhe, Schweißausbrüchen, Übelkeit, Erbrechen und Schlafstörungen zu rechnen ist.
Bei Auftreten einer manischen Verstimmung ist dieses Arzneimittel sofort abzusetzen. Das gleiche gilt für das Auftreten akut produktiver Symptome bei der Behandlung depressiver Syndrome im Verlauf schizophrener Erkrankungen.
Amitriptylinhydrochlorid kann die Krampfschwelle erniedrigen, daher kann es bei erhöhter Anfallsbereitschaft (z. B. Entzugssyndrom nach abruptem Absetzen von Benzodiazepinen oder Barbituraten) vermehrt zu Krampfanfällen kommen.
Saroten Tabs 50 mg darf nur nach strenger Nutzen-Risiko-Abwägung und entsprechenden Vorsichtsmaßnahmen angewendet werden bei:
- Prostatahyperplasie ohne Restharnbildung
- schweren Leber- oder Nierenschäden
- erhöhter Krampfbereitschaft
- Störungen der Blutbildung
Während die sedierende Wirkung von Amitriptylin meist unmittelbar in den ersten Stunden einsetzt, ist die stimmungsaufhellende Wirkung in der Regel erst nach 1 bis 3 Wochen zu erwarten.
Dem jeweiligen Risiko entsprechend (Auftrittswahrscheinlichkeit der Nebenwirkung und Risikolage des Patienten) sind in regelmäßigen Abständen Kontrollen von Blutdruck, EKG, Blutbild, Leberfunktion und ggf. EEG vorzunehmen. Eine bestehende Hypokaliämie ist vor Behandlungsbeginn auszugleichen.
Bei Patienten mit einem hirnorganischen Psychosyndrom ist die mögliche Erzeugung eines pharmakogenen Delirs zu bedenken.
Bei Patienten, die SSRIs (selektive Serotonin-Wiederaufnahmeinhibitoren) einnehmen, sollte eine gleichzeitige Behandlung mit Amitriptylin nur unter besonderer Vorsicht erfolgen.
Patienten mit der seltenen hereditären Galactose-Intoleranz, Lactasemangel oder Glucose-Galactose-Malabsorption sollten Saroten Tabs 50 mg nicht einnehmen.
Kinder und Jugendliche
Trizyklische Antidepressiva wie Saroten Tabs 50 mg sollten nicht zur Behandlung von Kindern und Jugendlichen unter 18 Jahren angewendet werden. In Studien zur Behandlung von Depressionen in dieser Altersgruppe zeigten trizyklische Antidepressiva keinen therapeutischen Nutzen. Studien mit anderen Antidepressiva (SSRI, SNRI) haben ein erhöhtes Risiko für das Auftreten von suizidalem Verhalten, Selbstschädigung und feindseligem Verhalten im Zusammenhang mit der Anwendung dieser Wirkstoffe gezeigt. Diese Risiken können auch für trizyklische Antidepressiva nicht ausgeschlossen werden.
Außerdem sind trizyklische Antidepressiva in allen Altersgruppen mit einem Risiko für kardiovaskuläre Nebenwirkungen verbunden (siehe auch Abschnitt 4.8 „Nebenwirkungen“). Darüber hinaus liegen keine Daten zur Sicherheit bei Langzeitanwendung bei Kindern und Jugendlichen bezüglich Wachstum, Reifung sowie zur kognitiven Entwicklung und Verhaltensentwicklung vor. Wird unter besonderer Berücksichtigung des Nutzen-Risiko-Verhältnisses Saroten Tabs 50 mg dennoch bei Kindern und Jugendlichen unter 18 Jahren verordnet, wird empfohlen, aufgrund des erhöhten Risikos für das Auftreten von Karies bei Kindern verstärkt auf die tägliche Zahnpflege zu achten.
Ältere oder geschwächte Patienten
Bei älteren oder geschwächten Patienten sowie Patienten mit hirnorganischen Veränderungen, Kreislauf- und Atmungsschwäche (chronisch obstruktive Ateminsuffizienz) sowie eingeschränkter Nieren- oder Leberfunktion ist Vorsicht geboten (Dosierungsanleitung beachten!).
Amitriptylin sollte mit Vorsicht angewendet werden bei Patienten mit Schilddrüsenüberfunktion und Patienten, die mit Schilddrüsen-Präparaten behandelt werden und bei Patienten mit paranoider Symptomatik.
Wie bei anderen Psychopharmaka beschrieben, könnte auch Amitriptylin das Ansprechen von Insulin und Glucose bei Diabetikern beeinflussen, so dass eine Anpassung der antidiabetischen Therapie notwendig ist. Die depressive Erkrankung selbst kann ebenso einen Einfluss auf den Glucosespiegel des Patienten haben.
Suizid/Suizidgedanken oder klinische Verschlechterung
Depressive Erkrankungen sind mit einem erhöhten Risiko für die Auslösung von Suizidgedanken, selbstschädigendem Verhalten und Suizid (Suizid-bezogene Ereignisse) verbunden. Dieses erhöhte Risiko besteht, bis es zu einer signifikanten Linderung der Symptome kommt. Da diese nicht unbedingt schon während der ersten Behandlungswochen auftritt, sollten die Patienten daher bis zum Eintritt einer Besserung engmaschig überwacht werden. Die bisherige klinische Erfahrung zeigt, dass das Suizidrisiko zu Beginn einer Behandlung ansteigen kann.
Bei Patienten mit suizidalem Verhalten in der Anamnese oder solchen, die vor der Therapie ausgeprägte Suizidabsichten hatten, ist das Risiko für die Auslösung von Suizidgedanken oder -versuchen erhöht. Sie sollten daher während der Behandlung besonders sorgfältig überwacht werden. Eine Meta-Analyse von Placebo-kontrollierten klinischen Studien zur Anwendung von Antidepressiva bei Erwachsenen mit psychiatrischen Störungen zeigte für Patienten unter 25 Jahren, die Antidepressiva einnahmen, ein erhöhtes Risiko für suizidales Verhalten im Vergleich zu Placebo.
Die Arzneimitteltherapie sollte mit einer engmaschigen Überwachung der Patienten, vor allem der Patienten mit hohem Suizidrisiko, insbesondere zu Beginn der Behandlung und nach Dosisanpassungen einhergehen. Patienten (und deren Betreuer) sind auf die Notwendigkeit einer Überwachung hinsichtlich jeder klinischen Verschlechterung, des Auftretens von suizidalem Verhalten oder Suizidgedanken und ungewöhnlicher Verhaltensänderungen hinzuweisen. Sie sollten unverzüglich medizinischen Rat einholen, wenn derartige Symptome auftreten.
4.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen
Die Wirkung von Alkohol und die Wirkung anderer zentraldämpfend wirkender Arzneimittel kann bei gleichzeitiger Einnahme von Saroten Tabs 50 mg verstärkt werden. Während der Behandlung darf kein Alkohol zu sich genommen werden.
Bei gleichzeitiger Verabreichung anderer Arzneimittel mit anticholinerger Wirkung ist mit einer Verstärkung peripherer und zentraler Effekte (insbesondere einem Delir) zu rechnen.
Die Wirkung sympathomimetischer Amine auf das vegetative Nervensystem kann durch gleichzeitige Gabe von Saroten Tabs 50 mg erheblich verstärkt werden, z. B. bei vasokonstringierenden Zusätzen bei Lokalanästhetika.
MAO-Hemmer vom irreversiblen Hemmtyp sollen in jedem Fall mindestens 14 Tage, MAO-Hemmer vom reversiblen Hemmtyp mindestens 1 Tag vor Beginn der Behandlung mit Saroten Tabs 50 mg abgesetzt werden. Andernfalls muss mit schweren Nebenwirkungen wie Erregung, Delir, Koma, Hyperpyrexie, Krampfanfällen und starken Blutdruckschwankungen gerechnet werden, (siehe Abschnitt 4.3).
Bei gleichzeitiger oder vorausgegangener Anwendung von Fluoxetin oder Fluvoxamin kann es durch Substratkonkurrenz zu einem Anstieg der Plasmakonzentration von Amitriptylin kommen. Es ist daher gegebenenfalls eine Dosisreduktion von Amitriptylin, Fluoxetin oder Fluvoxamin erforderlich.
Bei gleichzeitiger Anwendung von Arzneimitteln, die Wirkstoffe aus Johanniskraut (Hypericum) enthalten, kann die Konzentration von Amitriptylin im Blut verringert und dadurch die Wirksamkeit von Amitriptylin abgeschwächt werden.
Es kann zu einer Wirkungsabschwächung von Antihypertensiva vom Typ des Guanethidin bzw. des Clonidin kommen. Bei mit Clonidin behandelten Patienten besteht die Gefahr einer Rebound-Hypertension.
Arzneimittel, die ebenfalls das QT-Intervall verlängern (z. B. Antiarrhythmika Klasse IA oder III, Cisaprid, Antibiotika, Malaria-Mittel, Antihistaminika, Neuroleptika), zu einer Hypokaliämie führen (z. B. bestimmte Diuretika) oder den hepatischen Abbau von Amitriptylin hemmen können (z. B. MAO-Hemmer, Imidazol-Antimykotika) dürfen nicht gleichzeitig angewendet werden (siehe Abschnitt 4.3).
Bei einer Kombination mit Neuroleptika kann es zur Erhöhung der Blutspiegel trizyklischer Antidepressiva wie Amitriptylin kommen. Auch bei gleichzeitiger Behandlung mit Cimetidin kann der Blutspiegel von Amitriptylin erhöht werden.
Amitriptylinhydrochlorid kann die Wirkung von Cumarin-Derivaten (z. B. Phenprocoumon) beeinflussen. Bei gleichzeitiger Einnahme von Amitriptylinhydrochlorid und Cumarinen ist eine fortlaufende Kontrolle der Blutgerinnungswerte erforderlich.
4.6 Schwangerschaft und Stillzeit
Schwangerschaft
Zur Anwendung von Amitriptylin in der Schwangerschaft liegen keine ausreichenden Erfahrungen vor. Tierexperimentelle Studien haben nach hohen Dosen Amitriptylin Reproduktionstoxizität gezeigt (siehe auch Abschnitt 5.3). Das potenzielle Risiko für den Menschen ist nicht bekannt.
Amitriptylin sollte während der Schwangerschaft, insbesondere im ersten sowie im letzten Trimenon nicht angewendet werden, es sei denn, dies ist dringend erforderlich.
Nach Gabe höherer Dosierungen von Antidepressiva vor der Geburt wurden beim Neugeborenen Entzugserscheinungen in Form von Störungen der Herz- und Atemfunktion, Harn- und Stuhlentleerung sowie Unruhe beobachtet.
Stillzeit
Amitriptylin und seine Metaboliten gehen in die Muttermilch über (Milch/Plasma-Ratio ca. 1). Daher sollte es nicht während der Stillzeit eingenommen werden. Bei zwingender Indikation sollte abgestillt werden.
4.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen
Saroten Tabs 50 mg hat - individuell unterschiedlich großen - Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen.Dies gilt in besonderem Maße bei Behandlungsbeginn, bei Präparatewechsel sowie im Zusammenwirken mit anderen zentral wirkenden Arzneimitteln (Schmerzmittel, Schlafmittel, Psychopharmaka). Gleichzeitiger Genuss von Alkohol verschlechtert die Verkehrstüchtigkeit zusätzlich.
Daher sollten das Führen von Fahrzeugen, das Bedienen von Maschinen oder sonstige gefahrvolle Tätigkeiten ganz unterbleiben, zumindest jedoch während der ersten Tage der Behandlung unterlassen werden. Die Entscheidung ist in jedem Einzelfall durch den behandelnden Arzt unter Berücksichtigung der individuellen Reaktion und der jeweiligen Dosierung zu treffen.
4.8 Nebenwirkungen
Bei der Bewertung von Nebenwirkungen werden folgende Häufigkeiten zugrunde gelegt:
Sehr häufig Häufig Gelegentlich Selten Sehr selten Nicht bekannt
(> 1/10)
(> 1/100 bis < 1/10)
(> 1/1.000 bis < 1/100)
(> 1/10.000 bis < 1/1.000)
(< 1/10.000)
(Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar)
Erkrankungen des Blutes und des Lymphsystems
Gelegentlich: Blutbildveränderungen (insbesondere Leukopenien)
Sehr selten: Agranulozytose
Erkrankungen des Immunsystems Gelegentlich: allergische Reaktionen der Haut
Sehr selten: allergische Entzündungen der Lungenbläschen bzw. des Lungengewebes
(Alveolitis, Löffler-Syndrom)
Nicht bekannt: Ödeme (Gesicht, Zunge)
Stoffwechsel- und Ernährungsstörungen
Sehr häufig: Gewichtszunahme (insbesondere zu Beginn)
Nicht bekannt: Anorexie
Psychiatrische Erkrankungen
Sehr häufig: Aggression (insbesondere zu Beginn)
Häufig: innere Unruhe, Libidoverlust bzw. Impotenz. Bei älteren Patienten besteht ein
erhöhtes Risiko für das Auftreten von deliranten Syndromen.
Nicht bekannt: Verwirrtheit, Manie, Halluzination, Angst, Paranoia, suizidale Gedanken,
suizidales Verhalten
Fälle von suizidalen Gedanken oder suizidalem Verhalten während der Therapie mit Amitriptylin oder kurze Zeit nach Beendigung der Behandlung sind berichtet worden (siehe Abschnitt 4.4).
Erkrankungen des Nervensystems
Sehr häufig: Insbesondere zu Beginn: Benommenheit, Schwindel, Sprachstörungen, Tremor
Sehr selten: Zerebrale Krampfanfalle, motorische Störungen (Akathisie, Dyskinesien),
Polyneuropathien
Nicht bekannt: Kopfschmerzen, Konzentrationsmangel, Ataxie, Störungen des
Geschmacksvermögens
Augenerkrankungen
Sehr häufig: Akkommodationsstörungen (insbesondere zu Beginn)
Sehr selten: Glaukomanfälle
Nicht bekannt: Mydriasis
Erkrankungen des Ohrs und des Labyrinths Nicht bekannt: Tinnitus
Herzerkrankungen
Sehr häufig: Insbesondere zu Beginn: Tachykardie, Herzrhythmusstörungen
Gelegentlich: Kollapszustände, Erregungsleitungsstörungen. Eine bestehende
Herzmuskelschwäche (Herzinsuffizienz) kann verstärkt werden.
Sehr selten: Kardiomyopathien
In einem Fall wurde eine Hypersensitivitätsmyokarditis beobachtet.
Gefäßerkrankungen
Sehr häufig: Insbesondere zu Beginn: Hypotonie, orthostatische Dysregulation
Gelegentlich: Entzündliche Veränderungen der Gefäße (allergische Vaskulitis)
Nicht bekannt: Hyperthermie, Hypertension
Erkrankungen der Atemwege, des Brustraums und Mediastinums Sehr häufig: verstopfte Nase (insbesondere zu Beginn)
Erkrankungen des Gastrointestinaltrakts
Sehr häufig: Insbesondere zu Beginn: Mundtrockenheit, Obstipation
Gelegentlich: Paralytischer Ileus
Nicht bekannt: Diarrhoe
Leber- und Gallenerkrankungen
Sehr häufig: passageres Ansteigen der Leberenzymaktivität (insbesondere zu Beginn)
Gelegentlich: Leberfunktionsstörungen (z. B. cholestatische Hepatose)
Erkrankungen der Haut und des Unterhautzellgewebes Sehr häufig: Schwitzen (insbesondere zu Beginn)
Häufig: Hautausschläge
Nicht bekannt: Photosensibilisierung, Alopezie
Erkrankungen der Nieren und Harnwege Häufig: Miktionsstörungen
Gelegentlich: Harnsperre
Erkrankungen der Geschlechtsorgane und der Brustdrüse Gelegentlich: Galaktorrhoe
Nicht bekannt: Gynäkomastie
Allgemeine Erkrankungen und Beschwerden am Verabreichungsort Sehr häufig: Müdigkeit (insbesondere zu Beginn)
Häufig: Durstgefühl
Untersuchungen
Häufig: Hyponatriämie
Amitriptylin kann das QT-Intervall im EKG verlängern; sehr selten sind Torsades de Pointes aufgetreten. In diesen Fällen ist die Behandlung mit Amitriptylin abzubrechen.
In epidemiologischen Studien, die hauptsächlich mit Patienten durchgeführt wurden, die 50 Jahre oder älter waren, wurde bei denen, die mit Selektiven Serotonin-Wiederaufnahme-Inhibitoren (SSRI) oder tricyclischen Antidepressiva (TCA) behandelt wurden, ein erhöhtes Risiko für das Auftreten von Knochenbrüchen beobachtet. Der Mechanismus, der zu diesem Risiko führt, ist nicht bekannt.
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung dem Bundesinstitut für Arzneimittel und Medizinprodukte, Abt. Pharmakovigilanz, Kurt-Georg-Kiesinger-Allee 3, D-53175 Bonn, Website: http://www.bfarm.de anzuzeigen.
4.9 Überdosierung
Trizyklische Antidepressiva zeichnen sich durch eine erhebliche akute Toxizität aus. Kinder bzw. Kleinkinder sind besonders gefährdet.
Symptome
Überdosierungen mit Amitriptylin sind in erster Linie - abhängig von der aufgenommenen Menge -gekennzeichnet durch die unterschiedlichen Stadien einer ZNS-Beeinträchtigung (Verwirrung, Erregungszustände bis zu Krampfanfällen, Bewusstseinstrübung bis zum Koma, Atemdepression bis Atemstillstand) sowie Herz-Kreislauf-Symptome (Hypotonie, Tachykardie, EKG-Veränderungen wie PQ-, QT-Intervallverlängerung, Torsades de pointes, AV-Block II. oder III. Grades). Außerdem können anticholinerge Symptome (trockene Schleimhäute, Sehstörungen, Obstipation, Oligurie, Anurie) und eine metabolische Azidose auftreten.
Die Vergiftungssymptome treten meist innerhalb von 4 Stunden nach Einnahme auf und sind nach 24 Stunden voll ausgeprägt. Wegen der langen Halbwertszeiten und des enterohepatischen Kreislaufes, dem trizyklische Antidepressiva unterliegen, sind diese Patienten über einen Zeitraum von 4 bis 6 Tagen gefährdet.
Behandlung
So rasch wie möglich ist eine intensivmedizinische Behandlung einzuleiten. Innerhalb von 1-2 Stunden nach Einnahme kann eine Magenspülung aussichtsreich sein, gefolgt von der wiederholten Gabe von Aktivkohle. Die weitere Therapie erfolgt symptomatisch. Zum Einsatz kommen Volumensubstitution, Antikonvulsiva und u. U. auch Antiarrhythmika. Eine Alkalisierung des Plasmas mit Natriumhydrogencarbonat bzw. -lactat hat sich auch in der Behandlung der kardialen Komplikationen gut bewährt.
Bei schweren Vergiftungen (Bewusstlosigkeit, Herzrhythmusstörungen) bzw. Auftreten eines anticholinergen Syndroms steht zur Anwendung unter intensivmedizinischen Bedingungen (EKG-Kontrolle!) als Antidot Physostigminsalicylat zur Verfügung.
Auf Grund des großen Verteilungsvolumens und der relativ starken Plasma-Eiweiß-Bindung dürften forcierte Diurese oder Hämodialyse bei reinen Amitriptylin-Vergiftungen nur von geringem Nutzen sein.
5. PHARMAKOLOGISCHE EIGENSCHAFTEN
5.1 Pharmakodynamische Eigenschaften
Pharmakotherapeutische Gruppe: Psychoanaleptika, Antidepressiva, ATC-Code: N06AA09
Amitriptylin ist eine psychotrope Substanz aus der Klasse der trizyklischen Antidepressiva mit ausgeprägter sedierender Wirkungskomponente. Darüber hinaus zeigt Amitriptylin eine antinozizeptive Wirkung. Akut gegeben, zeigt Amitriptylin eine starke Hemmwirkung auf die neuronale Aufnahme von Noradrenalin und Serotonin und antagonistische Eigenschaften an den M-Cholinrezeptoren (M1 und M2), Histaminrezeptoren (H1 stärker als H2), an a-Adrenozeptoren (0,1 stärker als a2) und Serotoninrezeptoren (5-HT2 stärker als 5-HT1).
Amitriptylin ist in allen verhaltenspharmakologischen und biochemisch-pharmakologischen Experimenten, die derzeit als Modelle bei der Suche nach antidepressiven Substanzen benutzt werden, wirksam.
5.2 Pharmakokinetische Eigenschaften
Resorption
Nach oraler Gabe wird Amitriptylin langsam aber vollständig resorbiert. Auf Grund der häufig verzögerten Magen-Darm-Passage werden maximale Plasmakonzentrationen erst nach 1 bis 5 (-8) Stunden erreicht.
Die systemische Bioverfügbarkeit beträgt im Verhältnis zur intravenösen Injektion etwa 50%. Verteilung
Auf Grund seiner großen Lipophilie wird Amitriptylin im ganzen Organismus verteilt. Das Verteilungsvolumen beträgt 14 bis 18 l/kg.
Amitriptylin wird stark an Gewebs- und Plasma-Eiweiße gebunden; nur 3-6% liegen frei im Plasma vor (der aktive Metabolit Nortriptylin zu 8-13%).
Sowohl Amitriptylin als auch Nortriptylin treten in die Muttermilch über.
Biotransformation
Amitriptylin wird hauptsächlich in der Leber metabolisiert. Der durch N-Demethylierung (CYP3A4) entstehende Hauptmetabolit Nortriptylin ist ebenfalls pharmakologisch aktiv. Amitriptylin und Nortriptylin werden anschließend hydroxyliert; die entstehenden 10-Hydroxy-Metaboliten besitzen noch etwa die Hälfte der biologischen Aktivität von Amitriptylin.
Etwa 3-5% der Bevölkerung sind auf Grund genetisch bedingter Unterschiede im Cytochrom P450-System „poor metabolizer“ bzw. „schlechte Hydroxylierer“ Bei diesen Patienten können deshalb sehr hohe Plasmaspiegel auftreten.
Offenbar auf Grund verminderter Biotransformation treten bei älteren Patienten höhere Plasmakonzentrationen auf.
Die Ausscheidung der Metaboliten erfolgt in freier oder konjugierter Form. Unverändertes Amitriptylin wurde nur in geringen Mengen im Urin gefunden.
Die Plasma-Halbwertszeit von Amitriptylin beträgt nach oraler Gabe ca. 10 bis 28 Stunden; bei älteren Menschen ist die Halbwertszeit verlängert.
Die Plasma-Clearance wird mit 0,17-0,32 l/kg/h und für ältere Probanden mit 0,18-0,45 l/kg/h angegeben.
Pathophysiologische Variationen
Bei Patienten mit Niereninsuffizienz ist die Konzentration an unkonjugierten Metaboliten im Plasma gegenüber nierengesunden Patienten verringert, dagegen ist die Konzentration an konjugierten Metaboliten stark erhöht.
Bioverfügbarkeit
Eine im Jahr 1997 durchgeführte Bioverfügbarkeitsuntersuchung an 14 Probanden ergab im Vergleich zum Referenzpräparat:
|
Testpräparat |
Referenzpräparat: 2 ml Trinklösung mit 50 mg Amitriptylinhydrochlorid | |
|
Amitriptylin | ||
|
maximale Plasmakonzentration (Cmax) [Eg/H: |
18,99 (1,49) |
19,47 (1,5) |
|
Zeitpunkt der maximalen Plasmakonzentration (tmax) [h]: |
3 |
2 |
|
Fläche unter der Konzentrations-ZeitKurve (AUC«) [pg*h/l]: |
354,2 (1,51) |
314,8 (1,53) |
Angabe der Werte als geometrische Mittelwerte und in Klammern Streufaktoren (= geom. Standardabweichung)
Abb.: Mittlere Amitriptylin-Plasmaspiegelverläufe im Vergleich zu einem Referenzpräparat in einem
Konzentrations-Zeit-Diagramm
Konzentration [pg/1]
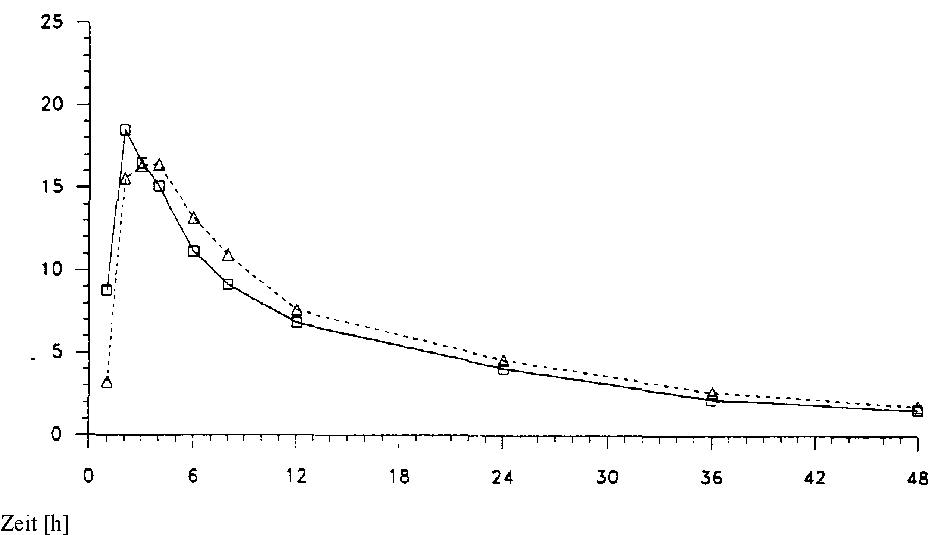
A -----A Testpräparat (Filmtablette)
□ ---□ Referenzpräparat (Trinklösung)
5.3 Präklinische Daten zur Sicherheit
In vitro blockiert Amitriptylin exprimierte HERG-Kanäle in mikromolaren Konzentrationen, die im oberen Bereich therapeutischer Plasmakonzentrationen liegen. Diese Kanäle sind für die Repolarisation im Herzen verantwortlich. Daher hat Amitriptylin das Potenzial, bestimmte Formen von Kammerherzrhythmusstörungen (Torsades de pointes) auszulösen.
Das genotoxische Potential von Amitriptylinhydrochlorid wurde in verschiedenen in vitro und in vivo Testsystemen untersucht. Obwohl die Ergebnisse zum Teil widersprüchlich sind, kann ein genotoxisches Potential, insbesondere im Hinblick auf mögliche Schädigungen von Chromosomen, nicht ausgeschlossen werden.
Langzeituntersuchungen auf ein tumorerzeugendes Potenzial wurden nicht durchgeführt.
In Untersuchungen zur Reproduktionstoxizität wurden nach sehr hohen Dosen bei verschiedenen Tierspezies fetotoxische und teratogene Effekte beobachtet. Von anderen Antidepressiva liegen Hinweise auf Verhaltensstörungen der pränatal exponierten Nachkommen im Tierexperiment vor. Für Amitriptylin sind keine entsprechenden Angaben bekannt.
6. PHARMAZEUTISCHE ANGABEN
6.1 Liste der sonstigen Bestandteile
Crosscarmellose-Natrium, Lactose-Monohydrat, Magnesiumstearat (Ph.Eur.), mikrokristalline Cellulose, Eisen(III)-hydroxid-oxid (E 172), Hypromellose, Macrogol 4000, Titandioxid (E 171).
6.2 Inkompatibilitäten
Nicht zutreffend.
6.3 Dauer der Haltbarkeit
2 Jahre
6.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung
Für dieses Arzneimittel sind keine besonderen Lagerungsbedingungen erforderlich.
6.5 Art und Inhalt des Behältnisses
Kunststoff-Weithalsdose (Polypropylen) mit Stopfen (Polyethylen) mit Schieber (Polypropylen) Packungen mit 20, 50 bzw. 100 Filmtabletten Klinikpackung mit 30 Filmtabletten
Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht.
6.6 Besondere Vorsichtsmaßnahmen für die Beseitigung und sonstige Hinweise zur Handhabung
Keine besonderen Anforderungen.
7. INHABER DER ZULASSUNG
Bayer Vital GmbH 51368 Leverkusen Deutschland Tel.: (0214) 30-5 13 48
Fax: (0214) 30-5 16 03
E-Mail: bayer-vital@bayerhealthcare.com
8. ZULASSUNGSNUMMER(N)
45198.00.00
9. DATUM DER ERTEILUNG DER ZULASSUNG / VERLÄNGERUNG DER ZULASSUNG
Datum der Erteilung der Zulassung: 26. Februar 2002 Datum der letzten Verlängerung der Zulassung: 22. August 2008
10. STAND DER INFORMATION
September 2014
11. VERKAUFSABGRENZUNG
Verschreibungspflichtig
12