Viatim
Sanofi Pasteur MSD GmbH
1. BEZEICHNUNG DES ARZNEIMITTELS
ViATIM, Suspension und Lösung zur Herstellung einer Injektionssuspension in einer Fertigspritze Inaktivierter Hepatitis A-Adsorbat- und Typhus-Polysaccharid-Impfstoff
2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Eine Doppelkammer-Fertigspritze enthält 0,5 ml inaktivierten Hepatitis A-Impfstoff und 0,5 ml Typhus-Polysaccharid-Impfstoff, die vor Verabreichung gemischt werden.
1 Dosis (1 ml) des gemischten Impfstoffs enthält:
Wirkstoffe:
Bestandteil aus der Suspension:
Inaktiviertes Hepatitis A-Virus, Stamm GBM1,2..................................160 Einheiten3
1 gezüchtet in humanen diploiden MRC-5 Zellen
2 adsorbiert an hydratisiertes Aluminiumhydroxid (enthält 0,3 mg Aluminium)
3 In Ermangelung eines international gültigen Referenzstandards für den Antigengehalt wird ein In-house-Referenzwert angegeben.
Bestandteil aus der Lösung:
Salmonella typhi (Stamm Ty 2) Vi-Kapselpolysaccharid.....................25 Mikrogramm
Vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt 6.1.
ViATIM kann Spuren von Neomycin enthalten, das während des Herstellungsverfahrens verwendet wird (siehe Abschnitt 4.3).
3. DARREICHUNGSFORM
Suspension und Lösung zur Herstellung einer Injektionssuspension in einer Fertigspritze
Der inaktivierte Hepatitis A-Impfstoff ist eine weißlich-trübe Suspension und der TyphusPolysaccharid-Impfstoff ist eine klare, farblose Lösung.
4. KLINISCHE ANGABEN
4.1 Anwendungsgebiete
ViATIM ist indiziert zur gleichzeitigen aktiven Immunisierung gegen Typhus und Hepatitis A ab 16 Jahren.
Bitte beachten Sie auch die aktuellen Empfehlungen der Ständigen Impfkommission (STIKO) am Robert Koch-Institut, aktuell abrufbar über www.stiko.de.
4.2 Dosierung und Art der Anwendung
Dosierung
Die empfohlene Dosis für Personen ab 16 Jahren ist 1 ml des gemischten Impfstoffs.
Ein Impfschutz wird bereits nach Verabreichung einer Dosis ViATIM erreicht. Schützende Antikörperkonzentrationen sind jedoch erst 14 Tage nach Verabreichung des Impfstoffs zu erwarten.
Zum Aufbau eines Langzeitschutzes vor Hepatitis A-Virusinfektionen wird die Verabreichung einer zweiten Dosis eines inaktivierten Hepatitis A-Impfstoffs empfohlen. Für den Fall, dass eine oder beide Hepatitis A-Impfungen mit ViATIM durchgeführt werden sollen, kann ViATIM wie folgt verabreicht werden:
Bei Personen, die bereits eine Dosis ViATIM erhalten haben,
- sollte entweder innerhalb von 36 Monaten, vorzugsweise innerhalb von 6 bis 12 Monaten, eine Dosis eines monovalenten Hepatitis A-Impfstoffs gegeben werden (siehe Abschnitt 5.1)
- oder kann, wenn gleichzeitig eine Wiederimpfung gegen Typhus erforderlich ist, eine zweite Dosis ViATIM gegeben werden, vorausgesetzt, dass seit der ersten Dosis ungefähr 36 Monate vergangen sind.
Bei Personen, die eine Dosis eines monovalenten Hepatitis A-Impfstoffs erhalten haben,
- kann ViATIM gegeben werden, wenn die zweite Impfung (Auffrischimpfung) gegen Hepatitis A gleichzeitig mit einer Impfung gegen Typhus verabreicht werden soll. In diesem Falle sollte der Kombinationsimpfstoff innerhalb von 36 Monaten, vorzugsweise 6 bis
12 Monate nach der ersten Dosis des Hepatitis A-Impfstoffs verabreicht werden.
Antikörper gegen das Hepatitis A-Virus persistieren vermutlich für einen langen Zeitraum (mehr als 10 Jahre) nach der zweiten Impfung (Auffrischimpfung).
Personen, bei denen weiterhin die Gefahr einer Typhus-Infektion besteht, sollten alle 3 Jahre mit einer Dosis eines Typhus-Vi-Polysaccharid-Impfstoffs wieder geimpft werden (siehe Abschnitt 5.1).
Kinder und Jugendliche
Die Sicherheit und Wirksamkeit von ViATIM bei Kindern und Jugendlichen unter 16 Jahren wurde bisher noch nicht untersucht. Es liegen keine Daten vor.
Art der Anwendung
ViATIM wird langsam intramuskulär, vorzugsweise in den Deltamuskel (M. deltoideus) am Oberarm verabreicht.
ViATIM darf nicht intravasal verabreicht werden.
ViATIM sollte aufgrund der variierenden Mengen von Fettgewebe im Bereich des Gesäßes nicht in die Gesäßregion und auch nicht intradermal verabreicht werden, da diese Arten der Anwendung zu einer abgeschwächten Immunantwort führen können.
ViATIM kann bei Patienten mit Thrombozytopenie oder bei Patienten mit Blutungsneigung subkutan verabreicht werden.
Hinweise zur Vorbereitung des Arzneimittels vor der Anwendung siehe Abschnitt 6.6.
4.3 Gegenanzeigen
Überempfindlichkeit gegen die Wirkstoffe oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile oder gegen Neomycin (Neomycin wird während der Herstellung verwendet; Spuren von Neomycin können im Impfstoff enthalten sein).
Personen mit einer schweren akuten fieberhaften Erkrankung sind von der Impfung zurückzustellen.
4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung
Bei der Durchführung von Impfungen ist grundsätzlich zu beachten, dass geeignete Behandlungsmöglichkeiten und Medikamente (z. B. Adrenalin) für den Fall von anaphylaktischen oder anaphylaktoiden Reaktionen nach Verabreichung des Impfstoffs bereitstehen.
Synkopen (Ohnmachtsanfälle) können besonders bei Jugendlichen nach oder sogar vor einer Impfung als psychogene Reaktion auf den Einstich mit der Injektionsnadel auftreten. Diese können während der Erholungsphase von neurologischen Symptomen wie vorübergehende Sehstörung, Parästhesie und tonisch-klonischen Bewegungen der Gliedmaßen begleitet sein. Daher sollten geimpfte Personen nach der Impfung für ungefähr 15 Minuten beobachtet werden. Es ist wichtig, dass im Vorfeld Maßnahmen ergriffen werden, um Verletzungen durch die Ohnmacht zu verhindern.
Die Immunogenität des Impfstoffs kann bei Patienten, die immunsuppressiv therapiert werden oder die an einer Immunschwäche leiden, eingeschränkt sein. Die Impfung sollte zurückgestellt werden, bis die Therapie beendet oder die Krankheit überwunden ist. HIV-Infizierte oder Patienten, die an einer chronischen Immunschwächekrankheit wie z. B. AIDS leiden, sollten aber geimpft werden, auch wenn die Antikörperbildung eingeschränkt sein kann.
Aufgrund der langen Inkubationszeit der Hepatitis A (zwischen 20 und 50 Tagen) kann nicht ausgeschlossen werden, dass zum Zeitpunkt der Impfung bereits eine Infektion mit dem Virus vorliegt, die sich jedoch noch nicht klinisch manifestiert. Es ist nicht bekannt, ob ViATIM bei diesen Personen den Ausbruch einer Hepatitis A verhindern kann.
ViATIM schützt nicht vor Infektionen der Leber, die durch andere Erreger wie beispielsweise Hepatitis B-Virus, Hepatitis C-Virus und Hepatitis E-Virus ausgelöst werden.
ViATIM schützt nur vor Infektionen, die durch Salmonella typhi ausgelöst werden. Ein Schutz vor Infektionen durch andere Salmonellen-Serotypen besteht nicht.
Wie alle Impfstoffe schützt ViATIM möglicherweise nicht alle Geimpften vollständig.
4.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen
ViATIM darf nicht mit anderen Impfstoffen, Impfstoffkomponenten oder Arzneimitteln gemischt werden.
Die zeitgleiche Verabreichung von ViATIM mit Td-IPV-Impfstoff (kombinierter, adsorbierter Tetanus-, niedrig dosierter Diphtherie- und inaktivierter Poliomyelitis-Impfstoff) an zwei unterschiedlichen Injektionsstellen war im Hinblick auf die Immunantwort einen Monat nach der Impfung für alle Valenzen - mit Ausnahme der Vi-Valenz - gegenüber der Verabreichung der beiden Impfstoffe zu verschiedenen Zeitpunkten nicht unterlegen. Dennoch war die Anti-Vi-Serokonversionsrate (> 4-facher Anstieg) bei zeitgleicher Verabreichung gegenüber der separaten Verabreichung bei Probanden, die vor der Impfung keine Seroprotektion aufwiesen, nicht unterlegen (siehe Abschnitt 5.1). Die Seroprotektionsrate (der prozentuale Anteil der Probanden, die den Schwellenwert schützender Anti-Vi-Antikörpertiter >1 pg/ml erreichen) stimmte im Umfang mit der erwarteten Immunantwort bei alleiniger Gabe von ViATIM überein. Es ist daher unwahrscheinlich, dass die zeitgleiche Verabreichung von ViATIM und Td-IPV an zwei unterschiedlichen Injektionsstellen klinische Konsequenzen haben wird. Daher kann eine zeitgleiche Verabreichung von ViATIM und Td-IPV an unterschiedlichen Injektionsstellen erfolgen.
Es wurden keine Wechselwirkungsstudien mit ViATIM und anderen inaktivierten Impfstoffen durchgeführt. Jedoch ist basierend auf den Daten der zeitgleichen Verabreichung des monovalenten Typhus-Vi-Polysaccharid-Impfstoffs mit Diphtherie-Tetanus (DT)-, Tetanus-inaktivierter Poliomyelitis (T-IPV)-, Tollwut-, Meningokokken Polysaccharid A/C- und Hepatitis B-Impfstoffen sowie der zeitgleichen Verabreichung des monovalenten Hepatitis A-Impfstoffs mit Hepatitis B-Impfstoffen keine Beeinträchtigung der Immunantwort auf diese Antigene zu erwarten.
Die zeitgleiche Verabreichung von ViATIM mit Gelbfieber-Impfstoff wurde nicht gezielt untersucht. Aufgrund der vorliegenden Daten bezüglich der zeitgleichen Verabreichung der Einzelimpfstoffe (Typhus-Vi-Polysaccharid-Impfstoff und inaktivierter Hepatitis A-Impfstoff) mit Impfstoff gegen Gelbfieber ist bei zeitgleicher Verabreichung von ViATIM mit einem Gelbfieber-Impfstoff jedoch keine Beeinträchtigung der Immunantwort gegen die einzelnen Antigene zu erwarten.
Ob die zeitgleiche Verabreichung von Immunglobulinen Auswirkungen auf die Immunogenität von ViATIM hat, wurde nicht untersucht. Eine Beeinträchtigung der Immunantwort kann daher nicht ausgeschlossen werden. Bei zeitgleicher Verabreichung von Immunglobulinen und monovalentem inaktiviertem Hepatitis A-Impfstoff waren die anti-HAV-Serokonversionsraten nicht verändert, jedoch können die anti-HAV-Antikörperkonzentrationen niedriger sein als nach alleiniger Verabreichung des monovalenten Impfstoffs.
4.6 Fertilität, Schwangerschaft und Stillzeit
Schwangerschaft
Daten über eine begrenzte Anzahl von exponierten Schwangeren (mehr als 150 Fälle mit monovalentem Typhus-Vi-Kapselpolysaccharid-Impfstoff, mehr als 40 Fälle mit monovalentem inaktiviertem Hepatitis A-Impfstoff und mehr als 10 Fälle mit ViATIM bzw. den beiden gleichzeitig verabreichten Einzelkomponenten) lassen nicht auf Nebenwirkungen von ViATIM auf die Schwangerschaft oder die Gesundheit des Fetus/Neugeborenen schließen. Bisher sind keine anderen einschlägigen epidemiologischen Daten verfügbar. Tierexperimentelle Studien lassen nicht auf direkte oder indirekte schädliche Auswirkungen auf Schwangerschaft, embryonale/fetale Entwicklung, Geburt oder postnatale Entwicklung schließen (siehe Abschnitt 5.3).
Bei der Anwendung in der Schwangerschaft ist Vorsicht geboten.
Besteht für die zu impfende Person nur ein Expositionsrisiko für Hepatitis A oder Typhus, sollte der monovalente Impfstoff verabreicht werden.
Stillzeit
Ob ViATIM in die Muttermilch ausgeschieden wird, ist nicht bekannt. Dies wurde in tierexperimentellen Studien nicht untersucht. Die Entscheidung, ob weiter gestillt oder abgestillt bzw. mit ViATIM geimpft werden sollte oder nicht, sollte sorgfältig abgewogen werden. Dabei sind der Vorteil des Stillens für das Kind und der mögliche Nutzen der Impfung für die Mutter in Betracht zu ziehen.
Fertilität
Es liegen keine Daten zur Fertilität vor.
4.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen
ViATIM hat einen zu vernachlässigenden Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen.
Gelegentlich (> 1/1.000 bis < 1/100) wurde Schwindel nach Verabreichung von ViATIM beobachtet (siehe Abschnitt 4.8).
4.8 Nebenwirkungen
a. Zusammenfassung des Verträglichkeitsprofils
Während klinischer Studien wurde am häufigsten über Reaktionen an der Injektionsstelle berichtet.
Über Schmerzen an der Injektionsstelle nach Verabreichung von ViATIM berichteten 89,9 % der Geimpften (starke Schmerzen bei 4,5 %). Bei zeitgleicher Verabreichung der Einzelimpfstoffe an unterschiedlichen Stellen gaben 83,2 % der Geimpften Schmerzen am Injektionsort an (starke Schmerzen bei 5,0 %), bezogen auf beide Injektionsstellen. 79,3 % berichteten über Schmerzen an der Typhus-Injektionsstelle (starke Schmerzen bei 5,0 %) und 50,3 % an der Hepatitis A-Injektionsstelle (starke Schmerzen bei 0,6 %).
Über Schmerzen an der Injektionsstelle von mehr als 3 Tagen Dauer nach Verabreichung von ViATIM berichteten 17,4 % der Geimpften. Nach Verabreichung des monovalenten Typhus-Vi-Impfstoffs waren es 2,8 %, nach Verabreichung des monovalenten Hepatitis A-Impfstoffs 0,6 % der Geimpften.
7,9 % der mit ViATIM Geimpften berichteten über starke Ödeme/Indurationen (> 5 cm) an der Injektionsstelle. Wurden die beiden monovalenten Impfstoffe zeitgleich an unterschiedlichen Körperstellen verabreicht, berichteten 1,7 % der Geimpften über starke Ödeme/Indurationen (1,1 % an der Injektionsstelle des Typhus-Vi-Impfstoffs und 0,6 % an der Injektionsstelle des Hepatitis A-Impfstoffs).
Die Häufigkeit von systemischen Reaktionen nach Verabreichung von ViATIM war vergleichbar mit der bei zeitgleicher Verabreichung der monovalenten Impfstoffe an unterschiedlichen Körperstellen.
Alle Reaktionen bildeten sich ohne Folgeerscheinungen zurück.
b. Tabellarische Auflistung der Nebenwirkungen
Die Daten zu den Nebenwirkungen stammen aus klinischen Studien sowie aus der weltweiten PostMarketing-Beobachtung.
Innerhalb einer Organsystemklasse sind die Nebenwirkungen nach abnehmenden Häufigkeiten, die wie folgt definiert sind, aufgeführt:
Sehr häufig (> 1/10)
Häufig (> 1/100, < 1/10)
Gelegentlich (> 1/1.000, < 1/100)
Selten (> 1/10.000, < 1/1.000)
Sehr selten (< 1/10.000)
Nicht bekannt (Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar)
Basierend auf Spontanmeldungen wurden diese Nebenwirkungen nach Markteinführung von ViATIM nur sehr selten berichtet. Da diese Angaben auf freiwilligen Spontanmeldungen aus einer Population, deren Größe nicht bekannt ist, basieren, ist es nicht immer möglich, die Häufigkeit der Nebenwirkung bzw. den Kausalzusammenhang mit der Impfstoffgabe zuverlässig einzuschätzen.
Innerhalb jeder Häufigkeitsgruppe werden die Nebenwirkungen nach abnehmendem Schweregrad angegeben.
Erkrankungen des Immunsystems
Nicht bekannt: anaphylaktische / anaphylaktoide Reaktionen einschließlich Schock, Serumkrankheit
Erkrankungen des Nervensystems Sehr häufig: Kopfschmerzen
Gelegentlich: Schwindel
Nicht bekannt: vasovagale Synkope als Reaktion auf die Injektion, Parästhesien
Erkrankungen des Gastrointestinaltrakts Häufig: Übelkeit, Durchfall
Nicht bekannt: Erbrechen, Bauchschmerzen
Erkrankungen der Haut und des Unterhautzellgewebes Gelegentlich: Juckreiz, Ausschlag Nicht bekannt: Urtikaria
Skelettmuskulatur-, Bindegewebs- und Knochenerkrankungen Sehr häufig: Myalgien Häufig: Arthralgien
Allgemeine Erkrankungen und Beschwerden am Verabreichungsort
Sehr häufig: Unwohlsein, Abgeschlagenheit, Beschwerden an der Injektionsstelle (Schmerzen, Induration, Ödeme und Erytheme)
Häufig: Fieber
Untersuchungen
Nicht bekannt: Anstieg der Transaminasen (leicht und reversibel)
Folgende Nebenwirkungen traten nach Anwendung des monovalenten Typhus-Vi-Polysaccharid-Impfstoffs bzw. des monovalenten inaktivierten Hepatitis A-Impfstoffs auf; sie wurden seit Markteinführung von ViATIM bislang nicht berichtet:
Erkrankungen der Atemwege, des Brustraums und Mediastinums Nicht bekannt: Verschlimmerung von Asthma
Allgemeine Erkrankungen und Beschwerden am Verabreichungsort Sehr selten: Knötchen am Injektionsort
c. Kinder und Jugendliche
Es liegen keine Daten zur Sicherheit von ViATIM bei Kindern und Jugendlichen unter 16 Jahren vor. Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie
ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels.
Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung dem
Bundesinstitut für Impfstoffe und biomedizinische Arzneimittel
Paul-Ehrlich-Institut
Paul-Ehrlich-Str. 51-59
63225 Langen
Tel: +49 6103 77 0
Fax: +49 6103 77 1234
Website: www.pei.de
anzuzeigen.
4.9 Überdosierung
In Verbindung mit ViATIM wurden Fälle von Überdosierung berichtet, wenn es zeitgleich mit Typhus-Polysaccharid- und/oder Hepatitis A-Impfstoffen angewendet wurde. Die berichteten Reaktionen entsprachen in ihrer Art den in Abschnitt 4.8 beschriebenen Nebenwirkungen.
5. PHARMAKOLOGISCHE EIGENSCHAFTEN
5.1 Pharmakodynamische Eigenschaften
Pharmakotherapeutische Gruppe: Viraler und bakterieller Impfstoff, kombiniert ATC-Code: J07CA10 Typhus-Hepatitis A
In vier klinischen Studien mit insgesamt 1.090 Probanden (Studien mit jeweils 179, 610, 243 bzw. 58 Personen) wurde die Immunantwort auf ViATIM untersucht.
14 Tage nach der ersten Impfung liegt die Seroprotektionsrate für HAV (% > 20 I.E./l) zwischen 95,6 % und 99,4 %; nach 28 Tagen zwischen 98,7 % und 100 %.
Die Seroprotektionsrate für Typhus Vi (% > 1 pg/ml) liegt nach 14 Tagen zwischen 83 % und 89 %, nach 28 Tagen zwischen 69,8 % und 91 %.
In einer Studie wurden die Seroprotektionsraten gegen das Vi-Antigen im Abstand von 1, 2 und 3 Jahren nach Verabreichung der ersten Dosis ViATIM sowie nach einer Auffrischimpfung 3 Jahre später untersucht (Tabelle 1).
Tabelle 1:
|
ViATIM | ||||
|
Jahr 1 |
Jahr 2 |
Jahr 3 |
28 Tage nach Auffrischimpfung 3 Jahre später | |
|
Anzahl der Geimpften |
139 |
124 |
112 |
46 |
|
Geimpfte mit Impfschutz in % (% > 1 pg/ml) |
44,6 |
40,3 |
32,1 |
69,6 |
|
(95 % Konfidenzintervall) |
(36,2-53,3) |
(31,6-49,5) |
(23,6-41,6) |
(54,2-82,3) |
Serologische Daten zeigen, dass Personen, die auf die erste Dosis ViATIM eine Immunantwort gezeigt haben, bis zu 36 Monate vor Hepatitis A geschützt sind. Die Seroprotektionsraten gegen das HAV-Antigen 1, 2 und 3 Jahre nach Verabreichung der ersten Dosis ViATIM sowie nach einer Auffrischimpfung 3 Jahre später sind in Tabelle 2 dargestellt:
Tabelle 2:
|
ViATIM | ||||
|
Jahr 1 |
Jahr 2 |
Jahr 3 |
28 Tage nach Auffrischimpfung 3 Jahre später | |
|
Anzahl der Geimpften |
140 |
124 |
112 |
46 |
|
% > 20 I.E./l |
99,3 |
98,4 |
99,1 |
100 |
|
(95 % Konfidenzintervall) |
(96,1-100) |
(94,3-99,8) |
(95,1-100) |
(92,3-100) |
Vergleichbare Ergebnisse wurden zu allen Zeitpunkten bei Personen der Kontrollgruppe beobachtet, denen zeitgleich ein monovalenter Typhus Vi-Polysaccharid-Impfstoff und ein monovalenter Hepatitis A-Impfstoff verabreicht wurde.
In einer offenen, randomisierten Studie wurde die Immunogenität einer zeitgleichen Verabreichung von ViATIM mit Td-IPV-Impfstoff (kombinierter, adsorbierter Tetanus-, niedrig dosierter Diphtherie-und inaktivierter Poliomyelitis-Impfstoff) an zwei unterschiedlichen Körperstellen mit der Immunogenität einer Verabreichung zu verschiedenen Zeitpunkten bei gesunden Erwachsenen verglichen. 28 Tage nach der Impfung wurden in der Per-Protocol-Population die folgenden Serokonversions- bzw. Seroprotektionsraten beobachtet:
Tabelle 3:
|
Gruppe A (zeitgleiche Verabreichung) |
Gruppe B (Verabreichung zu verschiedenen Zeitpunkten) | |
|
Anzahl der Geimpften |
N=161 |
N=154 |
|
Anti-HAV-Serokonversionsrate (> 20 mI.E./ml) n (%) [95 % KI] |
139 (100 %)* [97,3; 100,0] |
127 (100 %)** [97,1; 100,0] |
|
Anti-Vi-Serokonversionsrate (> 4-facher Anstieg) n (%) [95 % KI] |
134 (83,2 %) [76,7; 88,2] |
135 (87,7 %) [81,5; 92,0] |
|
Anti-D-Seroprotektionsrate (> 0,1 I.E./ml) n (%) [95 % KI] |
158 (98,1 %) [94,7; 99,4] |
149 (96,8 %) [92,6; 98,6] |
|
Anti-T-Seroprotektionsrate (> 0,1 I.E./ml) n (%) [95 % KI] |
161 (100 %) [97,7; 100,0] |
154 (100 %) [97,6; 100,0] |
|
Anti-Polio-1-{1/dil-} Seroprotektionsrate (> 5) n (%) [95% KI] |
161 (100 %) [97,7; 100,0] |
154 (100 %) [97,6; 100,0] |
|
Anti-Polio-2-{1/dil-} Seroprotektionsrate (> 5) n (%) [95 % KI] |
161 (100 %) [97,7; 100,0] |
154 (100 %) [97,6; 100,0] |
|
Anti-Polio-3-{1/dil-} Seroprotektionsrate (> 5) n (%) [95 % KI] |
161 (100 %) [97,7; 100,0] |
154 (100 %) [97,6; 100,0] |
* N=139 (initial HAV-seronegative Probanden) ** N=127 (initial HAV-seronegative Probanden)
Die Nichtunterlegenheit der zeitgleichen Verabreichung von ViATIM und des Td-IPV-Impfstoffs gegenüber der Verabreichung zu verschiedenen Zeitpunkten wurde für alle Valenzen mit Ausnahme der Vi-Valenz nachgewiesen.
Für die Vi-Valenz waren die Seroprotektionsraten (Anti-Vi-Titer > 1 gg/ml) von 7,5 % in Gruppe A und 7,1 % in Gruppe B an Tag 0 auf 86,3 % bzw. 94,8% 28 Tage nach der Impfung angestiegen. Bei initial nicht geschützten Probanden (Anti-Vi-Titer < 1 gg/ml) wurden 28 Tage nach der Impfung die folgenden Serokonversionsraten beobachtet:
Tabelle 4:
|
Gruppe A |
Gruppe B | |
|
(Zeitgleiche |
(Verabreichung zu verschiedenen |
|
Verabreichung) |
Zeitpunkten) | |
|
Anzahl der Geimpften |
N=149 |
N=143 |
|
Anti-Vi- Serokonversionsrate (> 4-facher Anstieg) n (%) [95 % KI] |
132 (88,6 %) [82,5; 92,8] |
128 (89,5 %) [83,4; 93,5] |
Bei initial nicht geschützten Probanden war die Anti-Vi-Serokonversionsrate (> 4-facher Anstieg) bei zeitgleicher Verabreichung der Impfstoffe gegenüber derjenigen bei Verabreichung zu verschiedenen Zeitpunkten nicht unterlegen.
Kinder und Jugendliche
Es liegen keine Daten zur Wirksamkeit von ViATIM bei Kindern und Jugendlichen unter 16 Jahren vor.
5.2 Pharmakokinetische Eigenschaften Für Impfstoffe nicht zutreffend
5.3 Präklinische Daten zur Sicherheit
Basierend auf den Studien zur Toxizität nach Einzeldosen und bei wiederholter Verabreichung sowie zur lokalen Verträglichkeit lassen die präklinischen Daten, die mit ViATIM oder den beiden in ViATIM enthaltenen monovalenten Impfstoffen erhalten wurden, keine besonderen Gefahren für den Menschen erkennen.
6. PHARMAZEUTISCHE ANGABEN
6.1 Liste der sonstigen Bestandteile
Inaktivierte Hepatitis A-Komponente:
Phenoxyethanol-Lösung
Formaldehyd
Medium 199 Hanks (ohne Phenolrot)*, ergänzt mit Polysorbat 80
* Medium 199 Hanks (ohne Phenolrot) ist ein Komplex aus Aminosäuren (einschließlich Phenylalanin), Mineralsalzen, Vitaminen und anderen Bestandteilen (einschließlich Glukose), gelöst in Wasser für Injektionszwecke und einem durch Zusatz von Salzsäure oder Natriumhydroxid angepassten pH-Wert.
Typhus-Vi-Polysaccharid-Komponente: gelöster Phosphatpuffer:
Natriumchlorid
Dinatriumhydrogenphosphat-Dihydrat Natriumdihydrogenphosphat-Dihydrat Wasser für Injektionszwecke
6.2 Inkompatibilitäten
Da keine Kompatibilitätsstudien durchgeführt wurden, darf dieser Impfstoff nicht mit anderen Impfstoffen oder Arzneimitteln gemischt werden.
6.3 Dauer der Haltbarkeit
3 Jahre
Das Verfalldatum des Impfstoffs ist auf der Doppelkammer-Fertigspritze und auf der Faltschachtel mit Monat und Jahr aufgedruckt. Nach Ablauf des angegebenen Monats darf der Impfstoff nicht mehr verwendet werden.
Der zubereitete Impfstoff ist unmittelbar nach dem Mischen der beiden Komponenten zu verabreichen.
6.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung
Im Kühlschrank lagern (2 °C - 8 °C).
Nicht einfrieren!
Das Behältnis in der Originalverpackung aufbewahren, um den Inhalt vor Licht zu schützen.
6.5 Art und Inhalt des Behältnisses
Doppelkammer-Fertigspritze (Glas): 0,5 ml Suspension in der hinteren Kammer (angrenzend an den Kolbenstopfen) und 0,5 ml Lösung in der vorderen Kammer (angrenzend an die Kanüle), mit einem Kolbenstopfen (Chlorobutyl- und Bromobutylgummi-Elastomer-Gemisch), einer Schutzkappe (Elastomer) und einem Trennstopfen (Elastomer). Packungsgrößen mit 1 oder 10 Fertigspritzen mit oder ohne beigepackte Kanüle.
Nicht alle zugelassenen Packungsgrößen und Handelsformen müssen erhältlich sein.
6.6 Besondere Vorsichtsmaßnahmen für die Beseitigung und sonstige Hinweise für die Handhabung
Die beiden Einzelkomponenten dürfen erst unmittelbar vor Verabreichung des Impfstoffs gemischt werden.
Den Impfstoff vor dem Mischen und noch einmal vor der Verabreichung sorgfältig schütteln, um eine homogene Suspension zu erhalten. Der Inhalt der beiden Kammern wird durch langsames Vorschieben des Kolbens gemischt. Verabreicht wird 1 ml Impfstoff.
Weitere Anweisungen für die Handhabung der Doppelkammer-Fertigspritze siehe auch Abschnitt 12.
Vor der Verabreichung sollte der Impfstoff visuell auf Fremdpartikel untersucht werden. Nach dem Mischen entsteht eine weißlich-trübe Suspension. Der Impfstoff darf nicht verabreicht werden, wenn sich unerwartete Fremdpartikel darin befinden.
Nicht verwendetes Arzneimittel oder Abfallmaterial ist entsprechend den lokalen Vorschriften zu beseitigen.
7. INHABER DER ZULASSUNG
Sanofi Pasteur MSD GmbH Paul-Ehrlich-Str. 1
69181 Leimen Tel.: 06224 594-0 Fax: 06224 594-33 E-Mail: ISI@spmsd.com Internet: www.spmsd.de
8. ZUL ASSUN GSNUMMER(N)
PEI.H.02832.01.1
9. DATUM DER ERTEILUNG DER ZULASSUNG/VERLÄNGERUNG DER ZULASSUNG
Datum der Erteilung der Zulassung 22. November 2002 Datum der letzten Verlängerung der Zulassung 04. April 2007
10. STAND DER INFORMATION
Februar 2015
11. VERKAUFSABGRENZUNG
Verschreibungspflichtig
12. HINWEISE
Gemäß § 22 Infektionsschutzgesetz müssen alle Schutzimpfungen vom Impfarzt mit dem Impfdatum, Handelsnamen, der Chargen-Bezeichnung, der Angabe der Krankheit, gegen die geimpft wurde, sowie Name, Anschrift und Unterschrift des impfenden Arztes in einen Impfausweis eingetragen werden.
Häufig unterbleiben indizierte Impfungen, weil bestimmte Umstände irrtümlicherweise als Kontraindikationen angesehen werden. Einzelheiten hierzu und weitere Informationen finden Sie in den jeweils aktuellen Empfehlungen der Ständigen Impfkommission (STIKO) am Robert KochInstitut, aktuell abrufbar über www.stiko.de.
Anweisungen für die Handhabung der Doppelkammer-Fertigspritze
1.)


2.)
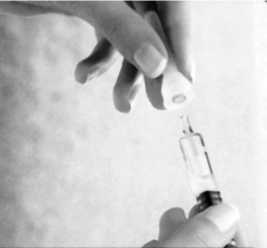
Entfernen Sie durch Drehen in Pfeilrichtung den Gummistopfen.
Bringen Sie eine Kanüle inklusive Kanülenschutz auf der Spritze an.
3.)
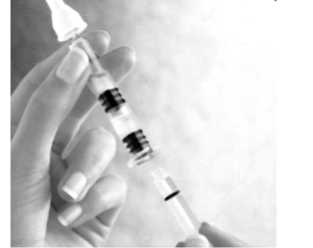
Schrauben Sie den Spritzenkolben in den Stopper.
4.)
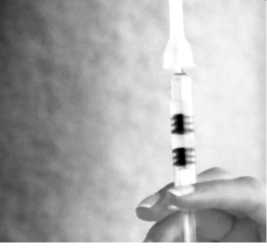
5.)
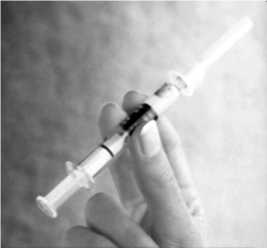
Schütteln Sie die Spritze, bis Sie eine homogene Suspension erhalten.
Mischen Sie die Impfstoffkomponenten, indem Sie den Kolben langsam nach oben drücken, wobei Sie die Spritze senkrecht halten.
6.)
Entfernen Sie den Kanülenschutz.
12/12