Xapro Creme
Gebrauchsinformation: Information für Patientinnen
Xapro® Creme, 1 mg / 1 g Vaginalcreme Estriol
Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen, denn sie enthält wichtige Informationen.
- Heben Sie die Packungsbeilage auf. Vielleicht möchten Sie diese später nochmals lesen.
- Wenn Sie weitere Fragen haben, wenden Sie sich an Ihren Arzt oder Apotheker.
- Dieses Arzneimittel wurde Ihnen persönlich verschrieben. Geben Sie es nicht an Dritte weiter. Es kann anderen Menschen schaden, auch wenn diese die gleichen Beschwerden haben wie Sie.
- Wenn Sie Nebenwirkungen bemerken, wenden Sie sich an Ihren Arzt oder Apotheker. Dies gilt auch für Nebenwirkungen, die nicht in dieser Packungsbeilage angegeben sind. Siehe Abschnitt 4.
Was in dieser Packungsbeilage steht
1. Was ist Xapro Creme und wofür wird sie angewendet?
2. Was sollten Sie vor der Anwendung von Xapro Creme beachten?
3. Wie ist Xapro Creme anzuwenden?
4. Welche Nebenwirkungen sind möglich?
5. Wie ist Xapro Creme aufzubewahren?
6. Inhalt der Packung und weitere Informationen
1. Was ist Xapro Creme und wofür wird sie angewendet?
Xapro Creme enthält ein weibliches Geschlechtshormon (Estrogen) zur Anwendung in der Scheide, das zur Behandlung lokaler Beschwerden geeignet ist.
Xapro Creme wird angewendet zur lokalen Behandlung von estrogenmangelbedingten Beschwerden im Bereich der Scheide bei Frauen nach der letzten Periodenblutung (Menopause).
2. Was sollten Sie vor der Anwendung von Xapro Creme beachten?
Xapro Creme darf nicht angewendet werden,
- wenn Sie allergisch gegen Estriol oder einen der in Abschnitt 6. genannten sonstigen Bestandteile dieses Arzneimittels sind,
- bei bestehendem oder früher aufgetretenem Brustkrebs bzw. einem entsprechenden Verdacht,
- bei anderen Tumoren, deren Wachstum durch die Zufuhr bestimmter weiblicher Geschlechtshormone (Estrogene) angeregt wird (v. a. Krebs der Gebärmutterschleimhaut), oder einem entsprechenden Verdacht,
- bei unbehandelter übermäßiger Verdickung der Gebärmutterschleimhaut (Endometriumhyperplasie),
- bei Blutungen aus der Scheide, deren Ursache vom Arzt nicht geklärt ist,
- bei bestehenden venösen thromboembolischen Erkrankungen (Blutgerinnselbildung in den tiefen Venen, Lungenembolie),
- bei schwerer Nierenfunktionsstörung.
Warnhinweise und Vorsichtsmaßnahmen
Bitte sprechen Sie mit Ihrem Arzt oder Apotheker, bevor Sie Xapro Creme anwenden.
Vor Beginn der Behandlung sowie in regelmäßigen, von Ihrem Arzt für Sie persönlich festgelegten Abständen (mindestens alle 3 Monate), wird Ihr Arzt feststellen, ob eine weitere Behandlung notwendig ist.
Medizinische Untersuchungen/Nachuntersuchungen:
Vor Beginn bzw. Wiederaufnahme der Behandlung sollte eine vollständige Erfassung aller wichtigen Krankheiten in Ihrer Vorgeschichte sowie in der Ihrer nahen Verwandten durchgeführt werden. Weiterhin sollte vor Beginn der Behandlung und in regelmäßigen Abständen während der Behandlung mit Xapro Creme eine sorgfältige körperliche und - im Speziellen - frauenärztliche Untersuchung durchgeführt werden, die sich in Häufigkeit und Art nach Ihrer persönlichen Gesundheitssituation richtet. Ihr Arzt sollte Ihnen erläutern, welche Veränderungen, z. B. unerwartete Blutungen aus der Scheide oder Veränderungen Ihrer Brüste, Sie ihm mitteilen müssen.
Scheideninfektionen sollten vor Beginn einer Behandlung mit Xapro Creme mit dafür bestimmten Arzneimitteln behandelt werden.
Situationen, die eine besondere ärztliche Überwachung erfordern:
Eine engmaschige Überwachung Ihres Gesundheitszustandes ist erforderlich, wenn bei Ihnen eine der folgenden Situationen oder Erkrankungen vorliegt oder früher vorlag bzw. sich während einer Schwangerschaft oder einer zurückliegenden Hormonbehandlung verschlechtert hat. Dies gilt auch für den Fall, dass eine der nachfolgend genannten Erkrankungen im Laufe der aktuellen Behandlung mit Xapro Creme auftritt bzw. sich verschlechtert.
Folgende Erkrankungen bzw. Risikofaktoren sind zu beachten:
- übermäßige Verdickung der Gebärmutterschleimhaut (Endometriumhyperplasie) in der Vorgeschichte (siehe unten),
- gutartige Geschwulst in der Muskelschicht der Gebärmutter (Leiomyom),
- Ansiedlung von Gebärmutterschleimhaut außerhalb der Gebärmutter (Endometriose),
- Risikofaktoren für estrogenabhängige Krebserkrankungen, z. B. Auftreten von Brustkrebs bei nahen Blutsverwandten (z. B. etwa Mutter, Großmutter, Schwestern),
- nachgewiesene Neigung zur Bildung von Blutgerinnseln in den tiefen Venen sowie in der Vergangenheit aufgetretene Blutgerinnsel in den Gefäßen (Thromboembolien),
- Migräne oder (starke) Kopfschmerzen,
- Schmetterlingsflechte (systemischer Lupus erythematodes - eine bestimmte Autoimmunerkrankung),
- Nierenfunktionsstörungen sowie durch Nierenerkrankungen hervorgerufene Flüssigkeitsansammlung im Körper (siehe auch Abschnitt „Xapro Creme darf nicht angewendet werden“),
- bestehende oder zurückliegende Lebererkrankungen (z. B. gutartige Lebergeschwulst -
Leberadenom), solange sich die relevanten Leberenzym-Werte nicht normalisiert haben;
- Bluthochdruck,
- Herzerkrankungen,
- gutartige Brusterkrankung mit Knotenbildung (fibrozystische Mastopathie).
Gründe für einen sofortigen Behandlungsabbruch:
Die Behandlung muss bei Auftreten einer Gegenanzeige sowie in den folgenden Situationen abgebrochen werden:
- Gelbsucht oder Verschlechterung der Leberfunktion,
- deutliche Erhöhung des Blutdrucks,
- neues Auftreten migräneartiger Kopfschmerzen,
- Schwangerschaft.
In verschiedenen Studien wurde für eine Hormonersatzbehandlung mit bestimmten systemisch angewendeten Estrogenen kombiniert mit Gelbkörperhormonen (Gestagenen) bzw. bei alleiniger Anwendung eines Estrogens ein erhöhtes Risiko für Brustkrebs, Blutgerinnselbildung in den Venen (Thrombose) und deren Verschleppung in die Lunge (Lungenembolie), koronare Herzerkrankung, Schlaganfall, wahrscheinliche Hirnleistungsstörung (Demenz), Eierstockkrebs und Gallenblasenerkrankungen festgestellt. Vergleichbar breit angelegte und aussagekräftige Studien zu den Risiken von in der Scheide angewendetem Estriol wurden nicht durchgeführt. Die wenigen zurzeit für die Anwendung von Estriol in der Scheide vorliegenden Daten weisen nicht darauf hin, dass die Risiken mit denen einer systemischen Hormonersatzbehandlung vergleichbar wären.
Übermäßige Verdickung der Gebärmutterschleimhaut (Endometriumhyperplasie):
Gelegentlich können während der Behandlung Blutungen auftreten. Sollten Durchbruch- oder Schmierblutungen nach einigen Monaten der Anwendung auftreten oder nach Beendigung der Behandlung anhalten, müssen die Ursachen abgeklärt werden. Zum Ausschluss einer bösartigen Entartung kann eine Gewebeentnahme von Gebärmutterschleimhaut erforderlich sein.
Das Risiko für eine Endometriumhyperplasie und für einen Gebärmutterkrebs ist bei einer längerfristigen systemischen, alleinigen Gabe von Estrogenen erhöht. Für in der Scheide angewendetes Estriol liegen diesbezüglich keine eindeutigen Belege vor. Um eine Stimulierung der Gebärmutterschleimhaut zu vermeiden, sollte die im Abschnitt „Art und Dauer der Anwendung“ genannte Dosierung (1-mal täglich 0,5 mg) nicht überschritten und maximal 3 Wochen lang angewendet werden.
Erbliches Angioödem:
Wenn Sie an einem erblichen Angioödem leiden, können Arzneimittel, die Estrogene enthalten, Symptome eines Angioödems auslösen oder verschlimmern. Sie sollten umgehend Ihren Arzt aufsuchen, wenn Sie Symptome eines Angioödems an sich bemerken - wie Schwellungen von Gesicht, Zunge und/oder Rachen und/oder Schluckschwierigkeiten oder Hautausschlag zusammen mit Atemproblemen.
Hinweis:
Bitte beachten Sie, dass die Behandlung mit Xapro Creme nicht empfängnisverhütend ist und nicht vor HIV oder anderen sexuell übertragbaren Krankheiten schützt.
Kinder und Jugendliche
Xapro Creme ist nicht zur Anwendung bei Kindern und Jugendlichen bestimmt.
Anwendung von Xapro Creme zusammen mit anderen Arzneimitteln
Informieren Sie Ihren Arzt oder Apotheker wenn Sie andere Arzneimittel einnehmen/anwenden, kürzlich andere Arzneimittel eingenommen/angewendet haben oder beabsichtigen andere Arzneimittel einzunehmen/anzuwenden.
Die Wirkungen von Xapro Creme können bei gleichzeitiger Anwendung anderer Arzneimittel abgeschwächt werden. Dazu zählen bestimmte Antibiotika wie z. B. Cephalosporine, Neomycin, Ampicillin und Tetracycline.
Schwangerschaft und Stillzeit
Wenn Sie schwanger sind oder stillen, oder wenn Sie vermuten, schwanger zu sein oder beabsichtigen, schwanger zu werden, fragen Sie vor der Anwendung dieses Arzneimittels Ihren Arzt oder Apotheker um Rat.
Fragen Sie vor der Einnahme/Anwendung aller Arzneimittel Ihren Arzt oder Apotheker um Rat. Schwangerschaft
Sie dürfen Xapro Creme in der Schwangerschaft nicht anwenden. Wenn Sie während der Behandlung mit Xapro Creme schwanger werden, muss die Behandlung sofort abgebrochen werden.
Die meisten zurzeit vorliegenden, relevanten epidemiologischen Studien, in denen ein Fetus unbeabsichtigt Estrogen ausgesetzt wurde, zeigen beim Fetus keine Missbildungen oder Giftwirkungen.
Allerdings liegen keine Daten darüber vor, in welchem Umfang das ungeborene Kind dem Estriol ausgesetzt ist, das in die Scheide eingeführt wird.
Stillzeit
Sie dürfen Xapro Creme in der Stillzeit nicht anwenden.
Verkehrstüchtigkeit und Fähigkeit zum Bedienen von Maschinen
Es sind keine besonderen Vorsichtsmaßnahmen erforderlich.
Xapro Creme enthält Propylenglycol.
Propylenglycol kann Schleimhautreizungen hervorrufen.
3. Wie ist Xapro Creme anzuwenden?
Wenden Sie dieses Arzneimittel immer genau nach Absprache mit Ihrem Arzt oder Apotheker an. Fragen Sie bei Ihrem Arzt oder Apotheker nach, wenn Sie sich nicht sicher sind.
Zu Beginn und bei der Fortführung der Behandlung von Estrogenmangelbeschwerden wird Ihr Arzt Ihnen die niedrigste wirksame Dosis verordnen und die Behandlungsdauer so kurz wie möglich halten (siehe auch Abschnitt „Besondere Vorsicht bei der Anwendung von Xapro Creme ist erforderlich:“).
Bitte sprechen Sie mit Ihrem Arzt, wenn Sie den Eindruck haben, dass die Wirkung von Xapro Creme zu stark oder zu schwach ist.
Art und Dauer der Anwendung
Dieses Arzneimittel ist zur vaginalen Anwendung bestimmt.
Xapro Creme wird am besten abends vor dem Schlafengehen mit Hilfe des Applikators tief in die Scheide eingeführt bzw. auf die zu behandelnden Stellen im Scheidenbereich dünn aufgetragen.
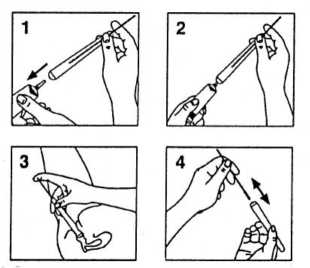
Hinweise zum Gebrauch des Applikators (Abbildungen 1 - 4):
Der grüne Stab des Applikators wird zunächst bis hinter den ersten Anschlag herausgezogen (er ragt dann ca. 2 cm aus dem Applikator). Danach wird die Tube geöffnet und der Applikator mit dem breiten Ende auf die Tube aufgesteckt (1).
Zur Anwendung 1/2 Applikatorfüllung Xapro Creme wird der Applikator durch Druck auf die Tube bis zum zweiten Anschlag mit der Creme gefüllt (2). Der grüne Stab ragt dann ca. 6 cm aus dem Applikator heraus.
Zur Anwendung 1 Applikatorfüllung Xapro Creme erfolgt die Füllung bis zum 3. Anschlag. Der grüne Stab ragt dann ca. 10 cm aus dem Applikator heraus.
Danach wird der Applikator von der Tube abgenommen und vorsichtig, in Rückenlage mit leicht angezogenen Beinen, möglichst tief in die Scheide eingeführt. Durch leichten Druck auf den grünen Stab wird die Creme dabei in die Scheide eingebracht (3). Dabei ist der grüne Stab vollständig bis zur Ausgangsposition hinter den ersten Anschlag einzuschieben.
Nach Gebrauch wird der Applikator mit warmem Wasser gereinigt. Hierzu kann der grüne Stab nach vorn aus dem breiten Ende des Applikators herausgedrückt und entnommen werden. Nach dem Abtrocknen wird der Applikator wieder zusammengesetzt (4).
Dosierung
Falls vom Arzt nicht anders verordnet, ist die übliche Dosis:
während der ersten 3 Wochen 1-mal täglich 0,5 mg (ausnahmsweise, falls erforderlich, bis höchstens 1,0 mg) Estriol. Danach ist auf eine Erhaltungstherapie von 2-mal wöchentlich 0,5 mg Estriol überzugehen. Eine Anwendung in der Scheide in höherer Dosierung ist nicht angezeigt.
Die Dosierung der Vaginalcreme soll nur mit Hilfe des beiliegenden Applikators erfolgen.
Wahl der verordneten Dosierung mit dem Applikator:
- 1 Applikatorfüllung enthält 1 g Xapro Creme mit 1,0 mg Estriol
- 1/2 Applikatorfüllung enthält 0,5 g Xapro Creme mit 0,5 mg Estriol.
Wenn Sie eine größere Menge Xapro Creme angewendet haben, als Sie sollten
Anzeichen einer möglichen Überdosierung sind Übelkeit, Erbrechen, Spannungsgefühl in den Brüsten und Blutungen aus der Scheide, die einige Tage später auftreten können. Fragen Sie Ihren Arzt um Rat, wenn Sie mehr als die empfohlene Menge an Xapro Creme angewendet haben.
Beschwerden einer Überdosierung lassen sich durch Verminderung der Dosis oder durch einen Behandlungsabbruch beseitigen.
Wenn Sie die Anwendung von Xapro Creme vergessen haben
- Bei täglicher Anwendung innerhalb der ersten (2 bis 3) Behandlungswochen:
Wenn Sie die vergessene Anwendung erst am nächsten Tag bemerken, sollten Sie diese nicht mehr nachholen. Fahren Sie in diesem Fall mit dem Dosierungsschema wie gewohnt fort.
- Bei 2-maliger Anwendung pro Woche:
Wenn Sie während der 2-maligen Anwendung pro Woche vergessen haben, Xapro Creme zur einmal gewählten Zeit anzuwenden, holen Sie dies so bald wie möglich nach.
Wenn Sie weitere Fragen zur Anwendung dieses Arzneimittels haben, wenden Sie sich an Ihren Arzt oder Apotheker.
Wie alle Arzneimittel kann auch dieses Arzneimittel Nebenwirkungen haben, die aber nicht bei jedem aufitreten müssen.
Bei den Häufigkeitsangaben zu Nebenwirkungen werden folgende Kategorien zugrunde gelegt:
Sehr häufig Häufig Gelegentlich Selten Sehr selten Nicht bekannt
mehr als 1 Behandelte von 10 1 bis 10 Behandelte von 100 1 bis 10 Behandelte von 1.000 1 bis 10 Behandelte von 10.000 weniger als 1 Behandelte von 10.000
Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar
Mögliche Nebenwirkungen:
Folgende Nebenwirkungen können während der Anwendung von Xapro Creme auftreten:
|
Systemorganklasse |
Nebenwirkungshäufigkeit | ||
|
Gelegentlich |
Selten |
Sehr selten | |
|
Gefäßerkrankungen |
Erhöhung des Blutdrucks | ||
|
Erkrankungen des MagenDarm-Trakts |
Übelkeit und andere Magen-DarmBeschwerden | ||
|
Skelettmuskulatur-, Bindegewebs- und Knochenerkrankungen |
Beinkrämpfe, „schwere Beine“ | ||
|
Erkrankungen der Geschlechtsorgane und der Brustdrüse |
Schmerzen und Spannungsgefühle in der Brust (während der ersten Wochen); Schmierblutungen; (vermehrter) Ausfluss |
Gebärmutter blutungen | |
|
Allgemeine Erkrankungen und Beschwerden am Verabreichungsort |
Ödeme mit vorübergehender Gewichtszunahme, Reizungen der Scheide mit Hitzegefühl, Juckreiz, Brennen und Rötungen |
(migräneartige) Kopfschmerzen | |
Arzneimittel, die wie Xapro Creme Estrogene enthalten, können Symptome eines Angioödems auslösen oder verschlimmern (siehe auch „Besondere Vorsicht bei der Anwendung von Xapro Creme ist erforderlich“).
Gegenmaßnahmen:
Treten bei Ihnen nach der Anwendung von Xapro Creme Nebenwirkungen auf, so informieren Sie bitte Ihren behandelnden Arzt, der dann über eventuell einzuleitende Gegenmaßnahmen entscheidet.
Nebenwirkungen, bei denen Sie gegebenenfalls sofort einen Arzt aufsuchen müssen oder bei denen ein Abbruch der Behandlung erforderlich ist, sind im Abschnitt „Besondere Vorsicht bei der Anwendung von Xapro( Creme ist erforderlich:“ aufgeführt.
Meldung von Nebenwirkungen
Wenn Sie Nebenwirkungen bemerken, wenden Sie sich an Ihren Arzt oder Apotheker. Dies gilt auch für Nebenwirkungen, die nicht in dieser Packungsbeilage angegeben sind. Sie können Nebenwirkungen auch direkt dem Bundesinstitut für Arzneimittel und Medizinprodukte, Abt. Pharmakovigilanz, Kurt-Georg-Kiesinger-Allee 3, D-53175, Bonn, Website: http://www.bfarm.de anzeigen. Indem Sie Nebenwirkungen melden, können Sie dazu beitragen, dass mehr Informationen über die Sicherheit dieses Arzneimittels zur Verfügung gestellt werden.
5. Wie ist Xapro Creme aufzubewahren?
Bewahren Sie dieses Arzneimittel für Kinder unzugänglich auf.
Sie dürfen das Arzneimittel nach dem auf dem Umkarton und auf der Tube nach „Verwendbar bis“ angegebenen Verfalldatum nicht mehr verwenden. Das Verfalldatum bezieht sich auf den letzten Tag des angegebenen Monats.
Nicht über 25 °C lagern.
Hinweis auf Haltbarkeit nach Anbruch:
Nach Anbruch soll Xapro Creme nicht länger als 6 Monate verwendet werden.
6. Inhalt der Packung und weitere Informationen
Was Xapro Creme enthält
- Der Wirkstoff ist: Estriol. 1 g Vaginalcreme enthält 1,0 mg Estriol.
- Die sonstigen Bestandteile sind: Dequaliniumchlorid, Duftstoffe (z. B. Zitronenöl), Docusat-Natrium, Propylenglycol, Dimeticon (350), selbstemulgierendes Glycerolmonostearat, mittelkettige Triglyceride, Glycerol(mono,di,tri)alkanoat (C8-C18), Macrogolcetylstearylether (Ph. Eur.) (25 EO), gereinigtes Wasser
Wie Xapro Creme aussieht und Inhalt der Packung:
weiße Vaginalcreme
Xapro Creme ist in Packungen mit 1 Tube zu 35 g Vaginalcreme und 1 Applikator und mit 1 Tube zu 50 g Vaginalcreme und 1 Applikator erhältlich.
Pharmazeutischer Unternehmer und Hersteller:
Jenapharm GmbH & Co. KG Otto-Schott-Straße 15 07745 Jena
Tel.: 03641 648888 Fax: 03641 648889
E-Mail: frauengesundheit@jenapharm.de
Diese Gebrauchsinformation wurde zuletzt überarbeitet im April 2014
8