Acular Augentropfen
PACKUNGSBEILAGE
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER ACULAR 5 mg/ml Augentropfen
Ketorolac-Trometamol
Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen.
- Heben Sie die Packungsbeilage auf. Vielleicht möchten Sie diese später nochmals lesen.
- Wenn Sie weitere Fragen haben, wenden Sie sich an Ihren Arzt oder Apotheker.
- Dieses Arzneimittel wurde Ihnen persönlich verschrieben. Geben Sie es nicht an Dritte weiter. Es kann anderen Menschen schaden, auch wenn diese dieselben Beschwerden haben wie Sie.
- Wenn eine der aufgeführten Nebenwirkungen Sie erheblich beeinträchtigt oder Sie Nebenwirkungen bemerken, die nicht in dieser Gebrauchsinformation angegeben sind, informieren Sie bitte Ihren Arzt oder Apotheker.
Diese Packungsbeilage beinhaltet:
1. Was ist ACULAR und wofür wird es angewendet?
2. Was müssen Sie vor der Anwendung von ACULAR beachten?
3. Wie ist ACULAR anzuwenden?
4. Welche Nebenwirkungen sind möglich?
5. Wie ist ACULAR aufzubewahren?
6. Weitere Informationen
1. WAS IST ACULAR UND WOFÜR WIRD ES ANGEWENDET?
ACULAR ist ein nichtsteroidales, entzündungshemmendes Arzneimittel.
Es wird zur Vorbeugung und Behandlung nichtinfektiöser Entzündungen des Auges nach Kataraktoperationen (grauer Star), die mit oder ohne Implantation einer intraokularen Linse erfolgen, angewendet.
2. WAS MÜSSEN SIE VOR DER ANWENDUNG VON ACULAR BEACHTEN?
ACULAR darf nicht angewendet werden,
- wenn Sie überempfindlich (allergisch) gegen Ketorolac-Trometamol oder einen der sonstigen Bestandteile von ACULAR sind.
- wenn Sie überempfindlich (allergisch) gegen Acetylsalicylsäure oder andere nichtsteroidale entzündungshemmende Wirkstoffe sind.
Besondere Vorsicht bei der Anwendung von ACULAR ist erforderlich,
wenn einer der folgenden Punkte bei Ihnen zutrifft.
Sie sollten ACULAR erst nach Rücksprache mit Ihrem Arzt anwenden,
• wenn Sie derzeit an einer der folgenden Erkrankungen leiden oder früher einmal gelitten haben,
- virale oder bakterielle Augenentzündungen
- Hornhautschädigungen
- Blutungsneigungen (z.B. Blutarmut) oder Magengeschwüre
- Diabetes
- rheumatoide Arthritis
- trockenes Auge
- Beschwerden beim Atmen (Bronchospasmen), Asthma nach Anwendung von nichtsteroidalen entzündungshemmenden Arzneimitteln
falls Sie kürzlich eine Augenoperation hatten
• wenn Sie Arzneimittel einnehmen, welche die Blutgerinnung hemmen (z.B. Antikoagulantien oder andere nichtsteroidale entzündungshemmende/antirheumatische Arzneimittel)
• wenn Sie Arzneimittel am Auge anwenden, die Kortikosteroide enthalten.
ACULAR kann
• die Zeichen einer Infektion maskieren
• die Wundheilung verlangsamen oder verzögern.
ACULAR sollte nicht zur Anwendung bei Kindern verschrieben werden.
Bei Anwendung von ACULAR mit anderen Arzneimitteln
Bitte informieren Sie Ihren Arzt oder Apotheker, wenn Sie andere Arzneimittel einnehmen / anwenden bzw. vor kurzem eingenommen / angewendet haben, auch wenn es sich um nicht verschreibungspflichtige Arzneimittel handelt.
Die gleichzeitige Anwendung von ACULAR und kortikosteroidhaltigen Arzneimitteln am Auge kann das Risiko von Wundheilungsstörungen erhöhen.
Wechselwirkungen mit anderen Arzneimitteln (z. B. Antibiotika, Beruhigungsmittel, ß-Blocker, Carboanhydrasehemmer, Miotika, Mydriatika, Lokalanästetika und Zykloplegika) sind bisher nicht bekannt.
Falls Sie noch weitere Medikamente am Auge anwenden, muss zwischen den Anwendungen der einzelnen Medikamente ein Abstand von mindestens 5 Minuten liegen. Wenden Sie Augensalben oder Augengele zum Schluß an.
Schwangerschaft und Stillzeit
Fragen Sie vor der Einnahme / Anwendung von allen Arzneimitteln Ihren Arzt oder Apotheker um Rat. ACULAR sollte bei Frauen im gebärfähigen Alter ohne schwangerschaftsverhütende Maßnahmen oder während der Schwangerschaft und Stillzeit nicht angewendet werden.
Verkehrstüchtigkeit und das Bedienen von Maschinen
Nach der Anwendung von ACULAR kann es zu vorübergehendem Schleiersehen kommen. Bis sich die Sicht geklärt hat, sollten Sie keine Fahrzeuge oder Maschinen bedienen.
Wichtige Informationen über bestimmte sonstige Bestandteile von ACULAR
ACULAR enthält Benzalkoniumchlorid als Konservierungsmittel.
Benzalkoniumchlorid kann Reizungen am Auge hervorrufen.
Kontaktlinsen müssen Sie vor der Anwendung entfernen und dürfen diese frühestens 15 Minuten nach der Anwendung wieder einsetzen. Benzalkoniumchlorid kann zur Verfärbung weicher Kontaktlinsen führen. Vermeiden Sie den Kontakt mit weichen Kontaktlinsen.
3. WIE IST ACULAR ANZUWENDEN?
Wenden Sie ACULAR immer genau nach Anweisung des Arztes an.
Bitte fragen Sie bei Ihrem Arzt oder Apotheker nach, wenn Sie sich nicht ganz sicher sind.
Falls vom Arzt nicht anders verordnet, ist die übliche Dosis 3 x täglich 1 Tropfen in das betroffene Auge. Mit der Anwendung 24 Stunden vor der Operation beginnen und 3-4 Wochen nach der Kataraktoperation fortsetzen.
Hinweise zur Anwendung
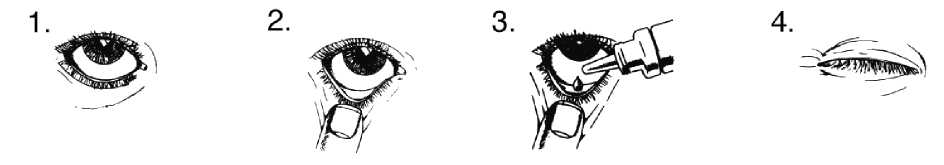
Waschen Sie sich vor jeder Anwendung die Hände und wenden Sie die Augentropfen wie folgt an:
1. Neigen Sie den Kopf leicht nach hinten und sehen Sie an die Decke.
2. Ziehen Sie das Unterlid vorsichtig nach unten, bis sich eine kleine Tasche gebildet hat.
3. Drücken Sie auf die umgedrehte Tropfflasche, damit ein Tropfen in Ihr Auge fällt.
4. Lassen Sie das Unterlid los und halten Sie das Auge 30 Sekunden lang geschlossen.
Um eine Verschmutzung oder eine Verletzung zu vermeiden, berühren Sie nicht die Tropferspitze mit dem Auge oder anderen Gegenständen.
Verschließen Sie die Flasche gleich nach der Anwendung.
Wenn Sie weitere Fragen zur Anwendung des Arzneimittels haben, fragen Sie Ihren Arzt oder Apotheker
Wenn Sie eine größere Menge von ACULAR angewendet haben, als Sie sollten
Es ist unwahrscheinlich, dass bei Anwendung von zu vielen Augentropfen Nebenwirkungen auftreten. Führen Sie die nächste Anwendung zum vorgesehenen Zeitpunkt durch.
Falls Sie aus Versehen dieses Arzneimittel trinken, sollten Sie zur Verdünnung Flüssigkeit trinken und setzen Sie sich bitte mit Ihrem Arzt oder Apotheker in Verbindung.
Wenn Sie die Anwendung von ACULAR vergessen haben
Wenn Sie eine Anwendung vergessen haben, holen Sie diese nach, sobald Sie das Versäumnis bemerken, es sei denn, die nächste Dosis steht bereits an. In diesem Fall lassen Sie die versäumte Anwendung aus. Wenden Sie die nächste Dosis wie vorgesehen an und setzen Sie dann die Behandlung planmäßig fort.
Wenden Sie nicht die doppelte Dosis an, wenn Sie die vorherige Anwendung vergessen haben.
Wenn Sie die Anwendung von ACULAR abbrechen
Wenden Sie ACULAR nach Anweisung Ihres Arztes an. Sprechen Sie mit Ihrem Arzt, bevor Sie die Behandlung ändern oder beenden.
Wenn Sie weitere Fragen zur Anwendung des Arzneimittels haben, fragen Sie Ihren Arzt oder Apotheker.
4. WELCHE NEBENWIRKUNGEN SIND MÖGLICH?
Wie alle Arzneimittel kann ACULAR Nebenwirkungen haben, die aber nicht bei jedem auftreten müssen.
Bei den Häufigkeitsangaben zu Nebenwirkungen werden folgende Kategorien zugrunde gelegt:
Sehr häufig: Häufig: Gelegentlich: Selten:
Sehr selten: Nicht bekannt:
mehr als 1 Behandelter von 10 1 bis 10 Behandelte von 100 1 bis 10 Behandelte von 1.000 1 bis 10 Behandelte von 10.000 weniger als 1 Behandelter von 10.000
Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar
Die folgenden Nebenwirkungen können unter ACULAR auftreten:
Häufig: Kopfschmerzen, Entzündung der Iris (Regenbogenhaut), entzündliche
Zellablagerungen im Auge, Blutungen der Netzhaut (lichtempfindliche Schicht des Auges), Schwellung der zentralen Netzhaut, Augenreizungen (einschließlich Brennen am Auge), Augenjucken, Schädigung des Auges, erhöhter Druck im Auge.
Nebenwirkungen, die die Hornhaut (Augenoberfläche) betreffen, sind wahrscheinlicher, wenn ACULAR mehr als 24 Stunden vor der Operation oder länger als 2 Wochen angewendet wird oder wenn Sie zur selben Zeit Augentropfen mit topischen Steroide (z. B. Kortison) anwenden oder wenn Sie ein Augenleiden an der Hornhaut haben. Bei Schmerzen, vermehrter Reizung im Auge oder Änderungen im Sehvermögen sollten Sie umgehend Ihren Arzt aufsuchen.
Seit der Vermarktung wurden Reizungen der Augen und Entzündungen der Iris und dem inneren Auge oder der Augenoberfläche (Hornhaut) nach der Anwendung von ACULAR beobachtet und werden als behandlungsbedingt angesehen.
Es liegen Berichte nach Markteinführung über Schwierigkeiten beim Atmen, pfeiffendes Atmen oder Husten oder Verschlechterung von Asthma bei Patienten vor, die entweder eine bekannte Überempfindlichkeit gegenüber Acetylsalicylsäure/nicht steroidalen entzündungshemmenden Arzneimitteln oder in der Vorgeschichte bei der Anwendung von ACULAR Asthma bekamen, das hierzu beigetragen haben könnte.
Akute Augeninfektionen können durch die Anwendung lokaler entzündungshemmender Arzneimittel, einschließlich ACULAR, überdeckt und nicht erkannt werden.
Informieren Sie bitte Ihren Arzt oder Apotheker, wenn eine der aufgeführten Nebenwirkungen Sie erheblich beeinträchtigt oder Sie Nebenwirkungen bemerken, die nicht in dieser Gebrauchsinformation angegeben sind.
5. WIE IST ACULAR AUFZUBEWAHREN?
Arzneimittel für Kinder unzugänglich aufbewahren.
Sie dürfen ACULAR nach dem auf dem Etikett und dem Umkarton nach „verwendbar bis“ angegebenen Verfalldatum nicht mehr anwenden. Das Verfalldatum bezieht sich auf den letzten Tag des Monats.
Für dieses Arzneimittel sind keine besonderen Lagerungsbedingungen erforderlich.
Nach Anbruch können die Augentropfen verunreinigt werden, was zu Augeninfektionen führen kann. Daher müssen Sie die Flasche vier Wochen nach dem erstmaligen Öffnen wegwerfen, auch wenn noch restliche Lösung vorhanden ist.
6. WEITERE INFORMATIONEN Was ACULAR enthält
Der Wirkstoff ist Ketorolac-Trometamol 5 mg/ml.
Die sonstigen Bestandteile sind Benzalkoniumchlorid, Natriumedetat (Ph.Eur.), Octoxinol 40, Natriumchlorid, Natriumhydroxid bzw. verdünnte Salzsäure (zur pH-Wert Einstellung) und gereinigtes Wasser.
Wie ACULAR aussieht und Inhalt der Packung
ACULAR ist eine klare, farblose bis blassgelbe Augentropfenlösung in einer Kunststoffflasche mit Schraubverschluss.
Jede Flasche enthält entweder 5 ml oder 10 ml Augentropfen.
Packungsgrößen: 1 x 5 ml, 3 x 5 ml oder 1 x 10 ml.
Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht. Zulassungsinhaber und Hersteller
Allergan Pharmaceuticals Ireland, Castlebar Road, Westport, County Mayo, Irland Mitvertreiber
Pharm-Allergan GmbH, Pforzheimer Straße 160, 76275 Ettlingen, Telefon (0 72 43) 5 01-0 Diese Gebrauchsinformation wurde zuletzt genehmigt im 01/2014.
6