Meto-Succinat Hct Sandoz 95/12,5 Mg Retardtabletten
Fachinformation (Zusammenfassung der Merkmale des Arzneimittels)
1. Bezeichnung des Arzneimittels
Meto-Succinat HCT Sandoz 95/12,5 mg Retardtabletten
2. Qualitative und quantitative Zusammensetzung
Wirkstoffe: Metoprololsuccinat (Ph. Eur.) und Hydrochlorothiazid
1 Retardtablette enthält 95 mg Metoprololsuccinat (Ph.Eur.) und 12,5 mg Hydrochlorothiazid.
Sonstige Bestandteile mit bekannter Wirkung: Lactose-Monohydrat, Glucose, Sucrose
Vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt 6.1.
3. Darreichungsform
Retardtablette
Hellgelbe, runde Retardtablette mit einseitiger Bruchkerbe
Die Bruchkerbe dient nur zum Teilen der Tablette um das Schlucken zu erleichtern, und nicht zum Teilen in gleiche Dosen.
4. Klinische Angaben
4.1 Anwendungsgebiete
Nicht organbedingter Bluthochdruck (essentielle Hypertonie).
Das Kombinationspräparat Meto-Succinat HCT Sandoz 95/12,5 mg ist nur dann zu empfehlen, wenn eine vorangegangene Therapie mit einem der Einzelwirkstoffe (retardiertes Metoprololsuccinat oder Hydrochlorothiazid) keine ausreichende Blutdrucknormalisierung bewirken konnte.
4.2 Dosierung und Art der Anwendung
Grundsätzlich sollte die blutdrucksenkende Behandlung mit der jeweils niedrigsten vorgesehenen Dosis eines Einzelwirkstoffes begonnen und bei Bedarf langsam gesteigert werden.
Die fixe Kombination Meto-Succinat HCT Sandoz 95/12,5 mg sollte erst nach vorangegangener Therapie mit entweder Hydrochlorothiazid oder
retardiertem Metoprololsuccinat angewendet werden, falls durch den entsprechenden Einzelwirkstoff kein ausreichender Therapieerfolg erzielt werden konnte.
Es gelten nachfolgende Dosierungsrichtlinien:
Als normale Tagesdosis soll 1 Retardtablette Meto-Succinat HCT Sandoz 95/12,5 mg eingenommen werden. Bei Bedarf kann die Dosis auf maximal 2 Retardtabletten täglich morgens als Einzeldosis erhöht werden.
Besonders bei gleichzeitigem Vorliegen einer ischämischen Herzerkrankung sollte Meto-Succinat HCT Sandoz 95/12,5 mg allmählich, d. h. über eine Periode von 7 bis 10 Tagen, abgesetzt werden, weil eine plötzliche Unterbrechung der Verabreichung zu einer Auslösung bzw. Zunahme der Symptome der ischämischen Herzerkrankung (z. B. Angina pectoris) führen kann.
Art und Dauer der Anwendung
Die Retardtabletten sind unzerkaut mit ausreichend Flüssigkeit (z. B. ein Glas Wasser) nach dem Essen einzunehmen.
Die Retardtabletten können geteilt werden, um die Einnahme zu erleichtern, aber nicht um geringere Dosierungen zu erreichen.
Es ist unbedingt darauf zu achten, dass die Tablettenhälften unmittelbar nacheinander eingenommen werden.
Die Dauer der Behandlung bestimmt der behandelnde Arzt.
Eine Unterbrechung oder Änderung der Dosierung darf nur auf ärztliche Anordnung erfolgen. Soll die Behandlung mit Meto-Succinat HCT Sandoz 95/12,5 mg nach längerer Anwendung unterbrochen oder abgesetzt werden, sollte dies grundsätzlich langsam ausschleichend erfolgen. Dies ist nötig, da abruptes Absetzen zur Minderdurchblutung des Herzmuskels (Herzischämie) mit neuerlicher Verschlimmerung einer Angina pectoris oder zu einem Herzinfarkt oder zum Wiederauftreten eines Bluthochdrucks führen kann.
Falls ein Patient eine zunehmende Bradykardie entwickelt, sollte Meto-Succinat HCT Sandoz 95/12,5 mg mit niedriger Dosierung gegeben oder ausschleichend abgesetzt werden.
Abruptes Absetzen von Beta-Blockern ist besonders bei Patienten mit hohem Risiko gefährlich und sollte deshalb vermieden werden. Falls die Therapie mit Metoprololsuccinat beendet werden soll, sollte dies allmählich über einen Zeitraum von mindestens 2 Wochen durchgeführt werden. Hierbei wird die Dosis jeweils um die Hälfte reduziert, bis schließlich eine ganze 25 mg Retardtablette auf eine halbe Retardtablette reduziert wird. Dabei kann eine reine Metoprolol-Retardtablette verabreicht werden. Die letzte Dosisstärke sollte vor dem Absetzen mindestens über 4 Tage gegeben werden. Falls Symptome auftreten, wird ein langsameres Absetzen empfohlen. Das plötzliche Absetzen von Beta-Blockern kann eine
chronische Herzmuskelschwäche verschlechtern und außerdem das Risiko für einen Herzinfarkt und plötzlichen Herztod erhöhen.
4.3
4.4
Gegenanzeigen
Meto-Succinat HCT Sandoz 95/12,5 mg darf nicht angewendet werden:
- bei Überempfindlichkeit gegen die Wirkstoffe Metoprololsuccinat, Hydrochlorothiazid oder verwandten Derivaten oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile
- bei Überempfindlichkeit gegenüber Sulfonamiden (mögliche Kreuzreaktionen beachten)
- bei AV-Block 2. und 3. Grades
- bei Sinusknoten-Syndrom
- bei sinutrialem Block
- bei kardiogenem Schock
- bei manifester Herzinsuffizienz, Lungenödem, Minderperfusion
- bei Patienten mit dauerhafter oder intermittierender inotroper Therapie mit Beta-Rezeptoragonisten
- bei Bradykardie (Ruhepuls kleiner als 50 Schläge pro Minute vor Behandlungsbeginn)
- bei Hypotonie (systolisch kleiner als 90 mmHg
- bei Azidose
- bei Spätstadien peripherer Durchblutungsstörungen
- bei bronchialer Hyperreagibilität
- bei gleichzeitiger Gabe von MAO-Hemmstoffen (Ausnahme MAO-B-Hemmstoffe)
- bei schwerer Niereninsuffizienz (Oligurie oder Anurie; Kreatinin-Clearance kleiner als 30 ml/min und/oder Serum-Kreatinin über 1,8 mg/dl) oder akuter Nierenentzündung (Glomerulonephritis)
- bei Koma und Praecoma hepaticum
- bei Hypokaliämie, die auf eine Behandlung nicht anspricht (unter 3,5 mmol/l)
- bei Hyperkalzämie
- bei Gicht
- bei schwerer Hyponatriämie
- bei Hypovolämie
- in der Schwangerschaft und Stillzeit (siehe 4.6 „Schwangerschaft und Stillzeit“).
Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung
Eine besonders sorgfältige ärztliche Überwachung ist erforderlich bei:
- AV-Block 1. Grades
- zuckerkranken Patienten mit stark schwankenden Blutzuckerwerten sowie bei strengem Fasten
- Patienten mit einem hormonproduzierenden Tumor des Nebennierenmarks (Phäochromozytom, vorherige Therapie mit aBlockern erforderlich)
- Patienten mit eingeschränkter Leber- oder Nierenfunktion (SerumKreatinin > 1,2 < 1,8 mg/dl)
- Patienten, die gleichzeitig mit Digitalispräparaten, Glucocorticoiden oder Laxanzien behandelt werden
- zerebrovaskulären Durchblutungsstörungen
- koronarer Herzkrankheit.
Beta-Rezeptorenblocker können die Empfindlichkeit gegenüber Allergenen und die Schwere anaphylaktischer Reaktionen, d. h. akuter allergischer Allgemeinreaktionen erhöhen. Deshalb ist eine strenge Indikationsstellung bei Patienten mit schweren Überempfindlichkeitsreaktionen in der Vorgeschichte und bei Patienten unter Therapie zur Schwächung bzw. Aufhebung der allergischen Reaktionsbereitschaft (Desensibilisierungstherapien: Vorsicht, überschießende anaphylaktische Reaktionen) geboten.
Bei Patienten mit einer Psoriasis in der Eigen- oder Familienanamnese sollte die Verordnung von Arzneimitteln, die Beta-Rezeptorenblocker enthalten, nur nach sorgfältiger Nutzen-Risiko-Abwägung erfolgen.
Die Therapie mit Meto-Succinat HCT Sandoz 95/12,5 mg sollte abgebrochen werden bei therapieresistenter Entgleisung des Elektrolythaushalts, orthostatischen Beschwerden (z. B. Schwarzwerden vor den Augen, Schwindel, evtl. Ohnmacht),
Überempfindlichkeitsreaktionen, starken Beschwerden im Magen- oder Darmtrakt, zentralnervösen Störungen, Pankreatitis, Blutbildveränderungen, bei akuter Gallenblasenentzündung, beim Auftreten einer Vaskulitis und Verschlimmerung einer bestehenden Kurzsichtigkeit.
Während der Behandlung mit Meto-Succinat HCT Sandoz 95/12,5 mg sollten die Patienten auf eine ausreichende Flüssigkeitsaufnahme achten und wegen des Kaliumverlustes kaliumreiche Nahrungsmittel zu sich nehmen (Bananen, Gemüse, Nüsse); evtl. ist wegen des erhöhten Kaliumverlustes eine gleichzeitige Therapie mit Kalium-sparenden Diuretika erforderlich.
Die Kaliumkontrollen sollten anfangs häufiger erfolgen. Wenn sich ein Gleichgewicht im Kaliumhaushalt eingestellt hat, genügt es, den SerumKalium-Spiegel seltener zu kontrollieren.
Ferner sollten Glucose, Harnsäure, Blutfette und Kreatinin im Serum in regelmäßigen Abständen kontrolliert werden.
Schwangerschaft
Bei Patientinnen mit Schwangerschaftswunsch sollte eine Umstellung auf eine alternative blutdrucksenkende Behandlung mit geeignetem Sicherheitsprofil für Schwangere erfolgen. Wird eine Schwangerschaft festgestellt, ist die Behandlung mit HCTZ unverzüglich zu beenden und, wenn erforderlich, eine alternative Therapie zu beginnen (siehe Abschnitt
4.3 und 4.6).
Hinweise
Die Anwendung von Meto-Succinat HCT Sandoz 95/12,5 mg kann bei Dopingkontrollen zu positiven Ergebnissen führen. Eine missbräuchliche Anwendung des Arzneimittels Meto-Succinat HCT Sandoz 95/12,5 mg zu Dopingzwecken kann die Gesundheit gefährden.
Patienten mit der seltenen hereditären Galactose- oder FructoseIntoleranz z. B. Galaktosämie, Lactase-Mangel, Glucose-Galactose-Malabsorption oder Saccharase-Isomaltase-Mangel sollten Meto-Succinat HCT Sandoz 95/12,5 mg nicht einnehmen.
Hinweis für Diabetiker
1 Retardtablette enthält weniger als 0,01 Broteinheiten (BE).
4.5
Wechselwirkungen mit anderen Arzneimitteln und sonstige
Wechselwirkungen
Folgende Wechselwirkungen zwischen dem vorliegenden Arzneimittel und
anderen Mitteln sind zu beachten:
- Bei gleichzeitiger Anwendung von Meto-Succinat HCT Sandoz 95/12,5 mg und Insulin oder oralen blutzuckersenkenden Medikamenten kann deren Wirkung verstärkt werden; die Symptome einer Hypoglykämie, besonders Tachykardie und Tremor, sind verschleiert oder abgemildert. Daher sind regelmäßige Blutzuckerkontrollen erforderlich.
- Die blutdrucksenkende Wirkung von Meto-Succinat HCT Sandoz 95/12,5 mg kann durch andere blutdrucksenkende Arzneimittel (besondere Vorsicht bei Prazosin), Barbiturate, Phenothiazine sowie trizyklische Antidepressiva, Vasodilatatoren und Alkoholgenuss verstärkt werden.
- Werden unter der Behandlung mit Meto-Succinat HCT Sandoz 95/12,5 mg zusätzlich Calciumantagonisten vom Nifedipin-Typ oder ACE-Hemmer eingenommen, kann der Blutdruck, insbesondere zu Behandlungsbeginn, stark abfallen und in Einzelfällen kann es zur Ausbildung einer Herzinsuffizienz kommen.
- Bei gleichzeitiger Anwendung von Calciumantagonisten vom Verapamiloder Diltiazem-Typ oder Antiarrhythmika ist eine sorgfältige Überwachung des Patienten angezeigt, da es zu Hypotonie,
Bradykardie oder anderen Herzrhythmusstörungen kommen kann. Während der Behandlung mit Meto-Succinat HCT Sandoz 95/12,5 mg muss deshalb die intravenöse Verabreichung von Calciumantagonisten oder Antiarrhythmika unterbleiben.
- Bei gleichzeitiger Anwendung von Meto-Succinat HCT Sandoz 95/12,5 mg und Reserpin, a-Methyldopa, Clonidin, Guanfacin und Herzglykosiden kann es zu einem stärkeren Absinken der Herzfrequenz bzw. zu einer Verzögerung der Erregungsleitung am Herzen kommen.
- Nach abruptem Absetzen von Clonidin bei gleichzeitiger Anwendung von Meto-Succinat HCT Sandoz 95/12,5 mg kann der Blutdruck überschießend ansteigen. Bei einer gleichzeitigen Behandlung mit Clonidin darf Clonidin erst abgesetzt werden, wenn einige Tage zuvor die Verabreichung von Meto-Succinat HCT Sandoz 95/12,5 mg beendet wurde. Anschließend kann Clonidin stufenweise abgesetzt werden.
- Rifampicin senkt die Plasmakonzentration von Metoprolol. Cimetidin, Hydrazalin und selektive Serotonin-Wiederaufnahmehemmer (SSRI), wie z. B. Paroxetin, Fluoxetin und Sertralin können die Plasmakonzentration von Metoprolol erhöhen.
- Die Ausscheidung anderer Medikamente kann durch Meto-Succinat HCT Sandoz 95/12,5 mg vermindert werden (z. B. Lidocain, Chinidin).
- Die dämpfenden Wirkungen von Meto-Succinat HCT Sandoz 95/12,5 mg und Alkohol können sich gegenseitig verstärken.
- Die negativ inotrope Wirkung von Meto-Succinat HCT Sandoz 95/12,5 mg und einem Narkotikum können sich addieren. Deshalb sollte der Narkosearzt über die Behandlung mit Meto-Succinat HCT Sandoz 95/12,5 mg informiert werden.
- Die blutdrucksenkende Wirkung von Meto-Succinat HCT Sandoz 95/12,5 mg kann vermindert werden durch gleichzeitige Einnahme von Schmerz- und Rheumamitteln (Salicylate, nicht-steroidale Antirheumatika, z. B. Indometacin). Bei hochdosierter Salicylateinnahme kann die toxische Wirkung des Salicylates auf das zentrale Nervensystem verstärkt werden.
- Die Wirkungen Blutzucker- und Harnsäure-senkender Medikamente sowie von Noradrenalin und Adrenalin können abgeschwächt werden.
- Bei vorhandener Hypokaliämie und/oder Hypomagnesiämie können die Wirkungen und Nebenwirkungen von Herzglykosiden verstärkt sein.
- Bei gleichzeitiger Einnahme von Laxanzien (auch Tee) oder Glucocorticoiden können erhöhte Kaliumverluste auftreten.
- Bei gleichzeitiger hochdosierter Behandlung mit Lithium-haltigen Arzneimitteln (gegen Depressionen) kann die Lithiumwirkung auf Herz und Gehirn zunehmen.
- Die Aufnahme von Hydrochlorothiazid kann durch die gleichzeitige Gabe von Colestyramin vermindert sein.
- In Einzelfällen sind Hämolysen durch Bildung von Antikörpern gegen Hydrochlorothiazid bei gleichzeitiger Einnahme von Methyldopa beschrieben worden.
Meto-Succinat HCT Sandoz 95/12,5 mg ist während Schwangerschaft und Stillzeit kontraindiziert (siehe Abschnitt 4.3 und 4.4).
Die Anwendung von HCTZ in der Schwangerschaft ist kontraindiziert (siehe Abschnitte 4.3 und 4.4).
Es liegen nur begrenzte Erfahrungen mit der Anwendung von Hydrochlorothiazid in der Schwangerschaft vor, insbesondere während des ersten Trimesters. Ergebnisse aus Tierstudien sind unzureichend. Hydrochlorothiazid ist plazentagängig. Auf Grund des pharmakologischen Wirkmechanismus von Hydrochlorothiazid kann es bei Anwendung während des zweiten und dritten Trimesters zu einer Störung der feto-plazentaren Perfusion und zu fetalen und neonatalen Auswirkungen wie Ikterus, Störung des Elektrolythaushalts und Thrombozytopenien kommen. Auf Grund des Risikos eines verringerten Plasmavolumens und einer plazentaren Hypoperfusion, ohne den Krankheitsverlauf günstig zu beeinflussen, sollte Hydrochlorothiazid bei Schwangerschaftsödemen, Schwangerschaftshypertonie oder einer Präeklampsie nicht zur Anwendung kommen.
4.7
4.8
Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen
Die Behandlung des Bluthochdrucks mit diesem Arzneimittel bedarf der regelmäßigen ärztlichen Kontrolle. Durch individuell auftretende unterschiedliche Reaktionen kann die Fähigkeit zur aktiven Teilnahme am Straßenverkehr, zum Bedienen von Maschinen oder zum Arbeiten ohne sicheren Halt beeinträchtigt werden. Dies gilt in verstärktem Maße bei Behandlungsbeginn, Dosiserhöhung, Präparatewechsel sowie im Zusammenwirken mit Alkohol.
Nebenwirkungen
Bei den Häufigkeitsangaben zu Nebenwirkungen werden folgende Kategorien zugrunde gelegt:
Sehr häufig Häufig Gelegentlich Selten Sehr selten Nicht bekannt
(> 1/10)
(> 1/100 bis < 1/10)
(> 1/1000 bis < 1/100)
(> 1/10 000 bis < 1/1000)
(< 1/10 000)
(Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar)
Erkrankungen des Blutes und des Lymphsystems
Selten: Blutbildveränderungen in Form einer Verminderung der roten Blutkörperchen (aplastische Anämie), Verminderung der Blutplättchen (Thrombozytopenie) und Leukozyten im Blut (Leukopenie), hochgradige Verminderung bestimmter weißer Blutkörperchen mit Infektneigung und schweren Allgemeinsymptomen (Agranulozytose).
Erkrankungen des Immunsystems
Selten: allergische Hauterscheinungen, Idiosynkrasie Sehr selten: allergischer Schnupfen
Stoffwechsel- und Ernährungsstörungen
Häufig: Ein latenter Diabetes mellitus kann erkennbar werden oder eine bereits bestehende Zuckerkrankheit sich verschlechtern (Symptome: Hyperglykämie, Glykosurie). Unter der Therapie kann es zu Störungen im Fettstoffwechsel kommen: Bei meist normalem Gesamtcholesterin wurde eine Verminderung des HDL-Cholesterins und eine Erhöhung der Triglyzeride im Plasma beobachtet.
Die Harnsäurewerte im Blut können sich erhöhen (Hyperurikämie); bei disponierten Patienten können Gichtanfälle ausgelöst werden. Die Anwendung von Meto-Succinat HCT Sandoz 95/12,5 mg kann bei langfristiger, kontinuierlicher Einnahme zu Veränderungen im Mineralstoffwechsel (Elektrolytveränderungen) führen, insbesondere zu einer Erniedrigung der Blutspiegel von Kalium (Hypokaliämie), Magnesium (Hypomagnesiämie), Natrium (Hyponatriämie) und Chlorid (Hypochlorämie) sowie zu einem erhöhten Calciumspiegel (Hyperkalzämie). Als Folge der Elektrolyt- und Flüssigkeitsverluste kann sich eine metabolische Alkalose entwickeln bzw. eine bereits bestehende metabolische Alkalose verschlechtern.
Selten: Nach längerem strengen Fasten oder schwerer körperlicher Belastung kann es bei gleichzeitiger Meto-Succinat HCT Sandoz 95/12,5 mg-Therapie zu Zuständen mit erniedrigtem Blutzucker (hypoglykämische Zustände) kommen. Warnzeichen eines erniedrigten Blutzuckers -insbesondere erhöhte Herzfrequenz (Tachykardie) und Zittern der Finger (Tremor) - können verschleiert werden.
Psychiatrische Erkrankungen
Gelegentlich: depressive Verstimmungszustände, Verwirrtheit, Halluzinationen
Selten: Nervosität, Ängstlichkeit
Sehr selten: Persönlichkeitsveränderungen (z. B. Gefühlsschwankungen)
Sehr häufig: Erschöpfung
Häufig: Benommenheit, Kopfschmerzen
Gelegentlich: Insbesondere zu Beginn der Behandlung zentralnervöse Störungen wie Müdigkeit, Schwindelgefühl, Schlafstörungen, Schlaflosigkeit, verstärkte Traumaktivität, Albträume, Konzentrationsstörungen. Diese Erscheinungen sind gewöhnlich leichterer Art und vorübergehend. Kribbeln in den Gliedmaßen, Muskelkrämpfe.
Selten: Muskelschwäche, Impotenz, Libido- und Potenzstörungen Sehr selten: Amnesie, Gedächtnisstörungen
Augenerkrankungen
Selten: Konjunktivitis und verminderter Tränenfluss (dies ist beim Tragen von Kontaktlinsen zu beachten); Augenreizung, geringgradige Sehstörungen (z. B. verschwommenes Sehen, Farbsehstörungen [Gelbsehen]) oder eine Verschlimmerung einer bestehenden Kurzsichtigkeit.
Sehr selten: Flimmern vor den Augen
Häufigkeit nicht bekannt: akute Myopie, akutes Engwinkelglaukom
Erkrankungen des Ohrs und des Labyrinths Sehr selten: Hörstörungen, Ohrensausen
Herzerkrankungen
Häufig: Palpitationen, Bradykardie, orthostatische Hypotonie (sehr selten mit Synkope)
Gelegentlich: Verstärkung einer Herzmuskelschwäche mit peripheren Ödemen (Flüssigkeitsansammlungen), kardiogener Schock bei Patienten mit akutem Herzinfarkt, Herzschmerzen
Selten: atrioventrikuläre Überleitungsstörungen, Arrhythmien
Sehr selten: Verstärkung der Anfälle bei Angina pectoris
Häufig: Kältegefühl in den Gliedmaßen Selten: Gefäßentzündung (Vaskulitis)
Sehr selten: Verstärkung (bis zur Gangrän) bereits bestehender peripherer Durchblutungsstörungen
Erkrankungen der Atemwege, des Brustraums und Mediastinums
Häufig: Atemnot bei Belastung (Belastungsdyspnoe)
Gelegentlich: Infolge einer möglichen Erhöhung des Atemwiderstandes kann es bei Patienten mit Neigung zu Verkrampfungen der Atemwege (bronchospastischen Reaktionen, z. B. bei asthmoider Bronchitis) insbesondere bei obstruktiven Atemwegserkrankungen zu einer Verengung der Atemwege und zu Atemnot kommen.
Selten: akute interstitielle Pneumonie
Sehr selten: allergisches Lungenödem mit Schocksymptomatik
Erkrankungen des Gastrointestinaltrakts
Häufig: vorübergehend Magen-Darm-Beschwerden wie Übelkeit, Leibschmerzen, Durchfall, Verstopfung
Gelegentlich: Erbrechen, Appetitlosigkeit, Krämpfe
Selten: Mundtrockenheit, Entzündung der Bauchspeicheldrüse
Leber- und Gallenerkrankungen
Selten: Erhöhung der Transaminasen GOT, GPT; Gelbsucht, intrahepatische Cholestase; akute Gallenblasenentzündung (bei bestehendem Gallensteinleiden)
Sehr selten: Hepatitis
Erkrankungen der Haut und des Unterhautzellgewebes
Gelegentlich: Hautreaktionen wie Rötung und Juckreiz sowie Hautausschläge (meist psoriasiforme und dystrophische Hautläsionen),
Schwitzen, stark juckende Quaddeln (Urtikaria), Lichtempfindlichkeit mit Auftreten von Hautausschlägen nach Lichteinwirkung
Selten: kleinflächige Einblutungen in der Haut und Schleimhaut (Purpura), Haarausfall, nekrotisierende Angiitis
Sehr selten: Arzneimittel, die Betarezeptoren-Blocker enthalten, können in Einzelfällen eine Schuppenflechte (Psoriasis vulgaris) auslösen, die Symptome dieser Erkrankung verschlechtern oder zu Schuppenflechteähnlichen (psoriasiformen) Hautausschlägen führen; kutaner Lupus erythematodes.
Skelettmuskulatur-, Bindegewebs- und Knochenerkrankungen
Sehr selten: Bei Langzeittherapie wurde in Einzelfällen eine Erkrankung der Gelenke (Arthropathie) und/oder Arthralgie (Gelenkschmerzen) beobachtet, wobei ein oder mehrere Gelenke betroffen sein können (Mono- und Polyarthritis).
Erkrankungen der Nieren und Harnwege
Selten: akute Nierenentzündung (interstitielle Nephritis)
Erkrankungen der Geschlechtsorgane und der Brustdrüse
Sehr selten: Induratio penis plastica (Peyronie-Krankheit)
Allgemeine Erkrankungen und Beschwerden am Verabreichungsort Gelegentlich: Gewichtszunahme
Selten: Arzneimittelfieber. Bei hoher Dosierung kann es, insbesondere bei Vorliegen von Venenerkrankungen, zu Thrombosen und Embolien kommen.
Sehr selten: Geschmacksstörungen
Untersuchungen
Gelegentlich: reversibler Anstieg stickstoffhaltiger, harnpflichtiger Stoffe (Harnstoff, Kreatinin) im Serum, vor allem zu Behandlungsbeginn.
Selten: Erhöhung der Blutfettwerte
Eine Verstärkung der Beschwerden bei Patienten mit intermittierendem Hinken (Claudicatio intermittens) oder mit Gefäßkrämpfen im Bereich der Zehen und Finger (Raynaud-Syndrom) ist beobachtet worden.
Die Symptome einer schweren Schilddrüsenüberfunktion (Thyreotoxikose) können maskiert werden.
4.9
Überdosierung
Symptome
Überdosierung kann zu schwerer Hypotonie, Herzinsuffizienz, kardiogenem Schock und Bradykardie bis zum Herzstillstand führen. Zusätzlich können Atembeschwerden, Bronchospasmen, Erbrechen, Bewusstseinsstörungen und auch generalisierte Krampfanfälle auftreten. Durch den Diuretika-Anteil von Meto-Succinat HCT Sandoz 95/12,5 mg muss auch mit einer länger als 24 Stunden anhaltenden Diurese und einer stärkeren Ausscheidung von Natrium und Chlorid gerechnet werden. Bei chronischer Überdosierung können Störungen des Kaliumhaushalts im Vordergrund stehen. Es kann sich eine Hypokaliämie entwickeln.
Maßnahmen
Bei Überdosierung oder bedrohlichem Abfall von Puls und/oder Blutdruck muss die Behandlung mit Meto-Succinat HCT Sandoz 95/12,5 mg abgebrochen werden.
Neben allgemeinen Maßnahmen der primären Giftelimination (induziertes Erbrechen, Magenspülung) oder Resorptions-mindernden Maßnahmen (medizinische Kohle) müssen unter intensivmedizinischen Bedingungen die vitalen Parameter sowie Wasser- und Elektrolythaushalt, Säure-BasenHaushalt, Blutzucker und harnpflichtige Substanzen überwacht und Abweichungen ggf. korrigiert werden. Als Gegenmittel können gegeben werden:
Atropin:
0,5-2,0 mg intravenös als Bolus Glucagon:
initial 1-10 mg intravenös,
dann 2-2,5 mg pro Stunde als Dauerinfusion.
Beta-Sympathomimetika in Abhängigkeit von Körpergewicht und Effekt: Dopamin, Dobutamin, Isoprenalin, Orciprenalin oder Adrenalin.
Bei therapierefraktärer Bradykardie sollte eine Schrittmachertherapie durchgeführt werden.
Bei Bronchospasmus können Beta-2-Sympathomimetika (als Aerosol, bei ungenügender Wirkung auch intravenös) oder Aminophyllin intravenös gegeben werden.
Bei Krampfanfällen empfiehlt sich die langsame i.v. Gabe von Diazepam.
Bei Störungen des Elektrolythaushalts und bei Flüssigkeitsverlust muss ein Ausgleich der Natrium- und Flüssigkeitsverluste durch Kochsalz-haltige Getränke, ggf. physiologische Kochsalzlösung i.v., erfolgen.
Bei chronischer Intoxikation und Hypokaliämie muss für einen Ausgleich des Kaliumdefizits gesorgt werden.
5.
5.1
Pharmakologische Eigenschaften Pharmakodynamische Eigenschaften
Pharmakotherapeutische Gruppe: Antihypertensiva
ATC-Code: C07BB02
Metoprolol
Metoprolol ist ein Beta-Rezeptorenblocker hat eine relative Selektivität zu den Beta-1-Rezeptoren (“Kardioselektivität”), die vorwiegend am Herzmuskel lokalisiert sind. Bei höheren Dosierungen hat Metoprolol allerdings auch einen Einfluss auf die Beta-2-Rezeptoren z. B. der Bronchien und Blutgefäße. Metoprolol hat keine intrinsische sympathomimetische Aktivität (ISA) und nur schwach ausgeprägte Membran-stabilisierende Wirkung. Die Substanz senkt in Abhängigkeit von der Höhe des Sympathikotonus die Frequenz und die Kontraktionskraft des Herzens, die AV-Überleitungsgeschwindigkeit und die Plasma-Renin-Aktivität. Metoprolol kann durch Hemmung von Beta-2-Rezeptoren eine Erhöhung des Tonus der glatten Muskulatur bewirken.
Hydrochlorothiazid
Hydrochlorothiazid ist ein Benzothiadiazin-Derivat, das wie andere Diuretika dieser Gruppe primär eine Mehrausscheidung von Elektrolyten bewirkt und sekundär durch das osmotisch gebundene Wasser den Harnfluss vergrößert.
Thiazid-Diuretika hemmen vorwiegend im distalen Tubulus die Natriumreabsorption, wobei maximal etwa 15 % des glomerulär filtrierten Natriums ausgeschieden werden können. Das Ausmaß der Chloridausscheidung entspricht etwa der Natriumausscheidung. Durch Hydrochlorothiazid nimmt auch die Kaliumausscheidung zu, die im Wesentlichen durch die Kaliumsekretion im distalen Tubulus und im Sammelrohr bestimmt wird (vermehrter Austausch zwischen Natrium- und Kalium-Ionen).
Durch hohe Hydrochlorothiazid-Dosen kann Bicarbonat infolge einer Hemmung der Carboanhydratase vermehrt ausgeschieden werden, wodurch der Urin alkalisiert wird.
Durch Azidose oder Alkalose wird die saluretische bzw. diuretische Wirkung des Hydrochlorothiazids nicht wesentlich beeinflusst.
Die glomeruläre Filtrationsrate wird initial geringgradig vermindert.
Während der Langzeittherapie mit Hydrochlorothiazid wird die Calciumausscheidung über die Niere reduziert, so dass eine Hyperkalziämie resultieren kann.
Bei hypertensiven Patienten hat Hydrochlorothiazid einen blutdrucksenkenden Effekt. Der Mechanismus ist bisher noch nicht ausreichend geklärt. Diskutiert wird u.a., dass die Gefäßtonus-mindernde Wirkung der Thiazid-Diuretika durch Abnahme der Natriumkonzentration in der Gefäßwand und damit durch eine verringerte Ansprechbarkeit auf Noradrenalin bedingt ist. Bei chronisch niereninsuffizienten Patienten (Kreatinin-Clearance unter 30 ml/min und/oder Serum-Kreatinin über 1,8 mg/100 ml) ist Hydrochlorothiazid praktisch unwirksam.
Die diuretische Wirkung tritt innerhalb 1-2 Stunden ein. Die diuretische Wirkdauer beträgt dosisabhängig 10-12 Stunden, die antihypertensive Wirkdauer ist noch länger (bis zu 24 Stunden).
Durch diese feste Kombination dieser beiden blutdrucksenkenden Substanzen mit unterschiedlichem Angriffspunkt erhält man einen additiven blutdrucksenkenden Effekt der Einzelkomponenten. Durch eine DiuretikaMonotherapie kommt es primär zu einer Verminderung des extrazellulären Flüssigkeitsraumes, was reaktiv zu einer Aktivierung des Renin-Angiotensin-Aldosteron-Systems führt. Ein Teil des blutdrucksenkenden Effektes geht damit verloren. Die Gegenregulation, d. h. die erhöhte Aktivität des Renin-Angiotensin-Aldosteron- und auch des sympathischen Systems kann durch gleichzeitige Gabe von Beta-Blockern gebremst werden.
5.2
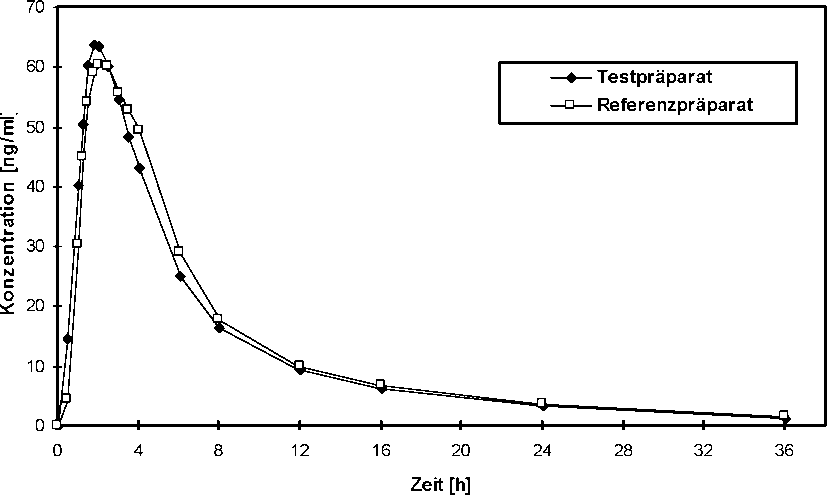
Pharmakokinetische Eigenschaften
Metoprolol wird nach oraler Applikation nahezu vollständig (ca. 95 %) aus dem Gastrointestinaltrakt resorbiert. Aufgrund eines ausgeprägten FirstPass-Metabolismus liegt die systemische Verfügbarkeit nur bei ca. 50 %. Maximale Plasmaspiegel werden nach 1,5-2 Stunden erreicht. Die Proteinbindung beträgt 12 %, das relative Verteilungsvolumen 5,6 l/kg. Metoprolol wird fast vollständig in der Leber metabolisiert. Zwei der drei Hauptmetaboliten zeigen schwach Beta-Rezeptoren-blockierende Eigenschaften, sind jedoch klinisch nicht relevant. Bei Leberzirrhose muss wegen der dann verminderten Metabolisierungsrate mit erhöhten Plasmaspiegeln an unverändertem Metoprolol gerechnet werden.
Die Elimination erfolgt überwiegend renal (ca. 95 %). Unverändertes Metoprolol macht ca. 10 % der Gesamtausscheidung aus. Die Eliminationshalbwertszeit von Metoprolol beträgt 3-5 Stunden.
Hydrochlorothiazid wird nach oraler Applikation aus dem Gastrointestinaltrakt zu ca. 80 % resorbiert. Die systemische Verfügbarkeit
beträgt ca. 70 %. Maximale Plasmakonzentrationen werden gewöhnlich nach 2-5 Stunden gemessen.
Die Plasmaproteinbindung von Hydrochlorothiazid beträgt 64 %; das relative Verteilungsvolumen beträgt 0,5 bis 1,1 l/kg.
Hydrochlorothiazid wird bei Gesunden unverändert vorwiegend renal ausgeschieden. Die Eliminationshalbwertszeit beträgt bei normaler Nierenfunktion 6-8 Stunden. Sie erhöht sich bei eingeschränkter Nierenfunktion und liegt bei terminal insuffizienten Patienten bei ca. 20 Stunden.
Bei eingeschränkter Nierenfunktion kann Hydrochlorothiazid als Folge der verzögerten renalen Exkretion kumulieren. Bei Nierenkranken liegen deshalb die Plasmaspiegel von Hydrochlorothiazid höher und nehmen auch langsamer ab als bei Gesunden.
Bei eingeschränkter Leberfunktion ist keine nennenswerte Beeinträchtigung der Pharmakokinetik zu erwarten, da Hydrochlorothiazid zu 95 % unverändert über die Nieren ausgeschieden wird. Dies gilt jedoch nicht für Patienten mit hepatogenem Hydrops, weil hierbei vielfach gleichzeitig eine Einschränkung der Nierenfunktion besteht.
5.3 Präklinische Daten zur Sicherheit
Metoprolol Akute Toxizität
Nach einmaliger oraler Anwendung an verschiedenen Tierarten zeigt Metoprolol eine niedrige Toxizität.
Chronische Toxizität
Untersuchungen zur chronischen Toxizität an verschiedenen Tierspezies erbrachten keine Hinweise auf Substanz-bedingte toxische Effekte.
Kanzerogenität
Es liegen Ergebnisse von Kanzerogenitätsstudien an Ratten und Mäusen vor, aus denen sich kein kanzerogenes Potenzial für den Menschen ableiten lässt.
Mutagenität
Metoprolol wurde keiner ausführlichen Mutagenitätsprüfung unterzogen; bisherige Untersuchungen ergaben keine Hinweise auf ein mutagenes Potenzial.
Reproduktionstoxikologie
Untersuchungen an zwei Tierspezies (Ratte, Kaninchen) haben keine Hinweise auf teratogene Eigenschaften von Metoprolol ergeben.
Hydrochlorothiazid
Akute Toxizität
Nach einmaliger oraler Anwendung an verschiedenen Tierarten zeigt Hydrochlorothiazid eine niedrige Toxizität.
Chronische Toxizität
In Untersuchungen zur subchronischen und chronischen Toxizität am Tier (Hund, Ratte) zeigten sich außer Veränderungen im Elektrolytgleichgewicht keine auffälligen Befunde.
Kanzerogenität
Langzeituntersuchungen mit Hydrochlorothiazid wurden an Ratten und Mäusen durchgeführt und zeigten keine relevanten Erhöhungen der Anzahl von Tumoren in den Dosisgruppen.
Mutagenität
In-vitro- und In-vivo-Mutagenitätstests zur Induktion von Gen- und Chromosomenmutationen durch Hydrochlorothiazid verliefen negativ.
Reproduktionstoxikologie
Hydrochlorothiazid passiert im Tierversuch die Plazenta. Untersuchungen an drei Tierarten (Ratte, Maus, Kaninchen) ergaben keine Hinweise auf eine teratogene Wirkung.
Hydrochlorothiazid geht in geringen Mengen in die Muttermilch über. Für Thiazid-Diuretika ist bekannt, dass sie die Laktation hemmen können.
6.
6.1
Pharmazeutische Angaben Liste der sonstigen Bestandteile
mikrokristalline Cellulose
Crospovidon
Glucose
Hypromellose
Lactose-Monohydrat
Macrogol 4000
Magnesiumstearat (Ph.Eur.)
Maisstärke
Polyacrylat-Dispersion 30 % hochdisperses Siliciumdioxid Sucrose Talkum
Titandioxid (E 171)
Eisen(III)-hydroxid-oxid (E 172)
6.2
6.3
6.4
6.5
6.6
7.
8.
9.
10. 11.
Inkompatibilitäten
Nicht zutreffend
Dauer der Haltbarkeit
30 Monate
Besondere Vorsichtsmaßnahmen für die Aufbewahrung
Nicht über 25 °C lagern
Art und Inhalt des Behältnisses
Aclar/Aluminium-Blister
Packungsgrößen mit 30, 50 und 100 Retardtabletten
Besondere Vorsichtsmaßnahmen für die Beseitigung
Keine speziellen Hinweise
Inhaber der Zulassung
Sandoz Pharmaceuticals GmbH Raiffeisenstraße 11 83607 Holzkirchen
Zulassungsnummer
58470.00.00
Datum der Erteilung der Zulassung
04.01.2006
Stand der Information
Oktober 2013
Verkaufsabgrenzung
Verschreibungspflichtig